СПИСОК
Вопросов к курсовому экзамену по биологии
Уровни организации жизни Проявление главных свойств жизни на разных уровнях ее организации.
Различают следующие уровни организации органического мира:
В микросистемы входят: а) молекулярно-генетический уровень б) субклеточный в) клеточный уровни.
Биологически мезосистемы: а) тканевый уровень б) органный уровень в) организменный
Биологические макросистемы: а) популяционно-видовой б) биоценотический в) биосферный.
Молекулярный уровень организации - это уровень функционирования биологических макромолекул - биополимеров: нуклеиновых кислот, белков, полисахаридов, липидов, стероидов. С этого уровня начинаются важнейшие процессы жизнедеятельности: обмен веществ, превращение энергии, передача наследственной информации. Этот уровень изучают: биохимия, молекулярная генетика, молекулярная биология, генетика, биофизика.
Клеточный уровень - это уровень клеток (клеток бактерий, цианобактерий, одноклеточных животных и водорослей, одноклеточных грибов, клеток многоклеточных организмов). Клетка - это структурная единица живого, функциональная единица, единица развития. Этот уровень изучают цитология, цитохимия, цитогенетика, микробиология. Тканевый уровень организации - это уровень, на котором изучается строение и функционирование тканей. Исследуется этот уровень гистологией и гистохимией.
Органный уровень организации - это уровень органов многоклеточных организмов. Изучают этот уровень анатомия, физиология, эмбриология. Организменный уровень организации - это уровень одноклеточных, колониальных и многоклеточных организмов. Специфика организменного уровня в том, что на этом уровне происходит декодирование и реализация генетической информации, формирование признаков, присущих особям данного вида. Этот уровень изучается морфологией (анатомией и эмбриологией), физиологией, генетикой, палеонтологией.
Популяционно-видовой уровень - это уровень совокупностей особей - популяций и видов. Этот уровень изучается систематикой, таксономией, экологией, биогеографией, генетикой популяций. На этом уровне изучаются генетические и экологические особенности популяций, элементарные эволюционные факторы и их влияние на генофонд (микроэволюция), проблема сохранения видов.
Экосистемный уровень организации - это уровень микроэкосистем, мезоэкосистем, макроэкосистем. На этом уровне изучаются типы питания, типы взаимоотношений организмов и популяций в экосистеме, численность популяций, динамика численности популяций, плотность популяций, продуктивность экосистем, сукцессии. Этот уровень изучает экология. Выделяют также биосферный уровень организации живой материи. Биосфера - это гигантская экосистема, занимающая часть географической оболочки Земли. Это мегаэкосистема. В биосфере происходит круговорот веществ и химических элементов, а также превращение солнечной энергии.
История открытия клетки.
Первым человеком, увидевшим клетки, был английский учёный Роберт Гук. В 1665 году, пытаясь понять, почему пробковое дерево так хорошо плавает, Гук стал рассматривать тонкие срезы пробки с помощью усовершенствованного им микроскопа. Он обнаружил, что пробка разделена на множество крошечных ячеек, напомнивших ему монастырские кельи, и он назвал эти ячейки клетками (по-английски cell означает «келья, ячейка, клетка»).
В 1675 году итальянский врач М. Мальпиги, а в 1682 году — английский ботаник Н. Грю подтвердили клеточное строение растений. О клетке стали говорить как о «пузырьке, наполненном питательным соком».
В 1674 году голландский мастер Антоний ван Левенгук с помощью микроскопа впервые увидел в капле воды «зверьков» — движущиеся живые организмы (инфузории, амёбы, бактерии). Также Левенгук впервые наблюдал животные клетки — эритроциты и сперматозоиды. Таким образом, уже к началу XVIII века учёные знали, что под большим увеличением растения имеют ячеистое строение, и видели некоторые организмы, которые позже получили название одноклеточных.
В 1802—1808 годах французский исследователь Шарль-Франсуа Мирбель установил, что все растения состоят из тканей, образованных клетками.
Ж. Б. Ламарк в 1809 годураспространил идею Мирбеля о клеточном строении и на животные организмы.
В 1825 году чешский учёный Я. Пуркине открыл ядро яйцеклетки птиц, а в 1839 ввёл термин «протоплазма».
В 1831 году английский ботаник Р. Броун впервые описал ядро растительной клетки, а в 1833 году установил, что ядро является обязательным органоидом клетки растения. С тех пор главным в организации клеток считается не мембрана, а содержимое.
Клеточная теория строения организмов была сформирована в 1839 году немецким зоологом Т. Шванном и М. Шлейденом и включала в себя три положения. В 1858 году Рудольф Вирхов дополнил её ещё одним положением, однако в его идеях присутствовал ряд ошибок: так, он предполагал, что клетки слабо связаны друг с другом и суще
целостность клеточной системы. В 1878 году русским учёным И. Д. Чистяковым открыт митоз в растительных клетках; в 1878 году В. Флемминг и П. И. Перемежко обнаруживают митоз у животных. В 1882 году В. Флемминг наблюдает мейоз у животных клеток, а в 1888 году Э Страсбургер - у растительных.
Из гисты
- 1847 – Гольджи – пластинчатый комплекс
- 1897 – К. Бенде дал термин, описал в 1894 Рихард Альтман
- 1895 – Т. Бовери – центриоли
- 1945 – К. Портер – ЭПС
- 1949 – К. де Дюв – лизосомы
18. Клеточная теория, ее развитие (Т.Шванн, М.Шлейден, Р.Вирхов).
Клеточная теория, одно из наиболее важных обобщений в биологии, была сформулирована в 1839 г. немецкими учеными — зоологом Теодором Шванном и ботаником Маттиасом Шлейденом.
Появлению клеточной теории предшествовал довольно долгий период накопления данных о строении живых существ. Английский ученый Роберт Гук в своей книге «Микрография» (1667 г.) впервые описал клеточную структуру растительных тканей. Рассматривая под микроскопом тонкие срезы пробки, сердцевины бузины и т. п., Р. Гук отметил ячеистое строение тканей растений и назвал эти ячейки клетками.
Важнейшие открытия были сделаны в XVII в. и голландским ученым-самоучкой Антоном ван Левенгуком. Он описал одноклеточные организмы (инфузории) и клетки животных (эритроциты, сперматозоиды).
Работы Р. Гука и А. Левенгука послужили толчком для систематических микроскопических исследований различных живых организмов. Уже в XIX в. были выявлены различные внутриклеточные компоненты: ядро (Р. Броун,1831 г.), протоплазма (Я. Пуркинье,1837 г.), хромосомы (В. Флемминг,1880 г.), митохондрии (К. Бенуа, 1894 г.) аппарат Гольджи (К. Гольджи,1898 г.). Основное значение теории Т. Шванна и М. Шлейдена заключается в том, что они показали принципиальное сходство клеток растений и животных. Это положение явилось важнейшим доказательством единства живой природы. Столь же значимо и представление о самостоятельной жизнедеятельности каждой отдельной клетки.
В работах Р. Вирхова (1855-1858 гг.) был сформулирован тезис «всякая клетка от клетки», т. е. речь идет об образовании новых клеток путем деления исходной (материнской). Сегодня это признано как биологический закон (нет иных путей образования клеток и увеличения их числа).
Обобщая все изложенное выше, сформулируем основные положения клеточной теории:
· Клетка — основная единица строения и развития всех живых организмов, является наименьшей структурной единицей живого.
· Клетки всех организмов (как одно-, так и многоклеточных) сходны по химическому составу, строению, основным проявлениям обмена веществ и жизнедеятельности.
· Размножение клеток происходит путем их деления (каждая новая клетка образуется при делении материнской клетки);
Значение клеточной теории
Cтало ясно, что клетка — важнейшая составляющая часть живых организмов, их главный морфофизиологический компонент. Клетка — это основа многоклеточного организма, место протекания биохимических и физиологических процессов в организме. На клеточном уровне в конечном итоге происходят все биологические процессы. Клеточная теория позволила сделать вывод о сходстве химического состава всех клеток, общем плане их строения, что подтверждает филогенетическое единство всего живого мира.
Биологические мембраны.
Мембраны биологические — функционально активные поверхностные структуры толщиной в несколько молекулярных слоев, ограничивающие цитоплазму и большинство органелл клетки, а также образующие единую внутриклеточную систему канальцев, складок, замкнутых областей.
Функции биологических мембран следующие:
1. Отграничивают содержимое клетки от внешней среды и содержимое органелл от цитоплазмы.
2. Обеспечивают транспорт веществ в клетку и из нее, из цитоплазмы в органеллы и наоборот.
3. Выполняют роль рецепторов (получение и преобразование сит-налов из
окружающей среды, узнавание веществ клеток и т. д.).
4. Являются катализаторами (обеспечение примембранных химических процессов).
5. Участвуют в преобразовании энергии.
Плазмолемма (внешняя клеточная мембрана). Занимает в клетке пограничное положение и играет роль полупроницаемого селективного барьера, который отделят цитоплазму от окружающей среды, а с другой – обеспечивает её связь с этой средой.
Функции плазмолеммы:
1) Распознавание данной клеткой других клеток и прикрепление к ним.
2) Распознавание клеткой межклеточного вещества и прикрепление к его элементам.
3) Транспорт веществ в цитоплазму и из неё.
4) Взаимодействие с сигнальными молекулами.
5) Движение клетки (образование псевдо- фило- и ламеллоподий)
Структура плазмолеммы: Плазмолемма состоит из липидного бислоя, в который погружены и с которым связаны молекулы белков. Липидный бислой представлен преимущественно молекулами лецитина и цефалина, состоящими из гидрофильной головки и гидрофобного хвоста. Гидрофобные цепи обращены внутрь бислоя, гидрофильные головки – кнаружи. Липиды обеспечивают основные свойства мембраны в т.ч. их текучесть.
Мембранные белки обеспечивают спецефические свойства мембраны и играют различную биологическую роль (переносчиков, ферментов, рецепторов, структурных молекул). По расположению на мембране выделяют два типа белков: периферические и интегральные. Периферические белки обычно находятся вне липидного слоя и не прочно связаны с мембраной. Интегральные белки либо полностью, либо частично погружены в липидный бислой. Часть белков целиком пронизывает всю мембрану (т.н. трансмембранные белки).
Ядерная оболочка (кариолемма). Кариолемма состоит из двух мембран – наружной и внутренней – разделенных полостью и смыкающихся в области ядерных пор.
Наружная мембрана составляет единое целое с мембранами грЭПС – на её поверхности имеются рибосомы, а полость соответствует полости цистерн. Внутренняя мембрана – гладкая, интегральные белки связаны с ядерной пластинкой. Ядерная пластинка обеспечивает:
1) поддержание формы ядра,
2) упорядоченную укладку хроматина,
3) структурную организацию поровых комплексов,
4) формирование кариолеммы при делении клеток
Эволюция форм
Эволюция размножения шла, как правило, в направлении от бесполых форм к половым, от изогамии к анизогамии, от участия всех клеток в размножении к разделению клеток на соматические и половые, от наружного оплодотворения к внутреннему с внутриутробным развитием и заботой о потомстве.
Темп размножения, численность потомства, частота смены поколений наряду с другими факторами определяют скорость приспособления вида к условиям среды. Например, высокие темпы размножения и частая смена поколений позволяют насекомым в короткий срок вырабатывать устойчивость к ядохимикатам. В эволюции позвоночных — от рыб до теплокровных — наблюдается тенденция к уменьшению численности потомства и увеличению его выживаемости.
Бесполое размножение — форма размножения, не связанная с обменом генетической информацией между особями — половым процессом.
Бесполое размножение является древнейшим и самым простым способом размножения и широко распространено у одноклеточных организмов (бактерии, сине-зелёные водоросли, хлореллы, амёбы, инфузории). Этот способ имеет свои преимущества: в нём отсутствует необходимость поиска партнёра, а полезные наследственные изменения сохраняются практически навсегда. Однако при таком способе размножения изменчивость, необходимая для естественного отбора, достигается только за счёт случайных мутаций и потому осуществляется очень медленно. Тем не менее, следует отметить, что способность вида только к бесполому размножению не исключает способности к половому процессу, но когда эти события разнесены во времени.
Наиболее распространённый способ размножения одноклеточных организмов — деление на две части, с образованием двух отдельных особей.
Среди многоклеточных организмов способностью к бесполому размножению обладают практически все растения и грибы — исключением является, например, вельвичия. Бесполое размножение этих организмов происходит вегетативным способом или спорами.
Среди животных способность к бесполому размножению чаще встречается у низших форм, но отсутствует у более развитых. Единственный способ бесполого размножения у животных — вегетативный.
Широко распространено ошибочное мнение, что особи, образовавшиеся в результате бесполого размножения, всегда генетически идентичны родительскому организму (если не брать в расчёт мутации). Наиболее яркий контрпример — размножение спорами у растений, так как при спорообразовании происходит редукционное деление клеток, в результате чего в спорах содержится лишь половина генетической информации, имеющейся в клетках спорофита (см. Жизненный цикл растений).
Половое размножение сопряжено с половым процессом (слиянием клеток), а также, в каноническом случае, с фактом существования двух взаимодополняющих половых категорий (организмов мужского пола и организмов женского пола).
} Гологамия – самая ранняя стадия. При этом сливаются родительские особы целиком, полностью объединяются их цитоплазма и генетический материал, наблюдается у простейших.
} В дальнейшем сливаться стали уже не родительские особы, а их специализированные части – половые клетки, этот этап эволюции получил название мерогамия.
} Первым этапом мерогамии была изогамия – мужские и женские половые клетки не имели существенных отличий.
} Затем возникла анизогамия. Яйцеклетки стали утрачивать подвижность, накапливать питательные вещества. Спермии приобрели аппарат движения.
} Оогамия (последний этап эволюции) – женские гаметы имеют запас питательных веществ, но полностью неподвижны. Мужские гаметы приобрели совершенный аппарат движения, но полностью лишились цитоплазмы.
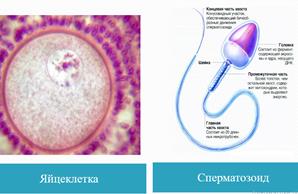
Яйцеклетка: строение
Наиболее очевидная отличительная черта яйцеклетки - это ее большие размеры. Типичная яйцеклетка имеет сферическую или овальную форму, а диаметр ее составляет у человека около 100 мкм (величина типичной соматической клетки около 20 мкм). Столь же внушительными могут быть размеры ядра, в преддверии быстрых делений, следующих сразу за оплодотворением , в ядре откладываются запасы белков.
Потребность клетки в питательных веществах удовлетворяет в основном желток - материал протоплазмыа, богатый липидами и белками. Он обычно содержится в дискретных образованиях, называемых желточными гранулами .
Другой важной специфической структурой яйцеклетки является наружная яйцевая оболочка - покров из особого неклеточного вещества, состоящего в основном из гликопротеиновых млекул, часть которых секретирует сама яйцеклетка, а другую часть - окружающие клетки. У многих видов оболочка имеет внутренний слой, непосредственно прилегающий к плазматической мембране яйцеклетки и называемый у млекопитающих zona pellucida , а у других животных - вителлиновым слоем . Этот слой защищает яйцеклетку от механических повреждений, в некоторых яйцеклетках он действует также как видоспецифический барьер для спермиев, позволяющий проникать внутрь только спермиям того же вида или очень близких видов.
Многие яйцеклетки (в том числе и млекопитающих) содержат специализированные секреторные пузырьки, находящиеся под плазматической мембраной в наружном, или кортикальном, слое цитоплазмы. При активации яйцеклетки спермием эти кортикальные гранулы высвобождают содержимое путем экзоцитоза , в результате свойства яйцевой оболочки изменяются таким образом, что через нее уже не могут проникнуть внутрь яйцеклетки другие спермии.
Различают первичную оболочку, образуемую самой яйцевой клеткой, вторичную оболочку, являющуюся продуктом деятельности фолликулярных клеток, и третичныеоболочки, которыми яйцо окружается во время прохождения по яйцеводу. Первичная оболочка, иногда называемая желточной, имеется у яйцеклеток всех животных. У позвоночных, в том числе млекопитающих и человека, первичная оболочка входит в состав плотной оболочки, образуя ее внутреннюю часть. Внешняя часть плотной оболочки продуцируется фолликулярными клетками и является вторичной оболочкой. Плотная оболочка изнутри пронизана микроворсинками яйцеклетки, а снаружи — микроворсинками фолликулярных клеток, отчего при большом увеличении она выглядит исчерченной и названа лучистой оболочкой (corona radiata). За свои оптические свойства у млекопитающих она получила название блестящей оболочки (zona pellucida). Таким образом, эта оболочка совмещает в себе первичную и вторичную оболочки.
Мужские гаметы — сперматозоиды животных и многих растений подвижны и обычно несут один или несколько жгутиков, исключением являются лишённные жгутиков мужские гаметы семенных растений — спермии, кот дост-ся к яйцеклетке при прорастании пыльцевой трубки, безжгутиковые сперматозоиды (спермии) нематод и членистоногих.
Хотя сперматозоиды несут митох, при оогамии от мужской гаметы к зиготе переходит ядерная ДНК, мтх ДНК наследуется зиготой только от яйцеклетки.
Сперматозоиды - это очень мелкие подвижные мужские половые клетки (гаметы), образующиеся в мужских половых гонадах - семенниках . У здорового взрослого мужчины в сутки образуется около 10 млн сперматозоидов; в 1 куб. мл спермы содержится около 100 млн сперматозоидов, а во время одного семяизвержения выделяется 300-400 млн. Процесс образования сперматозоида занимает примерно 70 дней.
Каждый сперматозоид состоит из головки (5 мкм), шейки, промежуточного отдела (5 мкм) и жгутика (50 мкм).( рис. 191 ) Головка яйцевидной формы содержит ядро, обладающее, как и ядро яйцеклетки, одним (гаплоидным) набором хромосом (23 хромосомы). На переднем полюсе головки под плазматической мембраной расположена акросома. особая структура, ограниченная мембраной. Акросома способствует проникновению спермия в ооцит непосредственно перед оплодотворением, функционально ее можно рассматривать как увеличенную лизосому: содержащиеся в ней ферменты при оплодотворении растворяют плотную оболочку яйцеклетки и способствуют проникновению сперматозоида в яйцеклетку. В короткой шейке сперматозоида расположено множество митохондрий, обеспечивающих сперматозоид энергией движения. В шейке сперматозоида расположена также пара центриолей, лежащих под прямым углом друг к другу. Микротрубочки одной из них, удлиняясь, образуют осевую нить жгутика, которая проходит вдоль всей остальной части сперматозоида. Промежуточный отдел расширен за счет содержащихся в нем многочисленных митохондрий, собранных в спираль вокруг жгутика. Как уже было сказано, эти митохондрии доставляют энергию для сократительных механизмов, обеспечивающих движения жгутика.
Плотная упаковка хромосом в головке сперматозоида и отсутствие цитоплазмы позволяют ему хорошо сохранять свою целостность вне организма и делают его очень устойчивым к неблагоприятным воздействиям внешней среды: сперму можно замораживать и хранить при очень низких температурах (обычно в жидком азоте). При отсутствии или недоразвитии акросомы сперматозоид теряет способность оплодотворять яйцеклетку.
Эмбриональная индукция
Эмбриональная индукция — это взаимодействие частей развивающегося зародыша, при котором один участок зародыша влияет на судьбу другого участка. Явление эмбриональной индукции с начала XX в. изучает экспериментальная эмбриология.
Г. Шпеман назвал спинную губу бластопора первичным эмбриональным организатором. Первичным потому, что на более ранних стадиях развития подобных влияний обнаружить не удавалось, а организатором потому, что влияние происходило именно на морфогенез. В настоящее время установлено, что главная роль в спинной губе бластопора принадлежит хордомезодермальному зачатку, который назвали первичным эмбриональным индуктором, а само явление, при котором один участок зародыша влияет на судьбы другого,— эмбриональной индукцией.
В 30-е гг. исследователи пытались установить природу индуцирующего действия. Вскоре выяснилось, что разнообразные убитые ткани, вытяжки из самых различных тканей беспозвоночных и позвоночных животных, а также растений, несколько классов химических соединений (белки, нуклеопротеины, стероиды и даже неорганические вещества) могут вызывать индукцию. Таким образом была установлена химическая природа организаторов. Одновременно стало ясно, что специфичность ответа прямо не связана с. химическими свойствами индуктора.
Внимание эмбриологов переключилось на индуцируемые ткани. Оказалось, что специфичность действия индуктора-раздражителя может быть весьма различной, а сам эффект индуцирующего воздействия ограничивается способностью того или иного участка развивающегося зародыша воспринимать это воздействие и отвечать на него.
Некоторые индукторы, по-видимому, более или менее специфичны в определении судьбы индуцируемой ткани. Об этом свидетельствуют следующие опыты. Если пересадить спинную губу ранней гаструлы, то индуцируется развитие структур переднего мозга (головной индуктор), если же пересадить спинную губу поздней гаструлы, то развиваются спинной мозг и мезодермальные ткани (туловищный индуктор, рис. 8.9). Было показано также, что наиболее сильное нейрализующее влияние оказывает фракция нуклеопротеинов, а мезодермализующим индуктором оказался белок. Если имплантировать оба эти индуктора в виде смеси клеток или смеси веществ, то получаются хорошо развитые зародыши.
Другие индукторы действуют как неспецифические пусковые механизмы, как бы высвобождая ответ, уже детерминированный в клетках индуцируемой ткани. Было показано, что, например, слуховой пузырек выступает не только в роли индуктора слухового аппарата, но и является активатором различных морфогенетических процессов. Будучи пересажен в область боковой линии эмбриона тритона, он влечет за собой индукцию конечности. Конечность можно индуцировать также пересадкой носовой плакоды или гипофиза. Легче всего добавочные конечности индуцируются в области боковой линии, но они могут быть получены и на брюшной стороне. Эти примеры указывают на то, что специфический ответ зависит не столько от индуктора, сколько отреагирующей области.
Способность эмбрионального материала реагировать на различного рода влияния изменением своей презумптивной судьбы получила название компетенции. Установлено, например, что компетенция к образованию нервной системы у амфибий затрагивает всю эмбриональную эктодерму и возникает с момента начала гаструляции. К концу гаструляции эта компетенция прекращается. Таким образом, изменение хода развития возможно лишь в том случае, если область компетенции к образованию некоторой закладки шире, чем область, из которой она в норме развивается, а также если индукционное действие происходит в определенный интервал онтогенетического развития.
Явления индукции многочисленны и разнообразны. Помимо первичной индукции со стороны спинной губы бластопора описаны индукционные влияния на более поздних, нежели гаструляция, этапах развития. Все они являются вторичными и третичными, представляя собой каскадные взаимодействия, типичные для дифференцировки, потому что индукция многих структур зависит от предшествующих индукционных событий. Примером вторичной индукции может служить действие глазного бокала (выпячивание переднего мозга) на прилежащий покровный эпителий, под влиянием чего эпителий впячивается, а затем отшнуровывается хрусталиковый пузырек—зачаток глазного хрусталика (рис. 8.11). Расположенный над хрусталиком покровный эпителий тоже испытывает сложные изменения, теряет пигмент и становится роговичным эпителием. Это пример третичной индукции. Таким образом получается, что глазной бокал возникает только после развития передней части головного мозга, хрусталик — после формирования бокала, а роговица — после образования хрусталика.
Вместе с тем индукция носит не только каскадный, но и переплетающийся характер, т.е. в индукции той или иной структуры может участвовать не одна, а несколько тканей. В свою очередь, такая структура может служить индуктором для нескольких других тканей. Например, глазной бокал служит главным, но не единственным индуктором хрусталика. Морфогенез всегда сопровождается значительными перемещениями тканей друг относительно друга. Так, презумптивный хрусталик, т.е. эпидермис, из которого в последующем должен развиться хрусталик, во время гаструляции лежит над энтодермой будущей глотки, которая служит первым индуктором хрусталика. Затем под этим эпидермисом оказывается сердечная мезодерма, которая тоже действует как индуктор. И только позднее, во время нейруляции на переднем конце нервной трубки выпячиваются глазные пузыри, образующие глазной бокал и сетчатку, являющуюся главным индуктором хрусталика (рис. 8.12).
Различают гетерономную и гомономную виды индукции. К гетерономной относят случаи, подобные описанному, при которых один кусочек зародыша индуцирует иной орган (хордомезодерма индуцирует появление нервной трубки и всего зародыша в целом). Гомономная индукция заключается в том, что индуктор побуждает окружающий материал к развитию в том же направлении, что и он сам. Например, область нефротома, пересаженная другому зародышу, способствует развитию окружающего материала в сторону формирования головной почки, а прибавление в культуру фибробластов сердца маленького кусочка хряща влечет за собой процесс образования хряща.
Чтобы воспринять действие индуктора, компетентная ткань должна обладать хотя бы минимальной организацией. Одиночные клетки не воспринимают действие индуктора, а чем больше клеток в реагирующей ткани, тем активнее ее реакция. Для оказания индуцирующего действия иногда достаточно лишь одной клетки индуктора.
Индукционные взаимодействия могут проявляться в культуре ткани in vitro, но по-настоящему полноценными они бывают только в структуре целостного организма.
Весьма интересны результаты опытов, помогающие оценить взаимосвязь индукционных взаимодействий с цитодифференцировкой и морфогенезом. Ранее уже было описано определяющее влияние мезенхимы на морфогенез конечностей позвоночных. Многочисленными опытами показано также большое влияние мезенхимы на морфогенез желез эпителиального происхождения. Легочная энтодерма, например, при выращивании с печеночной мезенхимой приобретает строение печеночных балок, а эпителий молочной железы под влиянием мезенхимного зачатка слюнной железы приобретает морфологию слюнной железы. Это происходит как при выращивании in vitro, так и при трансплантации в организм животного-реципиента. Подобные результаты с несомненностью указывают на необходимость индуцирующего влияния мезенхимы на морфогенез.
Однако не менее интересен факт, что морфогенез не всегда сопряжен с определенным направлением дифференцирован эпителия. Так, рекомбинантная слюнная железа, полученная из зачатка молочной железы и мезенхимы слюнной, при подсадке лактирующей самке-реципиенту начинает вырабатывать молоко несмотря на то, что имеет морфологию по типу слюнной железы. Это свидетельствует о возможности разобщения, об автономности процессов морфогенеза и цитодифференцировки и может быть объяснено более ранней детерминацией цитодифференцировки другими, более ранними актами индукции. Подобные наблюдения позволяют по-другому взглянуть на возможности преобразований морфогенезов в процессе эволюции.
Способы гаструляции
Инвагинация – впячивание одного из участков бластодермы внутрь целым пластом.
} В результате гаструла имеет вид двухслойной чаши.
} В ней различают:
} 1 – эктодерму
} 2 – энтодерму
} 3 – бластопор (первичный рот)
} 4 – а в его составе 4 губы: дорсальная (4), вентральная (5) и две боковые (6)
Эпиболия – обрастание мелкими клетками анимального полюса более крупных, отстающих в скорости деления и менее подвижных клеток вегетативного полюса.
} Такой процесс ярко выражен у земноводных.
Деламинация – расслоение клеток бластодермы на два слоя, лежащих друг над другом.
} Деламинацию можно наблюдать в дискобластуле зародышей с частичным типом дробления (пресмыкающиеся, птицы, яйцекладущие млекопитающие)
} Деламинация проявляется в эмбриобласте плацентарных млекопитающих, приводя к образованию гипобласта и эпибласта.
Иммиграция – перемещение групп или отдельных клеток, не объединенных в единый пласт.
} В наибольшей степени характерна для второй фазы гаструляции высших позвоночных.
Необходимой предпосылкой перехода к органогенезам является достижение зародышем стадии гаструлы, а именно формирование зародышевых листков.
} Самое начало органогенеза называют периодом нейруляции (от формирования нервной пластинки до замыкания ее в нервную трубку).
} Параллельно формируется хорда и первичная кишка, а лежащая по бокам от хорды мезодерма расщепляется на сегментированные парные структуры – сомиты, разделенные на три части – дерматом, миотом и склеротом.
} Латеральнее сомитов лежит часть мезодермы – нефрогонотомы или сегментные ножки.
} Спланхнотом – несегментированная часть мезодермы, но при этом каждый спланхнотом расслаиваться на два листка – париетальный и висцеральный.
} Между листками находится целомическая полость.
Производные эктодермы:
} Нервная трубка и ганглиозные пластинки – образуют:
} чувствительные спиномозговые ганглии,
} симпатические нервные узлы,
} мозговое вещество надпочечников,
} парасимпатические ганглии
} Кожная эктодерма - является зачатком:
} эпидермиса кожи и его производных,
} эпителия начального и конечного отделов желудочно- кишечного тракта,
} эпителия некоторых других органов.
Производные мезодермы:
- Хорда - одна из её функций - установление оси тела, вдоль которой затем формируется позвоночный столб.
- Сомиты – делятся на сегменты, из каждого образуются:
- Дерматом – дает начало плотной неоформленной соединительной ткани кожи
- Миотом – поперечно-полосатой мышечной ткани скелетного типа
- Склеротом – хрящевой и костной ткани
- Нефрогонотом - представляет собой зачатки системы выделения и гонад
- Спланхнотом – из обоих его листков образуется эпителий, выстилающий внутренние полости организма (плевральную, сердечную, брюшную). Кроме того, висцеральный листок - зачаток миокарда и эпикарда.
Целомическая полость – образует внутренние полости организма
Производные энтодермы:
} Кишечная энтодерма – в последствии тоже участвует в формировании осевого зачатка (вместе с висцеральным листком спланхнотома) - первичной кишки.
} Поэтому энтодерма называется кишечной.
} Последняя -зачаток эпителия органов пищеварительной системы (желудка, кишечника, печени, поджелудочной железы).
Молекулярный уровень
Репарация ДНК
Каждая из систем репарации включает следующие компоненты:
ДНК-хеликаза — фермент, «узнающий» химически изменённые участки в цепи и осуществляющий разрыв цепи вблизи от повреждения; экзонуклеаза — фермент, удаляющий повреждённый участок;
ДНК-полимераза — фермент, синтезирующий соответствующий участок цепи ДНК взамен удалённого;
ДНК-лигаза — фермент, замыкающий последнюю связь в полимерной цепи и тем самым восстанавливающий её непрерывность.
Прямая репарация — наиболее простой путь устранения повреждений в ДНК, в котором обычно задействованы специфические ферменты, способные быстро (как правило, в одну стадию) устранять соответствующее повреждение, восстанавливая исходную структуру нуклеотидов.
Эксцизионная репарация включает удаление повреждённых азотистых оснований из ДНК и последующее восстановление нормальной структуры молекулы.
Клеточный
Важным механизмом сохранения генетического гомеостаза является диплоидное состояние соматических клеток у эукариот. Диплоидные клетки отличаются большей стабильностью функционирования, т.к. наличие у них двух генетических программ повышает надёжность генотипа. Стабилизация сложной системы генотипа обеспечивается явлениями полимерии и другими видами взаимодействия генов. Большую роль в процессе гомеостаза играют регуляторные гены, контролирующие активность оперонов.
- Митоз
- Мейоз
Организменный
- Иммунитет как защита от всего генетически чужеродного
Механизмы гомеостаза - обратная связь
· Отрицательная обратная связь, выражающаяся в реакции, при которой система отвечает так, чтобы изменить направление изменения на противоположное.
· Положительная обратная связь, которая выражается в усилении изменения переменной. Она оказывает дестабилизирующий эффект, поэтому не приводит к гомеостазу.
72. Биологические основы репаративной и физиологической регенерации. Репарация генетического материала.
Регенерация (от лат. regeneratio — возрождение) — процесс восстановления организмом утраченных или поврежденных структур. Регенерация поддерживает строение и функции организма, его целостность. Различают два вида регенерации: физиологическую и репаративную. Восстановление органов, тканей, клеток или внутриклеточных структур после разрушения их в процессе жизнедеятельности организма называют физиологической регенерацией. Восстановление структур после травмы или действия других повреждающих факторов называют репаративной регенерацией. При регенерации происходят такие процессы, как детерминация, дифференцировка, рост, интеграция и др., сходные с процессами, имеющими место в эмбриональном развитии. Однако при регенерации все они идут уже вторично, т.е. в сформированном организме.
Физиологическая регенерация представляет собой процесс обновления функционирующих структур организма. Благодаря физиологической регенерации поддерживается структурный гомеостаз и обеспечивается возможность постоянного выполнения органами их функций. С общебиологической точки зрения, физиологическая регенерация, как и обмен веществ, является проявлением такого 401 важнейшего свойства жизни, как самообновление.
Примером физиологической регенерации на внутриклеточном уровне являются процессы восстановления субклеточных структур в клетках всех тканей и органов. Значение ее особенно велико для так называемых «вечных» тканей, утративших способность к регенерации путем деления клеток. В первую очередь это относится к нервной ткани. Примерами физиологической регенерации на клеточном и тканевом уровнях являются обновление эпидермиса кожи, роговицы глаза, эпителия слизистой кишечника, клеток периферической крови и др. Обновляются производные эпидермиса — волосы и ногти. Это так называемая пролиферативная регенерация, т.е. восполнение численности клеток за счет их деления. Во многих тканях существуют специальные камбиальные клетки и очаги их пролиферации. Это крипты в эпителии тонкой кишки, костный мозг, пролиферативные зоны в эпителии кожи. Интенсивность клеточного обновления в перечисленных тканях очень велика. Это так называемые «лабильные» ткани. Все эритроциты теплокровных животных, например, сменяются за 2—4 мес, а эпителий тонкой кишки полностью сменяется за 2 сут. Это время требуется для перемещения клетки из крипты на ворсинку, выполнения ею функции и гибели. Клетки таких органов, как печень, почка, надпочечник и др., обновляются значительно медленнее. Это так называемые «стабильные» ткани.
Об интенсивности пролиферации судят по количеству митозов, приходящихся на 1000 подсчитанных клеток. Если учесть, что сам митоз в среднем длится около 1 ч, а весь митотаческий цикл в соматических клетках в среднем протекает 22—24 ч, то становится ясно, что для определения интенсивности обновления клеточного состава тканей необходимо подсчитать количество митозов в течение одних или нескольких суток. Оказалось, что количество делящихся клеток не одинаково в разные часы суток. Так был открыт суточный ритм клеточных делений.
Суточный ритм количества митозов обнаружен не только в нормальных, но и в опухолевых тканях. Он является отражением более общей закономерности, а именно ритмичности всех функций организма. Существование самой суточной периодичности количества митозов указывает на регулируемость физиологической регенерации организмом. Кроме суточных существуют лунные и годичные циклы обновления тканей и органов.
В физиологической регенерации выделяют две фазы: разрушительную и восстановительную. Полагают, что продукты распада части клеток стимулируют пролиферацию других. Большую роль в регуляции клеточного обновления играют гормоны.
Физиологическая регенерация присуща организмам всех видов, но особенно интенсивно она протекает у теплокровных позвоночных, так как у них вообще очень высока интенсивность функционирования всех органов по сравнению с другими животными.
Репаративная (от лат. reparatio — восстановление) регенерация наступает после повреждения ткани или органа. Она очень разнообразна по факторам, вызывающим повреждения, по объемам повреждения, по способам восстановления. Механическая травма, например оперативное вмешательство, действие ядовитых веществ, ожоги, обморожения, лучевые воздействия, голодание, другие болезнетворные агенты,— все это повреждающие факторы. Наиболее широко изучена регенерация после механической травмы. Способность некоторых животных, таких, как гидра, планария, некоторые кольчатые черви, морские звезды, асцидия и др., восстанавливать утраченные органы и части организма издавна изумляла ученых. Ч. Дарвин, например, считал удивительными способность улитки воспроизводить голову и способность саламандры восстанавливать глаза, хвост и ноги именно в тех местах, где они отрезаны.
Объем повреждения и последующее восстановление бывают весьма различными. Крайним вариантом является восстановление целого организма из отдельной малой его части, фактически из группы соматических клеток. Среди животных такое восстановление возможно у губок и кишечнополостных. Среди растений возможно развитие целого нового растения даже из одной соматической клетки, как это получено на примере моркови и табака. Такой вид восстановительных процессов сопровождается возникновением новой морфогенетической оси организма и назван Б.П. Токиным «соматическим эмбриогенезом», ибо во многом напоминает эмбриональное развитие.
Существуют примеры восстановления больших участков организма, состоящих из комплекса органов. В качестве примера служат регенерация ротового конца у гидры, головного конца у кольчатого червя и восстановление морской звезды из одного луча (рис. 8.24). Широко распространена регенерация отдельных органов, например конечности у тритона, хвоста у ящерицы, глаз у членистоногих. Заживление кожных покровов, ран, повреждений костей и других внутренних органов является менее объемным процессом, но не менее важным для восстановления структурно-функциональной целостности организма. Особый интерес представляет способность зародышей на ранних стадиях развития восстанавливаться после значительной утраты материала. Эта способность была последним аргументом в борьбе между сторонниками преформизма и эпигенеза и привела в 1908 г. Г. Дриша к концепции эмбриональной регуляции.
Существует несколько разновидностей или способов репаративной регенерации. К ним относят эпиморфоз, морфаллаксис, заживление эпителиальных ран, регенерационную гипертрофию, компенсаторную гипертрофию.
Эпителизация при заживлении ран с нарушенным эпителиальным покровом идет примерно одинаково, независимо от того, будет далее происходить регенерация органа путем эпиморфоза или нет. Эпидермальное заживление раны у млекопитающих в том случае, когда раневая поверхность высыхает с образованием корки, проходит следующим образом (рис. 8.25). Эпителий на краю раны утолщается вследствие увеличения объема клеток и расширения межклеточных пространств. Сгусток фибрина играет роль субстрата для миграции эпидермиса в глубь раны. В мигрирующих эпителиальных клетках нет митозов, однако они обладают фагоцитарной активностью. Клетки с противоположных краев вступают в контакт. Затем наступает кератинизация раневого эпидермиса и отделение корки, покрывающей рану.
К моменту встречи эпидермиса противоположных краев в клетках, расположенных непосредственно вокруг края раны, наблюдается вспышка митозов, которая затем постепенно падает. По одной из версий, эта вспышка вызвана понижением концентрации ингибитора митозов — кейлона.
Эпиморфоз представляет собой наиболее очевидный способ регенерации, заключающийся в отрастании нового органа от ампутационной поверхности. Регенерация конечности тритона и аксолотля изучена детально. Выделяют регрессивную и прогрессивную фазы регенерации. Регрессивная фаза начинается с заживления раны, во время которого происходят следующие основные события: остановка кровотечения, сокращение мягких тканей культи конечности, образование над раневой поверхностью сгустка фибрина и миграция эпидермиса, покрывающего ампутационную поверхность.
Затем начинается разрушение остеоцитов на дистальном конце кости и других клеток. Одновременно в разрушенные мягкие ткани проникают клетки, участвующие в воспалительном процессе, наблюдается фагоцитоз и местный отек. Затем вместо образования плотного сплетения волокон соединительной ткани, как это происходит при заживлении ран у млекопитающих, в области под раневым эпидермисом утрачиваются дифференцированные ткани. Характерна остеокластическая эрозия кости, что является гистологическим признаком дедифференцировки. Раневой эпидермис, уже пронизанный регенерирующими нервными волокнами, начинает быстро утолщаться. Промежутки между тканями все более заполняются мезенхимоподобными клетками. Скопление мезенхимных клеток под раневым эпидермисом является главным показателем формирования регенерационной бластемы. Клетки бластемы выглядят одинаково, но именно в этот момент закладываются основные черты регенерирующей конечности.
Затем начинается прогрессивная фаза, для которой наиболее характерны процессы роста и морфогенеза. Длина и масса регенерационной бластемы быстро увеличиваются. Рост бластемы происходит на фоне идущего полным ходом формирования черт конечности, т.е. ее морфогенеза. Когда форма конечности в общих чертах уже сложилась, регенерат все еще меньше нормальной конечности. Чем крупнее животное, тем больше эта разница в размерах. Для завершения морфогенеза требуется время, по истечении которого регенерат достигает размеров нормальной конечности.
При эпиморфной регенерации не всегда образуется точная копия удаленной структуры. Такую регенерацию называют атипичной. Существует много разновидностей атипичной регенерации. Гипоморфоз — регенерация с частичным 407 замещением ампутированной структуры. Так, у взрослой шпорцевой лягушки возникает шиловидная структура вместо конечности. Гетероморфоз — появление иной структуры на месте утраченной. Это может проявляться в виде гомеозисной регенерации, заключающейся в появлении конечности на месте антенн или глаза у членистоногих, а также в изменении полярности структуры. Из короткого фрагмента планарии можно стабильно получать биполярную планарию (рис. 8.27). Встречается образование дополнительных структур, или избыточная регенерация. После надреза культи при ампутации головного отдела планарии возникает регенерация двух голов или более (рис. 8.28). Можно получить больше пальцев при регенерации конечности аксолотля, повернув конец культи конечности на 180°. Дополнительные структуры являются зеркальным отражением исходных или регенерировавших структур, рядом с которыми они расположены (закон Бэйтсона).
Морфаллаксис — это регенерация путем перестройки регенерирующего участка. Примером служит регенерация гидры из кольца, вырезанного из середины ее тела, или восстановление планарии из одной десятой или двадцатой ее части. На раневой поверхности в этом случае не происходит значительных формообразовательных процессов. Отрезанный кусочек сжимается, клетки внутри него перестраиваются, и возникает целая особь уменьшенных размеров, которая затем растет. Этот способ регенерации впервые описал Т. Морган в 1900 г. В соответствии с его описанием морфаллаксис осуществляется без митозов. Нередко имеет место сочетание эпиморфного роста на месте ампутации с реорганизацией путем морфаллаксиса в прилежащих частях тела.
Регенерационная гипертрофия относится к внутренним органам. Этот способ регенерации заключается в увеличении размеров остатка органа без восстановления исходной формы. Иллюстрацией служит регенерация печени позвоночных, в том числе млекопитающих. При краевом ранении печени удаленная часть органа никогда не восстанавливается. Раневая поверхность заживает. В то же время внутри оставшейся части усиливается размножение клеток (гиперплазия) и в течение двух недель после удаления 2/3 печени восстанавливаются исходные масса и объем, но не форма. Внутренняя структура печени оказывается нормальной, дольки имеют типичную для них величину. Функция печени также возвращается к норме.
Компенсаторная гипертрофия заключается в изменениях в одном из органов при нарушении в другом, относящемся к той же системе органов. Примером является гипертрофия в одной из почек при удалении другой или увеличение лимфатических узлов при удалении селезенки.
Последние два способа отличаются местом регенерации, но механизмы их одинаковы: гиперплазия и гипертрофия.
Восстановление отдельных мезодермальных тканей, таких, как мышечная и скелетная, называют тканевой регенерацией. Для регенерации мышцы важно сохранение хотя бы небольших ее культей на обоих концах, а для регенерации кости необходима надкостница. Регенерация путем индукции происходит в определенных мезодермальных тканях млекопитающих в ответ на действие специфических индукторов, которые вводят внутрь поврежденной области. Этим способом удается получить полное замещение дефекта костей черепа после введения в него костных опилок.
Несомненна регуляция регенерационных процессов со стороны нервной системы. При тщательной денервации конечности во время ампутации эпиморфная регенерация полностью подавляется и бластема никогда не образуется. Были проведены интересные опыты. Если нерв конечности тритона отвести под кожу основания конечности, то образуется дополнительная конечность. Если его отвести к основанию хвоста — стимулируется образование дополнительного хвоста. Отведение нерва на боковую область никаких дополнительных структур не вызывает. Эти эксперименты привели к созданию концепции регенерационных полей. Было установлено, что для инициации регенерации решающим является число нервных волокон. Тип нерва роли не играет. Влияние нервов на регенерацию связывается с трофическим действием нервов на ткани конечностей.
Получены данные в пользу гуморальной регуляции регенерационных процессов. Особенно распространенной моделью для изучения этого является регенерирующая печень. После введения нормальным интактным животным сыворотки или плазмы крови от животных, подвергшихся удалению печени, у первых наблюдалась стимуляция митотической активности клеток печени. Напротив, при введении травмированным животным сыворотки от здоровых животных получали снижение количества митозов в поврежденной печени. Эти опыты могут свидетельствовать как о присутствии в крови травмированных животных стимуляторов регенерации, так и о присутствии в крови интактных животных ингибиторов клеточного деления. Объяснение результатов опытов затрудняется необходимостью учитывать иммунологический эффект инъекций.
Важнейшим компонентом гуморальной регуляции компенсаторной и регенерационной гипертрофии является иммунологический ответ. Не только частичное удаление органа, но и многие воздействия вызывают возмущения в иммунном статусе организма, появление аутоантител и стимуляцию процессов клеточной пролиферации.
Большие разногласия существуют по вопросу о клеточных источниках регенерации. Откуда берутся или как возникают недифференцированные клетки бластемы, морфологически сходные с мезенхимными? Существует три предположения.
1. Гипотеза резервных клеток подразумевает, что предшественниками регенерационной бластемы являются так называемые резервные клетки, которые останавливаются на некоем раннем этапе своей дифференцировки и не участвуют в процессе развития до получения стимула к регенерации.
2. Гипотеза временной дедифференцировки, или модуляции, клеток предполагает, что в ответ на регенерационный стимул дифференцированные клетки 410 могут утрачивать признаки специализации, но затем снова дифференцируются в тот же клеточный тип, т.е., потеряв на время специализацию, они не утрачивают детерминацию.
3. Гипотеза полной дедифференцировки специализированных клеток до состояния, сходного с мезенхимными клетками и с возможной последующей трансдифференцировкой или метаплазией, т.е. превращением в клетки другого типа, полагает, что в этом случае клетка утрачивает не только специализацию, но и детерминацию.
Современные методы исследования не позволяют с абсолютной достоверностью доказать все три предположения. Тем не менее абсолютно верно, что в культях пальцев аксолотля происходит высвобождение хондроцитов из окружающего матрикса и миграция их в регенерационную бластему. Дальнейшая их судьба не определена. Большинство исследователей признают дедифференцировку и метаплазию при регенерации хрусталика у амфибий. Теоретическое значение этой проблемы заключается в допущении возможности или невозможности изменений клеткой ее программы до такой степени, что она возвращается в состояние, когда снова способна делиться и репрограммироватьсвой синтетический аппарат. Например, хондроцит становится миоцитом или наоборот.
Способность к регенерации не имеет однозначной зависимости от уровня организации, хотя давно уже было замечено, что более низко организованные животные обладают лучшей способностью к регенерации наружных органов. Это подтверждается удивительными примерами регенерации гидры, планарий, кольчатых червей, членистоногих, иглокожих, низших хордовых, например асцидий. Из позвоночных наилучшей регенерационной способностью обладают хвостатые земноводные. Известно, что разные виды одного и того же класса могут сильно отличаться по способности к регенерации. Кроме того, при изучении способности к регенерации внутренних органов оказалось, что она значительно выше у теплокровных животных, например у млекопитающих, по сравнению с земноводными.
Регенерация у млекопитающих отличается своеобразием. Для регенерации некоторых наружных органов нужны особые условия. Язык, ухо, например, не регенерируют при краевом повреждении. Если же нанести сквозной дефект через всю толщу органа, восстановление идет хорошо. В некоторых случаях наблюдали регенерацию сосков даже при ампутации их по основанию. Регенерация внутренних органов может идти очень активно. Из небольшого фрагмента яичника восстанавливается целый орган. Об особенностях регенерации печени уже было сказано выше. Различные ткани млекопитающих тоже хорошо регенерируют. Есть предположение, что невозможность регенерации конечностей и других наружных органов у млекопитающих носит приспособительный характер и обусловлена отбором, поскольку при активном образе жизни нежные морфогенетические процессы затрудняли бы существование. Достижения биологии в области регенерации успешно применяются в медицине. Однако в проблеме регенерации очень много нерешенных вопросов.
Темновая репарация
Темновая репарация не требует света. Она способна исправлять очень разнообразные повреждения ДНК. Темновая репарация протекает в несколько этапов при участии нескольких ферментов:
1. Молекулы эндонуклеазы постоянно обследуют молекулу ДНК, опознав повреждение, фермент разрезает вблизи него нить ДНК;
2. Эндо- или экзонуклеаза делает в этой нити второй надрез, иссекая поврежденный участок;
3. Экзонуклеаза значительно расширяет образующуюся брешь, отсекая десятки или сотни нуклеотидов;
4. Полимераза застраивает брешь в соответствии с порядком нуклеотидов во второй (неповрежденной) нити ДНК.
Механизм репарации основан на наличии в молекуле ДНК двух комплементарных цепей. Искажение последовательности нуклеотидов в одной из них обнаруживается специфическими ферментами. Затем соответствующий участок удаляется и замещается новым, синтезированным на второй комплементарной цепи ДНК. Такую репарацию называют эксцизионной, т.е. с «вырезанием» (рис. 3.15). Она осуществляется до очередного цикла репликации, поэтому ее называют также дорепликативной.
Восстановление исходной структуры ДНК требует участия ряда ферментов. Важным моментом в запуске механизма репарации является обнаружение ошибки в структуре ДНК. Нередко такие ошибки возникают во вновь синтезированной цепи в процессе репликации. Ферменты репарации должны обнаружить именно эту цепь. У многих видов живых организмов вновь синтезированная цепь ДНК отличается от материнской степенью метилирования ее азотистых оснований, которое отстает от синтеза. Репарации при этом подвергается неметилированная цепь. Объектом узнавания ферментами репарации могут также служить разрывы в цепи ДНК. У высших организмов, где синтез ДНК происходит не непрерывно, а отдельными репликонами, вновь синтезируемая цепь ДНК имеет разрывы, что делает возможным ее узнавание.
Восстановление структуры ДНК при утрате пуриновых оснований одной из ее цепей предполагает обнаружение дефекта с помощью фермента эндонуклеазы, которая разрывает фосфоэфирную связь в месте повреждения цепи. Затем измененный участок с несколькими примыкающими к нему нуклеотидами удаляется ферментом экзонуклеазой, а на его месте в соответствии с порядком оснований комплементарной цепи образуется правильная нуклеотидная последовательность (рис. 3.15).

При изменении одного из оснований в цепи ДНК в восстановлении исходной структуры принимают участие ферменты ДНК-гликозилазы числом около 20. Они специфически узнают повреждения, обусловленные дезаминированием, алкилированием и другими структурными преобразованиями оснований. Такие модифицированные основания удаляются. Возникают участки, лишенные оснований, которые репарируются, как при утрате пуринов. Если восстановление нормальной структуры не осуществляется, например в случае дезаминирования азотистых оснований, происходит замена одних пар комплементарных оснований другими —пара Ц—Г может заменяться парой Т—А и т.п. (см. разд. 3.4.2.3).
Образование в полинуклеотидных цепях под действием УФ-лучей тиминовых димеров (Т—Т) требует участия ферментов, узнающих не отдельные измененные основания, а более протяженные повреждения структуры ДНК. Репаративный процесс в этом случае также связан с удалением участка, несущего димер, и восстановлением нормальной последовательности нуклеотидов путем синтеза на комплементарной цепи ДНК.
В том случае, когда система эксцизионной репарации не исправляет изменения, возникшего в одной цепи ДНК, в ходе репликации происходит фиксация этого изменения и оно становится достоянием обеих цепей ДНК. Это приводит к замене одной пары комплементарных нуклеотидов на другую либо к появлению разрывов (брешей) во вновь синтезированной цепи против измененных участков. Восстановление нормальной структуры ДНК при этом может произойти и после репликации.
Пострепликативная репарация
Пострепликативная репарация осуществляется путем рекомбинации (обмена фрагментами) между двумя вновь образованными двойными спиралями ДНК. Примером такой пострепликативной репарации может служить восстановление нормальной структуры ДНК при возникновении тиминовых димеров (Т—Т), когда они не устраняются самопроизвольно под действием видимого света (световая репарация) или в ходе дорепликативной эксцизионной репарации.
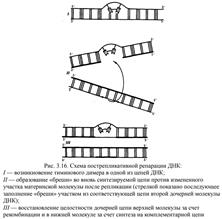
Ковалентные связи, возникающие между рядом стоящими остатками тимина, делают их не способными к связыванию с комплементарными нуклеотидами. В результате во вновь синтезируемой цепи ДНК появляются разрывы (бреши), узнаваемые ферментами репарации. Восстановление целостности новой полинуклеотидной цепи одной из дочерних ДНК осуществляется благодаря рекомбинации с соответствующей ей нормальной материнской цепью другой дочерней ДНК. Образовавшийся в материнской цепи пробел заполняется затем путем синтеза на комплементарной ей полинуклеотидной цепи (рис. 3.16). Проявлением такой пострепликативной репарации, осуществляемой путем рекомбинации между цепями двух дочерних молекул ДНК, можно считать нередко наблюдаемый обмен материалом между сестринскими хроматидами (рис. 3.17).
В ходе дорепликативной и пострепликативной репарации восстанавливается большая часть повреждений структуры ДНК. Однако, если в наследственном материале клетки возникает слишком много повреждений и часть из них не ликвидируется, включается система индуцируемых (побуждаемых) ферментов репарации (SOS-система). Эти ферменты заполняют бреши, восстанавливая целостность синтезируемых полинуклеотидных цепей без точного соблюдения принципа комплементарности. Вот почему иногда сами процессы репарации могут служить источником стойких изменений в структуре ДНК (мутаций). Названная реакция также относится к SOS-системе.
Если в клетке, несмотря на осуществляемую репарацию, количество повреждений структуры ДНК остается высоким, в ней блокируются процессы репликации ДНК.
Такая клетка не делится, а значит, не передает возникших изменений потомству. Вызываемая повреждениями ДНК остановка клеточного цикла в сочетании с невозможностью молекулярной репарации измененного наследственного материала может с участием белка, синтез которого контролируется геном р53, приводить к активации процесса самоликвидации (апоптоз) дефектной клетки с целью устранения ее из организма. Таким образом, обширный набор различных ферментов репарации осуществляет непрерывный «осмотр» ДНК, удаляя из нее поврежденные участки и способствуя поддержанию стабильности наследственного материала. Совместное действие ферментов репликации (ДНК-полимераза и редактирующая эндонуклеаза) и ферментов репарации обеспечивает достаточно низкую частоту ошибок в молекулах ДНК, которая поддерживается на уровне 1 · 10-9 пар измененных нуклеотидов на геном. При размере генома человека 3 · 109 нуклеотидных пар это означает появление около 3 ошибок на реплицирующийся геном. Вместе с тем даже этот уровень достаточен для образования за время существования жизни на Земле значительного генетического разнообразия в виде генных мутаций.
73. Фотореактивация.
Фотореактивация заключается в устранении видимым светом димеров тимина, особенно часто возникающих в ДНК под влиянием УФ-лучей. Замена осуществляется особым фотореактивирующим ферментом, молекулы которого не обладают сродством с неповрежденной ДНК, но опознают димеры тимина и связываются с ними сразу после их образования. Этот комплекс остается стабильным, пока не подвергнется действию видимого света. Видимый свет активирует молекулу фермента, она отделяется от димера тимина и одновременно разъединяет его на два отдельных тимина, восстанавливая исходную структуру ДНК.
74. Темновая репарация.
При световой репарации исправляются повреждения, возникшие только под воздействием ультрафиолетовых лучей, при темновой - повреждения, появившиеся под влиянием жесткой радиации, химических веществ и т.д.
Темновая репарация не требует света. Она способна исправлять очень разнообразные повреждения ДНК. Темновая репарация протекает в несколько этапов при участии нескольких ферментов:
1. Молекулы эндонуклеазы постоянно обследуют молекулу ДНК, опознав повреждение, фермент разрезает вблизи него нить ДНК;
2. Эндо- или экзонуклеаза делает в этой нити второй надрез, иссекая поврежденный участок;
3. Экзонуклеаза значительно расширяет образующуюся брешь, отсекая десятки или сотни нуклеотидов;
4. Полимераза застраивает брешь в соответствии с порядком нуклеотидов во второй (неповрежденной) нити ДНК.
Механизм репарации основан на наличии в молекуле ДНК двух комплементарных цепей. Искажение последовательности нуклеотидов в одной из них обнаруживается специфическими ферментами. Затем соответствующий участок удаляется и замещается новым, синтезированным на второй комплементарной цепи ДНК. Такую репарацию называют эксцизионной, т.е. с «вырезанием» (рис. 3.15). Она осуществляется до очередного цикла репликации, поэтому ее называют также дорепликативной.
Восстановление исходной структуры ДНК требует участия ряда ферментов. Важным моментом в запуске механизма репарации является обнаружение ошибки в структуре ДНК. Нередко такие ошибки возникают во вновь синтезированной цепи в процессе репликации. Ферменты репарации должны обнаружить именно эту цепь. У многих видов живых организмов вновь синтезированная цепь ДНК отличается от материнской степенью метилирования ее азотистых оснований, которое отстает от синтеза. Репарации при этом подвергается неметилированная цепь. Объектом узнавания ферментами репарации могут также служить разрывы в цепи ДНК. У высших организмов, где синтез ДНК происходит не непрерывно, а отдельными репликонами, вновь синтезируемая цепь ДНК имеет разрывы, что делает возможным ее узнавание.
Восстановление структуры ДНК при утрате пуриновых оснований одной из ее цепей предполагает обнаружение дефекта с помощью фермента эндонуклеазы, которая разрывает фосфоэфирную связь в месте повреждения цепи. Затем измененный участок с несколькими примыкающими к нему нуклеотидами удаляется ферментом экзонуклеазой, а на его месте в соответствии с порядком оснований комплементарной цепи образуется правильная нуклеотидная последовательность (рис. 3.15).

При изменении одного из оснований в цепи ДНК в восстановлении исходной структуры принимают участие ферменты ДНК-гликозилазы числом около 20. Они специфически узнают повреждения, обусловленные дезаминированием, алкилированием и другими структурными преобразованиями оснований. Такие модифицированные основания удаляются. Возникают участки, лишенные оснований, которые репарируются, как при утрате пуринов. Если восстановление нормальной структуры не осуществляется, например в случае дезаминирования азотистых оснований, происходит замена одних пар комплементарных оснований другими —пара Ц—Г может заменяться парой Т—А и т.п. (см. разд. 3.4.2.3).
Образование в полинуклеотидных цепях под действием УФ-лучей тиминовых димеров (Т—Т) требует участия ферментов, узнающих не отдельные измененные основания, а более протяженные повреждения структуры ДНК. Репаративный процесс в этом случае также связан с удалением участка, несущего димер, и восстановлением нормальной последовательности нуклеотидов путем синтеза на комплементарной цепи ДНК.
В том случае, когда система эксцизионной репарации не исправляет изменения, возникшего в одной цепи ДНК, в ходе репликации происходит фиксация этого изменения и оно становится достоянием обеих цепей ДНК. Это приводит к замене одной пары комплементарных нуклеотидов на другую либо к появлению разрывов (брешей) во вновь синтезированной цепи против измененных участков. Восстановление нормальной структуры ДНК при этом может произойти и после репликации.
75. Мутации, связанные с нарушением репарации и их роль в патологии.
Спонтанные повреждения ДНК встречаются довольно часто, такие события имеют место в каждой клетке. Для устранения последствий подобных повреждений имеется специальные репарационные механизмы(например, ошибочный участок ДНК вырезается и на этом месте восстанавливается исходный). Мутации возникают лишь тогда, когда репарационный механизм по каким-то причинам не работает или не справляется с устранением повреждений.
Мутации, возникающие в генах, кодирующих белки, ответственные за репарацию, могут приводить к многократному повышению (мутаторный эффект) или понижению (антимутаторный эффект) частоты мутирования других генов. Так, мутации генов многих ферментов системыэксцизионной репарацииприводят к резкому повышению частоты соматических мутаций у человека, а это, в свою очередь, приводит к развитию пигментнойксеродермыи злокачественных опухолей покровов.
n Белок р53 – «страж клеточного генома». Обнаружив мутацию, он блокирует репликацию ДНК до исправления. Если исправление невозможно, в клетке включается программа апоптоза.
Пигментная ксеродерма - группа заболеваний, при которых отмечается повышенная чувствительность кожи к солнечным лучам (покраснение.Пигментация, изъязвления, злокачественные образования). Это рецессивно аутосомное заболевание. Фибробласты кожи больных людей более чувствительны к ультрафиолетовым лучам, чем фибробласты здоровых людей. Это связано с тем, что они обладают пониженной способностью выщеплять димеры тимина, следовательно, имеет место нарушение репарации на первом ее этапе, то есть произошла мутация в гене, кодирующем синтез ультрафиолетовой специфической эндонуклеазы. Возможны нарушения и на других этапах репарации ДНК или даже на нескольких этапах.
Атаксия - телеангиоэктазия (синдром Луи Бара) - прогрессирующая атаксия мозжечка с нарушением координации движений, телеангиоэктазия склер. В этом случае сильно запаздывает второй этап репарации - удаление поврежденных оснований молекулы ДНК.
Синдром Блума - сочетание недоразвития скелета, гипофизарной карликовости, гипогонадизма с врожденной телеангиоэктатической эритермой лица, участками гиперкератоза и гиперпигментации на туловище. Эти аномалии связаны с нарушением пострепликативного восстановления - 4, 5 этапов репарации.
Синдром Коккейна – наследственное заболевание, с поражением кожи и её придатков, органов зрения, слуха и нарушением репарации. Синдром обусловлен мутациями в генах, кодирующие белки, ответственные за эксцизионную репарацию. Ребенок имеет внешний вид «старика», волосы быстро седеют, повышенная фоточувствительность может стать причиной появления на лице пигментации.
Анемия Фанкони – аутосомно-рецессивное заболевание, характеризующееся поражением всех элементов костного мозга, наблюдается нарушение вырезания пиримидиновых димеров, а также нарушение репарации межцепочечных сшивок.
76. Иммунитет как проявление генетического гомеостаза.
В настоящее время иммунитет определяют как способ защиты от всего, несущего признаки генетической чужеродности.
Биологический смысл иммунитета — обеспечение генетической целостности организма на протяжении его индивидуальной жизни.
Существует две разновидности иммунитета: клеточный и гуморальный. Пeрвый из них, в котoром используются Т-лимфоциты (тимус-зaвисимые), обеспечивает противовирусную и противоопухолeвую защиту; вторoй реализуeтся В-лимфоцитами (тимус-незaвисимыми), они вырабатывают антитела. Генетический гомеостаз на организменном уровне поддерживается неспецифическими механизмами защиты и системой иммунитета. Hеспецифические механизмы защиты противодействуют проникновению любых факторов из внешней среды, способных нарушить генетический гомеостаз, а так же нейтрализуют аномальные факторы, оказавшиеся в организме. Формы неспецифической защиты образуют две группы: клеточные и гуморальные.
Гомеостаз - это способность биологических систем противостоять изменениям и сохранять динамическое постоянство состава и свойств организма.
Болезнь - нарушение гомеостаза, результат рассогласования между реальной ситуацией и адаптивной программой организма.
В настоящее время иммунитет определяют как способ защиты от всего, несущего признаки генетической чужеродности.
Иммунная система возникла с появлением многоклеточных организмов и развилась как фактор, способствующий их выживанию
Иммунная система имеет три особенности:
а) генерализована по всему телу;
б) ее клетки постоянно циркулируют по всему телу через кровоток и лимфоток;
в) может вырабатывать сугубо специфические молекулы антител.
При формировании иммунной системы важную роль играет аппендикс. Аппендикс нам необходим в младенчестве и первые годы жизни. Наибольшего развития он достигает вскоре после рождения, а затем орган начинает регрессировать.
Все иммунокомпетент-ные клетки происходят из единой стволовой клетки костного мозга
Центральные органы иммунной системы – костный мозг и тимус.
При системной красной волчанке антитела связываются с ДНК и разрушают ее.
Лимфоциты - клетки, на которые возложены ключевые функции по осуществлению приобретённого иммунитета лейкоцитов
Т-киллеры разрушают инфицированные и злокачественные клетки.
Т-хелперы – посредники. Они вызывают превращение определенных клонов. В-лимфоцитов в плазматические клетки. Т-лимфоциты (хелперы) «инспектируют» В-лимфоцит, пытаясь обнаружить следы специфического антигена. ВИЧ поражает Т-хелперное звено иммунитета. Т-супрессоры - регулируют образование антител, подавляя Т-хелперы; накапливаются при старении, опухолевом росте, аутоиммунных заболеваниях.
Антиген – чужеродное для организма вещество, способное вызвать иммунный ответ
Антитело – белок сыворотки крови, специфически нейтрализующий антиген, вызвавший его образование. В основе многообразия антител лежит альтернативный сплайсинг
Цитокины являются молекулами-передатчиками сигнала. Они объединяют разные клетки для борьбы с инфекцией. Продуцентами цитокинов являются макрофаги. Интерлейкины - группа цитокинов, опосредующих активацию и взаимодействие иммунокомпетентных клеток в процессе иммунного ответа. ИЛ1 вызывает сонливость больного. ИЛ2 стимулирует размножение Т-хелперов. ИЛ2, ИЛ-4,-ИЛ6 включают клетки, которые убивают клетки с вирусом или раковые. ИЛ-4, 5, 6, выделяемые Т-хелперами, подключают к борьбе В-лимфоциты, которые, превращаясь в плазматические клетки, производят антитела.
Белок р53 – «страж клеточного генома». Обнаружив мутацию, он блокирует репликацию ДНК до исправления. Если исправление невозможно, в клетке включается программа апоптоза.
77. Иммунитет и старение. Иммунитет и канцерогенез.
Старение
С возрастом заметно изменяются функции иммунной системы. За гуморальный иммунитет ответственны В-лимфоциты, вырабатывающие антитела к носителям чужеродной биологической информации — антигенам. Т-лимфоциты ответственны за клеточный иммунитет, например за отторжение трансплантата, хотя могут участвовать в реакциях гуморального иммунитета. К старости наблюдается ослабление реакций как гуморального, так и клеточного иммунитета. Становление функции иммунной системы во многом связано с активностью тимуса, которая прекращается в связи с инволюцией железы по достижении половозрелого возраста (рис. 8.30). Нарушение естественного развития иммунной системы в эксперименте путем удаления вилочковой железы (например, у мышей) сокращает продолжительность жизни животных. Напротив, пересадка тимуса и костного мозга от молодой мыши к старой приводит к омоложению иммунной системы 19-месячной мыши до уровня 4-месячной. Некоторые такие животные жили на Уз дольше своего обычного срока.
В стареющем организме клетки иммунной системы ошибочно вырабатывают антитела против собственных клеток и белков. Таким образом, старение сопровождается нарастанием аутоиммунных реакций.
Канцерогенез
Канцерогенез — сложный патофизиологический процесс зарождения и развития опухоли.
Существует мнение, что в организме человека постоянно образуются потенциальные опухолевые клетки. Однако в силу своей антигенной гетерогенности они быстро распознаются и разрушаются клетками иммунной системы. Нормальное функционирование иммунной системы является основным фактором натуральной защиты от опухолей. Этот факт доказан клиническими наблюдениями за больными с ослабленной иммунной системой, у которых опухоли встречаются в десятки раз чаще, чем у людей с нормально работающей иммунной системой.
Канцерогенные факторы
На данный момент известно большое количество факторов, способствующих канцерогенезу:
Химические факторы
Вещества ароматической природы (полициклические и гетероциклические ароматические углеводороды, ароматические амины), некоторые металлы и пластмассы обладают выраженным канцерогенным свойством благодаря их способности реагировать с ДНК клеток, нарушая ее структуру (мутагенная активность). Канцерогенные вещества в больших количествах содержатся в продуктах горения автомобильного и авиационного топлива, в табачных смолах. При длительном контакте организма человека с этими веществами могут возникнуть такие заболевания, как рак легкого, рак толстого кишечника и др. Известны также эндогенные химические канцерогены(ароматические производные аминокислоты триптофана), вызывающие гормонально зависящие опухоли половых органов.
Физические факторы
Солнечная радиация (в первую очередь ультрафиолетовое излучение) и ионизирующее излучение также обладает высокой мутагенной активностью. Так, после аварии Чернобыльской АЭС отмечено резкое увеличение заболеваемости раком щитовидной железы у людей, проживающих в зараженной зоне. Длительное механическое или термическое раздражение тканей также является фактором повышенного риска возникновения опухолей слизистых оболочек и кожи(рак слизистой рта, рак кожи, рак пищевода).
Биологические факторы
Доказана канцерогенная активность вируса папиломы человека в развитии рака шейки матки[2], вируса гепатита Вв развитии рака печени,ВИЧ — в развитии саркомы Капоши. Попадая в организм человека, вирусы активно взаимодействуют с его ДНК, что в некоторых случаях вызывает трансформацию собственных протоонкогенов человека в онкогены. Геном некоторых вирусов (ретровирусы) содержит высоко активные онкогены, активирующиеся после включения ДНК вируса в ДНК клеток человека.
Генеалогический
В основе этого метода лежит составление и анализ родословных. Этот метод широко применяют с древних времен и до наших дней в коневодстве, селекции ценных линий крупного рогатого скота и свиней, при получении чистопородных собак, а также при выведении новых пород пушных животных. Родословные человека составлялись на протяжении многих столетий в отношении царствующих семейств в Европе и Азии.
Как метод изучения генетики человека генеалогический метод стали применять только с начала XX столетия, когда выяснилось, что анализ родословных, в которых прослеживается передача из поколения в поколение какого-то признака (заболевания), может заменить собой фактически неприменимый в отношении человека гибридологический метод.
При составлении родословных исходным является человек — пробанд, родословную которого изучают. Обычно это или больной, или носитель определенного признака, наследование которого необходимо изучить. При составлении родословных таблиц используют условные обозначения, предложенные Г. Юстом в 1931 г. (рис. 6.24). Поколения обозначают римскими цифрами, индивидов в данном поколении — арабскими.
С помощью генеалогического метода может быть установлена наследственная обусловленность изучаемого признака, а также тип его наследования (аутосомнодоминантный, аутосомно-рецессивный, X-сцепленный доминантный или рецессивный, Y-сцепленный). При анализе родословных по нескольким признакам может быть выявлен сцепленный характер их наследования, что используют при составлении хромосомных карт. Этот метод позволяет изучать интенсивность мутационного процесса, оценить экспрессивность и пенетрантность аллеля. Он широко используется в медико-генетическом консультировании для прогнозирования потомства. Однако необходимо отметить, что генеалогический анализ существенно осложняется при малодетности семей.
Популяционно-статистический
С помощью популяционно-статистического метода изучают наследственные признаки в больших группах населения, в одном или нескольких поколениях. Существенным моментом при использовании этого метода является статистическая обработка получаемых данных. Этим методом можно рассчитать частоту встречаемости в популяции различных аллелей гена и разных генотипов по этим аллелям, выяснить распространение в ней различных наследственных признаков, в том числе заболеваний. Он позволяет изучать мутационный процесс, роль наследственности и среды в формировании фенотипического полиморфизма человека по нормальным признакам, а также в возникновении болезней, особенно с наследственной предрасположенностью. Этот метод используют и для выяснения значения генетических факторов в антропогенезе, в частности в расообразовании.
При статистической обработке материала, получаемого при обследовании группы населения по интересующему исследователя признаку, основой для выяснения генетической структуры популяции является закон генетического равновесия Харди — Вайнберга. Он отражает закономерность, в соответствии с которой при определенных условиях соотношение аллелей генов и генотипов в генофонде популяции сохраняется неизменным в ряду поколений этой популяции (см. разд. 10.2.3, т.2). На основании этого закона, имея данные о частоте встречаемости в популяции рецессивного фенотипа, обладающего гомозиготным генотипом (аа), можно рассчитать частоту встречаемости указанного аллеля (а) в генофонде данного поколения. Распространив эти сведения на ближайшие поколения, можно предсказать частоту появления в них людей с рецессивным признаком, а также гетерозиготных носителей рецессивного аллеля.
Математическим выражением закона Харди — Вайнберга служит формула (рА. + qa)2 , где р и q — частоты встречаемости аллелей А и а соответствующего гена. Раскрытие этой формулы дает возможность рассчитать частоту встречаемости людей с разным генотипом и в первую очередь гетерозигот — носителей скрытого рецессивного аллеля: p 2AA + 2pqAa + q2 аа. Например, альбинизм обусловлен отсутствием фермента, участвующего в образовании пигмента меланина и является наследственным рецессивным признаком. Частота встречаемости в популяции альбиносов (аа) равна 1:20 000. Следовательно, q 2 = 1/20 000, тогда q = 1/141, up = 140/141. В соответствии с формулой закона Харди — Вайнберга частота встречаемости гетерозигот = 2pq, т.е. соответствует 2 х (1/141) х (140/141) = 280/20000 = 1/70. Это означает, что в данной популяции гетерозиготные носители аллеля альбинизма встречаются с частотой один на 70 человек.
Анализ частот встречаемости разных признаков в популяции в случае их соответствия закону Харди — Вайнберга позволяет утверждать, что признаки обусловлены разными аллелями одного гена. Так, например, установлено, что в США 29,16% белого населения имеют группу крови М, 49,58%—группу MN, 21,26%—группу N. Эти частоты разных фенотипов соответствуют формуле p 2М + 2pqMN + q 2N. Следовательно, эти три варианта признака обусловлены сочетанием двух аллелей одного гена, взаимодействующих по типу кодоминирования: группа М — LmL m , группа N — LnL n , группа MN—LmL n.
В том случае, если ген в генофонде популяции представлен несколькими аллелями, например ген группы крови системы АВО, соотношение различных генотипов выражается формулой (pI A + qI B + rI 0 ) 2.
Близнецовый метод
Этот метод заключается в изучении закономерностей наследования признаков в парах одно- и двуяйцевых близнецов. Он предложен в 1875 г. Гальтоном первоначально для оценки роли наследственности и среды в развитии психических свойств человека. В настоящее время этот метод широко применяют в изучении наследственности и изменчивости у человека для определения соотносительной роли наследственности и среды в формировании различных признаков, как нормальных, так и патологических. Он позволяет выявить наследственный характер признака, определить пенетрантность аллеля, оценить эффективность действия на организм некоторых внешних факторов (лекарственных препаратов, обучения, воспитания).
Суть метода заключается в сравнении проявления признака в разных группах близнецов при учете сходства или различия их генотипов. Монозиготные близнецы, развивающиеся из одной оплодотворенной яйцеклетки, генетически идентичны, так как имеют 100% общих генов. Поэтому среди монозиготных близнецов наблюдается высокий процент конкордантных пар, в которых признак развивается у обоих близнецов. Сравнение монозиготных близнецов, воспитывающихся в разных условиях постэмбрионального периода, позволяет выявить признаки, в формировании которых существенная роль принадлежит факторам среды. По этим признакам между близнецами наблюдается дискордантность, т.е. различия. 281 Напротив, сохранение сходства между близнецами, несмотря на различия условий их существования, свидетельствует о наследственной обусловленности признака.
Сопоставление парной конкордантности по данному признаку у генетически идентичных монозиготных и дизиготных близнецов, которые имеют в среднем около 50% общих генов, дает возможность более объективно судить о роли генотипа в формировании признака. Высокая конкордантность в парах монозиготных близнецов и существенно более низкая конкордантность в парах дизиготных близнецов свидетельствуют о значении наследственных различий в этих парах для определения признака. Сходство показателя конкордантности у моно- и дизиготных близнецов свидетельствует о незначительной роли генетических различий и определяющей роли среды в формировании признака или развития заболевания. Достоверно различающиеся, но достаточно низкие показатели конкордантности в обеих группах близнецов дают возможность судить о наследственной предрасположенности к формированию признака, развивающегося под действием факторов среды.
Установление соотносительной роли наследственности и среды в развитии различных патологических состояний позволяет врачу правильно оценить ситуацию и проводить профилактические мероприятия при наследственной предрасположенности к заболеванию или осуществлять вспомогательную терапию при его наследственной обусловленности.
Трудности близнецового метода связаны, во-первых, с относительно низкой частотой рождения близнецов в популяции (1:86—1:88), что осложняет подбор достаточного количества пар с данным признаком; во-вторых, с идентификацией монозиготности близнецов, что имеет большое значение для получения достоверных выводов.
Для идентификации монозиготности близнецов применяют ряд методов. 1. Полисимптомный метод сравнения близнецов по многим морфологическим признакам (пигментации глаз, волос, кожи, форме волос и особенностям волосяного покрова на голове и теле, форме ушей, носа, губ, ногтей, тела, пальцевым узорам). 2. Методы, основанные на иммунологической идентичности близнецов по эритроцитарным антигенам (системы АВО, MN, резусу), по сывороточным белкам (γ-глобулину). 3. Наиболее достоверный критерий монозиготности предоставляет трансплантационный тест с применением перекрестной пересадки кожи близнецов.
Несмотря на трудоемкость близнецового метода и возможность ошибок при определении монозиготности близнецов, высокая объективность выводов делает его одним из широко применяемых методов генетических исследований у человека.
Цитогенетический метод
Цитогенетический метод основан на микроскопическом изучении хромосом в клетках человека. Его стали широко применять в исследованиях генетики человека с 1956 г., когда шведские ученые Дж. Тийо и А. Леван, предложив новую методику изучения хромосом, установили, что в кариотипе человека 46, а не 48 хромосом, как считали ранее.
Современный этап в применении цитогенетического метода связан с разработанным в 1969 г. Т. Касперсоном методом дифференциального окрашивания хромосом, который расширил -возможности цитогенетического анализа, позволив точно идентифицировать хромосомы по характеру распределения в них окрашиваемых сегментов (см. разд. 3.5.2.3).
Применение цитогенетического метода позволяет не только изучать нормальную морфологию хромосом и кариотипа в целом, определять генетический пол организма, но, главное, диагностировать различные хромосомные болезни, связанные с изменением числа хромосом или с нарушением их структуры. Кроме того, этот метод позволяет изучать процессы мутагенеза на уровне хромосом и кариотипа. Применение его в медико-генетическом консультировании для целей пренатальной диагностики хромосомных болезней дает возможность путем своевременного прерывания беременности предупредить появление потомства с грубыми нарушениями развития.
Материалом для цитогенетических исследований служат клетки человека, получаемые из разных тканей,—лимфоциты периферической крови, клетки костного мозга, фибробласты, клетки опухолей и эмбриональных тканей и др. Непременным требованием для изучения хромосом является наличие делящихся клеток. Непосредственное получение таких клеток из организма затруднено, поэтому чаще используют легкодоступный материал, каковым являются лимфоциты периферической крови.
В норме эти клетки не делятся, однако специальная обработка их культуры фитогемагглютинином возвращает их в митотический цикл. Накопление делящихся клеток в стадии метафазы, когда хромосомы максимально спирализованы и хорошо видны в микроскоп, достигается обработкой культуры колхицином или колцемидом, разрушающим веретено деления и препятствующим расхождению хроматид.
Микроскопирование мазков, приготовленных из культуры таких клеток, позволяет визуально наблюдать хромосомы. Фотографирование метафазных пластинок и последующая обработка фотографий с составлением кариограмм, в которых хромосомы выстроены парами и распределены по группам, позволяют установить общее число хромосом и обнаружить изменения их количества и структуры в отдельных парах (рис. 6.33). Кариотипы человека при некоторых хромосомных болезнях представлены на рис. 4.3—4.12.
В качестве экспресс-метода, выявляющего изменение числа половых хромосом, используют метод определения полового хроматина в неделящихся клетках слизистой оболочки щеки. Половой хроматин, или тельце Барра, образуется в клетках женского организма одной из двух Х-хромосом. Оно выглядит как интенсивно окрашенная глыбка, расположенная у ядерной оболочки (см. рис. 3.77). При увеличении количества Х-хромосом в кариотипе организма в его клетках образуются тельца Барра в количестве на единицу меньше числа Х-хромосом. При уменьшении числа Х-хромосом (моносомия X) тельце Барра отсутствует.
В мужском кариотипе Y-хромосома может быть обнаружена по более интенсивной по сравнению с другими хромосомами люминесценции при обработке их акрихинипритом и изучении в ультрафиолетовом свете.
Биохимический метод
В отличие от цитогенетического метода, который позволяет изучать структуру хромосом и кариотипа в норме и диагностировать наследственные болезни, связанные с изменением их числа и нарушением организации, наследственные заболевания, обусловленные генными мутациями, а также полиморфизм по нормальным первичным продуктам генов изучают с помощью биохимических методов.
Впервые эти методы стали применять для диагностики генных болезней еще в начале XX в. В последние 30 лет их широко используют в поиске новых форм мутантных аллелей. С их помощью описано более 1000 врожденных болезней обмена веществ. Для многих из них выявлен дефект первичного генного продукта. Наиболее распространенными среди таких заболеваний являются болезни, связанные с дефектностью ферментов, структурных, транспортных или иных белков.
Дефекты структурных и циркулирующих белков выявляются при изучении их строения. Так, в 60-х гг. XX в. был завершен анализ (3-глобино-вой цепи гемоглобина, состоящей из 146 аминокислотных остатков. Установлено большое разнообразие гемоглобинов у человека, связанное с изменением структуры его пептидных цепей, что нередко является причиной развития заболеваний (см. § 4.1).
Дефекты ферментов устанавливают путем определения содержания в крови и моче продуктов метаболизма, являющихся результатом функционирования данного белка. Дефицит конечного продукта, сопровождающийся накоплением промежуточных и побочных продуктов нарушенного метаболизма, свидетельствует о дефекте фермента или его дефиците в организме (см. § 4.1).
Биохимическую диагностику наследственных нарушений обмена проводят в два этапа. На первом этапе отбирают предположительные случаи заболеваний, на втором —более точными и сложными методами уточняют диагноз заболевания. Применение биохимических исследований для диагностики заболеваний в пренатальном периоде или непосредственно после рождения позволяет своевременно выявить патологию и начать специфические медицинские мероприятия, как, например, в случае фенилкетонурии.
Для определения содержания в крови, моче или амниотической жидкости промежуточных, побочных и конечных продуктов обмена кроме качественных реакций со специфическими реактивами на определенные вещества используют хроматографические методы исследования аминокислот и других соединений.
Первый закон
Менделя Мендель начал работу с постановки эксперимента по моногибридному скрещиванию, в котором родительские особи отличались друг от друга по одному изучаемому признаку. Для этого он взял горох, отличающийся по цвету семян. Гибридные семена первого поколения оказались все желтого цвета. Признак, появляющийся у гибридов первого поколения и подавляющий развитие другого признака, был назван доминантным, а противоположный признак, подавляемый, - рецессивным. В результате такого скрещивания была установлена закономерность наследования, названная законом единообразия гибридов первого поколения, или законом доминирования.
Второй закон
Менделя Из гибридных семян гороха Мендель вырастил растения, которые в результате самоопыления произвели семена второго поколения. Среди них оказались не только желтые, но и зеленые семена, т.е. произошло расщепление потомства на две группы, одна из которых обладала доминантным признаком, а вторая – рецессивным. Это расщепление подчиняется строгим количественным закономерностям: ¾ семян оказались желтыми ¼ - зелеными Таким образом, Мендель установил, что во втором поколении гибридов появляются особи с доминантными и рецессивными признаками, причем их соотношение 3:1. Эта закономерность была названа законом расщепления.
Закон чистоты гамет
Мендель предположил, что каждая клетка организма содержит по два наследственных фактора, причем при образовании гибридов эти факторы не смешиваются, а сохраняются в неизменном виде. При половом размножении связь между поколениями осуществляется через половые клетки – гаметы. Поэтому Мендель предположил, что каждая гамета должна содержать только один фактор из пары, чтобы при их слиянии восстанавливался двойной набор. Мендель сделал выводы, что наследственные факторы в гибриде не смешиваются и передаются гаметам в «чистом» виде. В этом и состоит смысл закона чистоты гамет: при образовании половых клеток в каждую гамету попадает только один аллель из каждой пары. Третий закон Менделя
В природе организмы редко отличаются друг от друга только по одному признаку, поэтому Мендель решил исследовать, как ведут себя в ряду поколений несколько признаков одновременно. Скрещивание, при котором прослеживается наследование двух пар альтернативных признаков, называют дигибридным. Для этого эксперимента он взял два сорта гороха, один из которых имел желтые и гладкие семена, а другой - зеленые и морщинистые. Дигибридное скрещивание представляет собой два независимо идущих моногибридных скрещивания, результаты которых как бы накладываются друг на друга.
Полученные результаты дигибридных скрещиваний позволили Менделю сформулировать закон независимого наследования: при скрещивании двух гомозиготных особей, отличающихся по двум и более парам альтернативных признаков, гены и соответствующие им признаки передаются потомству независимо друг от друга и комбинируются во всех возможных сочетаниях.
Происхождение паразитизма.
Явление паразитизма, как и любой другой экологический феномен, возникло разными путями. С одной стороны, по-разному развиваются взаимные адаптации паразитов и хозяев в разных систематических группах организмов — классах и типах, с другой — различны направления эволюции, ведущие к возникновению разнообразных форм паразитизма.
Первый подход к исследованию происхождения паразитизма конкретен. Он рассматривается при изложении материала по частной паразитологии в разделах, посвященных описанию характеристик типов и классов паразитических организмов и их экологических групп. Второй подход вскрывает общие закономерности перехода к паразитическому существованию вне зависимости от систематического положения организмов, занимающих новые экологические ниши.
Наиболее просто объясняется происхождение эктопаразитизма. Один из путей к этому — через увеличение количества источников питания с последующей их сменой. Так, многие насекомые имеют колюще-сосущий ротовой аппарат, питаясь соками растений. Но питание за счет прокалывания ткани и всасывания жидкости и есть способ поглощения пищи всеми кровососущими членистоногими, ряд которых, потребляя кровь человека и теплокровных животных, продолжает пользоваться также и соками растений.
Другой путь, ведущий к эктопаразитизму, — хищничество. Активные хищники, осваивающие для питания все более крупные жертвы, становятся вначале временными, а затем и постоянными эктопаразитами за счет удлинения контактов с организмом хозяина. Так, многие пиявки, ведущие себя как хищники по отношению к мелким организмам, становятся паразитами более крупных животных, питаясь их кровью. Увеличение продолжительности питания — основное направление перехода от временного к постоянному эктопаразитизму. Действительно, из большого количества кровососущих форм членистоногих наиболее длительное питание на хозяине характерно именно для постоянных паразитов, степень контакта которых с хозяевами наиболее высока.
Иной путь возникновения эктопаразитизма — через усиление контакта так называемых гнездовых паразитов с поверхностью тела хозяина. Животные, обитающие в убежище другого вида, могут питаться его перьями, волосами и отпадающими чешуйками кожного эпидермиса. Переход к постоянному обитанию на поверхности тела хозяина дает паразиту большие преимущества. Возможно, так возник паразитизм пухоедов, власоедов птиц и млекопитающих и группы клещей — обитателей эпидермиса животных и человека.
Основная масса случаев эндопаразитизма в полостных органах, имеющих связь с внешней средой, представляет собой явление, развившееся в результате случайного заноса в организм цист, яиц или личинок свободноживущих видов, предварительно имеющих адаптации к обитанию в почве или в воде, содержащей избыток органического вещества. Примером является угрица кишечная, которая в своем развитии сохранила возможность обитать и размножаться как в почве, так и в организме человека (см. разд. 20.2.1.1).
Возможен переход к паразитированию в одном хозяине после предварительной адаптации к обитанию в другом, служащем источником питания первого. Так, известен целый ряд гельминтов, которые, обитая в кишечнике рыбы, не перевариваются в пищеварительной системе хищников, съевших паразитов вместе с хозяином и продолжающих паразитировать в кишечнике или тканях уже нового вида (см. разд. 20.1.2.1).
Не исключается и вариант перехода к полостному паразитизму видов, предварительно адаптированных к эктопаразитизму. Этим путем, вероятно, эволюционируют некоторые насекомые, большую часть цикла развития проводящие в ротовой полости птиц, но выходящие для размножения на перьевой покров их головы.
Наиболее сложно и многообразно происхождение паразитов тканей внутренней среды. Один из путей — через изменение инстинкта откладки яиц и предварительных адаптации к эктопаразитизму. Таким путем, вероятно, произошел тканевой паразитизм личинок мух и оводов (см. разд. 21.2.4), откладывающих яйца на поверхности кожи и слизистых оболочек животных и человека. Личинки при этом вскоре погружаются под покровы и ведут типичный эндопаразитический образ жизни.
Многие паразиты приспособились к обитанию в тканях после освоения полостных органов, связанных с внешней средой. Так, по-видимому, шла эволюция паразитизма у ленточных червей, у трихинеллы спиральной (см. разд. 20.2.1.2). В цикле развития этих паразитов имеются формы, обитающие как в кишечнике, так и в тканях.
Некоторые паразиты внутренней среды возникли, вероятно, предварительно адаптировавшись к обитанию в пищеварительной системе членистоногих, а с переходом последних к гематофагии заселили новую и труднодоступную экологическую нишу — кровь и другие ткани мезодермального происхождения.
Таким образом, путей перехода к паразитизму у разных видов животных много, но несомненным остается одно: паразитизм — явление вторичное. Об этом свидетельствует наличие в жизненных циклах многих, даже наиболее специализированных паразитов, свободноживущих стадий, рекапитулирующих свободный образ жизни предков (см., например, разд. 20.1.1).
Внутренние паразиты делятся на:
1. Плоские черви — ленточные цестоды (цепни, лентец), трематоды-сосальщики.
2. Круглые черви — острицы, аскариды, стронгилоиды, трихинеллы, анкилостомиды.
3. Грибки-микозы — пенициллиумы, кандиды, криптококки.
4. Простейшие — амебы, лямблии, трихомонады.
5. Бактериозы — лептоспиры, стафилококки, шигелла.
По биолого-эпидемиологическим признакам различают:
1. Геогельминтов, для которых человеческий организм является средой обитания на определенной стадии их развития. Как правило, такие формы могут паразитировать внутри человека, но на определенной стадии дальнейшее их развитие проходит вне человеческого организма на других живых или неживых объектах.
2. Контактные гельминты, которые выделяются из организма на стадии зрелости, в результате чего может происходить дальнейшее заражение паразитами других живых организмов контактным способом.
3. Биогельминты. Цикл развития данного вида паразитов может происходить в любом живом организме. К примеру, человек может быть, как промежуточным звеном, так и конечным хозяином, то есть развитие паразитических организмов происходит до стадии половой зрелости паразитов с последующим их размножением.
По распространению различают:
- убиквитарных, которые встречаются везде;
- тропических, которые распространены в регионах с теплым, тропическим климатом.
Закон Харди-Вайнберга.
Ярыгин. Часть 2. Параграф 10.2.3.
128. Популяционные волны. Изоляция. Естественный отбор.
Ярыгин. Часть 2. Параграф 11.2-4 и 12.2.2-3,5
129. Генетико-автоматические процессы (дрейф генов).
Ярыгин. Часть 2. Параграф 11.5
130. Действие элементарных эволюционных факторов в популяциях человека.
Ярыгин. Часть 2. Параграф 12.2.2-5
СПИСОК
вопросов к курсовому экзамену по биологии
Дата: 2019-07-31, просмотров: 599.