Теплоемкость тела(системы) численно равна количеству теплоты, которое необходимо сообщить телу, чтобы изменить его температуру на 1 К.
С=𝛿𝑄/𝑑𝑇
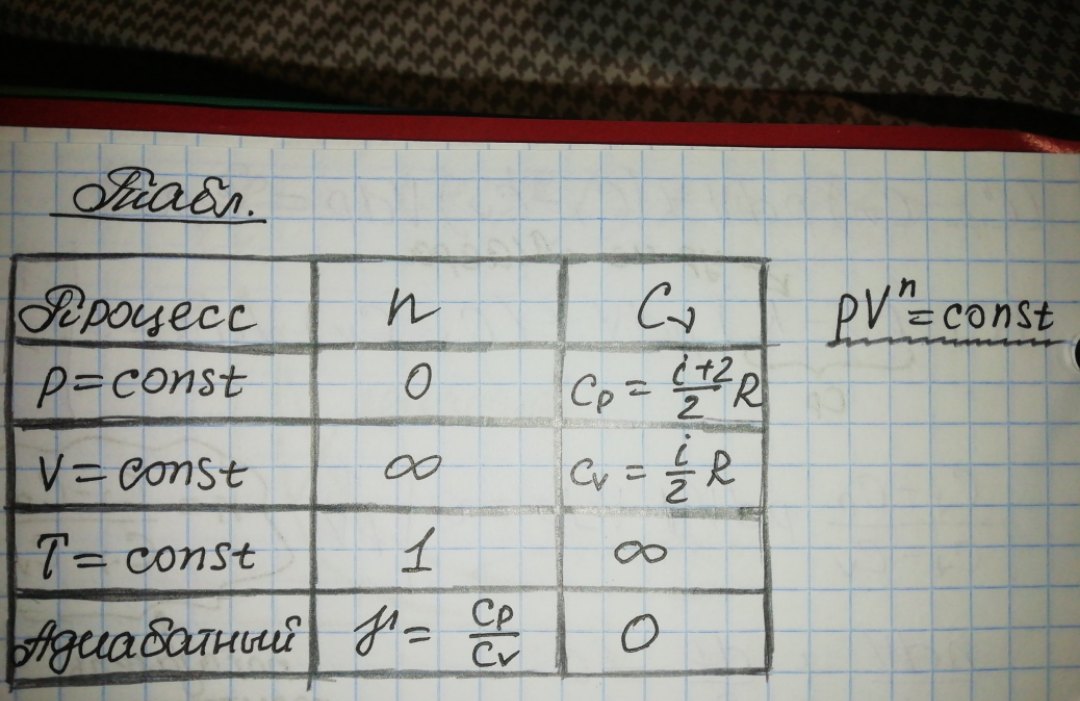
Процесс, в котором теплоемкость вещества не изменяется, называется политропным.
𝑝𝑉𝑛=𝑐𝑜𝑛𝑠𝑡

30. Обратимые и необратимые процессы. Тепловая машина и ее термический коэффициент полезного действия. 

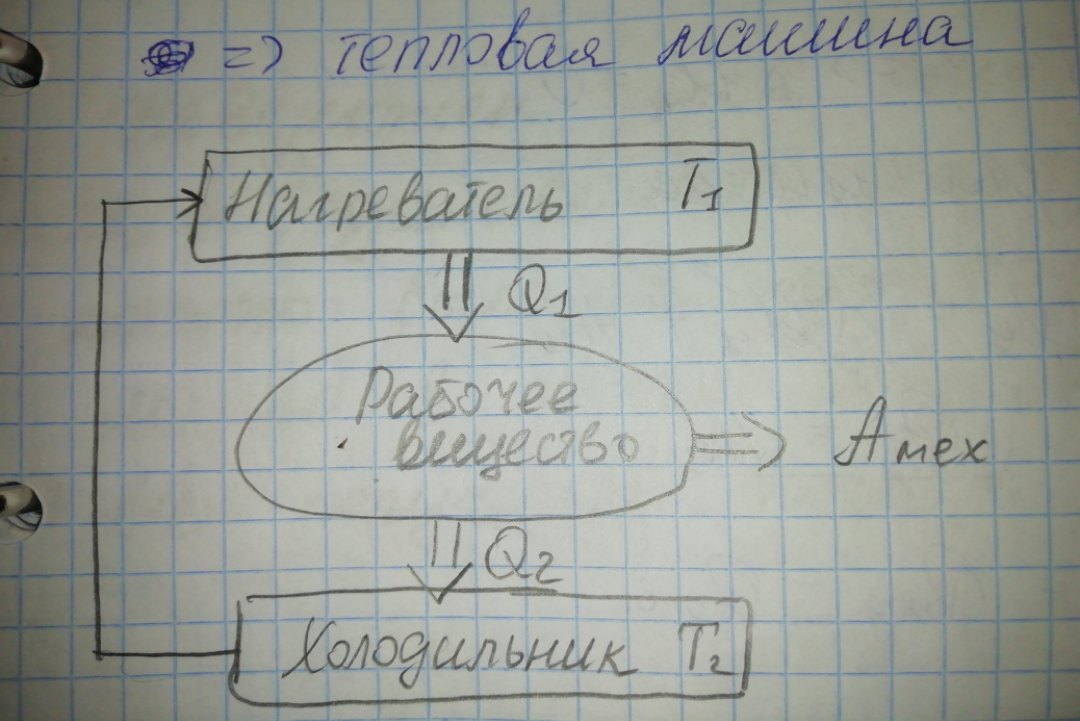

Второе начало термодинамики. Его различные формулировки.

Энтропия. Основные свойства энтропии. Формулировка второго начала термодинамики через энтропию.


33. Цикл Карно. Термический коэффициент полезного действия цикла Карно. 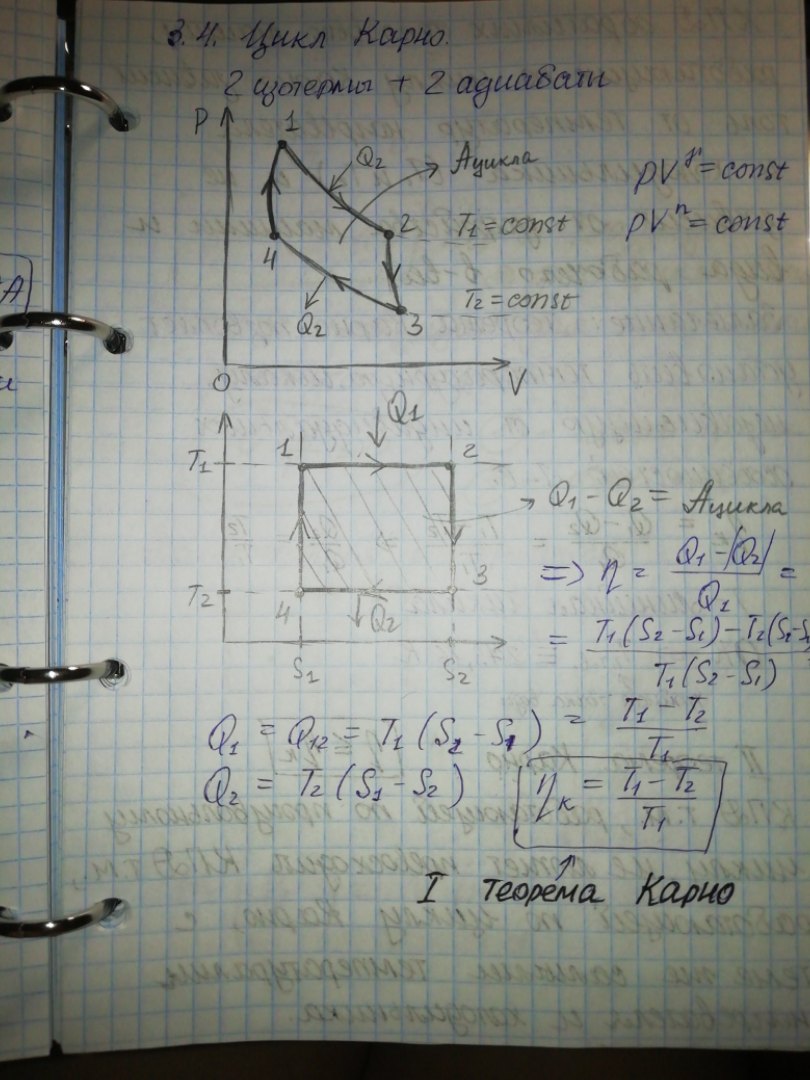
Понятие эффективного диаметра молекулы и эффективного сечения процесса столкновений. Среднее число столкновений одной молекулы газа в единицу времени. Средняя длина свободного пробега молекулы и ее зависимость от давления и температуры.
Эффективный диаметр молекулы - среднее расстояние между центрами молекул, на которое две молекулы сближаются при их столкновении.
Эффективное сечение столкновения - площадь поперечного сечения “коридора”, в который должны попасть центры соседних молекул, чтобы столкнуться с данной. 𝑆эфф=𝜋𝐷2эфф=4𝜋𝑅2
Среднее число столкновений одной молекулы газа в единицу времени.𝑁=𝑛〈𝑣〉𝑆эфф Средняя длина свободного пробега – расстояние, которое она пролетает между двумя последовательными соударениями.〈𝑙〉=〈𝑣〉𝜏=1/𝑛𝑆эфф ; 〈𝑙〉=𝑘𝑇/ 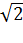 *4𝑝𝑅𝜋
*4𝑝𝑅𝜋
Явления переноса в газах. Закон Фика. Коэффициент диффузии. Закон Фурье. Коэффициент теплопроводности. Закон Ньютона для внутреннего трения. Коэффициент вязкости.
Явление переноса-явления, происходящие при нарушении равновесного состояния систем.
Закон Фика плотность диффузионного потока частиц пропорциональна градиенту концентрации частиц=−𝐷*(𝑑𝑛/𝑑𝑥)
Коэффициент диффузии 𝐷=(1/3)*〈𝑙〉〈𝑣〉
Закон теплопроводности Фурье: плотность теплового потока при теплопроводности пропорциональна градиенту температуры в системе. 𝑞=−𝜆*(𝑑𝑇/𝑑𝑥)
Коэффициент теплопроводности 𝜆=(1/3)*〈𝑙〉〈𝑣〉𝑐𝑣𝜌
Закон Ньютона для внутреннего трения определяет численные значения двух противоположно направленных сил, с которыми соседние слои молекул действуют друг на друга. 𝐹=𝜂*(𝑑𝑣/𝑑𝑧)*𝑑𝑆
Коэффициент динамической вязкости 𝜂=(1/3)*𝜌〈𝑙〉〈𝑣〉
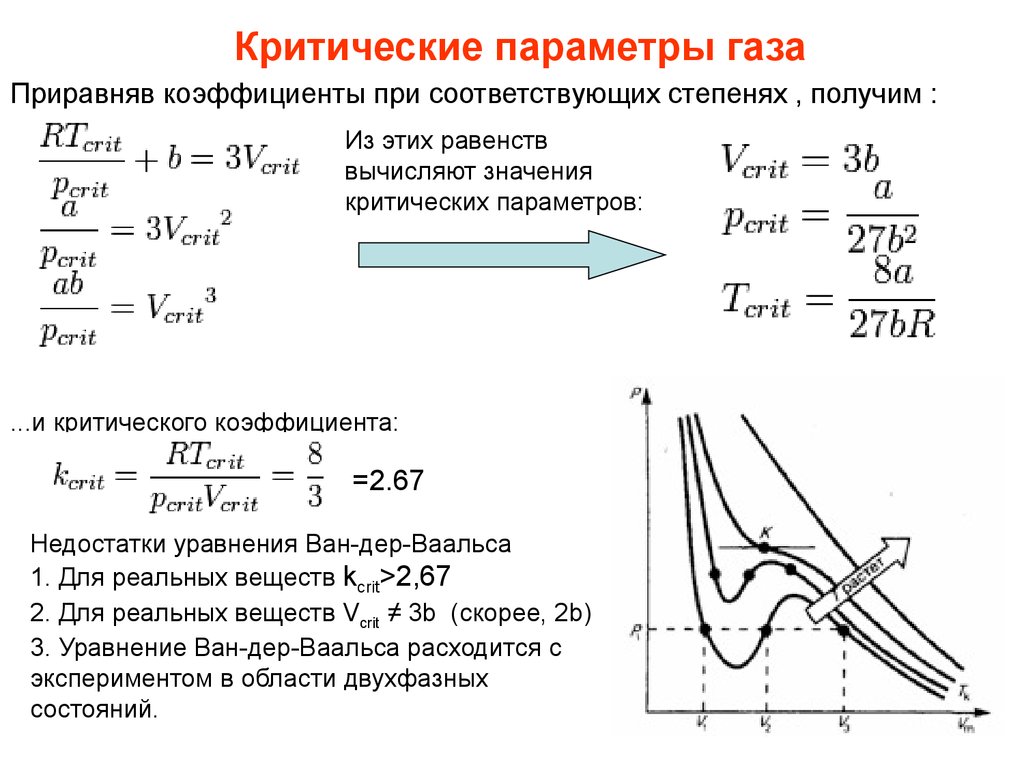
Реальные газы. Уравнение Ван-дер-Ваальса. Изотермы реального газа (теоретические и экспериментальные). Критические параметры реального газа.
Реальный газ-газ, который не описывается уравнением состояния идеального газа Менделеева-Клайперона(𝑝+(𝑎/𝑉2))∗(𝑉−𝑏)=𝑅𝑇,где p-давление, оказываемое на газ извне (равное давлению газа на стенки сосуда), a и b – постоянные Ван-дер-Ваальса, имеющие для разных газов различные значения, определяемые экспериментально.
Дата: 2019-07-30, просмотров: 512.