Основные процессы, которые поставляют и запасают энергию в клетках, могут быть в общей форме изображены следующим образом:
глюкоза пируват ® ацетил-СоА жирные кислоты
AДФ
АТФ
С02
Регуляция этой системы inter alia должна гарантировать постоянное поступление АТФ соразмерно с существующими в данный момент энергетическими потребностями, обеспечивать превращение избытка углеводов в жирные кислоты через пируват и ацетил-СоА и наряду с этим контролировать экономное расходование жирных кислот через ацетил-СоА как ключевой продукт для входа в цикл лимонной кислоты.
Цикл лимонной кислоты поставляет электроны в электронпереносящую систему, в которой поток электронов сопряжен с синтезом АТФ и в меньшей степени снабжает восстановительными эквивалентами системы биосинтеза промежуточных продуктов. В принципе цикл не может протекать быстрее, чем это позволяет использование образуемой АТФ. Если бы весь AДФ клетки превратился в АТФ , не могло бы быть никакого дальнейшего потока электронов от НАДH, который накапливается, к 02. Ввиду отсутствия НAД+, необходимого участника процессов дегидрирования цикла, последний перестал бы функционировать. Существуют более тонкие регуляторные приспособления, которые модулируют действие ферментов в самом цикле лимонной кислоты.
Сукцинатдегидрогеназа находится во внутренней митохондриальной мембране. Все остальные ферменты растворены в матриксе, заполняющем внутреннее пространство митохондрии. Измерения относительных количеств этих ферментов и концентраций их субстратов в митохондриях указывают, что каждая реакция протекает с одинаковой скоростью. Как только пируват (или другой потенциальный источник ацетил-СоА) поступает внутрь матрикса митохондрии, весь цикл протекает внутри этого отсека.
В некоторых участках стимуляция или ингибирование определяется относительными концентрациями НAДH/НAД, ATФ/AДФ или АМФ, ацетил-СоА/СоА или сукцинил-СоА/СоА. Когда эти отношения высоки, клетка достаточно обеспечена энергией и поток через цикл замедлен; когда же они низки, клетка испытывает потребность в энергии, и поток через цикл ускоряется.
Как необратимая реакция, соединяющая метаболизм углеводов с циклом лимонной кислоты, пируватдегидрогеназная реакция должна хорошо контролироваться. Это достигается двумя способами. Во-первых, фермент, который активируется несколькими интермедиаторами гликолиза, конкурентно ингибируется своими собственными продуктами - НAДH и ацетил-СоА. При прочих равных условиях увеличение соотношения НAДH/НAД+ от 1 до 3 вызывает 90%-е снижение скорости реакции, а увеличение отношения ацетил-СоА/СоА приводит к количественно подобному эффекту. Эффект проявляется мгновенно. Медленнее возникают, но дольше действуют эффекты другого регуляторного устройства. С сердцевиной каждой молекулы дигидролипоилтрансацетилазы связано около пяти молекул киназы пируватдегидрогеназы, которая за счет АТФ катализирует фосфорилирование серинового остатка в a-цепи пируватдегидрогеназного компонента. Будучи фосфорилирован, фермент не способен декарбоксилировать пируват.
Когда происходит окисление жирных кислот, пируватдегидрогеназа заметно ингибируется. По-видимому, это явление объясняется сопутствующими процессу окисления высокими концентрациями АТФ, ацетил-СоА и НAДH. Большинство тканей содержат избыток пируватдегидрогеназы, так что после приема корма в печени, а также в мышце и в жировой ткани у животных в состоянии покоя лишь 40, 15 и 10% пируватдегидрогеназы соответственно находится в активной, нефосфорилированной форме. Когда возрастает потребность в АТФ, концентрации НAД+, СоА и AДФ возрастают за счет использования НAДH, ацетил-СоА и АТФ, а киназа инактивируется. Однако фосфатаза продолжает функционировать вновь активируя дегидрогеназу. Повышение Са2+ может активировать митохондриальную фосфатазу.
Синтез цитрата - стадия, лимитирующая скорость цикла лимонной кислоты. Регуляция этой стадии совершается благодаря небольшому, но достаточно значимому ингибированию цитрат-синтетазы посредством НAДH и сукцинил-СоА. Основное же влияние на скорость синтеза цитрата оказывает поступление субстрата.
Активность изоцитратдегидрогеназы регулируется в зависимости от концентраций Mg2+, изоцитрата, НAД+, НAДH и АМФ. Кроме субстратсвязывающих центров для НAД+, изоцитрата и Mg2+ фермент имеет еще и положительные, и отрицательные эффекторные участки. Изоцитрат - положительный эффектор; его связывание кооперативно, т. е. связывание на каком-либо одном участке облегчает связывание на других. Оба участка связывания для АМР стимулируют активность фермента.
Таким образом, ферментная активность определяется отношениями НAД+/НAДH и АМФ/АТФ.
АМФ - положительный эффектор комплекса a-кетоглутаратде-гидрогеназы, который в этом отношении напоминает изоцитратдегидрогеназу. В области физиологических концентраций и сукцинил-СоА, и НAДH обладают ингибирующим действием, причем концентрация сукцинил-СоА, по-видимому, главный фактор, управляющий скоростью процесса. Сукцинатдегидрогеназа напоминает изоцитратдегидрогеназу в том отношении, что субстрат (сукцинат) выполняет функцию положительного аллостерического эффектора. Оксалоацетат - мощный ингибитор, однако неясно, действует ли этот контроль в нормальных условиях.[5,2000]
В цикле лимонной кислоты выполняют специфические функции четыре водорастворимых витамина группы В. Рибофлавин входит в состав ФАД, который является кофактором альфакетоглутаратдегидрогеназного комплекса и сукцинатдегидрогеназы. Ниацин входит в состав НАД, который является коферментом трех дегидрогеназ цикла: изоцитратдегидрогеназы, альфакетоглуторатдегидрогеназы и малатдегидрогеназы. Тиамин (витамин В1) входит в состав тиаминдифосфата, который является коферментом альфакетоглутаратдегидрогеназы. Пантотеновая кислота входит в состав кофермента А, который является кофактором, связывающим активные ацильные остатки.
Макроэргические соединения и макроэргические связи.
В клетках, освобождающаяся в результате катаболических процессов распада питательных веществ, свободная энергия может быть использована для осуществления многих химических реакций, протекающих с затратой энергии. Запасание энергии происходит в виде богатых энергией химических связей особого класса соединений, большинство из которых являются ангидридами фосфорной кислоты (нуклеозидтрифосфаты).
Существуют высокоэнергетические и низкоэнергетические фосфаты. Условной границей для этих двух групп соединений является величина свободной энергии гидролиза фосфатной связи. Следовательно, высокоэнергетические фосфаты имеют богатую энергией высокоэргическую (макроэргическую) связь.
Энергию связи определяют как разницу свободных энергий соединений, содержащего эту связь, и соединений, получающихся после ее разрыва. Макроэргическими (богатыми энергией) принято считать те связи, при гидролизе которых изменения свободной энергии системы составляют более 21 кДж/моль.
Центральную роль в энергообмене клеток всех типов осуществляет система адениновых нуклеотидов, которая включает в себя АТФ, АДФ и АМФ, а также неорганический фосфат и ионы магния. АТФ является термодинамически неустойчивой молекулой и гидролизуется с образованием АДФ и АМФ. Именно эта неустойчивость позволяет АТФ выполнять функцию переносчика химической энергии, необходимой для удовлетворения большей части энергетических потребностей клеток. К соединениям, обладающим богатой энергией связью, помимо АТФ, относится также УТФ, ЦТФ, ГТФ, ТТФ, креатинфосфат, пирофосфат, некоторые тиоэфиры (например, ацетил-КоА), фосфоенолпируват, 1,3-бифосфоглицерат и ряд других соединений.
При гидролизе АТФ в стандартных условиях изменение свободной энергии составляет -30,4 кДж/моль. В физиологических условиях реальная свободная энергия гидролиза концевой фосфатной связи АТФ будет иная и приближается к -50,0 кДж/моль.
Возможно несколько вариантов освобождения энергии фосфатных связей АТФ. Основной вариант - это отщепление концевого фосфата АТФ (АТФ+Н2О ®АДФ+Н3РО4). Другой вариант - пирофосфатное расщепление АТФ (АТФ+Н20 ®АМФ+Н4Р2О7). Этот тип реакции значительно реже используется в биохимических процессах.
Накопление энергии в специфических фосфатных связях АТФ лежит в основе механизма переноса энергии в живой клетке. Есть основания считать, что в клетке существуют три основных типа перехода энергии АТФ:
в энергию химических связей, в тепловую энергию и энергию, затрачиваемую на совершение работы (осмотической, электрической, механической и др.).[15,1997]
Витамин PP .
Витамин РР (никотиновая кислота, никотинамид, ниацин) называют антипеллагрическим витамином (от итал. Preventive pellagra – «предотвращающий пеллагру»), поскольку его отсутствие является причиной заболевания, называемого пеллагрой.
Никотиновая кислота известна давно, однако только в 1937 году она была выделена К. Эльвегеймом из экстракта печени и было показано, что введение никотиновой кислоты (или ее амида - никотинамида) или препаратов печени предохраняет от развития или излечивает от пеллагры.
Никотиновая кислота представляет собой соединение пиридинового ряда, содержащее карбоксильную группу (никотинамид отличается наличием амидной группы).
Витамин РР мало растворим в воде (порядка 1%), но хорошо растворим в водных растворах щелочей. Никотиновая кислота кристаллизуется в виде белых игл.
Наиболее характерными признаками пеллагры (от итал. pelle agra -шершавая кожа), являются поражения кожи (дерматиты), желудочно-кишечного тракта (диарея) и нарушения нервной деятельности (деменция).
Дерматиты чаще всего симметричны и поражают те участки кожи, которые подвержены влиянию прямых солнечных лучей: тыльную поверхность кистей рук, шею, лицо; кожа становится красной, затем коричневой и шершавой. Поражения кишечника выражаются в развитии анарексии, тошноты и болей в области живота, поноса. Диарея приводит к обезвоживанию организма. Слизистая оболочка толстого кишечника сначала воспаляется, затем изъязвляется. Специфичными для пеллагры являются стоматиты, гингивиты, поражения языка со вздутием и трещинами. Поражения мозга выражаются в головных болях, головокружениях, повышенной раздражимости, депрессии и других симптомах, включая психозы, психоневрозы, галлюцинации и другие. Симптомы пеллагры особенно резко выражены у больных с недостаточным белковым питанием. Установлено, что это объясняется недостатком триптофана, который является предшественником никотинамида, частично синтезируемого в тканях человека и животных, а также недостатком ряда других витаминов.
Витамин РР играет роль кофермента в НАД-зависимых дегидрогеназах (участниках тканевого дыхания), метаболизме углеводов и аминокислот, НАДФ-зависимых ферментах (пентозного шунта и синтеза липидов), НМН-зависимых энзимах (алкогольдегидрогеназа и маликфермент). Не менее важна роль его, как субстрата поли-АДФ-рибозилирования. Данный процесс участвует в сшивке хромосомных разрывов и в работе репаразной системы, а также имеет (при нехватке НАД) ключевое значение в механизме некробиоза и апоптоза клеток, особенно – высокоаэробных.[6,2000]
Показано, что ряд дегидрогеназ используют только НАД или НАДФ, другие могут катализировать окислительно-восстановительные реакции в присутствии любого из них. В процессе биологического окисления НАД и НАДФ выполняют роль промежуточных переносчиков электронов и протонов между окисляемым субстратом и флавиновыми ферментами.
Основными источниками никотиновой кислоты и ее амида являются рис, хлеб, картофель, мясо, печень, почки, морковь и другие продукты.[18,1989]
Микросомальное окисление.
Монооксигеназные реакции.
Живые организмы содержат группу многочисленных и разнообразных ферментов, получивших название монооксигеназ. В типичном случае один атом кислородной молекулы обнаруживается в новой гидроксидной группе субстрата, другой – восстанавливается до воды в процессе реакции. В соответствии с этим реакция должна протекать при участии фермента, субстрата, кислородаи какого-либо восстанавливающего агента.
Допамин-b-монооксигеназа, присутствующая в мозге и в хромаффинной ткани, катализирует гидроксилирование 3,4-диоксифенилэтиламина до норадреналина.
Фенолмонооксигеназы имеются у бактерий, растений, насекомых, а также в печени и коже млекопитающих. Полимеризация о-хинона, образовавшегося в результате цепочки реакции, катализируемых этими ферментами, лежит в основе образования меланина.[7,2000]
Диоксигеназные реакции.
Ферменты, катализирующие реакции, в которых оба атома молекулярного кислорода встраиваются в продукты реакции, называются диоксигеназами. Известные в настоящее время ферменты этой группы могут содержать в качестве активной группы гем или негемовое железо, а для действия некоторых необходим a-кетоглутарат.
Железо-a-кетоглутаратдиоксигеназы – железозависимые ферменты, катализирующие гидроксилирование субстрата в ходе процесса, в котором a-кетоглутарат подвергается окислительному декарбоксилированию до сукцината: М + О2 + a-кетоглутарат 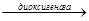 М-ОН + сукцинат + СО2 [5,2000]
М-ОН + сукцинат + СО2 [5,2000]
Цитохромы – ферменты редокс-цепи.
Дальнейший перенос электронов от КоQН2 на О2 осуществляет система цитохромов. Данная система состоит из ряда гемсодержащих белков (гемпротеинов), открытых в 1886 году К. Мак-Мунном. Все они имеют простетическую геминовую группу, близкую к гему гемоглобина. Цитохромы отличаются друг от друга не только простетической группой, но и белковыми компонентами. Все цитохромы, особенно в восстановленной форме, имеют характерные спектры поглощения, величины окислительно-восстановительных потенциалов также неодинаковы.
В имеющем широкое распространение механизме гидроксилирования путем введения одного атома кислорода функциональный атом железа находится в гемовой группе цитохрома – цитохрома Р450. Эти цитохромы обнаруживаются в мембранах печеночной ЭПС, в митохондриях коры надпочечников, в почечной щеточной кайме и в плазматических мембранах различных бактерий. Катализируемая реакция такая же, как у всех других монооксигеназ.
МН + О2 + 2е + 2Н+ ®МОН + Н2О
Цитохромы Р450 из печени относятся к числу индуцируемых ферментов; это означает, что количество присутствующего фермента может увеличиваться в 25 раз при введении одного из многочисленных чужеродных соединений, например фенобарбитала или метилхолантрена. Цитохромы обезвреживают ксенобиотики, а также лимитируют время, в течение которого могут сохранять свою активность некоторые наркотики. Лечение некоторых форм острой интоксикации может быть облегчено введением индуктора, который в этом случае вообще безвреден.
Цитохромы Р450 коры надпочечников находятся в митохондриальной мембране, где два отдельных фермента катализируют соответственно расщепление боковых цепей холестерина до прегненолона и реакции гидроксилирования различных стероидов.[2,1994]
Цитохром Р450 катализирует образование гидроксильных групп при синтезе желчных кислот, стероидных гормонов, при катаболизме ряда веществ и обмене чужеродных соединений.
Первая, обнаруженная в микросомах электронпереносящая система – это система восстановления цитохрома b5 за счет NADH; цитохром b5 восстанавливается NADH-цитохром b5-редуктазой, содержащей на молекуле один FAD, который совершает циклические переходы между полностью восстановленной и окисленной формами. Цитохром b5 прочно связан с ЭПС своей обширной гидрофобной областью. Хотя наружная поверхность области цитохрома, где находится гем, гидрофильна, она лежит в глубокой гидрофобной щели, причем карбоксильные группы пропионовой кислоты ориентированы наружу. Восстановленный цитохром b5 медленно самоокисляется с образованием супероксидного аниона. Этот механизм может быть основным генератором супероксида в клетках печени.[11,1989]
Дата: 2019-07-24, просмотров: 328.