Существуют следующие сульфидные фазы иттрия YS, Y5S7, d-Y2S3, γ‑Y2S3, YS2.
Результаты изучения кристаллохимических характеристик и некоторых физических свойств сульфидов собраны в табл.1. Данные по диаграмме состояния системы Y-S не обнаружены.
Предложение о фазовой диаграмме состояния можно сделать на основе кристаллохимических данных, имеющихся по системе Y-S. Моносульфид YS кристаллизуется в структурном типе NaCl. На основе YS существует дефектный твердый раствор типа вычитания серы до состава YS0,75 (Y4S3), при этом период решетки a уменьшается от 5,493 (YS) до 5,442 A° (Y4S3).
Соединение Y5S7 содержит две формульные единицы в элементарной ячейке. Полуторный сульфид d-Y2S3 кристаллизуется в структурном типе моноклинного Ho2S3 с 6 формульными единицами в ячейке. В ячейке дисульфида (полисульфида) иттрия содержится. 8 формульных единиц YS2.
Тетрагональный YS2 существует при температуре выше 500°C в интервале давлений 15-35 кбар. Кубический же YS2 образуется в интервале давлений 35-70 кбар.
Стехиометрический дисульфид иттрия даже в условиях высоких давлений и температур (500-1200°C) не существует.
1.1.3. Кристаллохимическая характеристика фаз в системе Mg-S, Y‑S.
Табл.1 Кристаллохимические свойства сульфидов иттрия и магния.
| Формула | Цвет | Сингония | Пространственная группа | Структурный тип | Период решетки, Å | Плотность г/см3 | |||
| a | b | c | пинкном | рентген | |||||
| MgS | Бесц. | кубическая | Fm3m | NaCl | 5,191 | 2,79 | |||
| YS | Рубиново красный | кубическая | Fm3m | NaCl | 5,477 5,493 5,495 | 4,51 | 4,92 | ||
| Y5S7 | Сине-черный | моноклинная | C2/m | Y5S7 | 12,67 12,768 | 3,81 3,803 | 11,45 11,550 | 4,19 4,10 | 4,18 4,09 |
| d-Y2S3 | Желтый | моноклинная | P2/m | d-Ho2S3 | 10,17 | 4,02 | 17,47 | 3,87 | 3,87 |
| γ- Y2S3 | Кубическая | Y4 3d | Th3P4 | 8,306 | |||||
| YS2 | коричнево-фиолетовый от темно серого до черного | тетрагональная кубическая | YS2 LaS2 | 7,71 7,72 7,797 | 4,25 3,6 3,9 | 4,35 4,35 4,32 | |||
Результаты изучения кристаллографических характеристик сульфидных фаз иттрия YS, Y5S7, d- Y2S3, g- Y2S3, YS2 собраны в табл.1. Сульфиды иттрия различного фазового состава можно получить как непосредственным синтезом из элементов, так и при реакции взаимодействия сероводорода с хлоридом или сероуглерода с полуторным окислом..Ито с сотрудниками, используя технику высоких давлений и температур, синтезировал непосредственно из компонентов g- Y2S3 в течение 3 мин. при давлении 70 кбар и температуре 10000С.
Моносульфид YS кристаллизуется в структурном типе NaCl, это подтверждает сравнение экспериментальных и вычисленных интенсивностей отражений. На основе YS существует дефектный твердый раствор типа вычитания серы до состава YS0,75 (Y4S3), при этом период решетки a уменьшается от 5,493 (YS) до 5,442 Å (Y4S3). Соединение Y5S7 содержит две формульные единицы в элементарной ячейке, размер которой и пространственная группа моноклинной сингонии определены на монокристалле.
Полуторный сульфид d- Y2S3 кристаллизируется в структурном типе моноклинного Ho2S3 c 6 формульными единицами в ячейке. В ячейке дисульфида (полисульфида) иттрия содержится 8 формульных единиц YS2. Рентгенограмма близка к кубическому дисульфиду церия, но содержит ряд дополнительных линий слабой интенсивности, которые укладываются в квадратичную форму для тетрагональной решетки. Тетрагональный YS2 существует при температуре свыше 5000С в интервале давлений ~ 15-35 кбар. “Кубический” же YS2 образуется в интервале давлений 35-70 кбар. Более хорошее согласие между рентгеновской экспериментальной плотностью для состава YS1,7 нежели для YS2 позволяет предположить, что стехиометрический дисульфид иттрия даже в условиях высоких давлений и температур (500-12000С) не существует. Этот факт еще ранее установили при обычных условиях синтеза авторы работы, которые считали, что полисульфид иттрия существует лишь в интервале концентраций YS1,72 - YS1,78 .
По своим магнитным свойствам сульфиды иттрия являются слабыми парамагнетиками. По электрофизическим свойствам YS2 и d- Y2S3 являются полупроводниками, Y4S3 , YS и Y5S7 обладают проводимостью металлического типа. Соединение Y5S7 по физическим свойствам можно скорее отнести к полуметаллам: удельное сопротивление r=2,4*10-2ом*см (293 К); температурный коэффициент сопротивления b=1,87*10-3ом*см*град-1; термо-э.д.с. a=14 мкв* град-1 (293 К); концентрация носителей n=3,7*1021см, постоянная Холла RH=1,7*10-3см3/кул.
Сульфиды иттрия хорошо растворяются в разбавленых неорганических (HCl, HNO3, H2SO4) и уксусной кислотах, окисляются растворами перманганата калия и иода, медленно окисляются при нагревании на воздухе. Сульфид Y2S3 устойчив при 15000 С, но легко диссоциирует при 17000 С, превращаясь в Y3S4.[1]
1.1.4. Фазовые равновесия в системе MgS –Ln2S3.
Серные соединения были изучены в их совокупности Патри, Флао, Доманжем, соединение MLn4S7 составили преимущественный объект работ Адольфа[5, 6, 7].
В этих системах имеются кубические тяжелые жидкости типа Th3P4, начиная с серных соединений Ln2S3 первых элементов группы редких (от La до Cd) их размеры очень уменьшены и соединения MLn2X4 этого типа не существуют. Сравнение этих тяжелых растворов с тяжелыми растворами системы селенидов CaSe – Ln2Se3, для которых соединения MLn2Se4 также не существуют, показывает, что размер гомогенных областей проходит в этих 2-х случаях одинаковую эволюцию, продвигаясь в группу редких элементов, с минимумом к Pr и максимумом к Sm. Второй сорт тяжелых растворов, наблюдаемых в этих системах – кубический тип NaCl. Они образуются добавлением халькогенов Ln2X3 редких металлов конца группы к халькогенам MX.
В случае с системами MgS- Ln2S3 которые изучены Палио, констатируют, что от Sm до Er размер гомогенной области линейно растет относительной разницы радиусов ионов при наличии двух металлов [6].
Два различных типа определенных соединений были идентифицированы, но лишь к концу серии редких элементов. Они имеют общую формулу MgLn2X4. Серные соединения MgLn2S4 – ромбические. Соединения MgLn4S7 были получены от Dy до Yb включительно.
Схемы рис.2 представляют системы серных соединений MgS - Ln2S3 при 1200°C.[3]
Табл. 2 Кристаллохимические данные для фаз, образующихся в системах MgS-Y2S3.
| Соединения | a(Å) | b(Å) | c(Å) | Структурный тип | Структура |
| MgY4S7 | 12 ,66 | 3,80 | 11,45 | FeY4S7 | Моноклинная |
| MgY2S4 | 12,60 | 12,73 | 3,77 | MnY2S4 | Ромбическая |
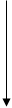 | 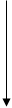 | 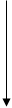 | 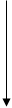 | ||||||
 | |||||||||

| |
Ce

| |

| |
 |
Sm


| |
 |
Tb



|
 |



|
Er


|



|
 |



|
Y
 - тип Тh3P4
- тип Тh3P4
 - тип NaCl
- тип NaCl
А - тип MnY2S4
С - шпинель
Рис. 2 Распределение фаз в системах MgS-Y2S3
Табл.3 Размеры гомогенной области ( n ) для системы Ln2S3-MgS при 12000 С
| Система | n |
| Sm2S3-MgS | 5 |
| Cd2S3-MgS | 17 |
| Dy2S3-MgS | 29 |
| Y2S3-MgS | 39 |
| Er2S3-MgS | 45 |
| Yb2S3-MgS | 47 |
| Lu2S3-MgS | 48 |
Рис.3 Зависимость n , гомогенной области типа NaCl , от разности радиусов ионов металлов Ln и Mg при T=12000 C для систем Ln2S3-MgS
Дата: 2019-07-24, просмотров: 276.