В природе моносахариды (монозы) распространены и имеют наибольшее значение пентозы общей формулы С5Н10О5 и гексозы общей формулы С6Н12О6, не могут гидролизоваться и превращаться в более простые углеводы. По химическому строению моносахариды представляют собой многоатомные спирты, имеющие альдегидную группу (альдегидоспирты, оксиальдегиды, альдозы — когда на конце углеродной цепи присутствует карбонильная группа) или кетонную группу (кетоспирты, оксикетоны, кетозы — когда карбонильная группа расположена в ином другом положении). Отсюда, глюкоза и фруктоза являются функциональными изомерами. Функциональные изомеры различаются и расположением гидроксильных групп, как это видно из сравнения структур глюкозы и галактозы. Такие пространственные изомеры называются диастереомерами. Они различаются физическими и химическими свойствами.

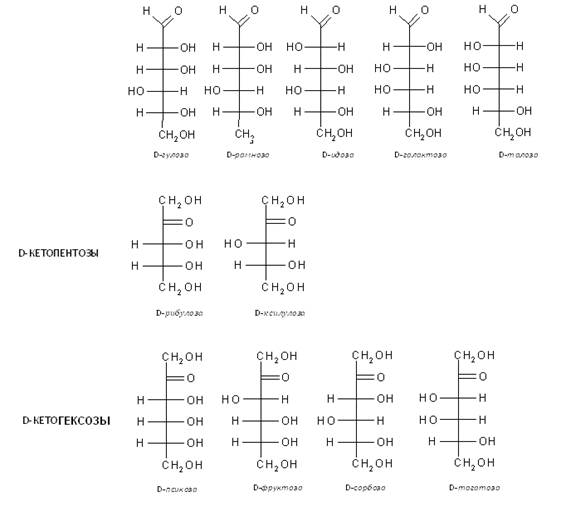
Для моносахаридов характерна оптическая изомерия (энантиомерия) (Э. Фишер). В их молекулах содержатся асимметрические (хиральные) атомы углерода (С*), находящиеся в sp 3-гибридизации и связанные с четырьмя различными атомами или их группами. Энантиомеры имеют идентичные физические и химические свойства. Число оптических стереоизомеров связано с числом асимметрических атомов углерода формулой N = 2n. 
 В общем случае молекула с "n" хиральными центрами имеет 2n стереоизомеров, которые представляют собой пары зеркальных антиподов.
В общем случае молекула с "n" хиральными центрами имеет 2n стереоизомеров, которые представляют собой пары зеркальных антиподов.
В качестве обозначения противоположных конфигураций редуцирующих сахаров с одинаковыми названиями применяются буквы D и L, которые указывают принадлежность к двум рядам. Последний асимметрический атом углерода определяет принадлежность к стереохимическому ряду. Гидроксильная группа справа – D – ряд; слева – L – ряд. В природе одни моносахариды встречаются больше в Д-конфигурации, чем в L, другие наоборот (L-арабиноза часто встречается в растениях, тогда как D-арабиноза обнаружена только в некоторых видах бактерий).
Поскольку молекулы сахаров построены несимметрично, то для них не может быть оптически неактивных мезоформ. Экспериментальный факт, фиксируемый поляриметром, вращения поляризованного света вправо обозначается знаком (+); вращение влево — знаком (-). Символы знаков D(+) – и L(-) могут очень часто не совпадать.
Изображенные линейными формулами альдозы во многом не отражают физические и химические свойства моносахаридов. Такие структуры возможны в растворах, и то в незначительных количествах (тысячные доли процента). Так в УФ - и ИК-спектрах моносахаридов отсутствуют полосы поглощения, характеризующие карбонильную группу. В действительности, моносахариды с 5 и более атомами углерода обычно встречаются в водном растворе в циклических формах, в которых карбонильная группа образует ковалентную связь с атомом кислорода гидроксильных групп. А.А. Колли (русский химик-органик), предложил для всех моносахаридов циклические структуры.
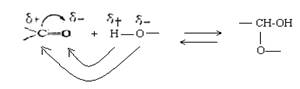
В карбонильной группе связь между атомами углерода и кислорода осуществляется двумя парами электронов. Электронное облако связи смещено к кислороду как более электроотрицательному атому, в результате чего он приобретает частичный отрицательный .заряд (δ-). В то же время карбонильный углерод в результате оттягивания от него электронов приобретает частичный положительный заряд (δ +):

Это обусловливает большую реакционную способность органических соединений, содержащих карбонильную группу: с одной стороны, атом углерода приобретает электрофильные свойства и способен активно взаимодействовать с нуклеофильными реагентами, а атом кислорода приобретает нуклеофильные свойства и способен присоединять электрофильные реагенты и замещаться ими; с другой стороны, на атоме углерода связи С=О концевой карбонильной группы положительный заряд сильнее притягивает электрон от атома водорода альдегидной группы, последний становится более подвижным и легко вступает в какие-либо реакции, например, окисляется (редуцируется) при рН > 7.
Отсюда, появление пятого гидроксила, названного гликозидным, является следствием внутримолекулярной реакции между карбонильной группой и одним из гидроксилов сахара. Известно, что взаимодействие альдегидов (кетонов) со спиртами приводит к образованию полуацеталей (полукеталей):
На связь между устойчивостью цикла и его строением обратил внимание немецкий химик А. Байер. В своей теории он исходил из предположения, что все циклы являются плоскими, а за меру устойчивости цикла принял любое отклонение валентных углов от "нормального" угла 109° 28':
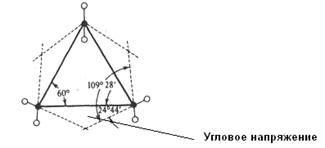
Такое отклонение создает в молекуле напряжение, которое, в свою очередь, понижает ее устойчивость. Расчет дал отклонение валентного угла от нормального для четырехчленного цикла +9°44', пятичленного 0°44', шестичленного -5° 16'.
Также позже было установлено, что пяти- и шестичленные циклы не находятся в одной плоскости, а принимают в пространстве определенную форму (конформацию: см. ниже — «кресло»: она устойчивее), что приводит к уменьшению углового напряжения, поэтому и к повышению устойчивости цикла.
Поэтому при образовании циклических структур сахаров-альдоз гидроксильная группа у предпоследнего (или пред-предпоследнего) реагирует с альдегидной группой, образуя пиранозный (или фуранозный) цикл, содержащий полуацетальную связь:
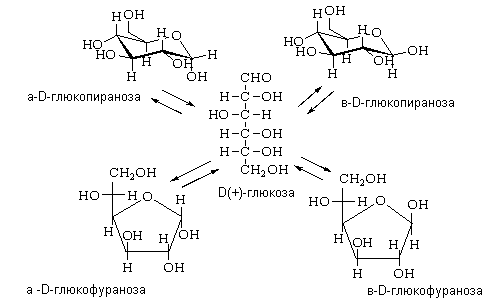
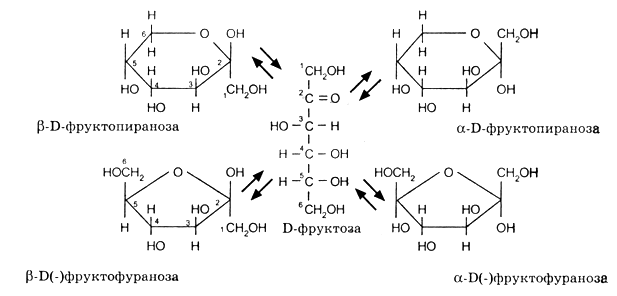
Сахара-кетозы также встречаются в форме α- и β-аномерных форм. В этих соединениях гидроксильная группа у предпоследнего (или последнего) реагирует с кетогруппой, образуя фуранозный (или пиранозный) цикл, содержащий полукетальную связь:
При образовании циклического полуацеталя сахаров появляется новый асимметрический атом углерода (аномерный центр (С-1)). Для указания его конфигурации используют обозначения a и b. α- и β-формы моноз превращаются друг в друга в водном растворе, этот процесс получил название мутаротации.
Возникновение циклических структур, существование которых предвидел Колли, обусловлено соответственно явлениями d- и g- оксициклотаутомерии.
Для D – ряда a - аномер имеет полуацетальный гидроксил внизу, b - аномер – вверху. Для L – ряда имеет место обратное отношение a - и b - аномеров.
Низкомолекулярные олигосахариды включают в себя также вещества, именуемые «сахара». Это — дисахариды (биозы — сложные сахара общей формулы С12Н22О11) и трисахариды (триозы – сложные сахара общей формулы С18Н32О16).
По химической структуре они представляют собой гликозиды, образованные в результате отщепления молекулы воды от двух (биозы) или трёх (триозы) моносахаридов за счет гидроксилов по одному от каждого из них. При этом один из гидроксилов является гликозидным. Если моносахариды все являются способными окисляться (редуцироваться), то среди олигосахаров существуют невосстанавливающие. Если отщепление молекулы воды произошло за счет гликозидных гидроксилов всех молекул моносахаридов, то образуется невосстанавливающие низкомолекулярные олигосахариды. Такие сахара существуют только в циклических конфигурациях и не могут переходить в цепные карбонильные формы и, следовательно, не обладают восстановительными свойствами. В частности, водные растворы их не реагируют с реактивом Фелинга, не подвергаются мутаротации и пр.
Если отщепление воды произошло за счет гликозидного гидроксила только одного из моносахаридов и негликозидного гидроксила других моносахаридов, то образуется восстанавливающие низкомолекулярные олигосахариды, в котором один из циклов сохраняет гликозидный гидроксил, способный в водных растворах изомеризоваться, превращаясь в цепную карбонильную форму.
Дата: 2019-07-24, просмотров: 413.