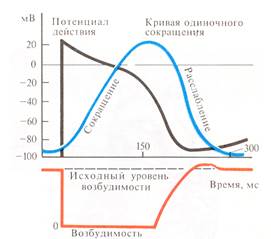
1 — быстрая деполяризация; 2 — ранняя начальная реполяризация; 3 — медленная реполяризация (плато); 4 — быстрая конечная реполяризация; 5 — абсолютная рефрактернисть; 6 — относительная рефрактернисть (уязвимый период); 7 — фаза экзальтации.
В фазу сокращения миокарда (продолжительность около 0,33 с) его возбуждение снижается (период абсолютной рефрактерности — продолжается 0,27 с, т.е. несколько короче длительности ПД) и сердце не отвечает на действие даже сверхпороговых раздражителей. Это состояние имеет очень важное значение для работы сердца. В случае отсутствия длительной фазы абсолютной рефрактерности у кардиомиоцитов сердечная мышца перешла бы в состояние тетануса и не смогла бы выполнять свои функции.
С началом фазы расслабления возбудимость кардиомиоцитов начинает повышаться (период относительной рефрактерности – 0,03 с) и сердце может ответить на действие сверх порогового раздражителя. Затем наступает короткий период супернормальной возбудимости (натриевые каналы к этому времени практически реактивированы, а разность потенциалов близка к критическому уровню деполяризации) — около 0,03 с, в это время сердечная мышца может отвечать сокращением на подпороговые раздражения.
Период повышенной возбудимости кардиологи называют «период уязвимости» сердца, так как если в этот момент в самом сердце возникнет другой источник возбуждения или слабое возбуждение придет извне, его ритмичная работа нарушится. Сердце ответит внеочередным сокращением (экстрасистола) или более серьезными нарушениями ритма.
В нормальных условиях расслабление миокарда после его сокращения обеспечивается вследствие выброса Са2+ из клетки и поглощения его СПР в результате работы Са-насоса. Выброс ионов Са2+ происходит посредством Са2+-насоса. Механизм, предотвращающий избыточное накопление Са2+ в кардиомиоцитах, чрезвычайно важен, так как защищает их от чрезмерно длительного и сильного сокращения (контрактура). Последняя может вызвать в сердце необратимые изменения в связи с резким снижением кровообращения участка миокарда, находящегося в длительном сокращении. В кардиологии применяют лекарственные средства, позволяющие снизить перегрузку кардиомиоцитов Са2+ специфическими ингибиторами Са2+-насосов.
Законы сокращения миокарда:
1. Сердце отвечает закону «все или ничего» — на пороговый раздражитель отвечает возбуждением всех волокон, на подпороговый — не отвечает.
2. Сердечная мышца сокращается по типу одиночного сокращения, т.к. длительная фаза абсолютной рефрактерности препятствует возникновению тетанических сокращений.
3. При распространении ПД по мембране ионы кальция поступают к сократительным белкам в основном из межклеточного пространства и вызывают те же процессы взаимодействия актиновых и миозиновых протофибрилл, что и в скелетном мышечном волокне. Расслабление кардиомиоцита обусловлено удалением кальция из протофибриллярного пространства кальциевым насосом в межклеточную среду. Важным процессом в сокращении кардиомиоцита является вход ионов кальция в клетку во время развития ПД. Наряду с тем, что входящий в клетку кальций увеличивает длительность ПД и как следствие, продолжительность рефрактерного периода, он является важнейшим фактором в регуляции силы сокращения миокарда. Удаление ионов кальция из межклеточных пространств приводит к полному разобщению процессов возбуждения и сокращения (электромеханическое сопряжение) — ПД остается практически в неизменном виде, так как по Na / Ca каналам в отсутствии ионов Са2+ в клетку входят дополнительно ионы Na, а сокращения кардиомиоцита не происходит.
Сила сокращений миокарда зависит от:
1. Количества актомиозиновых мостиков, которые образуются одновременно. Чем больше растянуто мышечное волокно в покое (в диастоле), тем сильнее оно будет сокращаться (закон Франка-Старлинга).
2. Чем больше ионов кальция входит в саркоплазму, тем больше сила сокращения кардиомиоцита. Накопившегося в нормальных условиях в саркоплазме кальция достаточно лишь для активации части миофиламентов и образования актомиозиновых комплексов. При повышении концентрации Са2+ число активированных миофиламентов и сократимость миокарда возрастают.
3. Саркоплазматический ретикулум сердца содержит небольшое количество ионов кальция, поэтому в сердце запас кальция пополняется при каждом ПД. Чем более продолжителен ПД, тем больше ионов кальция входит в кардиомиоцит. Таким образом, сила сокращения сердца регулируется продолжительностью ПД. Увеличение сократимости позволяет сердцу увеличить объем выброса крови при неизменном конечно-диастолическом объеме или сохранить выброс при повышении давления в аорте.
Экстрасистола. Способность к ритмической генерации импульсов, свойственная всем отделам проводящей системы сердца, не проявляется до тех пор пока роль водителя ритма выполняет СА-узел. Если на миокард в период диастолы, когда возбудимость восстанавливается, нанести раздражение, то возникает внеочередное сокращение — экстрасистола.
Различают экстрасистолы — синусовую, предсердную, желудочковую.
Одиночные экстрасистолы встречаются нередко у здоровых людей (при эмоциях) и не имеют большого клинического значения. Множественные экстрасистолы могут быть следствием сердечных заболеваний (ишемическая болезнь сердца, врожденные и приобретенные пороки сердца, артериальная гипертензия и др.) и внесердечных заболеваний (эндокринная патология: заболевания щитовидной железы; заболевания желудочно-кишечного тракта: желчнокаменная болезнь; заболевания почек и др.). Если внеочередное возбуждение возникает в СА-узле, то происходит раннее сокращение — синусовая экстрасистола. Следующее сокращение наступает после обычной паузы. Внеочередное возбуждение в проводящей системе желудочков приводит к возникновению желудочковой экстрасистолы.
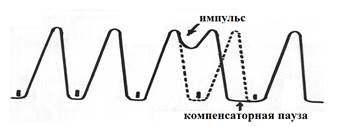
Желудочковая экстрасистола (схема)
Импульсы могут возникать в АВ-узле либо вблизи узла. Возбуждение быстро достигает волокон Пуркинье, распространяется по миокарду и вызывает его внеочередное сокращение. Такая экстрасистола называется желудочковой и она сопровождается полной компенсаторной паузой. При развитии такой экстрасистолы СА-узел посылает очередной импульс к желудочкам. Однако они уже сокращаются под влиянием внеочередного импульса, возникшего в АВ-узле, т.е. желудочки рефрактерны (невозбудимы), миокард не реагирует на раздражение. По окончании состояния невозбудимости проходит некоторое время пока из СА-узла поступит очередной импульс. Выпадение одного сокращения желудочков приводит к продолжительной компенсаторной паузе.
Локализацию очагов возбуждения в клинической практике определяют электрокардиографически. Основными электрофизиологическими механизмами экстрасистолий являются re-entry (см. дополнительные такты) и постдеполяризация.
Классификация экстрасистол:
По уровню возникновения: наджелудочковая (синусовая, предсердная, стволовая, из A-V соединения); желудочковая (из основания, межжелудочковой перегородки, правого и левого желудочка, верхушки).
По времени: ранние экстрасистолы — в ранней диастоле, «R на T»; в середине диастолы; поздние экстрасистолы — в конце диастолы (в момент регистрации зубца P); интерполированные экстрасистолы, которые возникают во время паузы между двумя сокращениями.
По частоте: одиночные и множественные (частые) более 6 -10 в 1 минуту; аллоритмия — правильное чередование экстрасистол и нормальных сокращений; бигеминия , тригеминия, квадригеминия; парные желудочковые экстрасистолы — две желудочковые экстрасистолы подряд;
По форме и интервалу сцепления: экстрасистолы имеющие одинаковый интервал сцепления и одинаковую форму — монотопные; одинаковый интервал сцепления и разную форму — полиморфные; экстрасистолы имеющие разный интервал сцепления и разную форму — политопные;
По причине: функциональные и органические экстрасистолы. Для функциональных экстрасистол характерно отсутствие органического поражения сердца и нарушения гемодинамики (чрезмерная физическая и/или эмоциональная нагрузка, курение, прием некоторых лекарственных препаратов, алкогольных напитков и т.д.). Органические экстрасистолы, отличающиеся более серьезным прогнозом, возникают, как правило, при заболеваниях сердечно-сосудистой системы (ишемическая болезнь сердца, врожденные и приобретенные пороки сердца, артериальная гипертензия и др.) и внесердечных заболеваниях (эндокринная патология: заболевания щитовидной железы; заболевания желудочно-кишечного тракта: желчнокаменная болезнь; заболевания почек и др.).
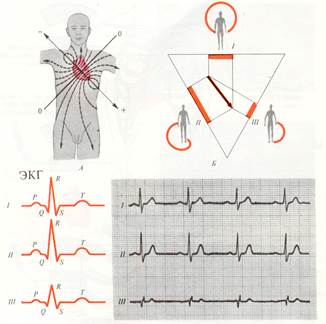 Электрические проявления сердечной деятельности. Электрокардиография, ее диагностическое значение
Электрические проявления сердечной деятельности. Электрокардиография, ее диагностическое значение
Возникшее в водителях ритма возбуждение распространяется по проводящей системе и миокарду и сопровождается появлением на поверхности клеток отрицательного потенциала. Процесс распространения возбуждения по сердцу создает разность потенциалов между возбужденными и невозбужденными участками сердца. Происходит синхронный разряд большого числа возбужденных единиц (кардиомиоцитов). Сердце становится мощным генератором биологического электричества. Суммарный потенциал возбужденных волокон настолько велик, что его можно зарегистрировать далеко за пределами сердца. Приложив электроды к определенным точкам тела, можно записать кривую, отражающую динамику разности потенциалов в течение сердечного цикла. Эту кривую, имеющую сложный характер, называют электрокардиограммой (ЭКГ), а метод исследования — электрокардиографией. ЭКГ получила широкое применение в медицине как диагностический метод, позволяющий установить характер ряда нарушений сердечной деятельности.
Существуют разные методы отведений для записи ЭКГ.
1. Отведения от конечностей:
а) биополярные (по методу Эйнтховена);
б) униполярные (по методу Гольдбергера).
2. Грудные (прекордиальные) отведения:
а) биполярные (по методу Нэба) (малый грудной треугольник);
б) униполярные (по методу Вильсона).
Поверхностные методики исследований организма не причиняют ему вреда, они основаны на регистрации внешних проявлений работы органов. Их называют неинвазивными (ЭКГ, ВКГ и др). Методики связанные с проникновением внутрь организма называются инвазивными.
Чаще для регистрации ЭКГ производят отведения потенциалов от конечностей по методу треугольника Эйнтховена В. (биполярное отведение).
В соответствии с этим методом используются три стандартные отведения:
I — правая рука — левая рука;
II — правая рука — левая нога;
III — левая рука — левая нога.
Кроме того, регистрируют три униполярных усиленных отведения по Гольдбергеру: aVR, aVL, aVF. При регистрации усиленных отведении два электрода, используемые для регистрации стандартных отведений, объединяются в один и регистрируется разность потенциалов объединенными и активными электродами. Так, при aVR активным является электрод наложенный на правую руку, при aVL ― на левую руку, при aVF ― на левую ногу.
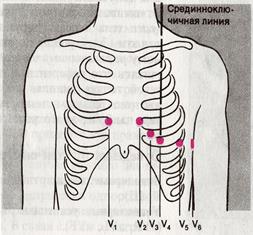
Для отведения от грудной клетки (по Вильсону, униполярное отведение) один электрод (активный) прикладывают к одной из 6 точек грудной клетки в области сердца. Другой (индифферентный) электрод прикладывается к правой руке или три соединенных вместе электрода накладываются на обе руки и левую ногу. В этом случае определяются электрические изменения только на участке грудного электрода. Обозначаются эти отведения буквами V1–V6. Таким образом, электроды V1 и V2 оказываются расположенными над правым желудочком, V3 и V4 ― над межжелудочковой перегородкой, V5 и V6 ― над левым желудочком. Отведения по Вильсону дают возможность судить о горизонтальной проекции векторных величин.
В итоге, на основании того, в каких структурах сердца наилучшим образом выявляют электрические процессы те или иные ЭКГ отведения, они могут быть сгруппированы следующим образом: V1, V2, V3, V4 ― передние, I, aVL, V5, V6 ― левые боковые, II, III, aVF ― нижние, aVR.
Дата: 2019-07-24, просмотров: 586.