Ход анализа.
Из фильтрата после разложения почвы отбирают аликвотную часть, соответствующую 0,2 г почвы, помещают в стакан на 100 мл и для удаления из раствора хлора прибавляют 5 мл конц. HNO3 и выпаривают на закрытой плитке досуха. Такую обработку повторяют еще 3-4 раза, прибавляя HNO3 по стенкам стакана для смывания с них следов хлора. К сухому остатку прибавляют 25 мл 10% раствора серной кислоты (65 мл конц. кислоты вливают в воду и доводят после охлаждения водой до 1 л), нагревают 10 минут до растворения осадка, прибавляют 15 мл дистиллированной воды и 2 мл конц. H3PO4 – для связывания окрашенных ионов железа, а так2,же для предупреждения гидролиза солей, образуемых ионами марганца высшей валентности. После перемешивания прибавляют 2-3 мл 1% раствора AgNO3 – для ускорения реакции и осаждения возможных следов хлора. Нагревают еще около 10 минут; если раствор помутнеет, то его отфильтровывают через плотный фильтр, промывают водой, подкисленной серной кислотой и доводят до объема около 45 мл. К нагретому раствору равномерно небольшими порциями прибавляют 2 г персульфата аммония и кипятят 2 минуты для быстрого и полного окисления марганца до марганцевой кислоты. При этом происходит энергичное разложение персульфата аммония и обильное выделение пузырьков озона.
Стакан с раствором охлаждают, окрашенный раствор переносят в мерную колбу на 50 мл, доводят водой до метки и колориметрируют на ФЭК-Н с зеленым светофильтром (№5, дл. Волны 536 нм) в 2 см кювете против 5% раствора серной кислоты. Содержание марганца вычисляют по калибровочному графику, приготовленному из 0,1 н. раствора KMnO4 (из фиксанала).
Вывод: Содержание марганца по калибровочному графику 2,25%.
1.9 Пероксидный метод определения титана
Ход анализа. Берут пипеткой 25 мл фильтрата от кремниевой кислоты и переносят в мерную колбу на 100 мл. Добавляют 25 % раствор NH4OH до появления мути. Образовавшийся осадок растворяют 5 % раствором H2SO4, добавляя ее по каплям и перемешивая раствор. После растворения осадка прибавляют 1 мл H3PO4 пл. 1,7 и 1 мл 30 % Н2О2, доливают 5 % серной кислотой до метки, тщательно перемешивают и через 10 мин измеряют оптическую плотность окрашенного раствора при длине волны 410 нм. Содержание титана в испытуемой пробе находят по калибровочному графику.
Для построения калибровочного графика в мерную колбу на 100 мл отбирают от 1 до 10 мл запасного стандартного раствора титана с содержанием в 1 мл 0,1 мг TiO2, прибавляют 80 мл 5 % раствора серной кислоты, 1 мл H3PO4 пл. 1,7 и 1 мл 30 % Н2О2, доливают серной кислотой до метки и перемешивают. Через 10 мин измеряют оптическую плотность при длине волны 410 нм. По полученным данным строят калибровочный график зависимости оптической плотности от концентрации TiO2 и находят содержание TiO2 в анализируемой пробе по формуле:
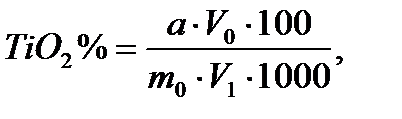
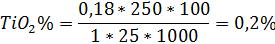
Определение кальция
Ход анализа. Из фильтрата после выделения полуторных оксидов отбирают пипеткой 25-50 мл и переносят в коническую колбу на 250 мл и доводят дистиллированной водой до 100 мл. Прибавляют 2-3 капли 1 % раствора Na2S и 1-2 мл 5 % раствора гидроксиламина, 15 мл 2 н. раствора NaOH (рН раствора становится около 13), перемешивают, вносят на кончике шпателя сухой порошок индикатора флуорексона и медленно титруют при постоянном помешивании 0,01 М раствором трилона Б до перехода окраски из зелено-оранжевой с сильной флюоресценцией в пурпурно-розовую с очень заметным понижением флюоресценции. Вместо флуорексона в качестве индикатора можно использовать мурексид в смеси с NaCl. Титрование ведут до перехода розовой окраски раствора в фиолетовую. Титрование рекомендуется проводить в присутствии перетитрованной пробы. Содержание СаО находят по формуле:
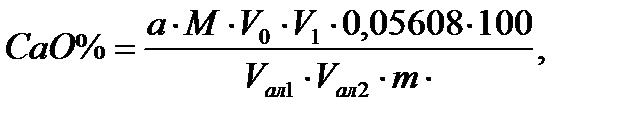
Дата: 2019-07-24, просмотров: 305.