Внедрение гетероатомов в систему цикла атомов углерода мало влияет на общую термодинамическую картину, но активирует реакцию раскрытия циклов.
Трехчленные гетероциклы легко вступают в реакции полимеризации.
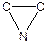
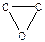
Четырехчленные гетероциклы также способны вступать в реакции полимеризации.
Пятичленные гетероциклы труднее вступают в реакции полимеризации (появляются термодинамические ограничения).
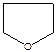 -тетрагидрофуран
-тетрагидрофуран 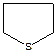 - тетрагидротиофен
- тетрагидротиофен
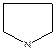 - тетрагидропиррол
- тетрагидропиррол
Шестичленные гетероциклы не способны вступать в реакции полимеризации.
Семичленные гетероциклы легко вступают в реакции полимеризации:
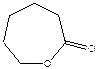 ε - капролактон
ε - капролактон
(также способен полимеризоваться: Qпол = -ΔH= -3.3 ккал/моль, ΔS = -2.5 энт. ед, Тпред ≈ 1300К).
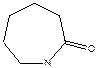 - капролактам
- капролактам
(способен полимеризоваться: Qпол = -ΔH = 3,3 ккал/моль, ΔS = -4 энт. ед, Тпред ≈ 830К).
Более крупные циклы с включением гетероатомов легко полимеризуются:
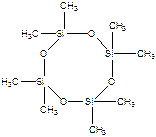 - гексаметилциклооктасилоксан
- гексаметилциклооктасилоксан
(легко полимеризуется: Qпол = -ΔH = -1,5 ккал/моль, ΔS = 46 энт. ед, полимеризация разрешена во всей области температур).
Термодинамически возможная степень превращения мономера в полимер рассчитывается по формуле:
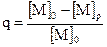 , (6.1)
, (6.1)
где [M]p – равновесная концентрация мономера, [M]0 – начальная концентрация мономера
Если [M]p=[M]0, то мономер полимеризоваться не будет; если [M]p >[M]0, то реакция не пойдет образующийся полимер будет термодинамически нестабильным.
Итак, выяснено, что существует область, в которой возможно протекание реакции, которая ограничивается предельными температурами (верхней или нижней). Следует также учесть, что мономеры и полимеры могут находиться в разных фазовых состояниях, это будет также влиять на термодинамические ограничения. Помимо этого полимеризация может проводиться в растворе, это также влияет на диапазон температур, в котором может проводиться полимеризация.
 Μ
Μ
Мж
Пж
(Мж)р
(Пж)р
Тпр (в р-ре) Тпрр (в массе) Т
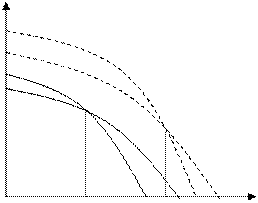
Рис. 6.1. Зависимость термодинамического потенциала от температуры при растворении
При растворении термодинамические потенциалы как мономера, так и полимера понижаются (самопроизвольные процессы). При этом точка пересечения кривых μ = f(T), т.е. Тпр может понизиться.
Влияние различных факторов на возможность протекания полимеризации:
1) Влияние давления на протекание полимеризации определяется зависимостью:
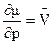 , (6.2)
, (6.2)
где 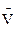 - парциальный мольный объем
- парциальный мольный объем
Рассматривая эту зависимость для мономера и полимера, можно получить зависимость предельной температуры от давления, которая имеет вид (аналог уравнения Клаперона-Клаузиуса):
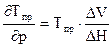 (6.3)
(6.3)
Где ∆V – разность объемов мономера и полимера , ∆Н – разность соответствующих энтальпий.
Таким образом, изменяя давление, можно изменить значение предельной температуры. Однако, требуется значительное изменение давления, чтобы существенно изменить предельную температуру.
В случае α-метилстирола при переходе от давления в 1 до 6500 бар Тпр возрастает от 61 ◦С до 170 ◦С.
2) Влияние кристаллизации полимера:
 Μ
Μ
М
Пам
Пкр
Тпр Тпркр Тппл Т
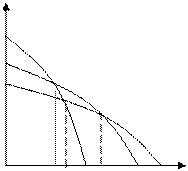
Рис. 6.2. Зависимость термодинамического потенциала от температуры при кристаллизации полимера
При кристаллизации изменение энтропии отрицательно и в соответствии со схемой Тпр повышается. Благодаря этому фактору удается осуществлять полимеризацию формальдегида при умеренных температурах, т. к. образующийся полиформальдегид кристаллизуется.
Для определения величин ΔHпол и ΔSпол можно использовать различные приемы, простейший путь основан на измерениях равновесной концентрация мономера в зависимости от предельной температуры:
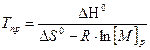 , (6.4)
, (6.4)
откуда 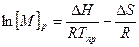 (6.5)
(6.5)
 |
ln[M]p
-ΔS/R
ΔH/R
1/Tпр
Рис. 6.3. Зависимость ln[M]p от 1/Tпр
Таким образом, из зависимости ln[M]p от 1/Tпр можно определить величины ∆Нпол и ∆Sпол.
6.1. Термодинамика поликонденсации
В процессе поликонденсации происходит химическое взаимодействие низкомолекулярных молекул a-R-b (группы a и b взаимодействуют между собой), приводящее к образованию удлиненных цепочек, т.е. к образованию олигомерных или полимерных молекул. Кроме того, могут образовываться циклы. Процесс поликонденсации часто происходит с выделением низкомолекулярного продукта (w).
Реакцию поликонденсации можно записать в виде:
 n a-R-b a-(R-X)n-1-R-b + (n-1)w
n a-R-b a-(R-X)n-1-R-b + (n-1)w
Поликонденсация может также быть бимолекулярной, когда конденсируются молекулы типа a-R-a или b-R-b.
Правило Ругли-Циглера:
Если процесс поликонденсации протекает при повышенных концентрациях мономера, то образуются линейные полимеры; при малых концентрациях мономера образуются циклы.
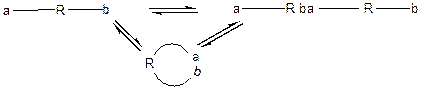
При достижении равновесного превращения мономера, состояние систем можно рассматривать как равновесие: линейный продукт↔циклический продукт конденсации (т.е. полимеризационное равновесие цикл – цепь). При этом равновесное содержание циклических форм можно определить как qцикл= [M]равн/[M]0. С уменьшением [M]0 qцикл растет и стремиться к 1 при [M]0→[M]равн.
Рассмотрим поликонденсацию с образованием линейных цепей:
 a-R-b + a-R-b a-R-ba-R-b + w
a-R-b + a-R-b a-R-ba-R-b + w
 M2 + a-R-b M3 + w
M2 + a-R-b M3 + w
………………………………….
 Mn-1 + a-R-b Mn + W
Mn-1 + a-R-b Mn + W
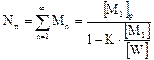 (6.1.1)
(6.1.1)
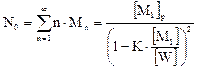 (6.1.2)
(6.1.2)
Получаем:
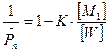 , (6.1.3)
, (6.1.3)
если n>>1, то 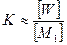 (6.1.4)
(6.1.4)
В это уравнение также как и в уравнение для полимеризационно-деполимеризационного равновесия входят концентрации только низкомолекулярных веществ, а концентрация полимера не входит. Характер равновесия процесса поликонденсации - квазигетерогенный.
Химия образования макромолекул
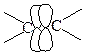 - имеется молекула с кратной связью, рассмотрим возможные пути активации для ее раскрытия.
- имеется молекула с кратной связью, рассмотрим возможные пути активации для ее раскрытия.
Пути активации:
1. активация с помощью свободных радикалов:

образуется промежуточный квазиаллильный радикал
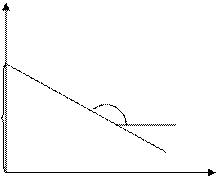
На рисунке 6.1.1. изображена зависимость потенциальной энергии от расстояния: 
U
- кривая отталкивания
- кривая притяжения
Еа - Qпол (тепловой эффект)
r0 r* r
Рис. 6.1.1. Зависимость потенциальной энергии от расстояния
Еа – энергия, необходимая для образования переходного состояния («квазиаллильного» радикала) – энергия активации, r* - переходный комплекс.
2. активация с помощью карбкатиона:
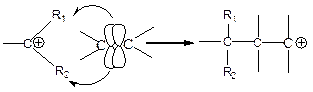
3. активация с помощью карбаниона:
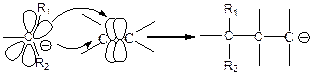
Итак, получаем, что существует 3 типа воздействия на кратную связь:
· воздействие свободных радикалов (радикальная полимеризация);
· воздействие катионов (катионная полимеризация);
· воздействие анионов (анионная полимеризация).
Вопросы для самостоятельной проработки:
- Как влияет наличие гетероатома в циклах, состоящих из атомов углерода, на реакцию полимеризации?
- Как рассчитывается термодинамически возможная степень превращения полимера в мономер?
- Какие существуют факторы, влияющие на возможность протекания полимеризации?
- В чем заключается правило Ругли-Циглера для процесса поликонденсации?
- Какие пути образования макромолекул известны в настоящее время?
Задачи для самостоятельного решения
3. Методы получения и структура основных типов полимеров
3.2. Термодинамика полимеризации
Вопросы 2501 – 2505, 2406 – 2409, 2310 – 2313
Дата: 2019-04-23, просмотров: 384.