Раздел №1. Введение. Основные понятия.
В последние десятилетия высокомолекулярные соединения (полимеры) прочно вошли в нашу жизнь. Полимеры - особый вид материалов, обладающих в зависимости от строения молекул самыми разнообразными свойствами и применяемыми в самых различных сферах жизни и деятельности человечества: в промышленности и сельском хозяйстве, в науке и технике, во всех видах транспорта. Современная медицина, как и наш повседневный быт, немыслимы без использования широкого круга полимерных материалов.
В настоящее время полимеры занимают 4 место по объему среди производимых и добываемых материалов. Распределение производимых и добываемых материалов по объему представлено на рис. 1.1, а объем производства и ассортимент основных производимых полимеров – на рис. 1.2.

Рис. 1.1. Место полимеров среди производимых и добываемых материалов
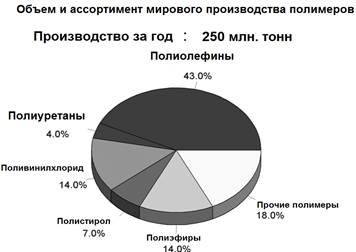
Рис. 1.2. Объем и ассортимент мирового производства полимеров
Какие же свойства отличают полимеры от обычных низкомолекулярных соединений (НМС) и позволяют выделить их в особый вид материалов?
Прежде всего, большая длина и гибкость макромолекул придают полимерам свойство высокоэластичности, т.е. способности к большим (порядка нескольких сотен процентов) обратимым деформациям.
Во-вторых, твёрдые полимерные тела - пластики сочетают высокие модули упругости, сопоставимые по величине с модулями упругости обычных твёрдых тел (неорганическое стекло, металлы, керамика), с высокими разрывными удлинениями (на порядок большими, чем у обычных твёрдых тел). Поэтому полимерные тела менее склонны к хрупкому разрушению.
В-третьих, благодаря высокой анизотропии формы макромолекул полимеров они легко ориентируются в механическом поле и образуют волокна с высокой прочностью в направлении ориентации.
Полимеры отличаются от низкомолекулярных соединений и тем, что при растворении проходят сначала через стадию набухания; вязкость разбавленных (до 1 %) растворов полимеров намного превышает вязкость растворов низкомолекулярных соединений той же концентрации. Концентрированные растворы и расплавы полимеров, как и все жидкости, обладают упруго-эластическими свойствами. Высокие молекулярные массы полимеров существенно расширяют спектр их времен релаксации по сравнению с низкомолекулярными жидкостями. Сочетание больших молекулярных масс с высокими межмолекулярными взаимодействиями обуславливают ряд аномальных вязко-упругих свойств полимерных жидкостей, не характерных для низкомолекулярных соединений.
Химические реакции полимеров протекают в большинстве случаев отлично от соответствующих реакций низкомолекулярных аналогов.
Перечисленные отличительные свойства полимеров позволили им войти в число наиболее широко используемых материалов.
Среди полимерных материалов, выпускаемых промышленностью, ведущие позиции занимают:
а) пластические массы и органические стекла;
б) синтетические каучуки;
в) синтетические и искусственные волокна;
г) плёнки и многочисленные декоративно-защитные покрытия (краски, лаки, эмали).
К высокомолекулярным соединениям относятся также и биологические полимеры (биополимеры), которые обладают рядом уникальных свойств, не характерных для низкомолекулярных соединений. Назовём некоторые из важнейших свойств биополимеров и их функции:
- нуклеиновые кислоты способны кодировать, хранить и передавать генетическую информацию на молекулярном уровне, являясь материальным субстратом наследственности;
- другой класс биополимеров - мышечные белки, способны превращать химическую энергию в механическую работу; эта их сократительная функция лежит в основе мышечной деятельности белков;
- ферменты, глобулярные белки, обладают каталитической функцией, они с большой скоростью и избирательностью осуществляют в живой природе все химические реакции обмена, распада одних и синтеза других веществ.
Все перечисленные выше особенности свойств полимеров связаны с их цепным строением. Именно цепное строение молекул полимеров является их важнейшим свойством, что позволяет дать им следующее определение:
Полимеры – особый класс химических соединений, специфика свойств которых определяется большой длиной, цепным строением и гибкостью составляющих их макромолекул.
n M → [ -M- ]n
В свою очередь под макромолекулой понимают совокупность атомов или атомных групп, различных или одинаковых по составу и строению, соединённых химическими связями в линейную или разветвлённую структуру, достаточно высокой молекулярной массы.
Вещества, у которых размеры молекул очень велики и в тысячи раз превышают размеры обычных, называются высокомолекулярными (ВМС).
Мономеры - низкомолекулярные соединения, способные вступать в реакции полимеризации и поликонденсации.

Составное звено – любые атомы или группы атомов, входящие в состав цепи полимера.
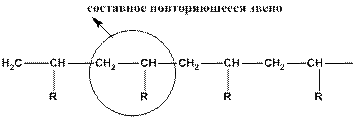
Составное повторяющееся звено (СПЗ) – наименьшее составное звено, повторением которого может быть описано строение регулярного полимера.
Пример: молекула полистирола
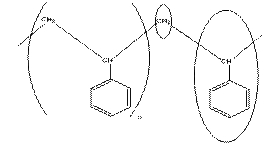
- в скобках выделено составное повторяющееся звено, а эллипсом – составные звенья.
Во многих случаях составное повторяющееся звено совпадает с мономерным звеном:
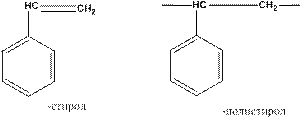
Но могут быть и случаи, когда они не совпадают:

Составное повторяющееся звено у полиэтилена – 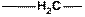
Мономерное звено – 
Степень полимеризации гомополимера - это количество составных (повторяющихся) звеньев, которые входят в макромолекулу.
Среднечисловая молекулярная масса Mn – произведение среднечисловой степени полимеризации Pn и молекулярной массы составного повторяющегося звена M0:
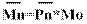
Достаточно высокая молекулярная масса полимеров - понятие относительное. Так, некоторые физико-химические свойства в ряду гомологов изменяются по кривой имеющей вид, представленный на рис. 1.3. Область I - резкое изменение свойств, например температуры плавления (Тпл), приходится на низкомолекулярное соединение (до нескольких сотен у.е.). В области III исследуемое свойство (Тпл) практически не зависит от молекулярной массы - это область высокомолекулярных соединений (молекулярные массы составляют десятки тысяч и выше, для многих полимеров молекулярные массы составляют несколько сотен тысяч у.е.). Наконец, промежуточной области II соответствуют олигомерные соединения с молекулярной массой от нескольких сотен до нескольких тысяч.

Рис. 1.3. Зависимость температуры плавления (Тпл) от молекулярной массы алканов
Таблица 1.1.
Примеры изменения свойств и применения веществ в зависимости от числа атомов С в цепи
| Число атомов С в цепи | Состояние | Применение |
| 1 - 4 5 - 11 10 - 16 16 - 25 25 - 50 1000 и более | газ жидкости средневязкие жидкости высоковязкие жидкости твердые тела полимеры | бытовые газы бензин масла и смазки моторные масла парафины, воск материалы (эластомеры, пластмассы) |
Вопросы для самостоятельной проработки:
1. Какое место занимают полимеры по объему производства в современной промышленности?
2. Назовите основные свойства полимеров, которые определяют их как особый вид материалов.
3. Дайте определение следующих понятий: полимер, высокомолекулярное соединение, макромолекула, составное звено, составное повторяющееся звено.
4. Напишите уравнение, определяющее взаимосвязь молекулярной массы и степени полимеризации.
5. Понятие о НМС, олигомере и полимере.
Номенклатура полимеров
В настоящее время существует 3 основных вида номенклатуры полимеров:
1. Номенклатура, основанная на названии мономеров (рациональная номенклатура);
2. Номенклатура, основанная на химической структуре полимерной цепи (систематическая номенклатура IUPAC);
3. Случайная номенклатура.
Номенклатура, основанная на химической структуре полимерной цепи (систематическая номенклатура IUPAC)
При помощи этой номенклатуры удобно называть органические полимеры, состоящие из одного вида составного повторяющегося звена и имеющие линейную цепь.
Формирование названия: приставка "поли" + (название СПЗ по номенклатуре IUPAC), СПЗ – составное повторяющееся звено.
· Необходимо идентифицировать СПЗ, т.е. выделить из структуры фрагмент, повторением которого можно получить структуру макромолекулы;
· Необходимо учесть расположение и ориентацию этого звена в цепи;
· Назвать СПЗ по номенклатуре IUPAC.
Таблица 2.1.2.1.
Названия основных полимеров
| Структура полимерной цепи | Название по IUPAC | Название по рациональной номенклатуре |
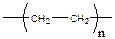
| Поли(метилен) | Полиэтилен ( сокращение - ПЭ) |
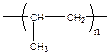
| Поли(1-метилэтилен) | Полипропилен ПП |
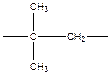
| Поли(1,1-диметил этилен) | Полиизобутилен ПИБ |
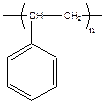
| Поли(1-фенилэтилен) | Полистирол ПС |
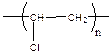
| Поли(1-хлорэтилен) | Поли(винилхлорид) ПВХ |
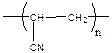
| Поли(1-цианоэтилен) | Поли(акрилонитрил) ПАН |
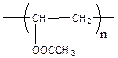
| Поли(1-ацетоксиэтилен) | Поли(винилацетат) ПВА |
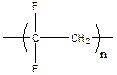
| Поли(1,1-дифторэтилен) | Поли(винилиденфторид) ПВФ |
2.1.3. Случайная номенклатура (в т.ч. торговые марки полимеров)
Закономерностей в образовании названий нет.
Примеры названий:
- Лавсан (терилен, дакрон, милар) - поли(этилентерефталат)
- винипласт (ПВХ) - поли(винилхлорид)
- тефлон (фторопласт-4) - поли(тетрафторэтилен)
-плексиглас (органическое стекло) - поли(метилметакрилат)
- Ргоfах, Ро1урго (США); данлай, донбанд (Япония), Ргораtеn (Великобритания) – полипропилен.
Таблица 2.1.3.1.
Торговые марки полипропилена
| Торговая марка | Изготовитель |
| ПП, PP | Томский нефтехимический з-д |
| Каплен | Московский нефтеперерабатывающий з-д, Кусковский химзавод (Москва, Капотня) |
| Бален | Уфаоргсинтез |
| Армлен | Полипластик-Технопол (Москва) |
| Томполен | Полимер Компаунд (г. Томск) |
| Нурален | Пластмассы (Москва) |
| Новолен | Барс (Москва) |
| Филен | Завод композиционных материалов и пластмасс (Томск) |
| Топлен | Фарм-Пласт (Тольятти) |
| Тана | (Северодонецк, Украина) |
| Липол | Лисичанскнефтеоргсинтез (ЛиНОС г. Лисичанск, Украина) |
Таблица 2.1.3.2.
Основные зарубежные аналоги отечественного полипропилена
| Торговая марка | Изготовитель |
| Acclear | BP Chemicals |
| Accpro (тальконаполненный) | BP Chemicals |
| Accucomp, Accuguard, Accutech | ALCO Compaunders |
| Adstryn | Basel |
| Bormod, Borpact, Borsoft | Borealis |
| Chisso | Chisso |
| Clyrel | Basel |
| Demilen | Vamp Tech |
| Eltex | BP Solvay Polyethilene |
| Hipol | Mitsui Petrochemicals |
| Koylene | Indian Petrochemicals |
| Prolen | Polibrasil Resians |
| Propathene | Lucite Internfnional |
| Slovalen | Plactcom |
| Stamylan P | SABI Euro-Petrochemicals |
| Tipplen | TVK |
| Juplene | SK Chemicale |
Классификация полимеров
По происхождению
- природные (существующие в природе): целлюлоза, крахмал, хитин, белки, нуклеиновые кислоты и др.
- синтетические полимеры (не существующие в природе, синтезированные): полиэтилен, полипропилен и др.
- искусственные (модификации природных полимеров, получаемые синтетически): нитроцеллюлоза, бензилцеллюлоза, метилцеллюлоза, ацетатцеллюлоза и др.
По областям применения
· пластические массы и органические стекла
· синтетические каучуки
Если Тст>Ткомн, то полимер относят к пластикам (стирол, ПВХ, полиметилметакрилат и др.)
Если Тст<Ткомн, то полимер относят к синтетическим каучукам (СК), где Тст – температура стеклования, Ткомн – комнатная температура
· синтетические и искусственные волокна
· пленки и многочисленные декоративно-защитные покрытия (лаки, краски, эмали)
· биомедицинские материалы.
Химическая классификация
Классификация осуществляется по типу атомов, входящих в цепь:
· органические полимеры (в состав входят органогенные элементы – С, N, O, P, S).Делятся на гомоцепные (в основной цепи содержатся только атомы углерода) и гетероцепные (в состав основной цепи входят другие атомы) К этому классу полимеров относятся биополимеры.
· элементоорганические полимеры (в составе основной цепи наряду с атомами углерода находятся атомы Si, Al, Ti, Ge, B).
· неорганические полимеры (в основной цепи не содержатся атомы углерода, например силиконы).
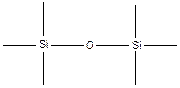
Вопросы для самостоятельной проработки:
1. Перечислите виды номенклатуры полимеров.
2. Как формируется номенклатура, основанная на названии мономеров?
3. Приведите примеры названий полимеров по номенклатуре, основанной на химической структуре полимерной цепи.
4. Назовите виды классификации полимеров. Приведите примеры.
5. Какие существуют виды сополимеров?
6. Каким образом осуществляется химическая классификация полимеров?
Задачи для самостоятельного решения*
2. Классификация и структурные формулы основных полимеров
2.1 Классификация полимеров
Вопросы2501 – 2502, 2403 – 2406, 2307
2.2. Структурные формулы основных полимеров
Вопросы 3501, 3402, 3303 – 3309
*Здесь и в дальнейшем задачи приведены из « Сборника тестовых заданий для тематического и итогового контроля по дисциплине «Химия и физика полимеров», Прокопов Н. И., Гервальд А. Ю., Зубов В. П., Литманович Е. А.,М.,МИТХТ, 2009г.
Конфигурация макромолекулы
Конфигурация – порядок расположения химических связей, соединяющих атомы или атомные группы в макромолекуле.
Конфигурация формируется в процессе синтеза и не может быть нарушена иным образом, как разрушением химических связей.
Виды конфигурационной изомерии:
Цис-транс изомерия
Характерна для группы полимеров, имеющих в цепи двойные связи.
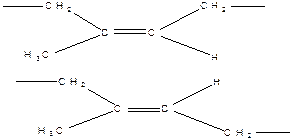 Цис-изомер
Цис-изомер
Транс-изомер
Локальная и цис-транс изомерии являются химическими видами изомерии.
Конформация макромолекул
Конформация – это форма, которую приобретают макромолекулы данного конфигурационного состава под действием теплового движения или физических полей.
Виды конформации:
· Конформация транс-зигзага
Представляет собой вытянутую цепь:
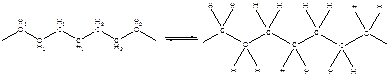
Возможно вращение вокруг связей по образующим конуса с углом при вершине 109˚28΄; движение ограничено, т. к. повернуть целый хвост за счет теплового движения трудно. При этом происходят частичные переходы транс-конформаций в свернутые (гош-конформации), а вытянутая цепь скручивается и переходит в конформацию “статистического клубка”.
· Конформация "клубок"
Представляет собой хаотично свернутую цепь:
 |
Клубок постоянно меняет свою форму за счет теплового движения.
Эта конформация может реализовываться и в растворе и в твердом теле.
Содержание полимера в клубке мало (около 5%), т.е. он является рыхлым (в промежутках находится растворитель или фрагменты других макромолекул)
Клубки имеют размер около 300-500 А˚.
· Конформация "глобула"
Представляет собой плотно заполненную атомами частицу, образующими в ней макромолекулу. Содержание полимера значительно выше, чем в клубке:
 |
Полимерные образования в "хорошем" растворителе (т.е. в котором взаимодействие между частицами растворителя и полимером больше, чем между частицами растворителя) находятся в виде набухших клубков, в "плохом" – степень набухания клубков уменьшается.
· Конформация "спираль"
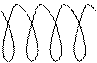 |
Представляет собой вытянутую спираль,
Характерна для биополимеров и для многих полимеров в кристаллическом состоянии.
Вопросы для самостоятельной проработки:
1. Какими основными параметрами характеризуются макромолекулы полимеров?
2. Назовите причины полидисперсности полимеров.
3. Какие существуют способы усреднения молекулярных масс макромолекул полимеров?
4. Чем отличается дифференциальное молекулярно-массовое распределение от интегрального распределения?
5. Перечислите виды конфигурационной изомерии макромолекул.
6. Какие виды конформации макромолекул полимеров Вы знаете?
Задачи для самостоятельного решения
1. Основные понятия и определения химии и физики полимеров
1.3. Понятие о конфигурации. Виды конфигурационной изомерии макромолекул
Вопросы 3501 – 3505, 3516 – 3520, 3406 – 3411, 3421 – 3423, 3312 – 3315, 3324 – 3326
1.4. Молекулярно-массовые характеристики полимеров
Вопросы 4501 – 4503, 4518 – 4521, 4404 – 4405, 4411 – 4413, 4416, 4422 – 4423, 4306 – 4310, 4314 – 4315, 4317
1.5. Дифференциальные и интегральные функции ММР
Вопросы 5501 – 5506, 5407 – 5414, 5315 - 5316
Раздел №4. Элементы, способные к образованию полимеров
Молекула полимера состоит из ряда связанных в цепь атомов:
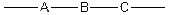
Рассмотрим, какие элементы Периодической системы Д. И. Менделеева (ПС) способны к образованию полимерных цепей.
Кислород, сера, селен
Атомы кислорода не способны к образованию длинных линейных цепочек; они способны образовывать лишь перекиси в виде 2-4 атомов кислорода,
Rn – O – O – Rm, соединенных в единую цепь, но и эти соединения являются малоустойчивыми.
Однако, единичные атомы кислорода могут встраиваться в цепи, образованные атомами других элементов (C, P, S, Si) (см. ниже).
Атомы серы способны соединяться между собой в протяженные линейные цепи, особенно при повышенных температурах, но эти цепи при охлаждении разрушаются.
Этот эффект давно известен как обратимый переход ромбической серы в пластическую серу.
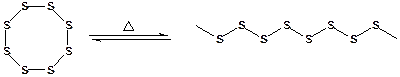
ромбическая сера пластическая сера
При понижении температуры пластическая сера превращается в кристаллическую (ромбическую) серу.
Полимеры, содержащие в главной цепи только атомы серы, не устойчивы и не имеют практического значения. Серосодержащие фрагменты с 1, 2 или несколькими атомами серы устойчивы и входят в состав ряда полимеров.
Аналогичными свойствами облают Se и Te.
Азот, бор, алюминий
Эти элементы не образуют длинных линейных цепочек и не способны к образованию собственных полимеров.
Азот способен к образованию азосоединений с участием лишь двух атомов азота −N=N−.
Азот, бор, алюминий могут быть элементами макромолекулярных цепочек в других составных частях полимерной структуры, либо входить как гетероатомы в основную цепь.
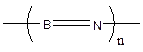
Углерод
Обладает высокой склонностью к образованию прочных ковалентных связей, как между собственными атомами, так и с другими атомами.
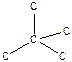 - структура алмаза
- структура алмаза
Это жесткая, разветвленная, 3-х мерная структура, полностью лишенная свойств, присущих линейным макромолекулам.
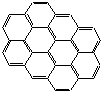 - двухмерная углерод-углеродная структура графена, графита и сажи
- двухмерная углерод-углеродная структура графена, графита и сажи
Возможно получение и линейной цепи из атомов углерода:
 - структура карбина
- структура карбина
или

При нагревании он превращается в графит.
Гораздо большие возможности по построению линейных макромолекул из атомов углерода открываются, когда 1 или 2 валентности углерода насыщаются другими атомами или группами.
Примеры:
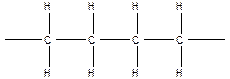 - полиэтилен
- полиэтилен
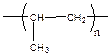 - полипропилен
- полипропилен
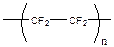 - политетрафторэтилен
- политетрафторэтилен
Также в составе основной цепи могут находиться различные группировки, содержащие гетероатомы:
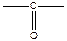 - карбонильная группировка
- карбонильная группировка
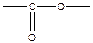 - сложно-эфирная группировка
- сложно-эфирная группировка
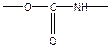 - уретановая группировка
- уретановая группировка
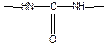 - карбамидная ( мочевинная) группировка
- карбамидная ( мочевинная) группировка
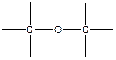 - простая эфирная или ацетальная группировка
- простая эфирная или ацетальная группировка
В составе цепи могут находиться и атомы металлов:
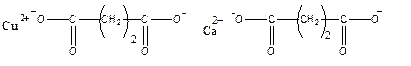
Кремний
Атомы кремния способны образовывать полимерные цепи:
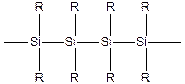
Но они химически не очень устойчивы и при окислении кремний связывается с кислородом, образуя очень прочные связи кремний-кислород.
В природе кремний встречается в виде кварца:
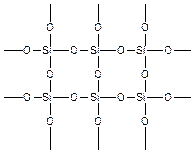
Это жесткая трехмерная структура, не проявляющая «полимерных» свойств линейных макромолекул. Линейные макромолекулы получают, заместив две валентности у каждого атома кремния на органические радикалы (CH3-, C2H5- и т. д.). При этом появляются кремний-органические полимеры.
Можно синтезировать кремнийсодержащие полимеры:
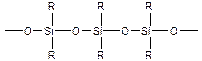 - полисилоксаны
- полисилоксаны
В цепь могут встраиваться атомы Al, B, Ti, Zn и некоторые другие.
Фосфор
Атомы фосфора могут образовывать полимеры, но в состав основной цепи должны входить и другие атомы (чаще всего кислород):
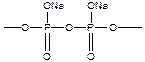 - полифосфаты
- полифосфаты
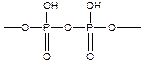 - полифосфорная кислота
- полифосфорная кислота
Остатки ортофосфорной кислоты входят в природные полимеры (нуклеиновые кислоты, ДНК и РНК):
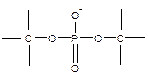
Таким образом, двух или поливалентные атомы (C, O, P, N, S, Si, Al, B и некоторые другие) могут находиться в виде элементов основной цепи макромолекул или находиться в боковых фрагментах; одновалентные атомы (H, F, Cl, J, Br и некоторые другие) могут выстраиваться только в качестве заместителей.
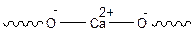
Химия полимеров построена на базе этих элементов.
Виды полимеров
Полимеры получают либо синтетически, либо извлекают из живых организмов (биополимеры), или же обработкой уже выделенных природных полимеров.
Далее будут рассмотрены синтетические способы получения полимеров.
Часть синтетически созданных полимеров существует в природе. Полимеры получаются из мономеров – низкомолекулярных веществ или в результате превращений готовых полимеров (синтетических или природных) – полимераналогичные превращения.
Примеры:
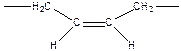
- 1,4-цис-полибутадиена в природе не существует, получают синтетически из бутадиена.
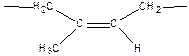
- 1,4-цис-полиизопрен существует в природе (натуральный каучук), но в природе синтезируется из глюкозы и других веществ (но не из изопрена, как в промышленности)
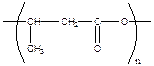
- этот полиэфир можно получить конденсацией поли-β-гидроксибутирата, в то же время он синтезируется и рядом бактерий.
Синтезы биополимеров в данном курсе рассматриваться не будут.
Многие природные полимеры очень сложно получить синтетически. Они получаются в живых организмах в результате протекания сложных биохимических реакций.
Важнейшие природные полимеры:
· Целлюлоза (является строительным материалом клеток всех растений)
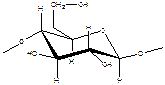
Молекула построена из соединенных между собой глюкозидными связями остатков глюкозы, образуется при фотосинтезе в растениях.
· Молекулы белков построены из соединенных между собой пептидными связями остатков 20 различных α-аминокислот. Порядок расположения аминокислотных звеньев определяется генетическим кодом.
Например:
· Белки
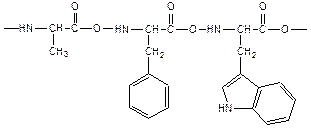
фенилаланин триптофан
· Нуклеиновые кислоты
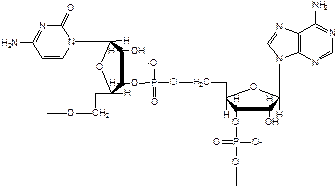
Молекулы построены из соединенных фосфорэфирными связями остатков сахаров (рибозы или дезоксирибозы) с химически присоединенными азотистыми основаниями. Порядок чередования оснований задает генетический код.
Рост цепи
Рост цепи протекает по следующей схеме:
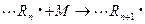
1) Присоединение растущей цепи к мономеру может осуществляться различными способами:
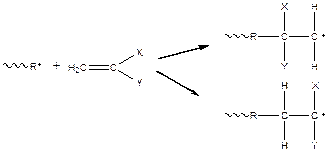
X, Y – заместители
В приведенном случае большое значение имеет сопряжение концевой группы R с атомами водорода или заместителями. В первом случае возможны стерические затруднения, если заместители и концевая группа имеют достаточно большой объем. Во втором случае присоединения происходит больший выигрыш энергии.
Из-за приведенной выше причины присоединение по типу "голова-хвост-голова-хвост" идет предпочтительней, чем "голова-голова-хвост-хвост". Только в случае, когда имеем маленькие заместители (или сопряжение мало) возможно образование структур "голова-голова-хвост-хвост". Подобное присоединение обнаруживается в случае мономеров с мало сопряженными и не создающими стерических затруднений заместителями (например, винилацетат). 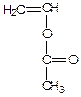
Структура «голова-голова» и в поливинилацетате и в получаемом из него поливиниловом спирте являются химическими дефектами, ухудшающими свойства полимера. Их количество в цепях растет с повышением температуры полимеризации.
2) При наличии нескольких мономеров может происходить сополимеризация, т.е. полимеризация, в результате которой образуется полимер, состоящий как из звеньев, образованных одним мономером, так и из звеньев, образованных другими мономерами.
3) Стереорегулярность.
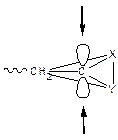 Как исходный мономер, так и концевое звено (конец растущего радикала) имеют плоскую конформацию, т.е. не имеют определенной пространственной конфигурации. При присоединении следующей молекулы мономера, т.е. при удлинении цепочки в этом звене создается псевдоасимметрический атом углерода.
Как исходный мономер, так и концевое звено (конец растущего радикала) имеют плоскую конформацию, т.е. не имеют определенной пространственной конфигурации. При присоединении следующей молекулы мономера, т.е. при удлинении цепочки в этом звене создается псевдоасимметрический атом углерода.
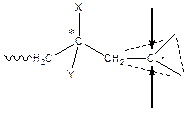 Как это происходит? Мономер может "атаковать" радикал с любой стороны, и при этом образуются или R- или S- стереоизомеры. Если бы радикал присоединял мономер только с «одной стороны», то образовывался полимер стереорегулярного строения. В этом случае образуются изотактические полимеры со строго упорядоченной структурой RRRRRR или SSSSSS.
Как это происходит? Мономер может "атаковать" радикал с любой стороны, и при этом образуются или R- или S- стереоизомеры. Если бы радикал присоединял мономер только с «одной стороны», то образовывался полимер стереорегулярного строения. В этом случае образуются изотактические полимеры со строго упорядоченной структурой RRRRRR или SSSSSS.
Если атака мономера реализуется регулярно то с одной, то с другой стороны, то образуется синдиотактический полимер, т.е. полимер с чередующимся строением RSRSRS.
Если присоединение происходит хаотично, то и звенья R- и S- входят в цепь беспорядочно, и образуются атактические полимеры RSRRSSRSSR.
Рассмотрим радикальную полимеризацию дивинилового мономера.
При атаке молекулы радикалом образуется следующая структура:
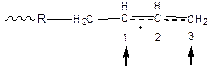
Эта структура является аллильным радикалом, в котором электронная плотность неспаренного электрона распределена примерно поровну между 1 и 3 атомами углерода. В зависимости от направления атаки (1 или 3 атом углерода) и строения переходного комплекса осуществляется 1,2-присоединение и 1,4-присоединение, образование цис- и транс-структур, изо-, синдио- или атактических полимеров.
Чаще всего полимеры, полученные радикальной полимеризацией, нестереорегулярны.
Обрыв цепи
Обрывом цепи называется реакция гибели активного центра.
Обрыв цепи может происходить по различным механизмам.
1. Бимолекулярный обрыв цепи
Бимолекулярный обрыв цепи – это реакция взаимодействия двух растущих макрорадикалов между собой:
 - рекомбинация
- рекомбинация
или
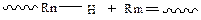
- диспропорционирование
Скорость реакции обрыва зависит от концентрации радикалов в системе:
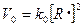 (8.2.1)
(8.2.1)
Рассмотрим факторы, влияющие на константу обрыва.
Скорость процесса определяется диффузией, т.е. в отличие от других реакций радикальной полимеризации, которые являются кинетически контролируемыми реакциями, реакции бимолекулярного обрыва являются диффузионно-контролируемыми. Макрорадикалам нужно сблизиться и развернуться в нужном направлении (2 стадии).

Лимитирующей стадией является не поступательная диффузия клубка, а диффузия конца цепи. Таким образом, константа обрыва в разбавленных растворах полимера не зависит от длины цепи.
Суммарная скорость реакции обрыва выражается следующим образом:
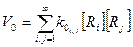 (8.2.2)
(8.2.2)
Константа обрыва является большой величиной: k0≈107÷108, реакция протекает быстро.
В области высоких конверсий, когда реакционная среда фактически является концентрированным раствором полимера, скорость бимолекулярного обрыва резко падает и становится зависящей от длины макрорадикала.
При этом наблюдается резкое ускорение полимеризации, получившее название гель-эффекта:


 Vp М
Vp М
 - область гель-эффекта
- область гель-эффекта

 - период стационарной скорости
- период стационарной скорости
100 q, %
q – степень превращения
Рис. 8.2.1. Гель-эффект
При этом существенно возрастает и молекулярная масса образующегося полимера. Интенсивность гель-эффекта зависит от физико-химических свойств концентрированных растворов полимеров в собственном мономере.
2. Ингибирование
В этом случае обрыв происходит в результате взаимодействия растущего радикала с низкомолекулярным соединением:
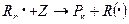
Низкомолекулярное соединение, которое, взаимодействуя с макрорадикалами, приводит к их гибели, называется ингибитором.
К ингибиторам могут относиться следующие классы веществ:
а) стабильные радикалы
Примеры:
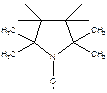 -N-оксидный радикал (в этом случае важно, чтобы объемные группы защищали от соединения двух N-оксидных радикалов).
-N-оксидный радикал (в этом случае важно, чтобы объемные группы защищали от соединения двух N-оксидных радикалов).
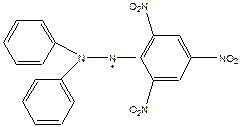
- дифенилпикрилгидразин
б) ароматические многоядерные молекулы
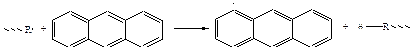
-образуется малоактивный радикал
в) хиноны
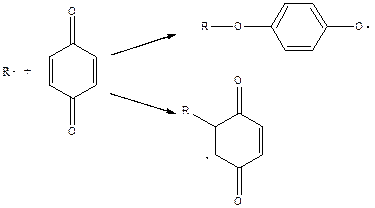
г) нитросоединения
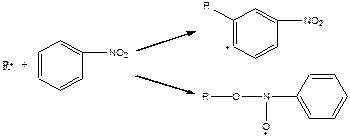
д) нитрозосоединения
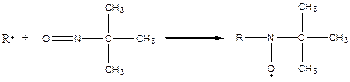
образовавшийся в результате реакции аддукт очень стабилен.
е) ионы переменных валентностей, образованные атомами в высоких степенях окисления (Fe3+, Cu2+).
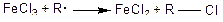

ж) некоторые элементы
О2, S, J2
Кислород:
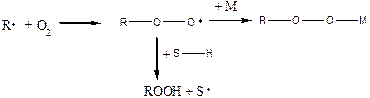
В последнем случае реакция может пойти в двух направлениях: может идти реакция с отрывом водорода и может идти реакция присоединения мономера к R-O-O• радикалу, если мономер достаточно активен. В этом случае получаются полимерные перекиси, образуется нестабильный полимер (по этой причине реакции радикальной полимеризации желательно проводить без доступа воздуха – работать либо в среде инертного газа, либо под вакуумом). В некоторых процессах кислород используется в строго дозирующихся количествах, например, в производстве полиэтилена для инициирования процесса и регулирования ММ образующегося полимера.
Сера:
Под действием радикала сера способна раскрывать свой цикл
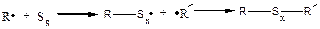
образуется сополимер, содержащий серу
Йод:

образуются йодалкилы и радикалы йода, которые могут далее атаковать мономер или рекомбинировать.
Передача цепи
Передача цепи происходит по следующему механизму:
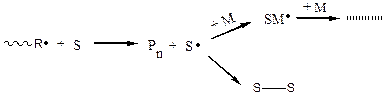
Далее может идти реакция гибели радикалов (рекомбинации), либо в присутствии мономера реакция, называемая реакцией передачи цепи (на схеме – верхняя реакция).
В результате скорость процесса не меняется, т. к. количество радикалов в системе не меняется, но происходит снижение молекулярной массы полимера; этим методом можно уменьшать (регулировать) молекулярные массы образующихся полимеров.
Примером соединений, способных к передаче цепи, являются соединения, имеющие подвижные атомы водорода:
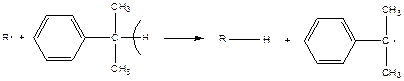
- происходит отщепление атомов водорода с образованием устойчивых радикалов.
В роли подобных соединений могут выступать и сами мономеры:
|
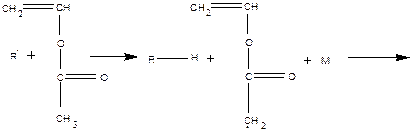
активный радикал
|
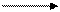
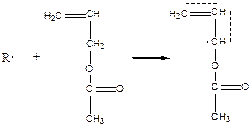 - происходит образование стабильного аллильного радикала. Образующийся радикал (1) далее вступает в реакцию (самопередача цепи). Если же, как, например, в случае аллилацетата (2), радикал малоактивен и практически не вступает в реакцию с новой молекулой мономера. Это называется деградационной передачей цепи.
- происходит образование стабильного аллильного радикала. Образующийся радикал (1) далее вступает в реакцию (самопередача цепи). Если же, как, например, в случае аллилацетата (2), радикал малоактивен и практически не вступает в реакцию с новой молекулой мономера. Это называется деградационной передачей цепи.
Передача цепи идет и в реакции с меркаптанами:

Эта реакция идет с высокой эффективностью, и, введением малых количеств передатчика удается понижать (регулировать) молекулярную массу полимеров.
С помощью некоторых передатчиков цепи можно синтезировать новые соединения с определенными концевыми группами (теломеры). Примером служит полимеризация в присутствии ССl4:
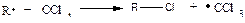
Далее радикалы вступают в реакцию, получаем олигомеры (теломеры) состава CCl3(M)nCl, длину которых можно варьировать. Гидролизом полученных соединений можно получать ценные продукты состава
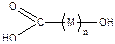 .
.
Таким образом, можно получать соединения с определенными концевыми группами и имеющими определенную длину.
Таблица 9.2.1.
Примеры полимеризации различных ненасыщенных мономеров
| Мономер | Тип инициирования | ||
| Радикальный | Анионный | Катионный | |
| 1. Этилен | + | + | + |
| 2. 1-Алкилолефины (α-олефины) (пропилен) | - | - | + |
| 3. 1,1-Диалкилолефины (изобутилен) | - | + | * |
| 4. Диены-1,3 (бутадиен, изопрен) | + | + | + |
| 5. Стирол, α-метилстирол | + | + | + |
| 6. Галогениро-ванные олефины (винилхлорид, винилиденхлорид) | + | - | - |
| 7. Сложные виниловые эфиры (винилацетат CH2 = CHOCOR) | + | - | - |
| 8. Акрилаты, метакрилаты | + | + | - |
| 9. Акрилонитрил, метакрилонитрил | + | + | - |
| 10. Акриламид, метакриламид | + | - | - |
| 11. Простые виниловые эфиры (винилэтиловый эфир) | - | - | + |
12. N-Винилкарбазол
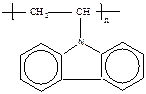
| + | - | + |
13. N-Винилпирролидон
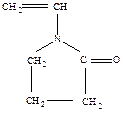
| + | - | - |
| 14. Альдегиды, кетоны | - | + | + |
2. Активные центры (ионы) могут существовать в процессах ионной полимеризации в различных формах:
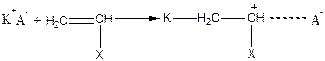
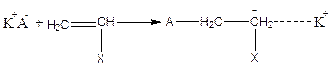
на конце наряду с ионом находится противоион, образуется ионная пара – (карбкатион + анион) или (карбанион + катион).
Могут существовать различные варианты взаимодействия карбкатиона и аниона. Если взаимодействие сильное, то образуется ионная пара: К+А-
При введении полярного растворителя можем получить сольватно-разделенную ионную пару или разделенные ионы:
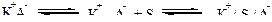 - сольватно-разделенная пара
- сольватно-разделенная пара
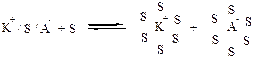 - разделенные ионы
- разделенные ионы
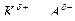

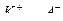

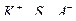

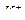
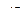
где S – молекула растворителя,
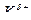
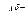 - поляризованная связь,
- поляризованная связь,
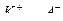 - контактная ионная пара,
- контактная ионная пара,
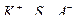 - сольватно-разделенная ионная пара,
- сольватно-разделенная ионная пара,
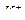
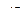 - свободные ионы.
- свободные ионы.
В реакциях радикальной полимеризации рост цепи не зависит от инициирующего радикала, а зависит только от реакционной способности мономера и радикала, в ионной полимеризации на протекание процесса влияет как реакционная способность молекулы мономера, так и состояние активного центра роста цепи.
Ионная полимеризация обычно протекает очень быстро (иногда реакция может пройти за несколько секунд). Это является как следствием высокой константы роста цепи, так и высокой концентрации активных центров вследствие отсутствия бимолекулярного обрыва цепи.
3) Инициаторы ионной полимеризации не только формируют активные центры, но и оказывают существенное влияние на константы роста цепи, на строение цепей, на обрыв цепи.
4) Кинетика ионной полимеризации и строение образующихся полимеров сильно зависят от природы среды. Обычно чем больше полярность среды, тем выше скорость процесса.
В радикальной полимеризации среда практически не влияет на скорость полимеризации, влияет лишь на ММ образующегося полимера.
Ионная полимеризация может протекать как в полярной, так и в неполярной среде.
Многие реакции ионной полимеризации протекают без обрыва кинетической и материальной цепи, могут образовываться т. н. "живые" полимеры.
При этом можно получать полимеры с узким ММР, количество цепей определяется количеством добавленного катализатора. Таким образом, возможно получение практически монодисперсных полимеров. Добавлением другого мономера можно получать блок-сополимеры.
5) Энергия активации обычно ниже, чем для радикальной полимеризации. Многие реакции имеют отрицательный температурный коэффициент (т. е. с понижением температуры скорость реакции может увеличиваться).
6) Для многих процессов ионной полимеризации характерно образование полимеров, имеющих регулярное и стереорегулярное строение.
Катионная полимеризация
В процессе катионной полимеризации инициатором процесса являются катионы. Поэтому в процесс вступают мономеры с кратной связью С=С, имеющие избыточную электронную плотность на двойной связи,
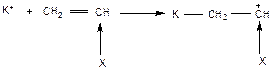
Образующийся катион стабилизируется электронодонорным действием заместителя и сопряжением с ним. Поэтому активными мономерами в катионной полимеризации будут:
изобутилен
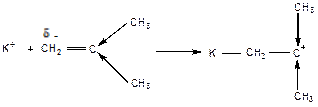
стирол
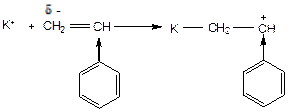
α-метилстирол
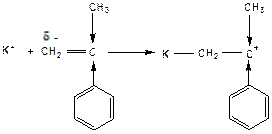
виниловые эфиры
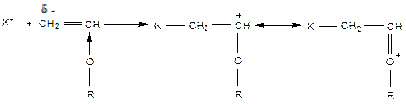
Не полимеризуются мономеры с электроно-акцепторными заместителями 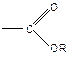 ,
, 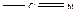 ,
, 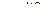 или в тех случаях, когда атака катиона направляется не на двойную связь, а на другую группу, например
или в тех случаях, когда атака катиона направляется не на двойную связь, а на другую группу, например
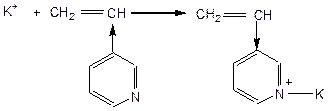
В процесс катионной полимеризации также вступают соединения с кратными связями 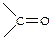 ,
, 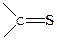 ,
, 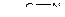 .
.
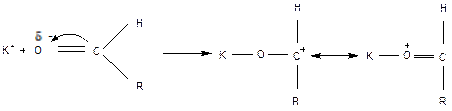
Образующийся катион стабилизируется вследствие наличной резонансной структуры «ониевого»
типа
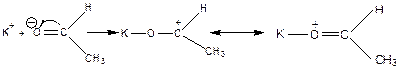
Не полимеризуются 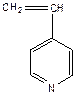 ,
, 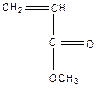
В катионную полимеризацию вступают большое количество циклических мономеров.
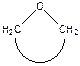
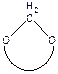
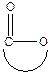
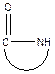
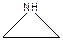
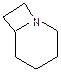
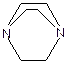
окиси циклически ацетали лактоны лактамы имины циклические амины
циклические эфиры
Могут существовать различные варианты атаки катиона на молекулу мономера:
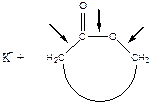
Чтобы определить место атаки катиона, необходимо сравнить стабильность образующихся продуктов. Это поможет определить строение получающегося полимера.
В случае лактона местом атаки является атом 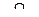 .
.
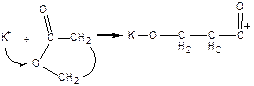
После раскрытия цикла образуется стабильный катион, способный атаковать следующие молекулы мономера с раскрытием цикла.
В случае циклических ацеталей:
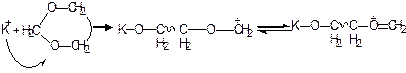
Стабилизация катиона, получаемого после раскрытия цикла, согласно вышеприведенной схеме, осуществляется благодаря тому, что его можно рассматривать как оксониевый ион.
В случае циклических эфиров и окисей олефинов, тиоэфиров и циклических иминов:
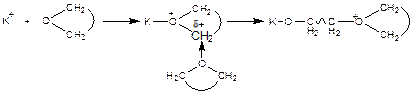
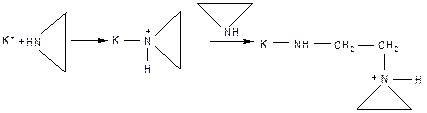
Стабилизированной формой является ониевый (оксониевый) или аммониевый катион. Рост цепи осуществляется при его атаке следующей молекулой мономера с регенерацией ониевого катиона.
Полимеризуются по катионному механизму и полициклические мономеры.
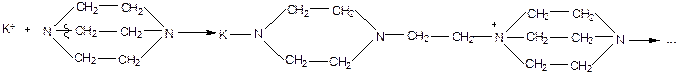
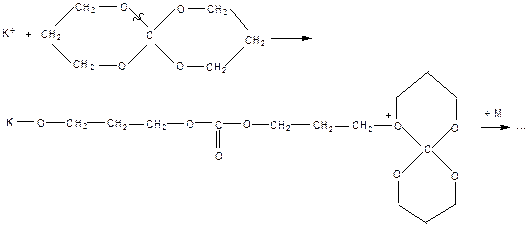
Кислоты Льюиса
Рассмотрим реакцию на примере получения полиизобутилена.
Мономером является изобутилен:
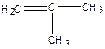
Рост цепи протекает следующим образом:
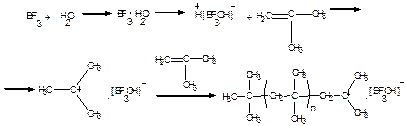
Ониевые соли
Ониевые соли R3O+X-, R4N+X- являются активными центрами полимеризации гетероциклических мономеров и могут использоваться как инициаторы их полимеризации. Соли арилиодония R2I+X- могут служить инициаторами катионной фотополимеризации, генерируя в процессе фотораспада сильную протонную кислоту:
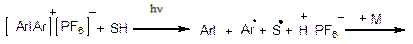 полимеризация
полимеризация
Влияние природы среды
Чем больше полярность среды, тем выше степень разделения ионов и выше скорость процесса.
В таблице 9.3.4.1. отражено влияние различных сред на скорость протекания полимеризации α-метилстирола под действием системы SnCl4•H2O:
Таблица 9.3.4.1.
Влияние различных сред на скорость протекания полимеризации α-метилстирола под действием SnCl4•H2O
| Растворитель | Диэлектрическая проницаемость среды, ε | Относительная скорость полимеризации |
| Циклогексан | 1,9 | 1 |
| Дихлорэтан | 10 | 2,6 |
| Нитроэтан | 28 | 16,3 |
| Нитробензол | 36 | 120 |
Таким образом, среда является эффективным регулятором процесса ионной полимеризации.
Среди важнейших полимеров, получаемых с помощью катионной полимеризации, можно выделить полиизобутилен (благодаря плохой газопроницаемости этого полимера, его часто применяют в производстве различных камер) и бутилкаучук, а также сополимеры триоксана и этиленоксида, поливинилизобутиловый эфир.
Вопросы для самостоятельной проработки:
1. Дайте определение ионной полимеризации. Назовите ее общие черты с радикальной полимеризацией.
2. Какие особенности характерны для процессов ионной полимеризации по сравнению с радикальной полимеризацией?
3. Назовите мономеры, которые полимеризуются по катионному механизму.
4. Перечислите типы инициаторов (катализаторов) катионной полимеризации. Приведите примеры соответствующих реакций.
5. От чего зависит степень полимеризации при катионной полимеризации?
6. Как влияет природа среды на скорость катионной полимеризации?
Задачи для самостоятельного решения
3. Методы получения и структура основных типов полимеров
3.1. Виды полимеризации. Инициирование и ингибирование полимеризации
Вопросы 1406 – 1407, 1316 – 1319
Слабые основания
H2O, NH3, NR2H
Эти инициаторы способны активизировать ограниченное количество мономеров, способных вступать в реакции анионной полимеризации (например, цианакрилаты).
Основания средней силы
К этой группе относятся соединения, имеющие карбоксильную группу, аминогруппу (-NH2), алкоголяты щелочных металлов, гидроксиды щелочных металлов.
Эти инициаторы способны вступать в реакции анионной полимеризации со стиролом, метакрилатами, акрилонитрилом.
Сильные основания
Алкилы щелочных или щелочноземельных металлов.
Эти инициаторы способны вступать в реакцию анионной полимеризации даже с изопреном.
Остановимся подробнее на сильных основаниях.
Противоионами могут выступать ионы Li, Na, K, Rb, Cs, Са, Mg, Zn или Al.
Металлорганические соединения этих элементов довольно устойчивы, способны диссоциировать, давая свободные ионы или образуя ионные пары К+Х-:

В отсутствие ингибиторов (см. ниже) реакции гибели нуклеофильных активных центров не происходит, поэтому подобные инициаторы приводят к образованию т. н. "живых цепей".
Часто в качестве инициатора анионной полимеризации используют бутиллитий - С4H9Li.
Возможно использовать в качестве возбудителей щелочные и щелочно-земельные металлы. Такая возможность обусловлена тем, что атомы металлов легко отщепляют электроны, образуя стабильные частицы (ионы):
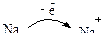
В качестве акцептора электрона могут выступать аммиак, ароматические соединения, а также непосредственно мономеры. Например, натрий в бескислородном растворителе с нафталином образует натрийнафталиновый комплекс с голубой окраской:
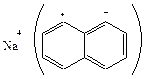
Этот комплекс легко отдает электрон мономеру, давая соответствующий анион-радикал M∙-, последние быстро рекомбинируют, образуя дианионы:
2М∙- → -ММ-
При участии дианионов цепь растет в оба конца.
В случае бутадиена реакцию можно записать следующим образом:

Видно, что при инициировании щелочными металлами образование металлорганических соединений происходит непосредственно в реакционной системе и при этом образуются дианионы, способные вести дальнейшее присоединение молекул мономера в обоих направлениях.
Можно использовать также для полимеризации трианионы, тетраанионы, полианионы, при этом образуются звездообразные макромолекулы с тремя, четырьмя и более лучами.
При замене ионы металла на ионы водорода, т. е. при реакции с соединениями, содержащими подвижный протон, образуется ковалентная связь С–Н и реакция прекращается.
Существуют основания, не имеющие заряда, но при их реакции с мономером заряд образуется. Примером может являться реакция образования бетаинов при инициировании триалкилфосфином:
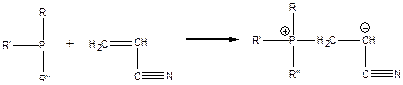
Рассмотрим влияние инициаторов анионной полимеризации на различные циклические мономеры.

- этиленоксид легко полимеризуется с большинством инициаторов анионной полимеризации (RO-, HO-, R-, -COO-, и т. д.), по механизму «живых цепей» образуя полимер с достаточно узким ММР ( 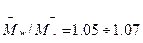 ), степень полимеризации определяется как отношение концентрации мономера в системе к концентрации инициатора:
), степень полимеризации определяется как отношение концентрации мономера в системе к концентрации инициатора:
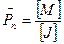 (10.2.1)
(10.2.1)
Также хорошо вступает в реакцию пропиленоксид. Можно получать этим методом двух и трехблочные сополимеры полиоксиэтилена и полиоксипропилена с различными значениями ГЛБ (ГЛБ определяет состав полученного сополимера).
Этим методом можно получать полиэтиленсульфид, полипропиленсульфид.
Легко идет реакция с лактоном пропионовой кислоты:
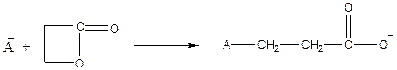
Хорошо также полимеризуются лактид молочной кислоты (лактон), гексаметилсилоксан.
При реакции с участием N-карбоксиангидридов α-аминокислот можно получать полипептиды:
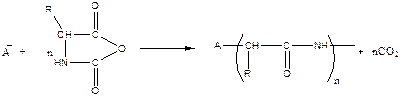
Реакции роста цепи
Реакция роста цепи может протекать с участием всех форм существования активных центров (ассоциаты металлорганических соединений (МОС) ↔ мономерная форма МОС ↔ контактные ионные пары ↔ сольватно-разделенные ионные пары ↔ свободные ионы). Отсутствие гибели активных центров позволяет определить вклад каждой из форм активного центра в суммарную скорость роста цепи. Так при полимеризации стирола константа скорости роста с участием свободного иона составляет примерно 104-105 л•моль/с (для сравнения константа скорости на ионных парах и в радикальной полимеризации составляет примерно 102 л•моль/с, т.е. свободный ион значительно активнее, чем ионная пара или свободный радикал). Поэтому даже при низких концентрациях свободных ионов их вклад в реакцию роста может быть значительным.
Катализаторы Циглера-Натта
Для стереорегулирования наиболее эффективными оказались катализаторы, названные катализаторами Циглера-Натта (по именам открывших и исследовавших их ученых).
Эти катализаторы представляют собой смеси ряда металлоорганических соединений (алюминийсодержащих, магнийсодержащих, цинксодержащих и некоторых других) с хлоридами некоторых переходных элементов (используются соединения d-элементов).
Наиболее известной системой является AlR3·TiCl3, где на поверхности кристалла TiCl3 образуется его комплекс (соединение) с AlR3, который является активным центром полимеризации. В случае пропилена (наиболее практически важный случай) можно получить изотактический полипропилен. Механизм процесса можно представить схемой: 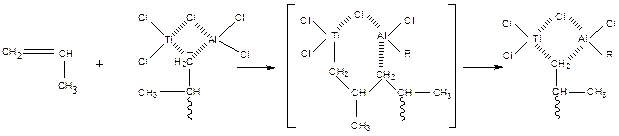
Пропилен полимеризуется с высокими скоростями с образованием изотактического полипропилена. По такому же механизму образуется линейный высокомолекулярный полиэтилен низкого давления.
Было обнаружено, что катализаторы Циглера-Натта позволяют получать целый ряд стереорегулярных полимеров. Один и тот же мономер в присутствии разных катализаторов полимеризуется с образованием различных продуктов. Например, при использовании разных катализаторов при полимеризации бутадиена можно наблюдать следующую картину:
Таблица 11.2
Строение бутадиена при использовании различных катализаторов
| Катализатор | Содержание изомеров, % масс. | |||
| Цис- | Транс- | 1,2- | 3,4- | |
| AlR3-TiCl4 | 96 | - | 0 | 4 |
| AlR3-Ti(OR)4 | 0 | 100 | 0 | 0 |
| AlR3-V(AсAс)3 (ацетилацетонат) | 0 | 0 | 0 | ~100 |
Т.е. варьируя структуру катализатора, можно получать полибутадиен различного строения.
Найдены и другие координационно-ионные катализаторы, позволяющие получать стереорегулярные полимеры. Примером могут быть соединения Ni, образующие π-комплексы с двойными связями диена и концом растущей цепи (π-аллильные комплексы).
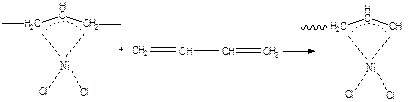
Специальным видом координационно-ионной полимеризации следует считать реакции, катализируемые соединениями вольфрама и некоторых других элементов. Эти соединения оказались активными в реакциях метатезиса олефинов. В случае циклоолефинов они вызывают полимеризацию с образованием полимеров, сохраняющих степень ненасыщенности исходных циклических мономеров. Это означает, что под действием катализатора рвутся сразу две связи 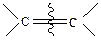 .
.
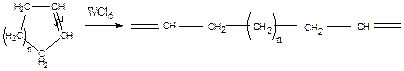
Предполагается, что активными центрами являются стабилизированные комплексообразованием карбены.
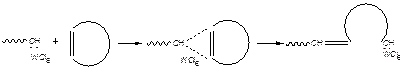
Вопросы для самостоятельной проработки:
1. Какие соединения являются возбудителями координационно-ионной полимеризации?
2. Возможно ли получение структур с определенным пространственным строением методом координационно-ионной полимеризации?
3. Какие катализаторы относятся к катализаторам Циглера-Натта? В чем их особенность?
Задачи для самостоятельного решения
3. Методы получения и структура основных типов полимеров
3.1. Виды полимеризации. Инициирование и ингибирование полимеризации
Вопрос 1319
3.4. Ионная и ионно-координационная полимеризация
Вопросы 4501 – 4503, 4404 – 4409, 4310 - 4315
Раздел №12. Сополимеризация
Радикальная сополимеризация
Радикальную сополимеризацию обычно инициируют теми же способами, что и радикальную гомополимеризацию. Для неё, в принципе, характерны те же механизмы роста, обрыва и передачи цепи. Рассмотрим сополимеризацию двух мономеров. Предполагая, что активность радикалов роста определяется лишь типом концевого звена, следует учитывать четыре элементарные реакции роста:
Таблица 12.1.1.
Элементарные реакции роста цепи

где Мi — мономер i-ого типа; ~R∙ j — макрорадикал, оканчивающийся звеном Mj, а kij — константа скорости присоединения Мj мономера к радикалу ~R∙ i. Рассматриваемая модель получила название "модель концевого звена" сополимеризации. Кинетическая обработка приведенной реакционной схемы в квазистационарном приближении позволяет установить связь между составом сополимеров и составом исходной смеси мономеров. В квазистационарном состоянии концентрации радикалов ~R∙ 1 и ~R∙ 2 постоянны, т.е. скорости перекрестного роста цепи равны между собой:

(12.1.1)
Скорости превращения мономеров при сополимеризации описываются уравнениями:

(12.1.2)
Из отношения скоростей этих реакций с учетом условия стационарности для концентраций радикалов (12.1.1) несложно получить следующее выражение, обычно называемое уравнением Майо-Льюиса, характеризующее на начальных стадиях превращения, когда без большой ошибки можно положить концентрации мономеров [M1] и [M2] величинами постоянными, зависимость состава получаемого сополимера от состава мономерной смеси:
 (12.1.3)
(12.1.3)
 |  |
где , а так называемые константы сополимеризации. Они представляют собой отношения констант скоростей присоединения к данному радикалу "своего" и "чужого" мономеров. Значение r1 и r2 зависят от химической природы реагирующих мономеров.
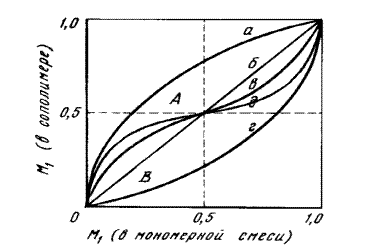
Рис. 12.1.1. Зависимость состава сополимера от состава смеси мономеров.
Зависимость состава сополимеров от состава смеси мономеров удобно характеризовать диаграммой "состав мономерной смеси - состав сополимера" (рис. 12.1.1.). Форма кривых на диаграмме составе зависит от значений r1 и r2. При этом возможны следующие случаи: 1) r1=r2=1, т.е. для всех соотношений концентраций мономеров в реакционной смеси состав сополимера равен составу исходной смеси (прямая б), 2) r1>1 и r2<1, т.е. для всех соотношений концентраций мономеров в исходной смеси сополимер обогащен звеньями М1 (кривая а), 3) r1<1 и r2>1, т.е. для всех исходных соотношений концентраций мономеров сополимер обогащен звеньями М2 (кривая г), и наконец, 4) r1<1 и r2<1, т.е. при малых содержаниях M1 в исходной смеси мономеров сополимер обогащен звеньями М1, а при больших — звеньями M2 (кривые в и д). В последнем случае наблюдается склонность к чередованию в сополимере звеньев М1 и М2, которая тем больше, чем ближе к нулю значения r1 и r2. Случай r1>1 и r2>1, которому должна соответствовать тенденция к раздельной полимеризации мономеров в смеси, обычно на практике не реализуется.
Величины r1 и r2 могут быть определены экспериментально. Знание их позволяет предсказать состав сополимера и распределение мономерных звеньев в цепях при любом соотношении мономеров в смеси. Значения r1 и r2 при радикальной сополимеризации и, следовательно, состав сополимера обычно слабо зависят от природы растворителя и очень мало меняются с температурой.
Рассмотрение величин r1 и r2 в рамках теории идеальной радикальной реакционной способности приводит к заключению, что r1*r2=1, т.е. константы скоростей присоединения одного из мономеров к обоим радикалам в одинаковое число раз больше констант скоростей присоединения другого мономера к этим радикалам. Имеется ряд систем, для которых это условие хорошо оправдывается на опыте. В таких случаях мономерные звенья обоих типов располагаются в макромолекулах случайно. Однако для многих систем r1*r2<1. Это отклонение связано с влиянием полярных и пространственных факторов, которые обусловливают тенденцию мономерных звеньев М1 и М2 к чередованию в макромолекулах. В таблице в качестве примеров приведены значения констант сополимеризации и их произведений для некоторых пар мономеров.
Таблица 12.1.2.
Константы радикальной сополимеризации некоторых мономеров.
| М1 | М2 | r1 | r2 | r1r2 |
| Стирол | Бутадиен | 0,80 | 1,40 | 1,12 |
| Стирол | Метилметакрилат | 0,52 | 0,46 | 0,24 |
| Стирол | Винилацетат | 55,0 | 0,01 | 0,55 |
| Стирол | Малеиновый ангидрид | 0,01 | 0 | 0 |
| Винилацетат | Винилхлорид | 0,23 | 1,70 | 0,39 |
| Метилакрилат | Винилхлорид | 9,0 | 0,08 | 0,75 |
12.2. "Схема Q - е" Алфрея – Прайса
Учет полярных факторов был сделан в рамках полуэмпирической схемы, называемой схемой "Q-е", в которой принимают, что
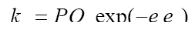 (12.2.1)
(12.2.1)
где Рi и Qj — параметры, соответствующие энергиям сопряжения в мономере (j) и радикале (i), согласно теории идеальной радикальной реакционной способности. Величины еi и еj учитывают поляризацию реагирующих мономеров.
 Тогда:
Тогда:
(12.2.2)
(12.2.3)
Используя эту схему, удалось оценить относительную реакционную способность мономеров и роль полярных факторов для большого числа пар сополимеризующихся мономеров. За стандартный мономер был принят стирол со значениями Q=1, е = −0,8. При сополимеризации стирола с другими мономерами (Mj) последние были охарактеризованы своими значениями Qj и еj, что дало возможность предсказать поведение этих мономеров в реакциях сополимеризации с другими мономерами, для которых также были установлены значения Q и е. Хотя схема "Q-е" не имеет полного теоретического обоснования, с практической точки зрения она оказалась полезной. Значения Q и е большинства мономеров собраны в справочной литературе.
Ионная сополимеризация
В катионной и анионной сополимеризации относительные активности мономеров часто очень сильно отличаются от таковых для радикальной сополимеризации. Поэтому при одинаковом соотношении сомономеров в смеси в зависимости от типа сополимеризации, могут быть получены сополимеры, резко различные по составу.
Таблица 12.3.1.
Влияние механизма реакции на состав продукта сополимеризации эквимолярной смеси стирола с метилметакрилатом
| Катализатор | Тип полимеризации | Содержание стирола в сополимере, % |
| SnCl4 | Катионная | 99 |
| Na | Анионная | < 1 |
| Пероксид бензоила | Радикальная | ≈ 50 |
Изучение зависимости состава сополимера от природы катализатора дает сведения о механизме реакции. В отличие от радикальной сополимеризации, состав сополимеров, о6разующихся при катионной и анионной сополимеризации, зависит от природы растворителя. Особенно сильно эта зависимость проявляется при анионной сополимеризации. Состав сополимеров зависит также от природы противоиона. При ионной полимеризации и сополимеризации в ряде случаев важную роль играет комплексообразование между активным центром и молекулой мономера, предшествующее включению последней в растущую цепь. Продолжительность жизни такого комплекса (т.е. время с момента его образования до включения очередной молекулы мономера в состав макромолекулы) может значительно превышать продолжительность жизни переходного состояния в обычных цепных реакциях (10-13 сек.), т.е. промежуточные комплексы могут оказаться достаточно стабильным. В таких случаях ионную полимеризацию или сополимеризацию называют координационно- ионной.
Условия комплексообразования, состав и строение комплексов зависят от природы растворителя. Возможно, что с этим связана одна из важных причин влияния растворителя на состав сополимеров.
Классификация процессов ПК
В основу классификации процессов поликонденсации могут быть положены различные признаки – структура образующихся продуктов, число и характеристика мономеров, участвующих в реакциях и т. д. В линейной поликонденсации участвуют бифункциональные мономеры, приводящие к получению линейных полимеров. Для проведения сетчатой (трехмерной) поликонденсации необходимо использование мономеров с тремя или большим числом функциональных групп. В этом случае образуются пространственно сшитые полимеры. Выделяют также циклополиконденсацию, приводящую обычно к получению лестничных полимеров, имеющих структуру двух параллельных цепей, соединенных поперечными связями.
Поликонденсацию, в которой участвуют бифункциональные мономеры одного типа, называют гомополиконденсацией. Типичным примером гомополиконденсации является синтез полиэфиров из оксикислот:
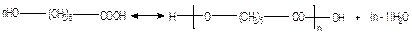
Поликонденсация, в которой участвуют мономеры различных типов, т. е. мономеры, содержащие функциональные группы, реагирующие только с функциональными группами другого мономера, называют гетерополиконденсацией (например, синтез полигексаметиленадипамида из гексаметилендиамина и адипиновой кислоты):
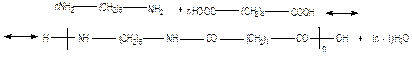
К сополиконденсации относят процессы с участием двух или большего числа мономеров, каждый из которых способен образовать собственный полимер. Например, по реакции сополиконденсации осуществляется синтез смешанного полиамида аминокопроновой и аминоэнантовой кислот:
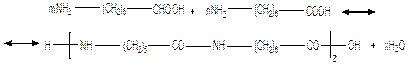
Интерсополиконденсация протекает с одновременным участием трех мономеров:
 ,
, 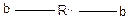 ,
, 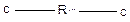 ;
;
у первых двух, называемых сомономерами, группы «a» и «b» между собой не взаимодействуют, а взаимодействуют только с функциональной группой «с» интермономера. Примером такой реакции может служить поликонденсация двух диаминов и дикарбоновой кислоты:
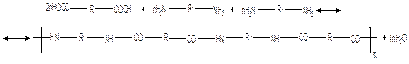
Полимеры, получаемые ПК
1. Полиэфиры получаются реакциями двухатомных спиртов с дикарбоновыми кислотами или их эфирами:
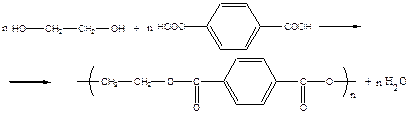
пример – получение полиэтилентерефталата (является одним из термостойких полимеров: tпл≈265°С).
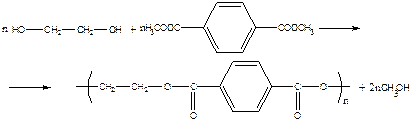
2. Полиамиды - получаются реакциями диаминов с дикарбоновыми кислотами:
Пример:
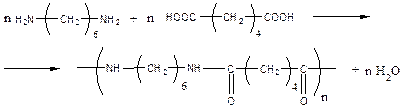
- реакция проводится в расплаве и получается полимер Nylon-66 (первая цифра - количество метиленовых групп в диамине, вторая – количество атомов углерода в дикарбоновой кислоте).
Для проведения реакции полиамидирования в более мягких условиях используют мономеры с «активированными» карбоксильными группами:
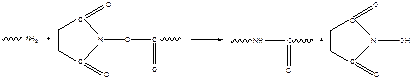
- «активированный» гидроксисукцин имидный эфир карбоновой кислоты
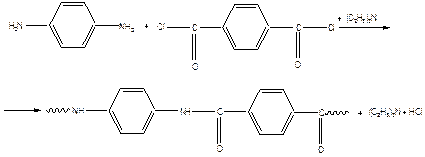
- хлорангидрид карбоновой кислоты
Для получения термо- и теплостойких полимеров реакцию поликонденсации проводят в несколько стадий.
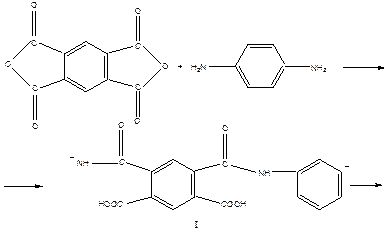
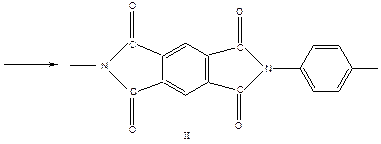
Поликарбонаты
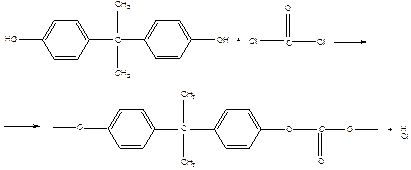
Полисульфоны
Пример: поликонденсация бис-фенола А и дихлордифенилсульфона
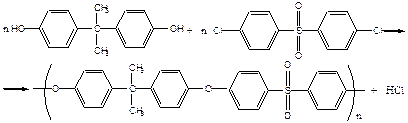
образующийся в процессе хлороводород связывают гидроксидом натрия, который добавляется в реакционную смесь.
Полисилоксаны
Пример: получение полидиалкилсилоксанов
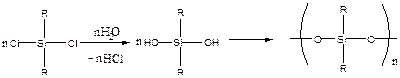
Большинство полисилоксанов обладают высокой термостойкостью.
6. Получение сетчатых (трехмерных) полимеров поликонденсацией (для этого необходимо присутствие полифункциональных мономеров)
Пример – получение фенолформальдегидных смол.
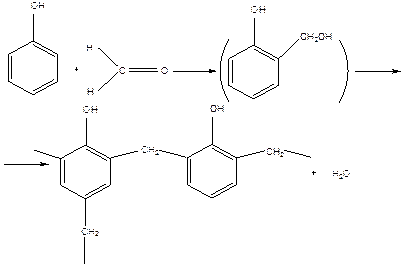
Эта реакция, открытая в 1909 г. Бакеландом, лежит в основе первого промышленного процесса получения пластмасс и композитов (резины, бакелит) и до сих пор находит широкое практическое применение.
Эпоксидные смолы
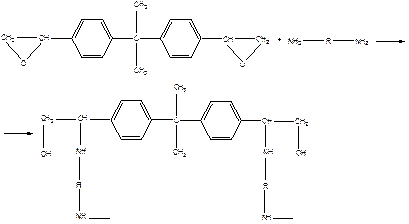
Благодаря тому, что реакция «отверждения» эпоксидных композиций происходит при умеренных температурах, без выделения низкомолекулярных продуктов и практически без усадки, ее широко используют для получения высокопрочных армированных композитов.
Полиуретаны
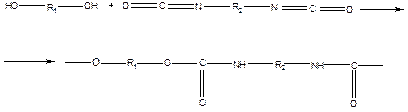
В реакцию «отверждения» в качестве гликолей обычно вводят олигомеры с М ~ 103 – 104 с концевыми гидроксильными группами на основе полиоксиэтилена, полибутадиена, полистирола и др. (олигомерная технология). Тем самым, получают целую серию материалов с широким спектром физико-механических свойств, гидрофильно-гидрофобного баланса, биосовместимости.
Полифениленоксид
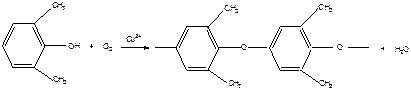
Продуктом является инженерный термопластик с высокими физико-механическими свойствами и теплостойкостью. При использовании незамещенных фенолов получают сшитые полимеры, не поддающиеся переработке.
Полианилин

Полианилин – это интенсивно окрашенный (синий или зеленый) полимер с высокой электропроводимостью.
Методы проведения ПК
1. Проведение ПК в расплаве
Если исходные мономеры и полимер устойчивы при температуре плавления (обычно 200 – 300 ◦С); для уменьшения вероятности протекания побочных реакций (окисление, деструкция) процесс проводят в атмосфере инертного газа и заканчивают обычно в вакууме для более полного удаления низкомолекулярных веществ, выделяющихся при ПК.
2. Проведение ПК в растворе
Возможность использования более низких температур, что имеет особое значение, когда мономеры или полимер неустойчивы при температуре плавление. Однако при введении растворителя скорость ПК уменьшается и возрастает вероятность циклизации. Кроме этого возникает проблема удаления из полимера растворителя и его регенерации.
3. Проведение ПК на границе раздела фаз
Исходные мономеры растворяют раздельно в двух несмешивающихся жидкостях. Как правило, в качестве одного из компонентов смеси используется бифункциональный галогенангидрид, растворенный в бензоле или хлороформе; второй компонент – бифункциональное соединение, содержащее подвижные атомы водорода, например, диамин или фенол, растворенное в воде (с добавкой соды или щелочи). Выделяющийся при реакции HCl растворяется в водной фазе, где связывается щелочью. Полимер образуется на границе раздела фаз в виде пленки и непрерывно извлекается (вытягивается) из реакционной среды. Иногда для увеличения скорости реакции проводят энергичное эмульгирование органической фазы в воде. Образующийся при этом полимер выпадает в виде хлопьев и коагулирует в комочки. Получаемые этим способом полимеры имеют высокую молекулярную массу.
Вопросы для самостоятельной проработки:
1. Какой процесс называют поликонденсацией?
2. Перечислите основные различия между полимеризационными и поликонденсационными процессами.
3. Классификация процессов поликонденсации.
4. Приведите примеры полимеров, получаемых процессом поликонденсации.
5. Как связана средняя степень ПК с глубиной превращения. Поликонденсационное равновесие и молекулярная масса полимеров.
6. Зависимость средней степени ПК (Р) от соотношения бифункциональных мономеров.
7. Как влияют добавки монофункциональных соединений на Рn?
8. Кинетика ПК.
9. Какие факторы влияют на реакции ограничения цепи (степени превращения) в процессах поликонденсации?
10. Основные способы проведения ПК.
Задачи для самостоятельного решения
3. Методы получения и структура основных типов полимеров
3.7. Ступенчатые процессы синтеза полимеров
Вопросы 7501 – 7503, 7512 – 7515, 7404 – 7407, 7416 – 7420, 7308 – 7311, 7321 – 7325
Раздел №1. Введение. Основные понятия.
В последние десятилетия высокомолекулярные соединения (полимеры) прочно вошли в нашу жизнь. Полимеры - особый вид материалов, обладающих в зависимости от строения молекул самыми разнообразными свойствами и применяемыми в самых различных сферах жизни и деятельности человечества: в промышленности и сельском хозяйстве, в науке и технике, во всех видах транспорта. Современная медицина, как и наш повседневный быт, немыслимы без использования широкого круга полимерных материалов.
В настоящее время полимеры занимают 4 место по объему среди производимых и добываемых материалов. Распределение производимых и добываемых материалов по объему представлено на рис. 1.1, а объем производства и ассортимент основных производимых полимеров – на рис. 1.2.

Рис. 1.1. Место полимеров среди производимых и добываемых материалов

Рис. 1.2. Объем и ассортимент мирового производства полимеров
Какие же свойства отличают полимеры от обычных низкомолекулярных соединений (НМС) и позволяют выделить их в особый вид материалов?
Прежде всего, большая длина и гибкость макромолекул придают полимерам свойство высокоэластичности, т.е. способности к большим (порядка нескольких сотен процентов) обратимым деформациям.
Во-вторых, твёрдые полимерные тела - пластики сочетают высокие модули упругости, сопоставимые по величине с модулями упругости обычных твёрдых тел (неорганическое стекло, металлы, керамика), с высокими разрывными удлинениями (на порядок большими, чем у обычных твёрдых тел). Поэтому полимерные тела менее склонны к хрупкому разрушению.
В-третьих, благодаря высокой анизотропии формы макромолекул полимеров они легко ориентируются в механическом поле и образуют волокна с высокой прочностью в направлении ориентации.
Полимеры отличаются от низкомолекулярных соединений и тем, что при растворении проходят сначала через стадию набухания; вязкость разбавленных (до 1 %) растворов полимеров намного превышает вязкость растворов низкомолекулярных соединений той же концентрации. Концентрированные растворы и расплавы полимеров, как и все жидкости, обладают упруго-эластическими свойствами. Высокие молекулярные массы полимеров существенно расширяют спектр их времен релаксации по сравнению с низкомолекулярными жидкостями. Сочетание больших молекулярных масс с высокими межмолекулярными взаимодействиями обуславливают ряд аномальных вязко-упругих свойств полимерных жидкостей, не характерных для низкомолекулярных соединений.
Химические реакции полимеров протекают в большинстве случаев отлично от соответствующих реакций низкомолекулярных аналогов.
Перечисленные отличительные свойства полимеров позволили им войти в число наиболее широко используемых материалов.
Среди полимерных материалов, выпускаемых промышленностью, ведущие позиции занимают:
а) пластические массы и органические стекла;
б) синтетические каучуки;
в) синтетические и искусственные волокна;
г) плёнки и многочисленные декоративно-защитные покрытия (краски, лаки, эмали).
К высокомолекулярным соединениям относятся также и биологические полимеры (биополимеры), которые обладают рядом уникальных свойств, не характерных для низкомолекулярных соединений. Назовём некоторые из важнейших свойств биополимеров и их функции:
- нуклеиновые кислоты способны кодировать, хранить и передавать генетическую информацию на молекулярном уровне, являясь материальным субстратом наследственности;
- другой класс биополимеров - мышечные белки, способны превращать химическую энергию в механическую работу; эта их сократительная функция лежит в основе мышечной деятельности белков;
- ферменты, глобулярные белки, обладают каталитической функцией, они с большой скоростью и избирательностью осуществляют в живой природе все химические реакции обмена, распада одних и синтеза других веществ.
Все перечисленные выше особенности свойств полимеров связаны с их цепным строением. Именно цепное строение молекул полимеров является их важнейшим свойством, что позволяет дать им следующее определение:
Полимеры – особый класс химических соединений, специфика свойств которых определяется большой длиной, цепным строением и гибкостью составляющих их макромолекул.
n M → [ -M- ]n
В свою очередь под макромолекулой понимают совокупность атомов или атомных групп, различных или одинаковых по составу и строению, соединённых химическими связями в линейную или разветвлённую структуру, достаточно высокой молекулярной массы.
Вещества, у которых размеры молекул очень велики и в тысячи раз превышают размеры обычных, называются высокомолекулярными (ВМС).
Мономеры - низкомолекулярные соединения, способные вступать в реакции полимеризации и поликонденсации.

Составное звено – любые атомы или группы атомов, входящие в состав цепи полимера.
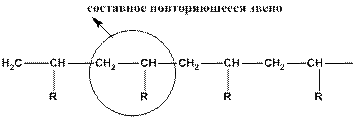
Составное повторяющееся звено (СПЗ) – наименьшее составное звено, повторением которого может быть описано строение регулярного полимера.
Пример: молекула полистирола

- в скобках выделено составное повторяющееся звено, а эллипсом – составные звенья.
Во многих случаях составное повторяющееся звено совпадает с мономерным звеном:

Но могут быть и случаи, когда они не совпадают:

Составное повторяющееся звено у полиэтилена – 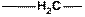
Мономерное звено – 
Степень полимеризации гомополимера - это количество составных (повторяющихся) звеньев, которые входят в макромолекулу.
Среднечисловая молекулярная масса Mn – произведение среднечисловой степени полимеризации Pn и молекулярной массы составного повторяющегося звена M0:
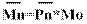
Достаточно высокая молекулярная масса полимеров - понятие относительное. Так, некоторые физико-химические свойства в ряду гомологов изменяются по кривой имеющей вид, представленный на рис. 1.3. Область I - резкое изменение свойств, например температуры плавления (Тпл), приходится на низкомолекулярное соединение (до нескольких сотен у.е.). В области III исследуемое свойство (Тпл) практически не зависит от молекулярной массы - это область высокомолекулярных соединений (молекулярные массы составляют десятки тысяч и выше, для многих полимеров молекулярные массы составляют несколько сотен тысяч у.е.). Наконец, промежуточной области II соответствуют олигомерные соединения с молекулярной массой от нескольких сотен до нескольких тысяч.

Рис. 1.3. Зависимость температуры плавления (Тпл) от молекулярной массы алканов
Таблица 1.1.
Примеры изменения свойств и применения веществ в зависимости от числа атомов С в цепи
| Число атомов С в цепи | Состояние | Применение |
| 1 - 4 5 - 11 10 - 16 16 - 25 25 - 50 1000 и более | газ жидкости средневязкие жидкости высоковязкие жидкости твердые тела полимеры | бытовые газы бензин масла и смазки моторные масла парафины, воск материалы (эластомеры, пластмассы) |
Вопросы для самостоятельной проработки:
1. Какое место занимают полимеры по объему производства в современной промышленности?
2. Назовите основные свойства полимеров, которые определяют их как особый вид материалов.
3. Дайте определение следующих понятий: полимер, высокомолекулярное соединение, макромолекула, составное звено, составное повторяющееся звено.
4. Напишите уравнение, определяющее взаимосвязь молекулярной массы и степени полимеризации.
5. Понятие о НМС, олигомере и полимере.
Раздел №2. Номенклатура и классификация полимеров
Номенклатура полимеров
В настоящее время существует 3 основных вида номенклатуры полимеров:
1. Номенклатура, основанная на названии мономеров (рациональная номенклатура);
2. Номенклатура, основанная на химической структуре полимерной цепи (систематическая номенклатура IUPAC);
3. Случайная номенклатура.
Дата: 2019-04-23, просмотров: 544.