Один и тот же тип эйкозаноида может действовать по паракринному и по аутокринному механизму. Например, ТХА2, продуцируемый тромбоцитами при их активации, действует на сами тромбоциты, увеличивая их способность к агрегации, и в то же время действует на окружающие ГМК кровеносных сосудов, способствуя их сокращению. Таким образом создаются условия для образования тромба и предотвращения кровотечения в области повреждения сосудов.
Эйкозаноиды действуют на клетки через специальные рецепторы. Некоторые рецепторы эйкозаноидов связаны с аденилатциклазной системой и протеинкиназой А - это рецепторы PGE, PGD, PCI. PGF2α, ТХА2 эндоперекиси (ГПЭТЕ) и лейкотриены действуют через механизмы, увеличивающие уровень кальция в цитозоле клеток-мишеней. Во многих клетках эйкозаноиды влияют на степень активации аденилатциклазной системы в ответ на действие других факторов, например гормонов. В этих случаях эйкозаноиды влияют на конформацию G-белков в плазматической мембране клеток. Если эйкозаноид связывается со стимулирующими Gs-белками, то эффект основного стимулирующего агента увеличивается; если с Gi-ингибирующими - эффект снижается. Эйкозаноиды действуют на клетки почти всех тканей организма. Избыточная продукция эйкозаноидов наблюдается при многих заболеваниях.
Роль эйкозаноидов в тромбообразовании
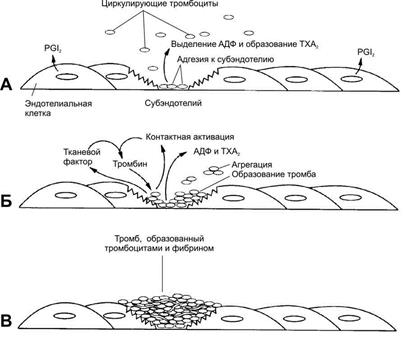
Свёртывание крови можно рассматривать как процесс, который поддерживается в состоянии равновесия противодействующими системами: свёртывания и противосвёртывания. В условиях патологии или при действии фармакологических средств это равновесие может смещаться в ту или другую сторону. В норме клетки эндотелия сосудов продуцируют простациклин I2, который препятствует агрегации тромбоцитов и сужению сосудов. При разрушении клеток эндотелия (например, в результате образования атеросклеротической бляшки) синтез PGI2 снижается. Тромбоциты контактируют с повреждённой стенкой сосуда, в результате чего активируется фосфолипаза А2. Это приводит к увеличению секреции ТХ А2, стимулирующего агрегацию тромбоцитов и образование тромба в области повреждения сосуда, что часто приводит к развитию инфаркта.
В норме клетки эндотелия продуцируют PG I2, который вызывает релаксацию ГМК и ингибирует агрегацию тромбоцитов. Тромбоциты в неактивном состоянии не продуцируют тромбоксаны. В области повреждения стенки сосуда преобладает действие TXА2, стимулирующего агрегацию тромбоцитов и сокращение стенок сосуда. В результате на повреждённом участке образуется тромб, происходит резкое сужение просвета сосуда. В миокарде это может привести к развитию инфаркта миокарда.
PGI2 является мощным ингибитором агрегации тромбоцитов, и было показано, что он синтезируется микросомальной фракцией гомогенатов кровеносных сосудов.
PGI2 обладает двумя важными фармакологическими свойствами, которые обусловливают противодействие PGI2 тромбоксану А2; дело в том, что PGI2 является наиболее мощным из всех известных в настоящее время ингибиторов агрегации тромбоцитов и, кроме того, расширяет сосуды. Предполагается, что в результате соприкосновения тромбоцитов с эндотелием нормальных кровеносных сосудов происходит высвобождение PGG2, субстрата для образования PGI2; действие этого механизма способствует предотвращению агрегации тромбоцитов и сужению кровеносных сосудов. Если же тромбоциты вступают в соприкосновение с эндотелием кровеносных сосудов, который имеет разрывы или повреждения вследствие патологических изменений, то из-за недостаточной концентрации фермента, катализирующего образование простацнклина PGI2, количество последнего снижается; при этом агрегирующее действие тромбоксана А2, который синтезируется из эндопероксида, должно превалировать над антиагрегирующим действием PGI2, что приводит к тромбозу и местному спазму сосудов.
Дата: 2019-05-29, просмотров: 318.