Эйкозаноиды
Эйкозаноиды - это общая группа физиологически и фармакологически активных соединений включающая в себя простаноиды (простагландины, простоциклины, тромбоксаны) и лейкотриены. Они имеют очень короткий Т1/2, поэтому оказывают эффекты как "гормоны местного действия".
История открытия
Еще в начале нашего века было известно, что водные и спиртовые экстракты, полученные из везикулярных (парных половых) желез многих видов животных и предстательной железы (простаты) человека, понижают кровяное давление у собак и кроликов. Тогда же было сделано предположение о существовании в предстательной железе "неизвестного сосудистого гормона". До 30-х годов это вещество оставалось загадочным; правда, никто из исследователей и не пытался выделить его из таких экстрактов и дать ему характеристику.
В 1930 г. два американских гинеколога, Курцрок и Либ, описали сокращение и расслабление изолированной полоски матки человека под действием человеческой спермы. Несколькими годами позже Гольдблатт в Англии и Ульф фон Эйлер в Швеции, независимо друг от друга, сообщили о том, что сперма, а также секреты семенных пузырьков предстательной железы вызывают сокращение гладких мышц.
Ульф фон Эйлер, шведский физиолог, с чьим именем связывают открытие простагландинов, обнаружил их (вернее, одно вещество) случайно в 1934 - 1936 гг., пытаясь изучить известную в то время субстанцию Р - вещество белковой природы, обладающее способностью понижать кровяное давление и стимулировать сокращение стенок кишечника. Однако, вопреки ожиданию, активное вещество экстрактов предстательной железы и семенной жидкости он обнаружил во фракции жирорастворимых кислот, а не в белковой фракции. У. Эйлер описал некоторые химические и фармакологические свойства активного экстракта, назвал его простагландином (от prostate glond), и предположил, что простагландин имеет широкое регуляторное значение в организме. Но ни выделить вещество в чистом виде, ни изучить химическую структуру в то время не позволял примитивный уровень аналитических способов исследования.
Работу над простагландинами продолжил ученик Эйлера С. Бергстрем, перед которым стояла задача выделить в кристаллическом виде активное начало, т.е. простагландин, из экстрактов простаты и семенной жидкости баранов. Вначале С. Бергстрему удалось сделать немногое: он выяснил только, что простагландин находится во фракциях вместе с ненасыщенными жирными оксикислотами, и вынужден был прервать дальнейшие исследования на несколько лет. Одной из главных причин, обусловивших этот перерыв, были затруднения с исходным материалом для выделения простагландинов - везикулярными железами барана, самым богатым простагландинами источником. Но поскольку уже к тому времени биохимики и фармакологи заинтересовались простагландинами, в 1956 г. в ряде стран северного полушария была организована специальная программа исследований простагландинов, в которую вошел и сбор замороженных везикулярных желез барана.
Уже в следующем году С. Бергстрем и Дж. Шьевалл получили несколько миллиграммов индивидуального вещества в кристаллическом состоянии и назвали его простагландин F за его растворимость в фосфатном буфере. Полученного количества хватило лишь на то, чтобы установить, что простагландин F - это ненасыщенная жирная кислота, определить температуру его плавления и продемонстрировать способность в концентрации всего 5*10 - 9 г в 1 мл раствора давать хороший эффект по сокращению гладкой мышцы. Затем в кристаллическом же состоянии было получено еще одно вещество подобного типа - простагландин Е (обозначение возникло от слова ester - эфир, которым извлекался этот простагландин). Оба соединения были одинакового молекулярного веса и очень сходного строения, но в корне различались биологическими свойствами: простагландин Е понижал кровяное давление, а простагландин F сокращал гладкую мускулатуру.
Работы по простагландинам развивались быстрыми темпами, и за 1972 - 1976 годы С. Бергстрем, Б. Самуэльссон и Дж. Вейн получили в чистом виде еще 10 простагландинов, установили их структуру и определили биологические свойства. В 1979 г. Б. Самуэльссон с коллегами открыл еще один тип соединений - близкие простагландинам лейкотриены.
Выделение простагландинов, изучение структуры и свойств - работа чрезвычайно трудная: мало того что их концентрации в объектах выделения очень низки, вещества эти крайне неустойчивы, они теряют свою биологическую активность, по которой следят за веществом в ходе его выделения, в течение 1 - 2 мин. Недаром за исследования простагландинов С. Бергстрему, Б. Самуэльссону и Дж. Вейну в 1982 г. была присуждена Нобелевская премия.
Сейчас известно уже около 30 природных простаноидов. Они разделены на группы A, B, C, D, E, F, G, I. Краткое обозначение простаноидов складывается из двух букв английского prostaglandine и tromboxane или русского написания, третья буква в этом обозначении указывает на принадлежность к той или иной группе, например: PGF, ПГF - простагландин F; ТхА, ТксА - тромбоксан А.
Биосинтез
После отделения арахидоновой кислоты от фосфолипида она выходит в цитозоль и в различных типах клеток превращается в разные эйкозаноиды. В клетках имеется 2 основных пути превращения арахидоновой кислоты: циклооксигеназный, приводящий к синтезу простагландинов, простациклинов и тромбоксанов, и липоксигеназный, заканчивающийся образованием лейкотриенов. (Рис.4)
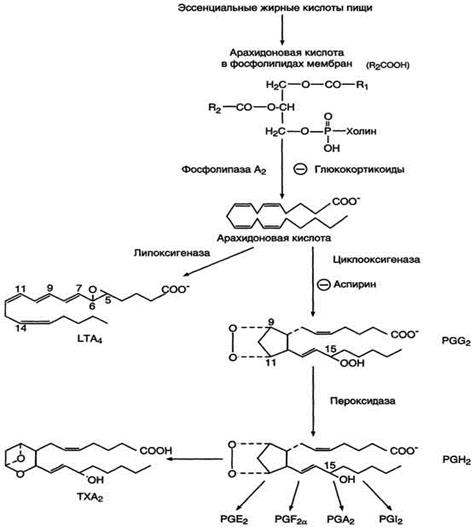
Рис.4 Синтез эйкозаноидов из арахидоновои кислоты.
Циклооксигеназный путь: синтез простагландинов и тромбоксанов
С20-три-, тетра - и пентаеновая жирные кислоты, служащие предшественниками простагландинов, входят в состав внутриклеточных фосфоглицеридов, из которых они высвобождаются под действием фосфолипазы А2. Активация фосфолипаз, ассоциированных с мембранами, происходит под действием многих факторов: гормонов, гистамина, цитокинов, механического воздействия. Этот процесс высвобождения предшественника, вероятно, играет роль регулирующей стадии в биосинтезе простагландинов, с помощью которой варьирует количество субстрата, подвергающегося последующему действию простагландинсинтазы. Последняя представляет собой связанный в мембране мультиферментный комплекс, содержащийся в микросомальной фракции тканевых гомогенатов. Необходимо отметить, что ингибиторное действие кортикостероидов на биосинтез простагландинов, связанное с торможением активности фосфолипазы А2, может служить объяснением антивоспалительного действия этих стероидных гормонов.
Фермент, катализирующий первый этап синтеза простагландинов, называется PG Н2 синтазой и имеет 2 каталитических центра. Один из них называют циклооксигеназой, другой - пероксидазой. Этот фермент представляет собой димер гликопротеинов, состоящий из идентичных полипептидных цепей. Фермент имеет гидрофобный домен, погружённый в липидный слой мембран ЭР, и каталитический домен, обращённый в полость ЭР. В активном центре циклооксигеназы находится тирозин (385), в активном центре пероксидазы - простетическая группа - гем. В организме имеются 2 типа циклооксигеназ (PGН2 синтаз). Циклооксигеназа 1 - конститутивный фермент, синтезирующийся с постоянной скоростью. Синтез циклооксигеназы 2 увеличивается при воспалении и индуцируется соответствующими медиаторами - цитокинами. Оба типа циклооксигеназ катализируют включение 4 атомов кислорода в арахидоновую кислоту и формирование пятичленного кольца. В результате образуется нестабильное гидропероксидпроизводное, называемое PG G2. Гидропероксид у 15-го атома углерода быстро восстанавливается до гидроксильной группы пероксидазой с образованием PG Н2. До образования PG Н2 путь синтеза разных типов простагландинов одинаков. Дальнейшие превращения PG Н2 специфичны для каждого типа клеток.
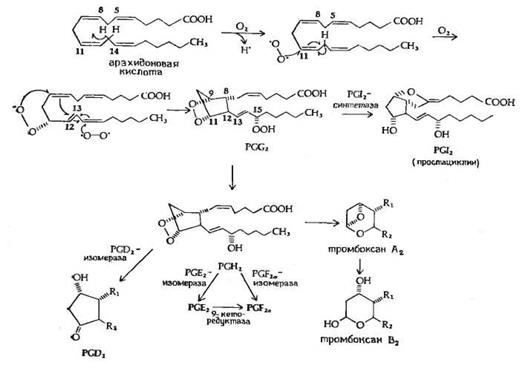
Рис.5. Предполагаемый механизм биосинтеза PGE2 и PGF2a из арахидоновой кислоты.
Биосинтез PGE2 и PGF2a, представленный на рис.5, начинается с арахидоновой кислоты и катализируется циклооксигеназой (М 70 000) жирных кислот, при этом образуется 15-оксиперокси-9-11-эндопероксид PGG2. Первая стадия в этой последовательности реакций приводит к потере атома водорода у С-13 с образованием свободного радикала. Эта стадия лимитирует скорость всего процесса. Затем происходят присоединение пероксидного радикала в положения 9 и 11 и образование 8,12 углерод-углеродной связи, которому предшествует изомеризация 11,12-двойной связи в 12,13-двойную связь и присоединение другого пероксидного радикала в положение 15, приводящее к изомеризации 12,13-двойной связи в 13,14-двойную связь. Все эти превращения рассматриваются как процесс одноэлектронного переноса, обозначенный на рисунке изогнутыми стрелками. Первый продукт этой последовательности реакций - это 15-оксиперокси-9,11-эндопероксид PGG2, существование которого было постулировано за несколько лет до его выделения и идентификации. PGG2 затем превращается в PGI2 или PGH2, вероятно, с помощью реакции пероксидазного типа. PGH2 является предшественником PGE2 и PGF2a в семенных пузырьках и других органах, а также тромбоксана А2 в тромбоцитах и легких.
Превращение арахидоновой кислоты в PGG2 блокируется ингибиторами циклооксигеназы жирных кислот. Наиболее известным среди этих ингибиторов являются аспирин (ацетилсалициловая кислота) и ряд других противовоспалительных лекарств (Рис.6). Торможение аспирином обусловлено переносом ацетильного остатка от молекулы аспирина к активному центру фермента с инактивацией последнего; такого рода механизм был предложен в качестве объяснения некоторых известных фармакологических эффектов аспирина.
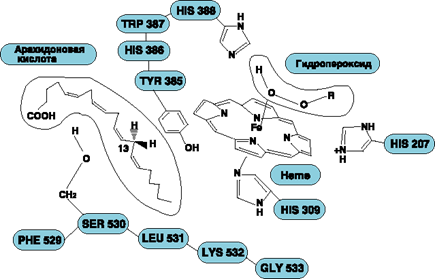
Рис.6. Молекулярный механизм ингибирования циклооксигеназы ацетилсалициловой кислотой.
Аспирин - препарат, подавляющий основные признаки воспаления. Механизм противовоспалительного действия аспирина стал понятен, когда обнаружили, что он ингибирует циклооксигеназу. Следовательно, он уменьшает синтез медиаторов воспаления и, таким образом, уменьшает воспалительную реакцию. Циклооксигеназа необратимо ингибируется путём ацетилирования серина в положении 530 в активном центре (Рис.6). Однако эффект действия аспирина не очень продолжителен, так как экспрессия гена этого фермента не нарушается и продуцируются новые молекулы фермента. Другие нестероидные противовоспалительные препараты (например, ибупрофен и ацетаминофен) действуют по конкурентному механизму, связываясь в активном центре фермента, и также снижают синтез простагландинов.
Стероидные препараты обладают гораздо более сильным противовоспалительным действием, чем препараты нестероидного ряда. Механизм их действия заключается в индукции синтеза белков - липокортинов (или макрокортинов), которые ингибируют активность фосфолипазы А2 и уменьшают синтез всех типов эйкозаноидов, так
как препятствуют освобождению субстрата для синтеза эйкозаноидов - арахидоновой кислоты (или её аналога).
Использование стероидных противовоспалительных препаратов особенно важно для больных, страдающих бронхиальной астмой. Развитие симптомов этого заболевания (бронхоспазм и экссудация слизи в просвет бронхов) обусловлено, в частности, избыточной продукцией лейкотриенов тучными клетками, лейкоцитами и клетками эпителия бронхов. Приём аспирина у больных, имеющих изоформу липоксигеназы с высокой активностью, может вызвать приступ бронхиальной астмы. Причина "аспириновой" бронхиальной астмы заключается в том, что аспирин и другие нестероидные противовоспалительные препараты ингибируют только циклооксигеназный путь превращений арахидоновой кислоты и, таким образом, увеличивают доступность субстрата для действия липоксигеназы и, соответственно, синтеза лейкотриенов. Стероидные препараты ингибируют использование арахидоновой кислоты и по липоксигеназному и по циклооксигеназному пути, поэтому они не могут вызывать бронхоспазма.
Структура и синтез лейкотриенов
Наличие 3 сопряжённых двойных связей обусловливает название "лейкотриен". Лейкотриены также образуются из эйкозаноевых кислот, однако в их структуре отсутствуют циклы, как у простагландинов, и они имеют 3 сопряжённые двойные связи, хотя общее число двойных связей в молекуле больше (рис.7). Лейкотриены С4, D4 и Е4 имеют заместители в виде трипептида глутатиона, дипептида глицилцистеина или цистеина, соответственно.
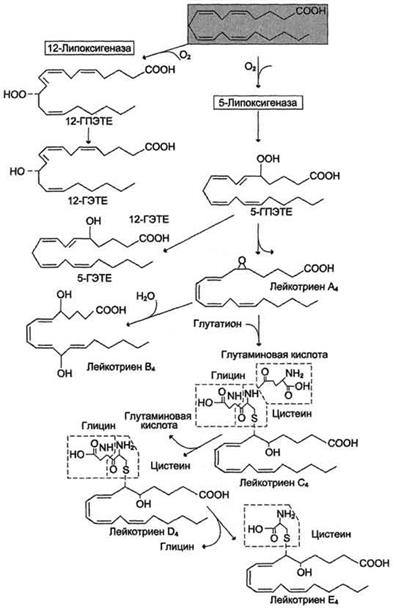
Рис.7. Липоксигеназный путь синтеза эикозаноидов.
Синтез лейкотриенов идёт по пути, отличному от пути синтеза простагландинов, и начинается с образования гидроксипероксидов - гидропероксидэйкозатетраеноатов (ГПЭТЕ). Эти вещества или восстанавливаются с образованием гидроксиэйкозатетроеноатов (ГЭТЕ) или превращаются в лейкотриены. ГЭТЕ отличаются по положению гидроксильной группы у 5-го, 12-го или 15-го атома углерода, например: 5-ГЭТЕ, 12-ГЭТЕ.
Липоксигеназы действуют в 5-й, 12-й или 15-й позиции арахидоновой кислоты в зависимости от типа ткани. Например, в тромбоцитах - 12-липоксигеназа, в эозинофилах - 15-липоксигеназа.
Глюкокортикоиды ингибируют синтез всех типов эйкозаноидов, так как ингибируют фосфолипазу А2, и таким образом уменьшают количество субстрата для их синтеза. Аспирин и другие противовоспалительные препараты нестероидного действия ингибируют только циклооксигеназный путь.
Другие типы лейкотриенов образуются из LTА4, LTВ4 образуется под действием эпоксидгидролазы в лейкоцитах и клетках эпителия сосудов. Другой путь приводит к образованию группы лейкотриенов: LTC4, LTD4, LTE4. Их синтез начинается с присоединения трипептида глутатиона к 6-му атому углерода с образованием LTС4 в реакции, катализируемой глутатион-8-трансферазой. В следующей реакции удаляется глутамат, и LTD4 содержит дипептид глицилцистеин. На последней стадии отщепляется глицин, и LTЕ4 содержит только цистеин.
Действие на нервную систему
Простагландины присутствуют в нервной ткани и освобождаются при раздражении периферических нервов. Введенные простагландины повышают температуру тела, оказывают седативное и транквилизирующее действие и являются антагонистами противосудорожных препаратов. Простагландины модулируют действие адренергическнх факторов, например норадреналина, и являются антагонистами некоторых эффектов этих катехоламинов.
Воспалительное действие
Основные источники простагландинов в очаге воспаления: тромбоциты, активированные лейкоциты, клетки эндотелия, тучные клетки.
Простагландины участвуют в формировании всех компонентов и многих проявлений воспаления. Наиболее выражено их влияние на: тонус стенок микрососудов (артериол, прекапилляров, капилляров, венул); адгезивно-агрегационные свойства тромбоцитов, лейкоцитов и эритроцитов (поэтому важна роль простагландинов в регуляции кровоснабжения тканей при воспалении, эмиграции в очаг воспаления лейкоцитов и фагоцитоза); образование других медиаторов воспаления; состояние системы гемостаза; проницаемость стенок микроциркуляторного русла; развитие лихорадки.
Эффекты лейкотриенов
Спазмогенное действие (на ГМК стенок сосудов, а также бронхиол и кишечника) не вызывает тахифилаксии, в связи с чем длительность эффекта лей-котриенов весьма велика. Спазм микрососудов, особенно артериол, в очаге воспаления приводит к развитию ишемии.
Положительный хемотаксический эффект по отношению к фагоцитам.
Повышение проницаемости мембран.
Введение простагландинов подопытным животным увеличивает воспалительную реакцию, вызванную, например, гистамином. Простагландины, образуемые в местах, связанных с повреждением, ожогами или вредными воздействиями, ведут себя как медиаторы воспалительной реакции. Способность таких агентов, как аспирин или другие лекарства, тормозить воспалительную реакцию, связана с их ингибирующим действием на простагландинсинтазу.
Иммунное действие
Ингибирующее действие простагландинов на иммунный ответ объясняется тем, что активация антигенами Т-лимфоцитов, имеющая значение в иммунологическом ответе, ингибируется PGE1. В противоположность этому сообщалось, что PGE1 усиливает иммуногенность (способность антигена вызывать иммунный ответ) клеток селезенки как in vivo, так и in vitro. Кроме того, макрофаги, которые в иммунологических реациях функционируют в тесном взаимодействии с лимфоцитами, изменяя их активность, также продуцируют и секретируют простагландины типа Е. Изучению роли простагландинов в модуляции иммунных реакций придается все большее значение. Предполагают, что продукция простагландинов злокачественными клетками может иметь отрицательные последствия для иммунной системы организма хозяина и, таким образом, может затруднить иммуннотерапевтические подходы к лечению новообразований у человека.
Воздействия на кожу
Воспалительные влияния простагландинов, описанные выше, частично являются результатом их способности вызывать местное увеличение секреции гистамина. В коже подопытных животных наблюдается увеличение проницаемости капилляров, а у человека отмечена стойкая эритема сосудов кожи (сильное покраснение кожи, вызванное расширением капилляров), сопровождаемая появлением волдырей и отека. Это воспалительное действие простагландинов можно предотвратить антивоспалительными агентами, в том числе аспирином.
Таблица 8-8. Характеристика биологического действия основных типов эйкозаноидов
| Эйкозаноид | Основное место синтеза | Основное биологическое действие |
| PG E2 | Большинство тканей, особенно почки | Расслабляет гладкую мускулатуру, расширяет сосуды, инициирует родовую активность, подавляет миграцию лимфоцитов, пролиферацию Т-клеток. |
| PG F2α | Большинство тканей | Сокращает гладкую мускулатуру, суживает сосуды, бронхи, стимулирует сокращения матки. |
| PG D3 | Клетки гладкой мускулатуры | Вызывает расширение сосудов, снижает агрегацию тромбоцитов и лейкоцитов. |
| PG I2 | Сердце, клетки эндотелия сосудов | Уменьшает агрегацию тромбоцитов, расширяет сосуды. В клетках-мишенях увеличивает образование цАМФ |
| TX A2 | Тромбоциты | Стимулирует агрегацию тромбоцитов, суживает сосуды и бронхи, в клетках уменьшает образование цАМФ. |
| TX A3 | Тромбоциты | Обладает функциями, одинаковыми с ТХ А2, но значительно менее эффективен. |
| LT B4 | Лейкоциты, клетки эпителия | Стимулирует хемотаксис и агрегацию лейкоцитов, освобождение лизосомальных ферментов лейкоцитов. Увеличивает проницаемость сосудов. |
| Группа лейкотриенов | Лейкоциты, альвеолярные макрофаги | Стимулируют расширение сосудов, увеличивают их проницаемость. |
Использование производных эйкозаноидов в качестве лекарств
Хотя действие всех типов эйкозаноидов до конца не изучено, имеются примеры успешного использования лекарств - аналогов эйкозаноидов для лечения различных заболеваний. Например, аналоги PGЕ1 и PGЕ2 подавляют секрецию соляной кислоты в желудке, блокируя гистаминовые рецепторы II типа в клетках слизистой оболочки желудка. Эти лекарства, известные как Н2-блокаторы, ускоряют заживление язв желудка и двенадцатиперстной кишки. Способность PGЕ2 и PGF2α стимулировать сокращение мускулатуры матки используют для стимуляции родовой деятельности.
Инактивация эйкозаноидов
Все типы эйкозаноидов быстро инактивируются. Т1/2 эйкозаноидов составляет от нескольких секунд до нескольких минут. Простагландины инактивируются путём окисления гидроксильной группы в положении 15, важнейшей для их активности, до кетогруппы. Двойная связь в положении 13 восстанавливается. Затем происходит β-окисление боковой цепи, а после него - ω-окисление. Конечные продукты (дикарбоновые кислоты) выделяются с мочой. Активный ТХA2
Эйкозаноиды
Эйкозаноиды - это общая группа физиологически и фармакологически активных соединений включающая в себя простаноиды (простагландины, простоциклины, тромбоксаны) и лейкотриены. Они имеют очень короткий Т1/2, поэтому оказывают эффекты как "гормоны местного действия".
История открытия
Еще в начале нашего века было известно, что водные и спиртовые экстракты, полученные из везикулярных (парных половых) желез многих видов животных и предстательной железы (простаты) человека, понижают кровяное давление у собак и кроликов. Тогда же было сделано предположение о существовании в предстательной железе "неизвестного сосудистого гормона". До 30-х годов это вещество оставалось загадочным; правда, никто из исследователей и не пытался выделить его из таких экстрактов и дать ему характеристику.
В 1930 г. два американских гинеколога, Курцрок и Либ, описали сокращение и расслабление изолированной полоски матки человека под действием человеческой спермы. Несколькими годами позже Гольдблатт в Англии и Ульф фон Эйлер в Швеции, независимо друг от друга, сообщили о том, что сперма, а также секреты семенных пузырьков предстательной железы вызывают сокращение гладких мышц.
Ульф фон Эйлер, шведский физиолог, с чьим именем связывают открытие простагландинов, обнаружил их (вернее, одно вещество) случайно в 1934 - 1936 гг., пытаясь изучить известную в то время субстанцию Р - вещество белковой природы, обладающее способностью понижать кровяное давление и стимулировать сокращение стенок кишечника. Однако, вопреки ожиданию, активное вещество экстрактов предстательной железы и семенной жидкости он обнаружил во фракции жирорастворимых кислот, а не в белковой фракции. У. Эйлер описал некоторые химические и фармакологические свойства активного экстракта, назвал его простагландином (от prostate glond), и предположил, что простагландин имеет широкое регуляторное значение в организме. Но ни выделить вещество в чистом виде, ни изучить химическую структуру в то время не позволял примитивный уровень аналитических способов исследования.
Работу над простагландинами продолжил ученик Эйлера С. Бергстрем, перед которым стояла задача выделить в кристаллическом виде активное начало, т.е. простагландин, из экстрактов простаты и семенной жидкости баранов. Вначале С. Бергстрему удалось сделать немногое: он выяснил только, что простагландин находится во фракциях вместе с ненасыщенными жирными оксикислотами, и вынужден был прервать дальнейшие исследования на несколько лет. Одной из главных причин, обусловивших этот перерыв, были затруднения с исходным материалом для выделения простагландинов - везикулярными железами барана, самым богатым простагландинами источником. Но поскольку уже к тому времени биохимики и фармакологи заинтересовались простагландинами, в 1956 г. в ряде стран северного полушария была организована специальная программа исследований простагландинов, в которую вошел и сбор замороженных везикулярных желез барана.
Уже в следующем году С. Бергстрем и Дж. Шьевалл получили несколько миллиграммов индивидуального вещества в кристаллическом состоянии и назвали его простагландин F за его растворимость в фосфатном буфере. Полученного количества хватило лишь на то, чтобы установить, что простагландин F - это ненасыщенная жирная кислота, определить температуру его плавления и продемонстрировать способность в концентрации всего 5*10 - 9 г в 1 мл раствора давать хороший эффект по сокращению гладкой мышцы. Затем в кристаллическом же состоянии было получено еще одно вещество подобного типа - простагландин Е (обозначение возникло от слова ester - эфир, которым извлекался этот простагландин). Оба соединения были одинакового молекулярного веса и очень сходного строения, но в корне различались биологическими свойствами: простагландин Е понижал кровяное давление, а простагландин F сокращал гладкую мускулатуру.
Работы по простагландинам развивались быстрыми темпами, и за 1972 - 1976 годы С. Бергстрем, Б. Самуэльссон и Дж. Вейн получили в чистом виде еще 10 простагландинов, установили их структуру и определили биологические свойства. В 1979 г. Б. Самуэльссон с коллегами открыл еще один тип соединений - близкие простагландинам лейкотриены.
Выделение простагландинов, изучение структуры и свойств - работа чрезвычайно трудная: мало того что их концентрации в объектах выделения очень низки, вещества эти крайне неустойчивы, они теряют свою биологическую активность, по которой следят за веществом в ходе его выделения, в течение 1 - 2 мин. Недаром за исследования простагландинов С. Бергстрему, Б. Самуэльссону и Дж. Вейну в 1982 г. была присуждена Нобелевская премия.
Сейчас известно уже около 30 природных простаноидов. Они разделены на группы A, B, C, D, E, F, G, I. Краткое обозначение простаноидов складывается из двух букв английского prostaglandine и tromboxane или русского написания, третья буква в этом обозначении указывает на принадлежность к той или иной группе, например: PGF, ПГF - простагландин F; ТхА, ТксА - тромбоксан А.
Субстраты для синтеза эйкозаноидов
Главный субстрат для синтеза эйкозаноидов у человека - арахидоновая кислота, так как её содержание в организме человека значительно больше остальных полиеновых кислот - предшественников эйкозаноидов.
В образовании эйкозанондов принимают участие также и другие незаменимые жирные кислоты (линолевая и а-линоленовая), но только после элонгации на два углеродных атома и десатурацнн, т.е. после превращения в 20-углеродные тетраеновые кислоты. Арахидоновая, 8,11,14-эйкозатриеновая и 5,8,11,14,17-эйкозапентаеновая кислоты - предшественники эйкозаноидов.
Полиеновые кислоты с 18 и 20 атомами углерода поступают в организм человека с пищей или образуются из незаменимых (эссенциальных) жирных кислот с 18 атомами углерода. (Рис.1)

Рис.1. Синтез полиеновых жирных кислот с 20 углеродными атомами в организме человека.
Полиеновые жирные кислоты, которые могут служить субстратами для синтеза эйкозаноидов, входят в состав глицерофосфолипидов мембран. Под действием ассоциированной с мембраной фосфолипазы А2 жирная кислота отщепляется от глицерофосфолипида и используется для синтеза эйкозаноидов.
Дата: 2019-05-29, просмотров: 326.