Каталитические системы дыхания
Окисление дыхательных субстратов в ходе дыхания осуществляется с участием ферментов. Ферменты как белковые катализаторы, помимо свойств, присущих неорганическим катализаторам, обладают рядом особенностей: высокой актианостью, высокой специфичностью по отношению к субстратам и высокой лабильностью. Их пространственная организации зависящая от нее активность изменяются под действием внешних и внутренних факторов. Эти свойства обеспечивают возможность тонкой регуляции обмена веществ на уровне ферментов.
Типы окислительно-восстановительных реакций. Существуют четыре способа окисления, и все они связаны с отнятием электронов:
1) непосредственная отдача электронов, например:
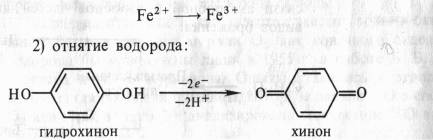
3) присоединение кислорода

4) образование промежуточного гидратированного соединения с последующим отнятием двух электронов и протонов:
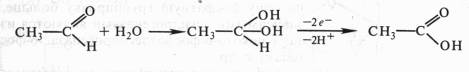
Оксидоредуктазы.
Поскольку окисление одного вещества (донора электронов и протонов) сопряжено с восстановлением другого соединения (их акцептора), ферменты, катализирующие эти реакции, называют оксидоредуктазами. Все они относятся к I классу ферментов:
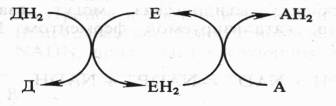
Донор (Д) отдает электроны и протоны, акцептор (А) принимает их, а энзим (Е) осуществляет реакцию переноса. Существуют три группы оксидоредуктаз:
а) анаэробные дегидрогеназы передают электроны различным промежуточным акцепторам, но не кислороду;
б) аэробные дегидрогеназы передают электроны различным акцепторам, в том числе кислороду;
в) оксидазы способны передавать электроны только кислороду.
Анаэробные дегидрогеназы. Это двухкомпонентные ферменты, коферментом которых может быть NAD+ (никотинамидадениндинуклеотид):
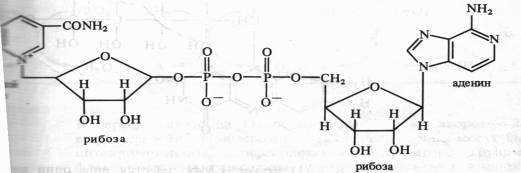
При окислении субстрата NAD+ превращается в восстановленную форму NADH, а второй протон субстрата диссоциирует в среду (NADH + Н + ). К анаэробным NAD-зависимым дегидрогеназам относятся такие ферменты, как алкогольдегидрогеназа, лактатдегидрогеназа, малатдегидрогеназа и др. Коферментом анаэробных дегидрогеназ может быть также NADP+ (никотинамидадениндинуклеотидфосфат), содержащий на одну фосфатную группировку больше, чем NAD + . NADP- зависимыми дегидрогеназами являются изоцитратдегидрогеназа, глюкозо-6-фосфатдегидрогеназа, 6-фосфоглюконатдегидрогеназа и др.
Субстратная специфичность фермента зависит от его белковой части. Многие NAD- и NADP-зависимые дегидрогеназы нуждаются в присутствии ионов двухвалентных металлов. Например, алкогольдегидрогеназа содержит ионы цинка.
Окисленные и восстановленные формы коферментов анаэробных дегидрогеназ могут взаимопревращаться в реакции, катализируемой ферментом NAD(Р)-трансгидрогеназой:
NADPH + NAD+ = NADP+ + NADH
Анаэробные дегидрогеназы передают водород, т. е. электроны и протоны, различным промежуточным переносчикам и аэробным дегидрогеназам.
Аэробные дегидрогеназы. Это также двухкомнонентные ферменты, получившие название флавиновых (флавопротеины).
Помимо белков, в их состав входит прочно связанная с ними простетическая группа — рибофлавин (витамин В2).
Различают два кофермента этой группы: флавинмононуклеотид (FMN), или желтый дыхательный фермент Варбурга, и флавинадениндинуклеотид (FAD).
FMN (рибофлавин-5-фосфат) содержит гетероциклическое азотистое основание — диметилизоаллоксазин, спирт рибит (производное рибозы) и фосфат:
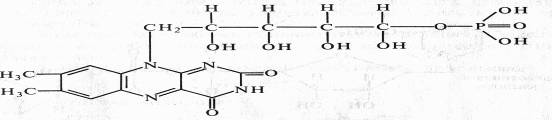
В FAD кроме FMN имеется еще один нуклеотид — аденозинмонофосфата:
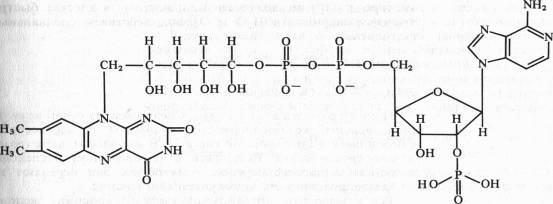
Активной группой в реакции присоединения и отдачи электронов и протонов в FMN и FAD служит изоаллоксазин. Взаимодействие с восстановленным переносчиком, например NADH, происходит следующим образом:
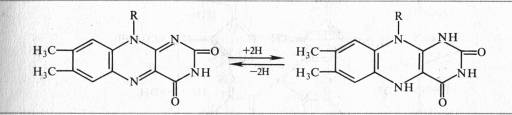
Примером дегидрогеназы, в состав которой входит FAD, является сукцинатдегидрогеназа. Доноры электронов для аэробных дегидрогеназ — анаэробные дегидрогеназы, а акцепторы — хиноны, цитохромы, кислород.
Цитохромная система. Среди оксидаз очень важную роль играют железосодержащие ферменты и переносчики, относящиеся к цитохромной системе. В нее входят цитохромы " и цитохромоксидаза. Включаясь в определенной последовательности в процесс переноса электронов, они передают их от флавопротеинов на молекулярный кислород.
Все компоненты цитохромной системы содержат железопорфириновую простетическую группу.
При переносе электронов цитохромами железо обратимо окисляется и восстанавливается, отдавая или приобретая электрон и изменяя таким образом свою валентность. В дыхательной цепи направление транспорта электронов определяется величиной окислительно-восстановительного потенциала цитохромов.
В этой системе передавать электроны непосредственно на кислород способна только цитохромоксидаза (цит. а + а3). Из всех известных оксидаз она имеет наибольшее сродство к кислороду. Ингибиторами цитохромоксидазы являются СО, цианид, азид. Б растительных митохондриях кроме цитохромоксидазы функционирует оксидаза, не подавляемая цианидом и названная альтернативной оксидазой. Например, в митохондриях початков ароидных активность цианидустойчивой оксидазы в 10 раз превышает активность цитохромоксидазы.
Пероксидаза и каталаза. К пероксидазам относят целую группу ферментов, использующих в качестве окислителя пероксид водорода: классическую пероксидазу, NAD-пероксидазу, NADP-пероксидазу, пероксидазу жирных кислот, глутатионпероксидазу, цитохромпероксидазу и др. Все они работают по следующей схеме, где А — субстраты:
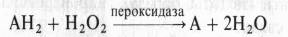
В последние 2 — 3 десятилетия показана полифункциональность пероксидаз. Помимо пероксидазной, у них имеется оксидазная функция, т. е. способность переносить электроны в отсутствие пероксидного кислорода на молекулярный кислород. Пероксидаза может также функционировать как анаэробная дегидрогеназа, например NADH-дегидрогеназа, передающая электроны от восстановленных пиридиновых нуклеотидов на разные акцепторы.
Пероксид водорода, помимо пероксидазы, расщепляется также каталазой, в результате чего образуется молекулярный кислород. В реакции участвуют две молекулы пероксида, одна из которых функционирует как донор, а другая — как акцептор электронов (см. выше).
Простетической группой пероксидазы и каталазы служит гем, в состав которого входит атом железа.
Оксигеназы. Наряду с оксидазами, которые используют молекулярный кислород как акцептор электронов, в клетках широко представлены оксигеназы, активирующие кислород, в результате чего он может присоединяться к органическим соединениям. Ферменты, внедряющие в субстрат два атома кислорода, называют диоксигеназами, а присоединяющие один атом кислорода — монооксигеназами или гидроксилазами. В качестве доноров электронов оксигеназы используют NAD(P)H, FADH2 и др.
Оксигеназы присутствуют во всех типах клеток. Они участвуют в гидроксилировании многих эндогенных соединений в частности аминокислот, фенолов, стеринов и др., а также в детоксикации чужеродных токсических веществ (ксенобиотиков).
Дихотомический путь
Регуляция гликолиза.
Интенсивность гликолиза контролируется в нескольких участках. Вовлечение глюкозы в процесс гликолиза регулируется на уровне Фермента гексокиназы по типу обратной связи: избыток продукта реакции (глюкозо-6-фосфата) аллостерически подавляет деятельность фермента.
Второй участок регуляции скорости гликолиза находится на уровне фосфофруктокиназы. Фермент аллостерически ингибируется высокой концентрацией АТР и активируется неорганическим фосфатом и ADP. Ингибирование АТР предотвращает развитие реакции в обратном направлении при высокой концентрации фруктозо-6-фосфата. Кроме того, фермент подавляется продуктом цикла Кребса — цитратом и через положительную обратную связь активируется собственным продуктом — фруктозо-1,6-дифосфатом (самоусиление).
Высокие концентрации АТР подавляют активность пируваткиназы, снижая сродство фермента к фосфоенолпирувату. Пируваткиназа подавляется также ацетил-СоА.
Наконец, пируВатдегидрогеназный комплекс, участвующий в образовании ацетил-СоА из пирувата, ингибируется высокими концентрациями АТР, а также NADH и собственным продуктом — ацетил-СоА.
Список использованной литературы
1.В.В. Полевой Физиология растений М.: Высшая школа 1989г.
2.Н.И. Якушкина Физиология растений М.: Просвещение 1993г.
Дыхание. Определение. Уравнение. Значение дыхания в жизни растительного организма. Специфика дыхания у растений
Образующиеся в ходе фотосинтеза сахара и другие органические соединения используются клетками растительного организма в качестве питательных веществ. Клетки незеленых частей и все клетки растения в темноте питаются веществами углеводной природы гетеротрофно и в этом принципиально не отличаются от животных клеток. Важнейшим этапом питания органическими веществами на клеточном уровне является процесс дыхания.
Клеточное дыхание — это окислительный, с участием кислорода распад органических питательных веществ, сопровождающийся образованием химически активных метаболитов и освобождением энергии, которые используются клетками для процессов жизнедеятельности.
Научные основы учения о роли кислорода в дыхании были заложены трудами A. Л. Лавуазье. В 1774 г. кислород независимо открыли Пристли и Шееле, а Лавуазье дал название этому элементу. Изучая одновременно процесс дыхания животных и горение, Лавуазье в 1773 — 1783 гг. пришел к выводу. что при дыхании, как и при горении, поглощается 02 и образуется С02, причем в том и другом случаях выделяется теплота. На основании своих опытов он заключил, что процесс горения состоит в присоединении кислорода к субстрату и что дыхание есть медленно текущее горение питательных веществ в живом организме.
Я. Ингенхауз в 1778—1780 гг. показал, что зеленые растения в темноте, а незеленые части растений и в темноте, и на свету поглощают кислород и выделяют С02 так же, как животные. Основателем учения о дыхании растений считают Н. Т. Соссюра. В 1797—1804 гг., впервые широко использовав количественный анализ, он установил, что в темноте растения поглощают столько же кислорода, сколько выделяется С02, т.е. соотношение С02/02, как правило, равно 1. При этом одновременно с С02 образуется и вода. Мнение Соссюра о том. что описанный им газообмен у растений является процессом дыхания и что этот процесс обеспечивает растительный организм энергией, долгое время не признавалось. Утверждалось, что в ночное время растения выделяют тот С02, который не был использован при фотосинтезе, и что этот С02 не имеет отношения к дыханию.
Однако постепенно накапливалось все больше данных о том, что дыхание животных и растений протекает однотипно, несмотря на отсутствие у растений специальных дыхательных органов, причем основным субстратом дыхания служат сахара. И. П. Бородин (1876) в серии точных опытов установил, что интенсивность дыхания листоносных побегов в темноте в первую очередь зависит от количества углеводов, накопленных ими на свету.
Во второй половине XIX в. в результате изучения дыхания у растительных и животных объектов общее уравнение этого процесса приняло следующий вид:
С6Н12О6 + 602 ► 6С02 + 6Н20 + энергия (2875 кДж/моль)
ЗНАЧЕНИЕ ДЫХАНИЯ В ЖИЗНИ РАСТЕНИЯ
Дыхание — один из центральных процессов обмена веществ растительного организма. Выделяющаяся при дыхании энергия тратится как на процессы роста, так и нa поддержание в активном состоянии уже закончивших рост органов растения. Вместе с тем значение дыхания не ограничивается тем, что это процесс, поставляющий энергию. Дыхание, подобно фотосинтезу, сложный окислительно_восстановительный процесc, идущий через ряд этапов. На его промежуточных стадиях образуются органические соединения, которые затем используются в различных метаболических реакциях. К промежуточным соединениям относят органические кислоты и пентозы образующиеся при разных путях дыхательного распада. Таким образом, процесс дыхания — источник многих метаболитов. Несмотря на то что процесс дыхания в суммарном виде противоположен фотосинтезу, в некоторых случаях они могут дополнять друг друга. Оба процесса являются поставщиками как энергетических эквивалентов (АТФ, НАДФ-Н), так и метаболитов. Как видно из суммарного уравнения, в процессе дыхания образуется также вода. Эта вода в крайних условиях обезвоживания может быть использована растением и предохранить его от гибели. В некоторых случаях, когда энергия дыхания выделяется в виде тепла, дыхание ведет к бесполезной потере сухого вещества. В этой связи при рассмотрении процесса дыхания надо помнить, что не всегда усиление процесса дыхания является полезным для растительного организма.
Дата: 2019-05-29, просмотров: 348.