2.3.1. Определение массовой доли сухих веществ. Содержание массовой доли влаги и сухих веществ определяют высушиванием навески в сушильном шкафу или рефрактометрическим методом.
Высушивание в сушильном шкафу. Метод основан на выделении гигроскопической влаги из исследуемого объекта при определенной температуре. Высушивание проводят до постоянной массы или ускоренными методами при повышенной температуре в течение заданного времени.
Высушивание образцов проводят с прокаленным песком, который придает навеске пористость, увеличивает поверхность испарения, препятствует образованию корочки, затрудняющей удаление влаги.
Очень влажные образцы подсушивают на водяной или песчаной бане. Для высушивания используют фарфоровые чашки, стеклянные или алюминиевые бюксы, предварительно высушенные и взвешенные.
Методика определения. В чашку или бюксу помещают навеску подготовленной пробы, бюксу закрывают крышкой и взвешивают на весах с указанной точностью, затем тщательно перемешивают навеску с песком с помощью стеклянной палочки, равномерно распределяя содержимое по внутренним стенкам чашки или бюксы, после чего помещают их в сушильный шкаф (крышку бюксы - отдельно) и проводят высушивание при 130єC в 30 мин, с момента установления заданной температуры.
После окончания высушивания бюксу закрывают крышкой. Бюксы и чашки переносят в эксикатор, охлаждают 20-30 мин и взвешивают.
Массовую долю сухих веществ (Х, %) вычисляют по формуле:
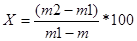
где: m – масса бюксы (чашки) с песком и палочкой, г;
m 1– масса бюксы (чашки) с навеской, песком и палочкой до высушивания, г;
m 2– масса бюксы (чашки) с навеской, песком и палочкой после высушивания, г.
Расхождение между результатами параллельных определений не должно превышать 0,5%. За конечный результат принимают среднее арифметическое значение двух параллельных определений.
2.3.2.Определение содержания соли методом Мора Определение соли методом Мора основано на реакции обмена между хлористым натрием и азотнокислым серебром в присутствии индикатора хромата калия, в результате чего в нейтральном растворе после осаждения всех ионов хлора образуется кирпично-красный осадок.
Методика определения. В химический стакан на 100 см3 взвесить 20г подготовленной пробы, прибавить небольшое количество дистиллированной воды и тщательно размешать стеклянной палочкой. Полученную смесь количественно перенести в мерную колбу на 250 см3, долить до ѕ ее объема дистиллированной водой, закрыть пробкой. Содержимое колбы тщательно перемешать и поставить на 30 минут для настаивания. После этого долить колбу до метки дистиллированной водой, закрыть пробкой, тщательно перемешать и профильтровать через сухой складчатый фильтр в чистую коническую колбу на 200 см3.
Из фильтрата пипеткой взять 10 см3 и перенести в коническую колбу на 50 см3, добавить 3-4 капли насыщенного раствора хромовокислого калия и оттитровать 0,05 моль/дм3 или 0,1 моль/дм3 раствором азотнокислого серебра до появления красно-бурой окраски, не исчезающей в течение 0,5 минуты. Процентное содержание поваренной соли рассчитайте по формуле:

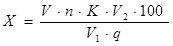
где: V – объем раствора азотнокислого серебра, израсходованного на титрование, см3;
n – количество хлористого натрия, соответствующее 1 см3 раствора азотнокислого серебра (для 0,05 моль/дм3 = 0,00292; для 0,1 моль/дм3 = 0,00585), г;
К – поправочный коэффициент к 0,05 моль/дм3 или 0,1 моль/дм3 раствора AgNO 3 ;
V 1 – объем фильтрата, взятый для титрования, см3;
q – масса навески, г;
V 2 – количество дистиллированной воды, взятой для настаивания, см3.
Дата: 2019-05-28, просмотров: 320.