ВЫПУСКНАЯ КВАЛИФИКАЦИОННАЯ (ДИПЛОМНАЯ) РАБОТА
На тему « Влияние загрязнения атмосферного воздуха
На состояние рябины обыкновенной
( Sorbus aucuparia L .) »
Научные руководители:
к.б.н., доцент Закамская Е.С.
к.б.н., доцент Скочилова Е.А.
Рецензент:
начальник отдела контроля атмосферного воздуха и промышленных выбросов филиал «ЦЛАТИ по РМЭ» ФГУ «ЦЛАТИ по ПФО»
Остривная М.В.
Студент _________________
Йошкар-Ола, 2007
Оглавление
Введение. 3
1. Обзор литературы.. 5
1.1. Атмосферный воздух и источники его загрязнения. 5
1.2. Действие загрязняющих веществ на растения. 7
1.3. Характеристика приоритетных загрязнителей воздуха и их отрицательного воздействия на древесные растения. 10
1.3.1 Диоксид серы.. 10
1.3.2 Окись углерода. 17
1.3.3 Оксиды азота. 19
1.3.4 Аммиак. 20
1.3.5 Пыль. 21
1.4 Устойчивость рябины обыкновенной. 23
2. Объект и методы исследования. 25
2.1. Объект исследования. 25
2.2. Методы исследования. 29
2.2.1 Методы анализа атмосферного воздуха. 29
2.2.2. Определение содержания серы в листьях рябины обыкновенной. 35
2.2.3. Исследование изменения морфометрических показателей рябины обыкновенной. 37
3. Результаты исследования и обсуждение результатов. 38
3.1.Характеристика атмосферного воздуха в городе Йошкар-Ола. 38
3.1.1. Содержание пыли. 39
3.1.2. Содержание диоксида азота. 41
3.1.3. Содержание углерода оксида. 42
3.1.4. Содержание аммиака. 44
3.1.5. Содержание ангидрида сернистого. 45
3.1.6. Расчет единичного индекса загрязненности атмосферы.. 46
3.2. Содержание серы в листьях рябины обыкновенной. 47
3.3. Изменение длины годичного побега рябины обыкновенной. 50
3.4 Изменение морфометрических показателей листовой пластинки рябины обыкновенной. 52
Выводы.. 61
Список литературы.. 62
Приложения. 69
Введение
В настоящее время исследования городской среды и связанные с ними теоретические и прикладные экологические проблемы необычайно актуальны, так как города становятся основной средой обитания человека. В последние десятилетия наблюдается интенсивное насыщение атмосферы городов газообразными и пылевидными отходами транспортных средств и промышленных предприятий (Воскресенская, 2004). Они вызывают ухудшение условий существования человека и других организмов, создавая угрозу здоровью населения, нарушению климата в локальных и глобальных масштабах (Калверт, 1988). В связи с этим остро ощущается потребность в научно-обоснованных и рациональных мероприятиях по предотвращению загрязнения атмосферы и сохранению нормальных условий жизни, труда и отдыха людей и биосферы в целом (Илькун, 1978).
Среди компонентов живого вещества биосферы наиболее существенным фактором нейтрализации газообразных токсикантов является растительность и особенно древесно-кустарниковые насаждения и естественные лесные массивы (Сергейчик, 1984). Поэтому одним из перспективных подходов для биологической характеристики воздушной среды является оценка состояния древесных растений по степени их газоустойчивости к промышленным выбросам (Соловьева, 2001).
Выполняя санитарно-гигиенические, архитектурные, хозяйственно-экономические и другие функции, зеленые насаждения несут огромную нагрузку (Рунова, 2004). Возможности их многогранны, но это совсем не значит, что они беспредельны. Растения отрицательно реагируют на наличие в воздухе даже в малых дозах токсических веществ. Они гораздо сильнее реагируют на те концентрации вредных веществ, которые у людей и животных не оставляют видимых явлений отравлений. Таким образом, они выполняют индикаторную функцию (Сергейчик, 1984).
В зонах повышенной загазованности, запыленности и перегрева атмосферного воздуха выявлена повсеместная повреждаемость растений. Установлено, что велика повреждаемость растений дымом со значительной концентрацией двуокиси серы, окиси азота и углерода, сероводорода, аммиака и других (Битюкова, 2004). Многие из этих соединений, растворяясь в воде, образуют вредные для растений кислоты (Майснер, 1981).
Растения в условиях урбанизированной (техногенной) среды, сохраняя внешне неизменный вид, претерпевают значительные изменения биохимического состава и физиологических процессов (Илькун, 1978). Промышленные газы и аэрозоли могут оказывать на растения комплексное и индивидуальное воздействие. Но нередко эффект повреждения вызывается одним, преобладающим в среде, соединением (Майснер, 1981).
Для оценки и прогноза состояния древостоя необходима ранняя диагностика нарушения жизнедеятельности древесных растений, подвергнутых воздействию газовых токсикантов. В первую очередь повреждения проявляются на физиолого-биохимическом уровне, затем распространяются на ультраструктурный и клеточный уровни и лишь после этого развиваются видимые признаки повреждения – хлорозы и некрозы тканей листа, опадание листьев, торможение роста (Горышина, 1991).
Целью данной работы является оценка влияния загрязнения воздушного бассейна города Йошкар-Олы на морфометрические показатели рябины обыкновенной (Sorbus aucuparia L.).
Для реализации данной цели были поставлены следующие задачи:
1. Исследовать степень загрязнения атмосферного воздуха в различных районах города Йошкар-Олы.
2. Определить концентрацию серы в листьях рябины обыкновенной в зависимости от района произрастания.
3. Установить влияние диоксида серы, содержащегося в атмосферном воздухе на морфометрические показатели рябины обыкновенной.
По результатам исследований опубликована одна печатная работа.
Обзор литературы
Диоксид серы
Среди серосодержащих техногенных эмиссий наиболее фитотоксична двуокись серы. Установлено, что SO2 является сильнодействующим ассимиляционным ядом (Сергейчик, 1984). В тоже время SO2 является местным ядом, убивающим только те участки мезофилла листа, в которые он проник, не затрагивая, существенно, жизнедеятельность соседних участков мезофилла. Растений, абсолютно устойчивых к сернистому газу, как и к другим вредным промышленным отходам, практически нет. Растения, у которых участки повреждений составляют до 20 % общей площади листьев, относят к слабоповреждаемым. У среднеповреждаемых видов участки повреждений составляют до 50 % и у сильноповреждаемых - свыше 50 %. Более восприимчивыми к сернистому ангидриду оказались липа сердцелистная (Tilia cordata L.), клен остролистный (Acer platanoides L.), рябина обыкновенная (Sorbus aucuparia L.), черемуха обыкновенная (Padus racemosa (Lam.) Gilib.), смородина черная (Ribes nigrum L.) и другие (Николаевский, 1979).
Поступление. Диоксид серы, прежде всего, воздействует на клетки, которые регулируют открывание устьиц. Степень их открывания в начальный период является основным параметром, определяющим интенсивность воздействия загрязнителя (Калверт, 1988). Даже при очень малых концентрациях диоксид серы способен оказывать стимулирующее действие, в результате которого устьица остаются постоянно открытыми. В тоже время при высоких концентрациях диоксида серы устьица закрываются. Кроме того, в случае высокой влажности устьица открываются, в случае низкой – закрываются (Илькун, 1978).
Попав в межклеточное пространство листа, загрязняющее вещество вступает в контакт с мембраной окружающей клетку. При нарушении целостности этой полупроницаемой мембраны нарушается баланс питательных веществ и процесс поступления ионов. Пройдя в клетку, диоксид серы взаимодействует с митохондриями и хлоропластами, в том числе и с их мембранами, что может привести к весьма серьезным последствиям (Павлов, 2003).
Потребность. Сера необходима для нормального роста растений, и присутствие SO2 может оказывать влияние и на усвояемость серы. Растения потребляют серу в восстановленном состоянии (Горышина, 1991). В присутствии SO2 основным продуктом становится сульфат; присутствует также цистеин, глютатион и, по меньшей мере, одно не идентифицированное вещество. Основными промежуточными соединениями при восстановлении сульфатов являются сульфиты (Лесные экосистемы.., 1990).
Механизм токсического действия SO2 детально обсуждается в ряде монографий (Илькун, 1979; Николаевский, 1979; Гудериан, 1979) и научных статей отечественных и зарубежных авторов. Сернистый ангидрид в воздухе постепенно окисляется до серного и растворяется в воде, образуя мельчайшие капельки серной кислоты, повреждающей листья (Романова, 2005).
Механизм фототоксического действия заключается в неспецифическом нарушении деятельности многих ферментов вследствие подкисления цитоплазмы и нарушения ионного режима. Наблюдаются нарушения метаболизма органических соединений, фотосинтетических структур, происходит накопление балластных токсических продуктов, транспортных путей миграции энергии от хлоропластов к центрам их использования, появляются автокаталитические цепные реакции свободнорадикального и фотодинамического окисления (Николаевский, 1978, 1979). Токсичность сернистого газа значительно увеличивается в присутствии других загрязнителей - окислов азота и озона.
Различают 2 группы повреждений, связанных с действием SO2:
1. видимые, выражающиеся в деформации, пятнистости и некрозах ассимиляционных органов;
2. скрытые, проявляющиеся в снижении продуктивности за счет ингибирования фотосинтеза, изменении метаболизма, увеличении восприимчивости к болезням и вредителям, ускорении старения растений (Лесные экосистемы.., 1990).
Морфологические повреждения. Это соединение адсорбируется на поверхности растения, в основном на его листьях, и оказывает на него вредное влияние. Обычно поражаются края листовой поверхности, а центральные зоны листа, примыкающие к осевой и главным боковым жилкам, остаются здоровыми (Кулагин, 1974). Появляются пятна на участках между жилками и краях листа. Потом эти участки приобретают желтый и красно-оранжевый цвет и отмирают. При длительном воздействии сернистого газа подавляется рост растений, в некоторых случаях отмирают верхушки побегов.
Физиологические повреждения. Сернистый ангидрид и другие кислые газы, проникая внутрь листа, нарушают процесс фотосинтеза, связывая, в частности, каталитически активное железо. Процессы окисления протекают с участием свободных радикалов, образованных из двуокиси серы в результате химических реакций (Лесные экосистемы.., 1990). Они окисляют ненасыщенные жирные кислоты мембран, тем самым, изменяя их проницаемость, что в дальнейшем отрицательно влияет на процессы дыхания, фотосинтеза.
Фотосинтетический аппарат клетки проявляет высокую чувствительность к SO2 , которая может нарушать световую и темновую стадии фотосинтеза, воздействуя на состояние хлорофилла, активность ферментов, электронтранспортную цепь или ламеллярную структуру гран. SO2 уменьшает скорость выделения кислорода, но не влияет на скорость поглощения кислорода в процессе дыхания. По мнению японских исследователей, SO2 инактивирует первичный донор электронов или сам реакционный центр цепи переноса электронов. 1∙10-6 SO2 в течение 6 часов обработки листьев существенно снижает ациклическое фосфорилирование (Сергейчик, 1984). Аккумуляция в тканях избыточного количества серы приводит к нарушению работы регуляторных механизмов и патологическим явлениям, вследствие чего наблюдается депрессия роста клеток, тканей и органов, нарушаются синтетические и обменные процессы. Причиной этому является подавление синтеза АТФ и изменение активности ферментных систем (Илькун, 1978).
В условиях выключенного фотосинтеза, но продолжающегося поступления солнечной энергии хлорофилл начинает, как флуоресцирующее вещество проявлять фототодинамическое действие, которое сводится к фотоокислениям. Фотоокислению подвергаются разнообразные вещества – белки, фосфатиды, аминокислоты и др. Поэтому под влиянием сернистого ангидрида происходит их разрушение, ведущее к отмиранию клеток и сопровождаемое снижением окисляемости клеточного содержимого. С повышением интенсивности освещения токсичность сернистого ангидрида возрастает, и наоборот (Кулагин, 1974).
Анатомические повреждения. При частых или постоянных воздействиях низких концентраций газов в тканях растений постепенно накапливаются токсичные соединения серы (Кулагин, 1974). Нинова Д. (1970) под влиянием SO2 обнаружила уменьшение объема межклетников в губчатой ткани, усиленное развитие кутикулы, удлинение клеток палисадной ткани. Уменьшается объем клеток ассимиляционной паренхимы наряду с уменьшением толщины столбчатой, губчатой ткани и всего листа (Сергейчик, 1984).
Биохимия. Сернистый газ снижает содержание в растениях дисахаров и способствует увеличению количества крахмала. Причиной этого является активизация и дезактивация различных ферментов, стимуляция и подавление синтеза специфических ДНК и РНК (Майснер, 1981). Согласно Мальхотра (1977), биохимическим порогом фитотоксического действия SO2 является концентрация 0,05∙10-6 . Однако существует мнение, что пороговой является величина, в 5 раз меньшая (0,01∙10-6), при которой обнаруживается изменения содержания галактолипидов мембран тилакоидов (Сергейчик, 1984). Диоксид серы ингибирует различные биохимические реакции. Сульфиты, обладающие слабокислотными свойствами, дезактивируют некоторые ферменты, блокируя активные центры, препятствуя протеканию основной химической реакции; это явление известно как конкурентное ингибирование (Илькун, 1978). Диоксид серы является конкурентным ингибитором дифосфаткарбоксилазы, препятствующим фиксации СО2 в процессе фотосинтеза. Обладая свойствами свободных радикалов, SO2 нарушает протонный градиент, с которым связано образование АТФ (Лесные экосистемы.., 1990).
Загрязнение воздуха SO2 вызывает нарушение азотного обмена древесных растений, глубина и направленность которого зависят от возраста и биологических особенностей вида. Появление видимых симптомов повреждения коррелирует с накоплением в листьях значительного количества путресцина, глютамина, аммиака. Малые дозы SO2 увеличивают, а высокие уменьшают содержание общего и белкового азота. Для устойчивых видов отмечается рост содержания водорастворимых белков альбуминов – белков нерастворимого остатка. У неустойчивых (относится рябина) – превращения белков направлены в сторону уменьшения содержания альбуминов, глобулинов и увеличения высокомолекулярных белков (Шацкая, 1983). Повышение концентрации SO2 сопровождается снижением общего количества фосфатов, которые необходимы для роста и развития растений. Одновременно с увеличением или уменьшением общего фосфора синхронно и в том же направлении изменяется содержание неорганического фосфора. При скрытых поражениях листьев количество кислотонерастворимых фосфорных соединений уменьшается (Сергейчик, 1984). При наличии видимых повреждений их количество вначале быстро возрастает, а с повышением степени повреждения листьев – превышает контрольные величины незначительно (Илькун, 1979). Загрязнение воздуха SO2 также нарушает углеводный обмен. При скрытых и начальных повреждениях листьев уменьшается содержание дисахаров, но значительно увеличивается содержание крахмала. Более сильные повреждения – ослабляют гидролиз и синтез крахмала с одновременным уменьшением содержания моно- и дисахаров (Лесные экосистемы.., 1990). В этом случае не только изменяется скорость взаимопревращения углеводов, но и происходит подавление фотосинтетической деятельности листьев (Илькун, 1982).
Хотя точный механизм действия SO2 на молекулярном уровне неизвестен, можно предположить, что основную роль играют присутствие избыточного количества окисленных форм серы, нарушение баланса с восстановленными формами и воздействие на жизненно важные ферменты.
Адаптации. Под влиянием SO2 у растений усиливаются признаки ксероморфности: уменьшается площадь листовых пластинок, увеличивается степень жилкования и количество устьиц, размеры клеток устьичного аппарата уменьшаются (Сергейчик, 1984). Добровольский И.А., Щербак Н.О. (1976) установили, что в процессе приспособления к условиям загрязнения у растений наблюдается мелкоклетность, утолщение клеточных оболочек.
Последствия от диоксида серы: обожженные листья после газовой атаки не опадают сразу же, а продолжают оставаться в кроне. Однако продолжительность их жизни заметно сокращается, и они опадают на 4-6 недель раньше по сравнению со здоровыми листьями (Николаевский, 1969). При остром поражении (более 2 мг/м3) уже через 1-2 часа происходит побурение и гибель листьев, чаще отдельных их участков в виде пятнышек с четко очерченной границей между живыми и отмершими клетками и тканями. При слабом поражении (менее 0,5 мг/м3) и длительном действии диоксида серы листья обесцвечиваются (Хвастунов, 1999).
Влияние погодных условий. Установлено, что эффект влияния SO2 на растения зависит от особенностей сопутствующих метеорологических факторов: повторяемости, продолжительности и мощности температурных инверсий, скорости ветра, наличия туманов. С повышением температуры и относительной влажности воздуха увеличивается опасность повреждения растений. Наибольшую чувствительность к SO2 листья обнаруживают в диапазоне 18-400С, а наименьшую – при температуре, близкой к 40С. В пределах 4 – 180С изменения в газочувствительности незначительны (Крокер, 1950). Цан (1963) установил, что устойчивость кустов смородины к SO2 значительно возрастает по мере снижения влажности воздуха. Так, 8-часовое воздействие SO2 в концентрации 0,8∙10-6 при относительной влажности 87% сопровождалось появлением сильных некрозов ассимиляционных органов. Степень повреждающего действия SO2 в концентрации 4∙10-6 при 42% относительной влажности воздуха уменьшалась вдвое. При понижении влажности воздуха до 29% повреждающий эффект токсиканта отсутствовал. Эти данные хорошо согласуются с выводами Томаса и Хендрикса о снижении газочувствительности растений в 10 раз в случае падения влажности воздуха от 100 до 0%. Различия в газочувствительности растений в зависимости от условий влажности отражают неодинаковое накопление загрязнителя в органах ассимиляции. Оно увеличивается по мере повышения тургорного давления и более полного открывания устьиц (Сергейчик, 1984). Инверсии и слабые ветры способствуют сильному возрастанию фитотоксичности SO2 при скоплении в районах с пониженным рельефом местности. Фитотоксичность SO2 увеличивается в условиях засухи (Николаевский, 1969) и крайне холодной зимы.
Влияние времени суток. Газочувствительность растений изменяется в течение суток. Она наиболее высока в предполуденное время, спустя 4-5 часа, после рассвета. Ранним утром, вечером и ночью газочувствительность падает (Лесные экосистемы.., 1990). В экспериментах по определению количества поглощаемой SO2 в темновой и световой периоды было показано, что ночью в листьях накапливается в 3 раза меньше серы, чем днем (Майснер, 1981). Имеются данные о резком ослаблении фитотоксичности SO2 в затенении. Под пологом дубово-липового леса по сравнению с его опушкой газовые ожоги исчезают не только у световых, более ксероморфных, но и у теневых листьев (Кулагин, 1974).
Окись углерода
Окись углерода малотоксична для растений, но считается, что зеленые насаждения не способны очищать от нее атмосферу (Николайкина, 2003). Повышение концентрации CO2 в атмосфере, даже без учета глобального потепления, способно привести к значительному изменению структуры и функционирования экосистем, что скажется неблагоприятно на растениях (Алексеев и др., 1999). Удвоение концентрации CO2 в атмосфере влияет на древесные растения за счет:
· снижения обмена веществ, через устьичный аппарат;
· усиления фотосинтеза.
В большинстве случаев это приводит к усилению прироста деревьев и эффективности водопоглощения.
Морфология. Длительное выдерживание растений при высокой концентрации CO2 сопровождается увеличением площади и толщины листа, стимуляцией роста побегов второго порядка, усилением ветвления или кущения (Павлов, 2003), также увеличивается длина стеблей и корней, количество цветков, плодов и семян, возрастает доля корней и запасающих органов. Наблюдается увеличение продолжительности жизни, изменение времени смены фаз развития, увеличивается число клеток мезофилла и хлоропластов (Романова, 2005).
Биохимия. Исходя из физиологических особенностей, пользу от повышения CO2 могут извлечь С3-растения, к которым относятся практически все деревья. У С3-растений на первой стадии фиксации молекула CO2 связывается с рибулозодифосфатом, содержащим 5-углеродный сахар. В результате реакции, происходящей под действием фермента рибулозодифосфаткарбоксилазы, образуется короткоживущее нестабильное соединение, включающее 6-углеродный сахар. Оно распадается на два производных, которые содержат по три атома углерода – отсюда и название «С3-растения». С диоксидом углерода за активный центр рибулозодифосфаткарбоксилазы конкурирует кислород атмосферного воздуха. Если побеждает кислород, растение теряет энергию, так как во время утилизации кислорода не происходит фиксации CO2 (Калверт, 1988). По мере увеличения концентрации CO2 вероятность связаться с активным центром фермента повышается. Однако у этих растений, в условиях возросшей концентрации CO2 сначала происходит усиление фотосинтеза, но после временной активации наступает его торможение (Соловьев и др.,1989). Транспортная система растения полигенна и зависит от многих факторов (энергетических, гормональных и др.), поэтому не может быстро перестроиться. Поэтому при длительном воздействии на растение CO2, в условиях повышенной концентрации, фотосинтез снижается из-за избыточного накопления крахмала в хлоропластах (Мокроносов, 1992).
Физиология. Наиболее часто наблюдаемая реакция растений на повышение концентрации CO2 - уменьшение устьичной щели и, как следствие, уменьшение проводимости водяного пара. Экспериментальные данные об изменениях числа устьиц на единице площади листьев при повышении концентрации CO2 в современных условиях еще крайне ограничены и противоречивы. В то же время, установлено, что в предыдущие геологические эпохи число устьиц на единице поверхности листа при низком содержании CO2 в атмосфере увеличивалось, а при высоком – снижалось (Романова, 2005).
При изменении концентрации CO2 в широких пределах, в растениях, представляющих наиболее северные леса умеренной полосы, усиливается фотосинтез (Соловьев и др., 1989).
Изменение концентрации CO2 должно быть строго сбалансировано с потребление азота, фосфора, других питательных веществ, света, воды, без нарушения экологического равновесия (Алексеев и др., 1999). Нарушение баланса, безусловно, скажется на устойчивости растений и их продуктивности (Павлов, 2003).
Оксиды азота
Среди них наиболее распространенными загрязнителями воздуха являются оксид азота NO(II) и диоксид азота NO2 (IY).
Оксид азота NO – бесцветный тяжелый газ, кислородом воздуха окисляется до диоксида азота.
Диоксид азота NO2 - газ коричнево-бурого цвета (плотностью 1,49 кг/м3), который, реагируя с влагой воздуха, превращается в азотную и азотистую кислоты. Время жизни NO2 в атмосфере около 3 суток. NO2 обусловливает фотохимическое загрязнение атмосферы, поскольку реагирует с другими веществами: с диоксидом серы SO2, кислородом, углеводородами. Диоксид азота в пять раз токсичнее оксида азота. В атмосфере оксид и диоксид азота находятся в динамическом равновесии, превращаясь друг в друга в результате фотохимических реакций, в которых участвуют в качестве катализатора. Их соотношение в воздухе зависит от интенсивности солнечного излучения, концентрации окислителей и других факторов (Косулина, 1993) .
Оксиды азота вызывают сходные с диоксидом серы физико-биохимические повреждения у древесных пород (Хвастунов, 1999).
Морфология. В городском воздухе, в зонах с повышенным содержанием окислов азота, наблюдается «позеленение» стволов и нижних ветвей деревьев, что способствует интенсивному разрастанию на коре деревьев мелких водорослей зеленого цвета. Они получают необходимое им обильное азотное питание непосредственно из воздуха. На листьях появляются темно-коричневые или темные почки, расположенные между жилками и по краю листа (Косулина, 1993). В концентрациях более 2 мг/м3 вызывают глубокие повреждения листьев. Отличительной особенностью их являются буровато-черные участки, чаще всего у вершины и у периферии листовой пластинки (Хвастунов, 1999).
Физиология. Двуокись азота ингибирует транспирацию в освещенных листьях, вызывая частичное закрывание устьиц (Илькун, 1978). Действие газообразных NO2 и NO2 в концентрациях не приводящих к появлению видимых повреждений, вызывает понижение интенсивности фотосинтеза. Комбинированное действие этих газов аддитивно, однако эффект воздействия NO проявляется быстрее, чем эффект действия NO2 . Ингибирование фотосинтеза под действием NOx может быть вызвано конкуренцией за НАДФН, происходящих в хлоропластах процессов восстановления нитрита и ассимиляцией СО2. Закисление, вызванное NO2 влияет на транспорт электронов и фотофосфорилирование (Трахтенберг, 1994). Под действием NO2 происходит разбухание мембран хлоропластов (Загрязнение воздуха.., 1988).
По сообщению Г. Хаута (1975) NO2 в 1,5-5 раз менее токсичен для растений по сравнению с SO2 . Хаут считает, что безвредная концентрация NO2 составляет 0,35 мг/м3 , при длительном действии на растения и 0,8 мг/м3 при газации 30 мин. Фитотоксичность окислов азота повышается при одновременном проникновении их в листья вместе с сернистым газом и озоном (Илькун, 1978).
Аммиак
Аммиак для растений менее токсичен, чем сернистый газ, однако при длительном воздействии даже низких его концентраций обнаруживаются заметные признаки повреждения растений (Соловьева, 2003).
Морфология. Повышенные концентрации аммиака вызывают появление темных, почти черных, пятен некрозов на обеих поверхностях листа, опадание листьев (Павлов, 2003).
Физиология. Биохимические и структурные изменения мембран могут происходить под действием образующегося из диоксида азота NH3 , не включенного в аминосоединения. NH3 ингибирует фотосинтез путем разобщения электронного транспорта и приводит к структурным нарушениям (Загрязнение воздуха.., 1988).
Пыль
Пыль, представляет собой взвешенные в воздухе или осевшие на поверхности тех или иных объектов твердые частицы наземного (в том числе промышленного), вулканического, органического или космического происхождения. Наибольшей фитотоксичностью обладают пылевые выбросы алюминиевых заводов, электростанций, металлургических предприятий, асбестовых, цементных заводов, предприятий бытовой химии и ряда других. В общем объеме антропогенных выбросов промышленная пыль разнообразных производств составляет всего 10% и более, но последствия ее фитотоксического действия подчас бывает трудно оценить (Хвастунов,1999).
Степень отрицательного воздействия промышленной пыли на растения зависит от ряда факторов, среди которых основными являются ее химический состав и растворимость в воде, скорость оседания пылевых частиц и продолжительность удерживания их на поверхности, возможность образования воздухонепроницаемых корок (Соловьева, 2001).
Токсическое действие промышленной пыли оказывает на растения прямой и косвенный эффект. Прямой эффект обычно связан с наличием острых повреждений, вызванных тремя типами фитотоксических воздействий: механическим, физическим, химическим (Соловьев и др., 1989).
Механическое воздействие пыли оценивается не только количеством пыли осевшей на надземных органах растений, но и характером распределения пылевых частиц на листовых пластинках. При этом важно учитывать связь осевшей пыли со структурными элементами листа – устьицами, через которые осуществляется газообмен растений (Тищенко, 1993). Твердые частицы обычно распределяются по поверхности очагами, скапливаясь на кончике листа и по его периферии. Механическая закупорка твердыми частицами устьичной щели может нарушить устьичную регуляцию и соответственно процессы газообмена и транспирации (Косулина, 1993).
Физическое действие пыли может проявиться в изменении оптических свойств света, проходящего через слой пыли. Это приводит к резкому повышению адсорбции длинноволнового излучения. В результате запыленные листья суммарно поглощают больше лучистой энергии за счет инфракрасного излучения, что приводит к повышению температуры запыленных листьев. Чем плотнее слой пыли, тем выше температурный градиент листа, а, следовательно, больший расход воды на транспирацию. Повышение транспирации приводит к усиленному расходованию запаса влаги из корнеобитаемого слоя почвы и при ограниченном запасе влаги в засушливые периоды способствует установлению глубокого водного дефицита. Повышение температуры запыленных листьев в сочетании с водным дефицитом является причиной подавления фотосинтетической активности и других физиологических функций растений (Соловьева, 2001).
Химическое действие пыли обусловлено фитотоксичностью составляющих ее частиц и их растворимостью в воде, гидратированной из воздуха или транспирационной, присутствующей на поверхности листа (Хван, 2003). Проникая через устьица или кутикулярные покровы во внутренние ткани листа, растворы солей, обычно в виде ионов, вызывают разнообразные структурные повреждения тканей и зеленых пигментов.
Косвенный эффект воздействия промышленной пыли всегда бывает трудно оценить, так как повреждения проявляются обычно по прошествии длительного времени, носят хронический характер и часто скрыты от глаз наблюдателя (Илькун, 1978). Это объясняется тем, что депрессирующее влияние пыли может сказываться на разнообразных компонентах растительных ценозов, приводя к угнетению их роста, возникновению морфологических аномалий, исчезновению неустойчивых видов, изменению химического состава почв, гибели микрофлоры и прочее (Рунова, 2004).
Даже слабое, но постоянное воздействие пылевых выбросов на определенные структурные и функциональные звенья экосистемы вызывает нарушение естественных биологических сообществ и снижение общей устойчивости к другим внешним повреждающим воздействиям. Ослабленные деревья, как правило, становятся объектами массового заселения стволовыми вредителями или грибных инфекций, приводящих к быстрому отмиранию древостоев (Соловьева, 2003).
Физиология. Пыль сильно ослабляет газообмен, процессы дыхания и фотосинтеза, вызывает угнетение растений и затрудняет их рост, снижает продуктивность и скорость возобновления, упрощает породный состав в результате исчезновения неустойчивых видов сообщества (Соловьев, 1989).
Объект исследования
Систематика:CORMOPHYTA - Высшие растения
Отдел: Maqnoliophyta (Anthophyta) – Цветковые или покрытосеменные
Класс: Maqnoliopsida (Dicotyledones) – Магнолиопсиды или двудомные
Подкласс: Rosidae - Розиды
Порядок: Rosales - Розоцветные
Семейство: Rosaceae – Розовые (розоцветные)
Подсемейство: Maloideae – Яблоневые
Род: Sorbus - Рябина
Вид: Sorbus aucuparia L. – Рябина обыкновенная (Сергиевская, 2002).
Ареал. Область распространения рябины обыкновенной охватывает почти всю Европу. Она занимает большую часть лесной и лесостепной зон европейской части СНГ. Растет в лесах Сибири, Дальнего Востока, в горных лесах Карпат, Крыма и Кавказа (Бродович, 1979). Также отличается очень широкой экологической амплитудой (Онтогенетический.., 2000). В подлеске хвойных и смешанных лесов отдельными деревьями или группами, по лесным опушкам, вырубкам и гарям, оврагам, по берегам рек и ручьев, (Восточно-европейские..,1994). В РМЭ рябина обыкновенная встречается по всей территории очень часто, в лиственных, смешанных и хвойных лесах (Абрамов, 2000). Существует 84 вида рябины, в нашей стране растет 43 вида.
Морфологическое описание.
Жизненная форма. Одноствольное или многоствольное дерево или крупный кустарник до 15-20 м высотой, 30-40 см в диаметре. Ствол прямой. Кора гладкая, серая. Крона ажурная, шарообразная или яйцевидная (Онтогенетический.., 2000).
Корневая система у рябины имеет неглубокий стержневой корень и хорошо развитые в радиальном направлении ветвящиеся корни (Харитонович, 1968).
Побеги двух типов: удлиненные вегетативные и укороченные генеративные голые и покрыты сверху блестящей сероватой пленкой (Атрохин и др., 1982). Часто встречаются укороченные побеги (Валягина-Малютина, 2001).
Почки войлочно-пушистые, заостренные, 0,8-2 см длиной, с 4-6 кроющими чешуями. Расположение почек спиральное. Листовой рубец узкий, с 5 следами, но снаружи, чаще видны 3-4 следа (Валягина-Малютина, 2001).
Листья сложные, непарноперистые (Сергиевская, 2002), очередные, продолговато-эллиптические с 9-15 (реже 17) листочками (Бродович, 1979), покрытые у основания железками. Общий черешок длиной 8-17см (Онтогенетический.., 2000). Листочки продолговатые, острые, длиной 2-7см и шириной около 2 см, по краям просто- и двоякопильчатые, у основания цельнокрайние, с верхней стороны темно-зеленые, с нижней - серо-зеленые, жилкование несовершенноперистое (Атрохин и др.,1982). Конечный листочек часто к основанию более суженный, иногда сросшийся с 1-2 верхними боковыми листочками (Онтогенетический..,2000).
Цветки с пятичленным околоцветником обоеполые, мелкие, диаметром до 1см., собраны в крупные щитковидные соцветия 10-15см в диаметре (Кречетова, 1997) на концах укороченных побегов желтовато-белые или зеленоватые, длиной 5-10см, ароматные, горько-миндального запаха. Цветки появляются после распускания листьев, в мае-июне. Опыляется жуками, мухами (Сергиевская, 2002).
Плоды округлые яблочки, мелкие, диаметром 6-10 мм., 2-5-гнездные, оранжево-красные, блестящие (Бродович, 1979). На вкус горько-кислые, с 2-6 семенами терпкие, со своеобразным запахом, созревают в сентябре-октябре.
Семена с эндоспермом, обычно в количестве 3 штук, мелкие, сплюснутой формы, на концах острые или с загнутыми концами, трехгранные, коричневые, длиной около 4 мм, шириной 2 мм, толщиной 1мм (Онтогенетический.., 2000). Семенная кожура светло- или темно-коричневая, блестящая. Всхожесть высокая.
Проростки однопобеговые с двумя овальными семядольными и двумя ассимилирующими листьями. Семядольные листья эллиптической или слегка яйцевидной формы, с коротким черешком, суженным основанием, 6-7 мм длиной и 3-4 мм шириной (Онтогенетический.., 2000).
Ритм сезонного развития. Живет рябина до 150 и более лет. Растет быстро, за 1 год вырастает на 0,5м. В первом десятилетии в благоприятных экологических условиях рябина обыкновенная является быстрорастущей древесной породой. Во втором – энергия ее роста в высоту снижается. Под пологом леса, особенно на бедных почвах, она растет небольшим деревцем или кустарником (Харитонович, 1968).
Возобновление. После рубки рябина успешно возобновляется пневой порослью, отличающейся в первые годы быстрым ростом.
Размножение отводками. В лесные культуры рябину высаживают 2-летними сеянцами. В пределах своего обширного естественного ареала успешно размножается семенным путем (Харитонович, 1968). Образует пневую поросль и корневые отпрыски (Атрохин и др., 1982).
Расселение. По лесам, опушкам и открытым местам способствуют птицы. Самосев рябины появляется не только в лиственных и хвойно-лиственных лесах, но и в чисто хвойных. Однако лучше всего она разрастается на вырубках и других более освещенных местах. Под пологом ее кустов и зарослей часто поселяется ель и пихта, которые затем ее перерастают. В искусственных степных лесопосадках рябина расселяется с помощью птиц.
Экология вида. Одни авторы относят рябину обыкновенную к теневыносливым видам (Харитонович, 1968; Атрохин и др., 1982), другие напротив к достаточно светолюбивым (Бродович, 1979), однако и те и другие считают, что она может мириться с большим затенением, но не цветет в таких местах и выглядит угнетенной. Морозоустойчива и заморозками не повреждается, засухо- и жароустойчива (Харитонович, 1968) К почве рябина нетребовательна. (Атрохин и др., 1982).
Эдафический фактор: к почве рябина нетребовательна. (Атрохин и др., 1982). Удовлетворительно растет на подзолистых и дерново-подзолистых, суглинистых и супесчаных почвах лесной зоны, на серых и темно-серых суглинках и деградированных черноземах лесостепи, на черноземных почвах степной зоны и в горах на горно-лесных бурых почвах (Харитонович , 1968). Однако интенсивнее она растет на свежих глубоких плодородных супесчаных и суглинистых почвах (Бродович, 1979). Для произрастания этой породы непригодны засоленные, торфяно-болотные почвы и глубокие выщелоченные пески (Харитонович, 1968).
Применение. Рябина – ценная древесная порода, дает качественную красноватую древесину (Бродович, 1979), которая идет на изготовление различных столярных изделий, мебели, музыкальных инструментов; она огнестойка и с трудом загорается. Кора применяется для выделки самых дорогих и тонких кож. Листья рябины выделяют летучие вещества, убивающие бактерии (Онтогенетический.., 2000).
В медицине. Содержащиеся в ягодах рябины вещества повышают устойчивость организма к кислородному голоданию. Рябина укрепляет организм, способствует налаживанию обмена веществ, при помощи препаратов рябины лечат головные боли. Благодаря содержанию в рябине биологически активных веществ ее используют в борьбе с раком. С помощью отвара цветков рябины лечат зоб. Сорбит понижает содержание жира в печени, холестерина в крови и используется как заменитель сахара.
В народной медицине используют плоды, цветки, листья рябины обыкновенной. Они обладают желчегонным и мочегонным свойствами, а также противовоспалительным, витаминным, потогонным действием, понижают кровяное давление, повышают свертываемость крови.
В озеленении. Рябина и ее формы – красивые декоративные растения, широко используемые в зеленом строительстве (Бродович, 1979). Часто разводится в садах и парках. Выращивается в виде промышленной культуры повсеместно (Валягина-Малютина, 2001).
Методы исследования
Исследования проводились на базе филиала «Центр лабораторного анализа и технических измерений по Республике Марий Эл» (филиал «ЦЛАТИ по РМЭ» ФГУ «ЦЛАТИ по Приволжскому федеральному округу»).
Для определения района исследования использовали Государственный доклад о состоянии окружающей природной среды Республики Марий Эл в 2003 году и Ежегодный доклад о состоянии окружающей природной среды Республики Марий Эл в 2004 году.
Содержание пыли
Пылевидные частицы, содержащиеся в воздухе во взвешенном состоянии, оседают на надземных органах растений при соприкосновении с ними или под действием гравитационных и электрических сил. Осевшие на листьях пылевидные частицы создают дополнительный экран на пути проникновения лучей к хлоропластам, в большей или меньшей мере поступают во внутренние ткани листа и тем самым нарушают его нормальную жизнедеятельность (Соловьева, 2001).
Многие растения обладают пылеустойчивостью, например, такие как: вяз гладкий (Uimus laevis L.), липа сердцелистная (Tilia cordata L.), ель колючая (Picea pungens Engelm.), каштан конский (Aesculus hippocastanum L.), клен остролистный (Acer platanoides L.), можжевельник обыкновенный (Juniperus communis L.), черемуха обыкновенная (Padus racemosa (Lam.) Gilib.) и другие (Хвастунов, 1999). Задержке пыли способствует наличие на листьях опушения, так же противодействуют процессу оседания пыли, часто выпадающие осадки, смывающие с поверхности листа осевшие частицы и вымывающие адсорбированные поверхностными тканями ингредиенты.
Запыленность атмосферы нарушает работу устьичного аппарата растений, ограничивает процесс транспирации, ослабевает процесс фотосинтеза, понижает уровень сахаров в тканях, темпы накопления сухого вещества и роста растений (Артамонов, 1986).
Нами был проведен лабораторный анализ отобранных проб воздуха на наличие пыли в атмосферной среде города Йошкар-Олы.
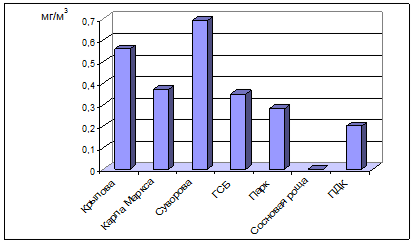
Рис 1. Содержание пыли в атмосферном воздухе.
Как можно видеть из рисунка 1, высокая концентрация пыли в воздушной среде города была обнаружена на всех исследуемых улицах, кроме Сосновой рощи. На улице Суворова содержание исследуемого загрязнителя было наибольшим и составило 0,69 мкг/м3. На улице Крылова содержание пыли составило 0,56 мкг/м3. Для улиц Карла Маркса и Героев Сталинградской битвы показатели по данному загрязнителю имели примерно одинаковые средние значения и составили 0,37 и 0,35 мкг/м3 соответственно. Достаточно низкие показатели по концентрации пыли были получены в Парке культуры и отдыха XXX-летия ВЛКСМ и составляли 0,28 мкг/м3.
Таким образом, содержание исследуемого загрязнителя в воздухе колебалось в пределах от 0,28 до 0,69 мкг/м3. Причем превышение содержания пыли по сравнению с ПДК было выявлено на всех исследуемых улицах, за исключением контрольной. Установленная предельно-допустимая концентрация для данного загрязнителя в атмосферном воздухе составляет 0,2 мкг/м3 (табл. 4) (Руководство по контролю…, 1991). На улице Суворова содержание пыли по сравнению с ПДК составило 3,45 ПДК. В остальных перечисленных районах наблюдения концентрация пыли гораздо ниже, но и там наблюдается превышение предельно допустимой концентрации.
Содержание диоксида азота
Другим не менее опасным загрязнителем воздуха является и диоксид азота. Даже при незначительных его концентрациях происходит изменение цвета листьев и хвои, а при кратковременном действии больших доз обнаруживаются буровато – черные участки, изменения эпидермы растений (на вершине и по периферии листовой пластинки появляются буровато – черные участки, кончики хвоинок приобретают темно-красный цвет). По А.И. Хвастунову (1999), пороговая концентрация диоксида азота, принимаемая в качестве максимальной разовой для растений, составляет 0,02 мг/м3. Двуокись азота даже в очень слабых концентрациях (0,01 мг/м3) вызывает нарушение азотного обмена у растений, а так же влияние окислов азота оказывает отрицательное действие на процесс фотосинтеза (Артамонов, 1986). ПДК, установленное для диоксида азота, составляет 0,04 мг/м3 (табл. 4) (Руководство по контролю…, 1991).
Таким образом, из результатов проделанной нами работы видно, что показатели данного загрязнителя ни на одной из улиц не превысили ПДК (рис. 2). Наибольшая степень загрязнения диоксидом азота характерна для улицы Крылова (около завода ММЗ) и составила 0,033 мг/м3, а наименьшая для Сосновой рощи, где равнялась 0,004 мг/м3. Также низкие значения отмечены в Парке культуры и отдыха XXX-летия ВЛКСМ - 0,009 мг/м3. Лабораторный анализ проб воздуха, отобранных возле Мясокомбината и на улице Героев Сталинградской битвы, показал следующие результаты - 0,017 и 0,013 мг/м3 соответственно.
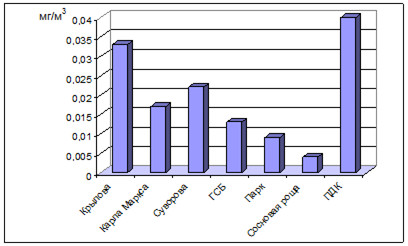
Рис. 2. Содержание диоксида азота в атмосферном воздухе.
Необходимо отметить, что растения, интенсивно поглощающие и усваивающие окислы азота и дающие большую биомассу, могут играть важную роль в очистке окружающей среды от этих фитотоксикантов.
Содержание углерода оксида
Соединения углерода являются наиболее распространенными веществами, поступающими в атмосферу в результате сжигания и переработке органического топлива. Особенно высокая концентрация угарного газа в воздухе наблюдается на перекрестках больших автомагистралей при скоплении автотранспорта, а так же на улицах с интенсивным движением. Угарный газ является сравнительно малотоксичным для растений, поскольку они обладают способностью окислять его до углекислого газа и связывать затем в фотосинтетическом цикле. Отрицательное влияние СО на растения проявляется при сравнительно высоких концентрациях – более 1%.
Показано, что угарный газ вызывает уменьшение проницаемости клеточных мембран. Одна из характерных особенностей действия угарного газа – его способность к образованию комплексов с железо- и медьпротеидами (например, цитохромоксидазой), что подавляет процесс дыхания растений (Артамонов, 1986).
Наши исследования по выявлению оксида углерода в атмосферном воздухе города Йошкар-Олы показали наиболее высокое его содержание на улице Карла Маркса, концентрация анализируемого вещества равнялась 2,0 мг/м3. На улицах Крылова, Суворова (около завода «ММЗ») и в Парке культуры и отдыха XXX-летия ВЛКСМ концентрация оксида углерода имела одинаковое значение и равнялась 1,7 мг/м3. Минимальное значение по данному показателю выявлено нами для улицы Героев Сталинградской битвы и в Сосновой роще, где составляло 1,3 и 1,4 мг/м3. Установленная предельно-допустимая концентрация для данного загрязнителя равна 3,0 мг/м3 (Руководство по контролю…, 1991). За период нашего наблюдения превышение концентрации оксида углерода относительно уровня ПДК не наблюдалось.
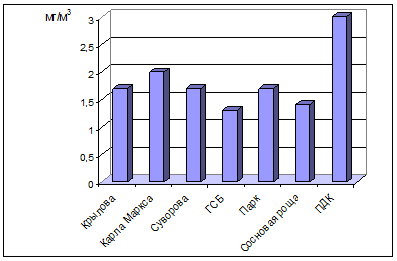
Рис. 4. Содержание оксида углерода в атмосферном воздухе.
Следует напомнить, что влияние угарного газа отрицательно сказывается на жизнедеятельности растений, но в большей степени на здоровье человека. По содержанию в выхлопных газах оксид углерода занимает первое место, однако он столь же эффективно поглощается растениями. Интенсивность связывания СО у разных видов растений различна. Отмечено активное усвоение угарного газа, кленом, осиной, елью (Артамонов, 1986). В результате первичного окисления из окиси углерода образуется углекислый газ, который потребляется растениями в ходе фотосинтеза.
Содержание аммиака
В последние годы все чаще обнаруживаются поражения на растениях, вызванные действием аммиака. В непосредственном близости от крупных животноводческих комплексов повреждаются хвойные деревья в результате разложения мочевины и мочевой кислоты или при сжигании нечистот, содержащих аммиак. В меньших размерах те же явления наблюдаются вблизи коксохимических заводов и предприятий по производству удобрений и мочевины (Илькун, 1978).
ПДК, установленная для аммиака составляет 0,1 мг/м3 (табл. 4) (Руководство по контролю…, 1991). Таким образом, из результатов проделанной нами работы видно, что показатели данного загрязнителя ни на одной из улиц не превысили ПДК (рис. 5). Наибольшая степень загрязнения аммиаком характерна для улиц Суворова (около завода ММЗ) и для Парка культуры и отдыха XXX-летия ВЛКСМ и составила 0,053 и 0,051 мг/м3 соответственно, Чуть меньше обнаружено на улице Крылова (около завода Искож) – 0,04 мг/м3. Для улицы Карла Маркса степень загрязнения составила 0,032 мг/м3, а наименьшая степень загрязнения NH3 была выявлена на улице Героев Сталинградской битвы и равнялась 0,022 мг/м3, в Сосновой роще среднее значение концентрации этого газа равно 0,019 мг/м3 .
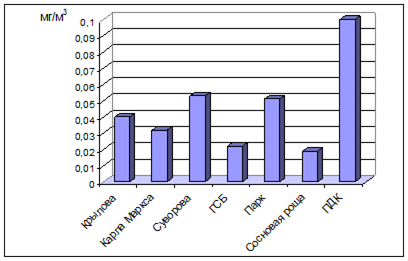
Рис. 5. Содержание аммиака в атмосферном воздухе.
Содержание ангидрида сернистого
По четырех балльной шкале опасности сернистый ангидрид относиться к третьему классу токсикантов. Серный ангидрид благодаря высокой гигроскопичности быстро реагирует с водяным паром атмосферы и превращается в аэрозоль серной кислоты, который проникает в хлоропласты и взаимодействует с зеленым пигментов хлорофиллом, вызывая превращение его в феофетин. Этот процесс сопровождается падением уровня каратиноидов, снижением уровня фотосинтеза (Соловьева, 2003).
Как свидетельствуют полученные в ходе лабораторного анализа показатели концентраций ангидрида сернистого, наиболее высокое его содержание в атмосферном воздухе обнаружено на улице Крылова – 0,45 мг/м3 (рис. 3). По сравнению с ПДК, установленной для ангидрида сернистого, равной 0,03 мг/м3 (табл. 4), наблюдается превышение в 15 раз. На улицах Карла Маркса и Суворова выявлено превышение концентрации сернистого ангидрида в воздухе в 12,3 и 5 раза соответственно. Самое низкое содержание SO2 в воздухе обнаружено в Парке культуры и отдыха XXX-летия ВЛКСМ и на улице Героев Сталинградской битвы равное 0,09 и 0,07 мг/м3 соответственно, но даже здесь наблюдается превышение в 3-2,3 раза. Только в Сосновой роще, выбранной нами в качестве контрольной точки, содержание в атмосферном воздухе сернистого ангидрида нами практически не выявлено.
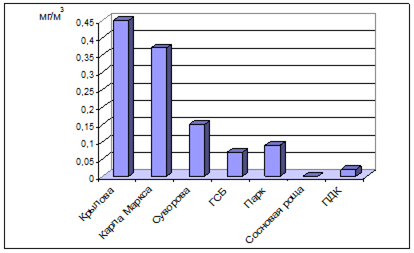
Рис. 3. Содержание сернистого ангидрида в атмосферном воздухе.
Очень важно учитывать при создании санитарно-защитных зон и при озеленении города газопоглотительную способность и устойчивость растений к SO2. Прекрасными объектами для озеленения загазованных районов по Н.П. Красинскому и Е.И. Князевой (1950) являются тополь серебристый (Populus alba L.), клен яснелистный (Acer negundo L.), ива белая (Ulmus laevus L.). Рябину обыкновенную (Sorbus aucuparia L.) данные авторы отнесли к нерекомендуемому виду для озеленения промышленных территорий, так как данный вид имеет крайне низкую газоустойчивость (Кулагин, 1974).
Содержание серы в листьях рябины обыкновенной
В отличие от некоторого регулирования корнями поглощения катионов и анионов из почвы, растения практически не способны регулировать поглощение вредных веществ ассимилирующими органами из воздуха. Это приводит к тому, что вредные компоненты накапливаются в листовом аппарате растений (Кулагин, 1974).
Действие вредных веществ зависит от их вида, концентрации, длительности воздействия, а так же от относительной восприимчивости видов растений к различным загрязнителям. Для растений одним из наиболее опасных загрязнителей атмосферы является, сернистый ангидрид (Методические указания.., 1992). Максимально допустимая разовая концентрация SO2 для растений равна 0,02 мг/м3. Подавление фотосинтеза у наземных растений уже ощутимо при концентрации SO2 0,03 – 0,05 мг/м3. Концентрация SO2 свыше 0,4 мг/м3 даже при кратковременном воздействии может вызвать тяжелые нарушения в органах ассимиляции и некрозные изменения (Майснер, 1981).
В то же время сера входит в число основных питательных элементов, необходимых для жизни растения. Она поступает в них, главным образом, в виде сульфатов. В последнее время появились данные о том, что растения в качестве источника серы способны использовать SO2 атмосферы. Благоприятный эффект низких концентраций SO2 в воздухе наблюдается на рост растений при отсутствии SO4 в питательной среде (Гудериан, 1979). Однако подобное действие диоксид серы может оказывать лишь в концентрациях, не превышающих 0,2 мг/м3. В большинстве серосодержащих органических соединений сера находится в восстановленной форме. Процесс восстановления сульфата, обеспечивающий включение серы в серосодержащие аминокислоты, локализован преимущественно в листьях (в хлоропластах) и является ключевым в ассимиляции серы высшими растениями. Включение серы в органические вещества происходит следующим путем: активирование сульфата, восстановление серы и, наконец, само включение (Лесные экосистемы.., 1990).
Сера входит в состав важнейших аминокислот – цистеина и метионина, которые могут находиться в растениях как в свободном виде, так и в составе белков. Одна из основных функций серы в белках и полипептидах – участие SH-групп в образовании ковалентных, водородных, меркаптидных связей, поддерживающих трехмерную структуру белка. Другая важнейшая функция серы в растительном организме состоит в поддержании определенного уровня окислительно-восстановительного потенциала клетки. Сера входит также в состав важнейших биологических соединений – коэнзима А и витаминов (липоевой кислоты, биотина, тиамина).
Недостаточное снабжение растений серой тормозит синтез серосодержащих аминокислот и белков, снижает фотосинтез и скорость роста растений, особенно надземной части. В острых случаях нарушается формирование хлоропластов и возможен их распад (Сергейчик, 1984).
Нами был проведен лабораторный анализ по выявлению содержания серы в листьях рябины обыкновенной, в шести различных районах города. Наши исследования показали, что самая высокая концентрация серы, обнаружена в листьях рябины обыкновенной, произрастающей на улице Крылова и равнялась 1,4 мг/г. Интересно, что для этой же улицы характерна самая высокая концентрация сернистого ангидрида в воздухе 0,45 мг/м3 (табл. 6). На улице Карла Маркса концентрация серы в листьях составляла 1,2 мг/г, а концентрация сернистого ангидрида в воздухе имела значение 0,37 мг/м3. Разница между этими двумя точками статистически не значима (Р>0,05). На улице Суворова (около завода «ММЗ»), концентрация серы в листьях составила 1,0 мг/г, а концентрация сернистого ангидрида в воздухе - 0,15 мг/м3. Почти одинаковые значения концентрации серы в листьях были получены в Парке культуры и отдыха XXX-летия ВЛКСМ и на улице Героев Сталинградской битвы и равнялись 0,86 и 0,85 мг/г, в то время как содержание сернистого ангидрида в воздухе на этих же улицах составило 0,09 и 0,07 мг/м3 соответственно (табл. 6). Наименьшая концентрация серы в листьях была обнаружена на улице Кирпичной (Сосновая роща) и была равна 0,47 мг/г, а в воздухе содержание SO2 нами практически не обнаружено (табл. 6).
Таблица 6 - Содержание серы в листьях рябины обыкновенной
| Районы исследования | Концентрация серы в листьях, мг/г | Концентрация SO2 в атмосфере, мг/м3 |
| ул. Крылова | 1,4±0,025 | 0,45±0,051 |
| ул. Карла Маркса | 1,2±0,023 | 0,37±0,043 |
| ул. Суворова | 1,0±0,018 | 0,15±0,021 |
| ул. Героев Сталинградской битвы | 0,85±0,005 | 0,070±0,0011 |
| Парк культуры и отдыха ХХХ-летия ВЛКСМ | 0,86±0,004 | 0,094±0,0015 |
| Сосновая роща | 0,47±0,001 | 0,001 |
Таким образом, из результатов нашей работы видно, что существует прямая зависимость между содержанием сернистого ангидрида в воздухе и содержанием серы в листьях. Данная зависимость установлена с помощью корреляционного анализа r = 0,94 (Р<0,005) (рис. 6).
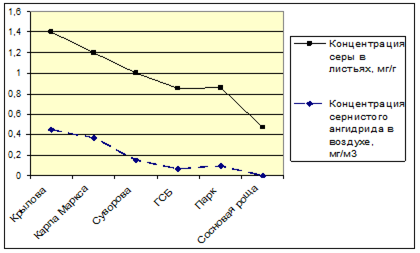
Рис. 6. Зависимость между содержанием сернистого ангидрида в воздухе и серы в листьях рябины обыкновенной.
Выводы
Проведенные нами исследования позволяют сделать следующие выводы:
1. Установлено превышение содержания сернистого ангидрида в атмосферном воздухе. На улице Крылова в 15 раз, на улице Карла Маркса в 12,3 раза, на улице Суворова – в 5 раз, в Парке ХХХ летия ВЛКСМ – в 3,13 раза, на улице Героев Сталинградской битвы – в 2,3 раза. Концентрация пыли на всех пяти исследуемых улицах также превышала предельно-допустимые значения. Остальные загрязняющие вещества содержаться в пределах нормы.
2. Выявлена прямая корреляционная зависимость между содержанием сернистого газа в атмосферном воздухе и содержанием серы в листьях рябины обыкновенной.
3. Установлена обратная корреляционная зависимость длины прироста годичного побега, длины и ширины листовой пластинки и площади сложного листа рябины обыкновенной от содержания диоксида серы в атмосферном воздухе.
4. Признак длина черешка сложного листа рябины обыкновенной не зависит от загрязнения атмосферного воздуха сернистым ангидридом.
Список литературы
1. Абрамов, Н.В. Флора Республики Марий Эл: инвентаризация, районирование, охрана и проблемы рационального использования ее ресурсов / Н.В. Абрамов. – Йошкар-Ола: МарГУ, 2000. – 164 с.
2. Андреева, М.В. Изменение морфологии листа Populus tremula L. в загрязнённом воздухе / М.В. Андреева, Н. Н. Семчук // Учён. зап. ИСХиПР НовГУ. Великий Новгород, 2005. Т. 13, вып. 2. С. 107–110.
3. Антипов, В.Г. Устойчивость древесных растений к промышленным газам / В.Г. Антипов. - Минск: Наука и техника, 1979 – 216 с.
4. Артамонов, В.И. Растения и чистота природной среды / В.И. Артамонов. – М.: Наука, 1986. – 172 с.
5. Атрохин, В.Г. Древесные породы мира. Т. 3 Древесные породы СССР / В.Г. Атрохин, К.К. Калуцкий, Ф.Т. Тюриков. – М.: Лесн. пром-сть, 1982. – 264 с.
6. Битюкова, В.Р. Тенденции атмосферного загрязнения в городах России / В.Р. Битюкова, А.А. Попов // Экол. пром-ть России. – 2004. С.4 – 7.
7. Благоустройство городов и поселков / Герасимов Н. А.[и др.]. М - Л., 1950 – 160 с.
8. Бродович, Т.М. Деревья и кустарники запада УССР. Атлас / Т.М. Бродович, М.М. Бродович. - Львов: Высшая школа, 1979. – 251 с.
9. Булгаков, М.В. Опыт создания защитных насаждений в городе Красноуральске / М.В. Булгаков // Растительность и промышленные загрязнения. Охрана природы на Урале. - Свердловск, 1964, - Вып. 4. С. 153-169.
10. Валягина–Малютина, Е.Т. Деревья и кустарники зимой. Определитель древесных и кустарниковых пород по побегам и почкам в безлиственном состоянии / Е.Т. Валягина - Малютина.- М.: КМК, 2001. – 281 с.
11. Вехов, Н.К. Декоративные деревья и кустарники. В сб.: Озеленение городов / Н.К. Вехов. - М., 1954 - 167 с.
12. Влияние загрязнения атмосферы на лесные экосистемы. Лекции / В. Соловьев [и др.]. - Л.: ЛТА, 1989. - 48с.
13. Воскресенская, О.Л. Организм и среда: факториальная экология / О.Л. Воскресенская, Е.А. Скочилова и др. – Йошкар-Ола, 2005. – 175 с.
14. Воскресенская, О.Л. Экология города Йошкар-Олы / О.Л. Воскресенская, Е.А. Алябышева и др. – Йошкар-Ола, 2004. – 200 с.
15. Галактионов, И.И. Декоративная дендрология / И.И. Галактионов, А.В. Ву, В.В. Осин. - М., 1967,. – 240 с.
16. Гейнрих, Д. Экология / Д. Гейнрих, М. Гергт ; пер. с нем. Н. Н. Гринченко. – М.: Рыбари, 2003. – 287 с.
17. Гелашвили, Д.Б. Количественные методы оценки загрязнения атмосферного воздуха / Экологический мониторинг. Методы биологического и физико-химического мониторинга. Ч IV. – Н. Новгород: Изд-во ННГУ, 2000 – 427 с.
18. Гетко, Н.В. Растения в техногенной среде: Структура и функция ассимиляционного аппарата / Н.В. Гетко. – Минск: Наука и техника, 1989. – 208 с.
19. Гетта, Я.К. Озеленение промышленных предприятий / Я.К. Гетта. - Кемерово, 1957. – 170 с.
20. Голицын, А.Н. Основы промышленной экологии: учебник / А.Н. Голицын. – М.: Академия, 2002. – 240 с.
21. Горышина, Т.К. Растение в городе / Т.К. Горышина. – Л.: Изд-во ЛГУ, 1991. – 148 с.
22. ГОСТ 17.2.4.05 – 83. Гравиметрический метод определения взвешенных частиц пыли.
23. Государственный доклад о состоянии окружающей природной среды Республики Марий Эл в 2003 году. – Йошкар-Ола, 2004. – 179 с.
24. Гудериан, Р. Загрязнение воздушной среды / Р. Гудериан. – М.: Мир, 1979. – 200 с.
25. Жизнь растений в 6 томах. Цветковые растения / Под ред. Акад. АН СССР А.Л. Тахтаджяна. – М.: Просвещение, 1981. – Т. 5, Ч. 2. – 512с.
26. Жукова, Л.А. Популяционная жизнь луговых растений / Л.А. Жукова. – Йошкар-Ола: РИИК «Ланар», 1995. – 225 с.
27. Загрязнение воздуха и жизнь растений / Под ред. Майкла Трешоу. – Л.: Гидрометеоиздат, 1988. – 535 с.
28. Илькун, Г.М. Загрязнители атмосферы и растения / Г.М. Илькун. – Киев: Наукова думка, 1978. – 246 с.
29. Илькун, Г.М. Отфильтровывание воздуха от поллютантов древесными растениями / Г.М. Илькун. - Таллин, 1982. – 138 с.
30. Исаченко, Х.М. Влияние задымляемости на рост и состояние древесной растительности / Х.М. Исаченко // Сов. ботаника - 1938. - №1. - С. 118-123.
31. Калверт, С. Защита атмосферы от промышленных загрязнений / С Калверт, Г. Инглунд. – М.: Металлургия, 1988. – 286 с.
32. Косулина, Л.Г. Физиология устойчивости растений к неблагоприятным факторам среды / Л.Г. Косулина, Э.К. Луценко, В.А. Аксенова. – Ростов н/Д : Изд-во Рост. ун-та, 1993. – 240 с.
33. Кречетова, Н.В. Дендрология, лесные культуры. Цветки, стробилы, семена, проростки (всходы) древесных и кустарниковых пород / Н.В. Кречетова. – Йошкар-Ола: МарГТУ, 1997. – 52 с.
34. Крокер, В. Рост растений / В. Крокер. – М.: Изд-во иностр. лит-ры, 1950. – 250 с.
35. Кузьмина, Н.А., Кузьмина А.И. // Вестник Башкирского университета. Фоторегуляция роста и некоторых физиологических показателей проростков и каллусной ткани твердой пшеницы. 2001. № 2 (I). С. 140-142.
36. Кулагин, Ю.З. Древесные растения и промышленная среда / Ю.З. Кулагин. М.: Наука, 1974. – 127 с.
37. Кулагин, Ю.З. Лесообразующие виды, техногенез и прогнозирование / Ю.З. Кулагин. - М. Наука, 1980. – 114 с.
38. Кулагин, Ю.З. О способности древесных растений к повторному облиствению / Ю.З. Кулагин // Ботанический журнал – 1966. - №51.
39. Кунцевич, И.П. Ассортимент газоустойчивых древесно-кустарниковых растений / И.П. Кунцевич, Т.Н. Турчинская // Информационное письмо. Акад. коммун. хоз. им. К.Д. Памфилова - 1954. - №39. С. 12-15.
40. Лакин, Г.Ф. Биометрия / Г.Ф. Лакин – М.: Высш. шк., 1980. – 293 с.
41. Лесные экосистемы и атмосферное загрязнение / В. А. Алексеев [и др.]. – Л.: Наука, 1990. – 197 с.
42. Майснер, А.Д. Жизнь растений в неблагоприятных условиях / А.Д. Майснер. – Минск: Высш. школа, 1981. – 98с.
43. Мокроносов, А.Т. Фотосинтез: физиолого-экологические и биохимические аспекты / А.Т. Мокроносов, В.Ф. Гавриленко. – М., 1992. – 236 с.
44. Николаевский, В.С. Биологические основы газоустойчивости растений / В.С. Николаевский. – Новосибирск: Наука, 1979. – 280 с.
45. Николаевский, В.С. Роль растительности в регуляции чистоты атмосферного воздуха / В. С. Николаевский. – Л., 1978. – 277 с.
46. Николаевский, В.С. Современное состояние проблемы газоустойчивости растений / В.С. Николаевский. – Пермск. ун-т, 1969.
47. Николайкин, Н.И. Экология / Н.И. Николайкин, Н.Е. Николайкина, О.П. Мелехова.– М.: Дрофа, 2003. – 624 с.
48. Одум, Ю. Основы экологии. / Ю. Одум. – М.: Мир, 1975. – 345 с.
49. Онтогенетический атлас лекарственных растений. – Йошкар-Ола: Мар.гос.ун-т, 2000. – 268 с.
50. Степановских, А.С. Охрана окружающей среды: / А.С. Степановских. – М.: ЮНИТИ-ДАНА, 2001. – 559 с.
51. Павлов, И.Н. Глобальные изменения среды обитания древесных растений. Монография / И.Н. Павлов. - Красноярск: СибГТУ, 2003. – 156 с.
52. Работнов, Т.А. Вопросы изучения состава популяций для целей фитоценологии // Проблемы ботаники. – 1950б. – Вып.1. – С. 465 – 483.
53. Романова, А.К. Физиолого-биохимические признаки и молекулярные механизмы адаптации растений к повышенной концентрации CO2 в атмосфере / А.К. Романова // Физиология растений. – 2005. – Т. 52, №1. - С. 123-132.
54. Рост концентрации CO2 в атмосфере – всеобщее благо? / Алексеев [и др.] // Природа. – 1999. - №9. С. 13 – 16.
55. Руководство по контролю загрязнения атмосферы. – Л.: Гидрометиздат, 1979. – 448 с.
56. Руководящий документ: Руководство по контролю загрязнений атмосферы РД 52.04.186 – 89. – М.: 1991. - 694 с.
57. Рунова, Е.М. Экологический мониторинг лесных биоценозов в зонах промышленных выбросов / Е.М. Рунова // Природные и интеллектуальные ресурсы Сибири. – Томск: ТГУ, 2004. – С. 132 – 135.
58. Рябинин, В.М. Лес и промышленные газы / В.М. Рябинин. - М., 1965. – 297 с.
59. Сборник методик и инструктивных материалов по определению вредных веществ для контроля источников загрязнения окружающей среды. – Краснодар: Северный Кавказ, 1993. – 224 с.
60. Сергейчик, С.А. Древесные растения и оптимизация промышленной среды / С.А. Сергейчик. - Минск: Наука и техника, 1984. – 168 с.
61. Сергиевская, Е.В. Систематика высших растений. Практический курс / Е.В. Сергиевская.– СПб.: Лань, 2002. – 448 с.
62. Соловьева, О.С. Пылезадерживающая способность древесных растений в зонах разного загрязнения г. Йошкар-Олы / О.С. Соловьева // Актуальные проблемы экологии и охраны окружающей среды. Ч. 1.- Тольятти: ВуиТ, 2004. – С. 256 – 261.
63. Соловьева, О.С. Функциональные и физиологические особенности древесных растений в условиях городской среды: автореферат / О.С. Соловьева. – Йошкар-Ола, 2003. – 22 с.
64. Тарабрин, В.П. Устойчивость древесных растений в условиях промышленного загрязнения среды: автореферат / В.П Тарабрин. – Киев, 1974. – 364 с.
65. Тищенко, Н.Ф. Охрана атмосферного воздуха : справочник : в 2-х ч. Ч. 1. Выделение вредных веществ / Н.Ф. Тищенко, А.Н. Тищенко. – М.: Химия, 1993. – 192 с.
66. Тищенко, Н.Ф. Охрана атмосферного воздуха: справочник: в 2-х ч. Ч. 2. Распределение вредных веществ / Н.Ф. Тищенко, А.Н. Тищенко. – М.: Химия, 1993. – 314 с.
67. Трахтенберг, И.М. Тяжелые металлы во внешней среде: современные гигиенические и токсикологические аспекты / И.М. Трахтенберг, В.С. Колесников, В.П. Луковенко. – Минск: Наука и техника, 1994. – 286 с.
68. Трифонова, Т.А. Прикладная экология / Т.А. Трифонова, Н.В. Селиванова, Н.В. Мищенко. – М.: Академический Проект: Традиция, 2005. – 384 с.
69. Тутаюк, В.Х. Анатомия и морфология растений / В.Х. Тутаюк. – М., 1972. – 335 с.
70. Уранов, А.А. Возрастной спектр фитоценопопуляций как функция времени и энергетических волновых процессов // Бюлл. Науки, 1975. - №2. – С. 17 – 29.
71. Харитонович, Ф.Н. Биология и экология древесных пород / Ф.Н. Харитонович. - М.: Лесная промышленность, 1968. – 304 с.
72. Хван, Т.А. Промышленная экология / Т.А. Хван. – Ростов-на-Дону: Феникс, 2003. – 315 с.
73. Хвастунов, А.И. Экологические проблемы малых и средних промышленных городов: оценка антропогенного воздействия / А.И. Хвастунов. – Йошкар-Ола: МарГТУ, 1999. – 248 с.
74. Ценопопуляции растений (основные понятия и структура) – М.: Наука, 1976. – 216 с.
75. Ценопопуляции растений (очерки популяционной биологии) – М.: Наука, 1988. – 236 с.
76. Чекрыгин, В.В. Особенности регулирования светового режима в насаждениях яблони Западного Предкавказья / В.В Чекрыгин, к.б.н. // автореферат. - Краснодар, 2005. - 250 с.
77. Шаблиовский, В.В. Повреждения дымовыми отходами на промплощадках цветной металлургии / В.В. Шаблиовский. - М., 1950. – 257 с.
78. Шацкая, Р.М. Влияние промышленной среды на содержание азотистых соединений в древесных растениях / Р.М. Шацкая, к.б.н. // автореферат. – Кишинев, 1983. – 22 с.
79. Экология и охрана природы: Методические указания к выполнению лабораторных работ для студентов специальности 31.12 Часть 1. / Р.Р. Иванова, Е.М. Романов, Е.Н. Щеглова.- Йошкар-Ола.: МарПИ, 1992. – 64 с.
80. Henry A. Forests and trees in relation of hyqiene / A.Henry. L., 1920.
81. Thomae K. Von der Industriefestiqkeit unserer Geholze / K. Thomae // Gartenwelt, Hannover – Wulfel, 1959. - №14.
82. Briggs W. R. // Annu. Rev. Cell Dev. Biol. 1999. V. 15. P. 33-62
83. Ahmad M. // Current Opinion in Plant Biology. 1999. V. 2. P. 230-235
84. Lin C. // Trends in plant science. 2000. V. 5. № 8. P. 337-342
ПРИЛОЖЕНИЕ 1
Содержание загрязняющих веществ в разных районах города
| Районы исследования | Концентрация SO2 в атмосфере, мг/м3 | Концентрация NO2 в атмосфере, мг/м3 | Концентрация CO2 в атмосфере, мг/м3 | Концентрация NH3 в атмосфере, мг/м3 | Концентрация пыли в атмосфере, мг/м3 |
| ул. Крылова | 0,45±0,051 | 0,033±0,0041 | 1,7±0,25 | 0,04±0,005 | 0,56±0,062 |
| ул. Карла Маркса | 0,37±0,043 | 0,017±0,0021 | 2,01±0,3 | 0,032±0,004 | 0,37±0,041 |
| ул. Суворова | 0,15±0,021 | 0,019±0,0022 | 1,7±0,25 | 0,049±0,0053 | 0,69±0,072 |
| ул. Героев Сталинградской битвы | 0,070±0,0011 | 0,013±0,0020 | 1,3±0,2 | 0,022±0,0034 | 0,35±0,040 |
| Парк культуры и отдыха ХХХ-летия ВЛКСМ | 0,094±0,0015 | 0,009±0,00011 | 1,7±0,25 | 0,048±0,0051 | 0,28±0,032 |
| Сосновая роща | 0,001±0,009 | 0,004±0,007 | 1,4±0,3 | 0,019±0,0022 | 0 |
| ПДК (для древесных видов) | 0,03 | 0,04 | 3,0 | 0,1 | 0,2 |
ПРИЛОЖЕНИЕ 2
Средние значения прироста длины годичного побега рябины обыкновенной
| Районы исследования | Х ± m, мм | Сv ± m, % | Концентрация SO2, мг/м3 |
| ул. Крылова | 48±1,67 | 24,5±2,45 | 0,45±0,051 |
| ул. Карла Маркса | 52±1,96 | 26,6±2,66 | 0,37±0,043 |
| ул. Суворова | 66±3,38 | 36,2±3,62 | 0,15±0,021 |
| ул. Героев Сталинградской битвы | 66,2±2,35 | 25,2±2,52 | 0,07±0,0011 |
| Парк культуры и отдыха ХХХ-летия ВЛКСМ | 71±3,54 | 35,2±3,52 | 0,094±0,0015 |
| Сосновая роща | 81,8±3,13 | 27,0±2,70 | 0,001 |
ПРИЛОЖЕНИЕ 3
Средние значения показателей длины и ширины листовой пластинки рябины обыкновенной
| Районы исследования | Длина листа | Ширина листа | Концентрация SO2, мг/м3 | ||
| Х ± m, мм | Сv ± m, % | Х ± m, мм | Сv ± m, % | ||
| ул. Крылова | 171±2,71 | 15,9±1,2 | 167,6±3,26 | 19,6±1,8 | 0,45±0,051 |
| ул. Карла Маркса | 170,8±1,96 | 15,6±1,3 | 170,4±2,77 | 16,3±1,6 | 0,37±0,043 |
| ул. Суворова | 183,2±2,97 | 16,2±1,5 | 180±3,26 | 18,1±1,7 | 0,15±0,021 |
| ул. Героев Сталинградской битвы | 183,4±2,78 | 15,2±1,5 | 182,3±2,66 | 14,7±1,5 | 0,070±0,001 |
| Парк культуры и отдыха ХХХ-летия ВЛКСМ | 185,2±2,82 | 15,2±1,4 | 183±3,10 | 16,9±1,4 | 0,094±0,001 |
| Сосновая роща | 190,5±2,19 | 11,5±1,2 | 187±3,32 | 17,8±1,6 | 0,001 |
ПРИЛОЖЕНИЕ 4
Средние значения показателей площади листовой пластинки и удельной поверхностной плотности
| Районы исследования | Площадь листовой пластинки | УППЛ |
| Х ± m, мм2 | Х ± m, мг | |
| ул. Крылова | 727,7±35,42 | 76,13±5,21 |
| ул. Карла Маркса | 936,16±40,19 | 55,88±2,09 |
| ул. Суворова | 932,43±31,16 | 61,7±2,38 |
| ул. Героев Сталинградской битвы | 1194,1±44,88 | 48,34±2,08 |
| Парк культуры и отдыха ХХХ-летия ВЛКСМ | 1079,95±41,06 | 40,80±1,42 |
| Сосновая роща | 1302,08±61,28 | 44,42±3,53 |
|
Средние значения показателей длины черешка рябины обыкновенной
| Районы исследования | Длина черешка | Концентрация SO2 мг/м3 |
| Х ± m, мм | ||
| ул. Крылова | 35,96±0,78 | 0,45±0,051 |
| ул. Карла Маркса | 32,27±0,68 | 0,37±0,043 |
| ул. Суворова | 34,03±0,79 | 0,15±0,021 |
| ул. Героев Сталинградской битвы | 38,85±0,86 | 0,070±0,001 |
| Парк культуры и отдыха ХХХ-летия ВЛКСМ | 35,51±0,59 | 0,094±0,001 |
| Сосновая роща | 37,1±0,79 | 0,001 |
ВЫПУСКНАЯ КВАЛИФИКАЦИОННАЯ (ДИПЛОМНАЯ) РАБОТА
Дата: 2019-05-28, просмотров: 423.