Наряду с изучением адсорбентов-ферритов с развитой пористой структурой представляют интерес адсорбенты с магнитными свойствами, полученные путем механического смешивания или совместного осаждения магнитных порошков с гидроксидами металлов. Этот метод синтеза по сравнению с другими имеет ряд преимуществ. Во-первых, использование магнитных порошков позволяет за счет структуры матрицы регулировать пористость и удельную поверхность синтезируемых магнитных адсорбентов в желаемом направлении. Во-вторых, в зависимости от процентного содержания магнитного порошка в составе образца и величины его намагниченности можно изменять структурные и физико-химические свойства получаемых адсорбентов в достаточно широких пределах.
Кроме того, данный метод получения адсорбентов с магнитными свойствами дает возможность в достаточно широких пределах регулировать структуру матрицы, а соответственно и структурные параметры синтезированных образцов [21, 22]. Все это наряду со специфическими свойствами указанных адсорбентов расширяет возможность их использования в разных сорбционных процессах.
Существует расхождение между теоретическими расчетами и экспериментальными данными. По теории с возрастанием концентрации (20-50%) магнитной компоненты Vs и Sуд должна уменьшаться, на практике же наблюдается обратное. Причина таких расхождений обусловлена участием твердых частиц порошка в формировании структуры адсорбентов. Механизм их действия связан с образованием жесткого каркаса, препятствующего сжатию гидроксида во время сушки. Аналогично изменяется и удельная поверхность синтезируемых адсорбентов, которые из-за наличия более открытой структуры несколько выше теоретически рассчитанной.
Условия получения адсорбентов оказывают существенное влияние на их адсорбционно-структурные характеристики. Одна картина наблюдается при внесении магнитного порошка в отмытый гель с последующим механическим перемешиванием и другая — при внесении порошка в солевой раствор, т.е. перед осаждением гидроксида. Разница заключается в том, что образцы, полученные по второму методу, имеют на 10—12% более высокие значения Vs и удельные поверхности. Причина данных расхождений состоит в том, что при механическом перемешивании гидроксида вследствие нарушения гидратных оболочек коллоидных частиц происходит неполная стабилизация системы, сопровождающаяся снятием фактора устойчивости отдельных участков поверхности частиц, в результате чего частицы, слипаясь в этих местах, образуют пространственную сетку, в петлях которой будет находиться дисперсионная среда. При сильном падении агрегативной устойчивости между частицами в местах их соприкосновения может происходить полное вытеснение прослоек дисперсионной среды и осуществляться непосредственный контакт между частицами. Причем с повышением частичной концентрации количество контактов, приходящихся на единицу объема системы, и скорость взаимодействия частиц возрастают.
Увеличение числа контактов между частицами — результат их более плотной объемной упаковки, сопровождающейся, как правило, уменьшением сорбционной емкости и сокращением удельной поверхности образцов за счет недоступности поверхности частиц гидроксида для молекул адсорбата. При совместном осаждении гидрогеля с магнитным порошком протекание указанных процессов весьма ограничено вследствие резкого уменьшения дисперсной фазы и концентрации вещества, а также из-за отсутствия интенсивного механического перемешивания, способствующего образованию коагуляционных структур и т.д.
Все это вызывает формирование пестропористой структуры образцов в результате упаковки первичных частиц и вторичных агрегатов частиц, ответственных за образование мезо- и макропор.
Природа магнитного порошка определяет как магнитные, так и сорбционные свойства получаемых адсорбентов. Если первое из них очевидно, то второе имеет неявные очертания. Дело в том, что удельная поверхность получаемых магнитных адсорбентов практически находится в прямой зависимости от процентного содержания в их составе порошка. Отклонения от этой зависимости могут быть обусловлены некоторым действием порошка на структуру гидроксидов.
Отсюда очевидно, что излишнее содержание магнитного порошка в составе адсорбента ухудшает его структурные параметры и сорбционные характеристики. Основную ответственность за изменение указанных структурных параметров по сравнению с исходными образцами несет магнитный порошок, собственный вклад которого в структуру шпинельсодержащего адсорбента составляет величину, практически приближающуюся к нулю.
С ростом содержания шпинельного порошка в составе адсорбента тенденция сокращения удельной поверхности и сорбционной емкости получаемых образцов по отношению к носителю увеличивается.
Кроме того, адсорбционно-структурные свойства магнитнаполненных адсорбентов, так же, как и других пористых материалов, в значительной степени зависят от структуры носителя, обеспечивающей эффективность очистки жидких сред, содержащих примеси с различным размером молекул.
1.1.3. Углеминеральные магнитные сорбенты
Многообразие задач, решаемых сорбционными методами, требует и разнообразия адсорбентов, отличающихся по структуре, химической природе поверхности и другим эксплуатационным характеристикам.
Синтез таких адсорбентов может быть осуществлен путем наполнения гидроксида магнитным компонентом [10] и модифицирующей органической добавкой [23]. Сочетание этих двух операций позволяет, с одной стороны, придать получаемым адсорбентам магнитные свойства, а с другой — гидрофобные и тем самым приблизить их к углеродным адсорбентам со специфическими способностями.
Степень гидрофобизации поверхности таких адсорбентов определяется процентным содержанием и природой органической углеобразующей добавки: с ростом ее молекулярной массы зауглероженность образца увеличивается. Одна из причин этого — более высокая энергия взаимодействия добавки с поверхностью модифицируемого вещества и минимальная ее улетучиваемость в процессе термической обработки.
Гидрофобные адсорбенты с магнитными свойствами расширяют их возможности при решении многих производственных и экологических задач, где использование обычных адсорбентов создает некоторые технологические затруднения. Так, например, аварийные разливы нефти или тяжелых нефтепродуктов на поверхности воды могут быть удалены магнитными углеродными адсорбентами. Для этого достаточно покрыть пятна адсорбентом с последующим удалением его вместе с поглощенным веществом путем магнитной сепарации.
Сопоставление сорбционных данных гидрофильных [10] и гидрофобных магнитнаполненных образцов показывает, что по своим структурным параметрам они отличаются друг от друга. Так, например, сорбционная емкость гидрофобных магнитных адсорбентов выше, чем в аналогичных гидрофильных образцах.
Максимальное внесение органической углеобразующей добавки вызвано требованиями, предъявляемыми к получаемому адсорбенту: среди них необходимая механическая прочность, степень гидрофобизации поверхности и экономический фактор. Каждое требование имеет определенные ограничения, соблюдение которых является неотъемлемой частью синтеза адсорбентов с заданными эксплуатационными характеристиками. Так, например, для получения механически прочных пористых материалов излишнее содержание угля сопровождается потерей механической прочности. Для избежания этого количество органической добавки, адсорбированной на поверхности коллоидных частиц, должно обеспечивать непосредственный контакт между частицами гидроксида, а не через углеродные оболочки. Таким образом, адсорбированный слой модифицирующей добавки в зависимости от ее природы не должен превышать одного или двух молекулярных слоев. В противном случае образуются порошкообразные адсорбенты с сокращенным объемом микро- и мезопор, которые, как было отмечено, полностью или частично закупорены образующимся углем. Данное обстоятельство вынуждает придерживаться золотой середины, которая, помимо сказанного, в некоторой степени определяется и стоимостью модифицирующего агента. Однако трудно предсказать количественное содержание органического модифицирующего агента, необходимого для удовлетворения упомянутых выше требований.
Решение этой задачи обычно осуществляли опытным путем и, как показала практика, содержание модифицирующего вещества в зависимости от его природы, молекулярной массы и дисперсности частиц гидроксида колеблется от 2 до 5 мас.%.
Магнитные характеристики адсорбентов одного и того же состава практически не отличаются между собой. Незначительное присутствие в их составе углеродной компоненты не оказывает заметного изменения ни на магнитную индукцию насыщения, ни на остаточную индукцию.
Иначе говоря, по магнитным параметрам, кроме поверхностных, а соответственно и сорбционных свойств, рассматриваемые пористые материалы не отличаются друг от друга. Поэтому с целью увеличения их разнообразия по структурным параметрам и для повышения эффективности в различных процессах, связанных с очисткой и разделением органических сред, синтез адсорбентов данного типа может быть осуществлен как с использованием структурно отличающихся индивидуальных гидроксидов, так и бинарных систем разного состава.
Для гидрофобных магнитных адсорбентов в отличие от гидрофильных на первый план выступает их структура и ее стабильность при температуре зауглероживания поверхности.
В связи с этим одно из основных требований синтеза магнитных гидрофобных адсорбентов — подбор высокопористых термостабильных носителей. Дело в том, что малоактивные носители, как и аналогичные адсорбенты, не представляют практического интереса, тем более что зауглероживание их поверхности направлено не на развитие, а на сокращение удельной поверхности.
Вторым необходимым условием получения гидрофобных адсорбентов является выбор высокомолекулярного водорастворимого органического вещества — модификатора, обладающего высокой энергией связи с поверхностью коллоидных частиц, и определение его процентного содержания, необходимого для полной гидрофобизации поверхности адсорбента. Это минимальные, но необходимые требования, соблюдение которых — успех синтеза гидрофобных, активных адсорбентов.
Привлекательность данного направления исследований состоит еще и в том, что оно требует разработки принципиально новых методов и нестандартных решений.
Изотермы адсорбции
Изотермы адсорбции являются одной из важнейших характеристик адсорбентов, т.к. при их анализе можно установить многие характеристики сорбента (удельную поверхность, размер пор, предположить их форму, характер сорбции и т.п.).
Для получения изотерм адсорбции очень важен правильный выбор адсорбтива.
Адсорбтив должен быть химически инертным по отношению к поверхности твердого тела; давление насыщенных паров при температуре опыта должно быть достаточно большим, чтобы его можно было точно измерить в соответствующем, довольно широком интервале относительных давлений (~0,001 < р/ро < ~0,5); однако, чтобы удобнее было проводить эксперимент, р0 не должно превышать 1—2 атм. Кроме того, рабочие температуры должны быть такими, чтобы их можно было легко получить при помощи обычных хладагентов, а именно азота (т. кип. 77 К), кислорода (Ткип. 90 К), охлаждающей смеси на основе диоксида углерода (195 К), тающего льда (273 К) или при помощи подходящих термостатов (в интервале от 253 до 323 К). Наконец, желательно, чтобы форма молекул адсорбата не слишком отличалась от сферической, с тем чтобы свести к минимуму неопределенность в величине ат (площадь, занимаемая молекулой адсорбата в плотном монослое) из-за возможной различной ориентации на поверхности. В первое время кислород часто применялся как адсорбат при определении удельной поверхности по методу БЭТ, причем адсорбция измерялась при температуре его кипения. Однако, когда жидкий азот стал вполне доступным, использование кислорода резко сократилось. Помимо того что жидкий кислород как хладагент небезопасен, при температуре 90 К трудно исключить возможность его хемосорбции.
В литературе [26, 83] приводятся десятки тысяч изотерм адсорбции, полученных для самых различных твердых тел.
Существует также несколько теорий, объясняющих вид изотерм адсорбции. Так, например, если происходит хемосорбция (молекулы адсорбтива связываются с частицами адсорбента при помощи химического взаимодействия), то данный вид взаимодействия хорошо описывает теория мономолекулярной адсорбции Ленгмюра. Согласно этой теории, адсорбция молекул адсорбтива происходит на активных центрах, всегда существующих на поверхности адсорбента. Такими центрами могут быть пики и возвышения, имеющиеся на любой, даже самой гладкой поверхности. В результате большой ненасыщенности силового поля около таких пиков и выступов эти участки обладают способностью удерживать налетающие молекулы газа. Вследствие малого радиуса действия адсорбционных сил, имеющих природу, близкую к химической, и способности их к насыщению, каждый активный центр, адсорбируя молекулу адсорбтива, становится уже неспособным к дальнейшей адсорбции. В результате этого на поверхности адсорбента может образоваться только мономолекулярный слой адсорбтива. И изотерма адсорбции примет следующий вид (рис.1).
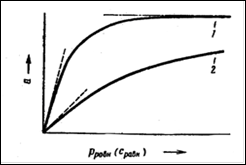
Рис. 1. Обычный вид изотерм адсорбции при различных температурах:
1 — изотерма, отвечающая температуре Т1; 2—изотерма, отвечающая температуре Т2 (Т1< Т2).
Однако, наряду с изотермами адсорбции, вид которых показан на рис. 1, довольно часто на практике встречаются изотермы, не имеющие второго участка, почти параллельного оси давлений и отвечающего насыщению поверхности адсорбента молекулами адсорбтива. Вид таких изотерм изображен на рис.2. Как можно видеть, в точке А изотерма Ленгмюра круто поднимается кверху. Очевидно, связывание адсорбтива адсорбентом не прекращается после образования мономолекулярного слоя, а продолжается дальше. Форму подобных изотерм нельзя объяснить как следствие капиллярной конденсации, так как такая изотерма наблюдается и у непористых адсорбентов, когда капиллярная конденсация невозможна.
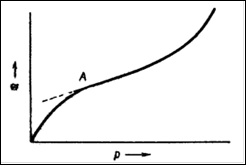
Рис. 2. Вид изотермы, характерной для полимолекулярной адсорбции.
Для объяснения этого явления Поляни предложил теорию полимолекулярной сорбции Рассмотрим кратко исходные положения этой теории, особенно пригодной в случае адсорбции паров на твердом теле:
- Адсорбция обусловливается чисто физическими силами.
- На поверхности адсорбента нет активных центров, а адсорбционные силы действуют вблизи от поверхности адсорбента и образуют около этой поверхности со стороны газовой фазы непрерывное силовое поле.
- Адсорбционные силы действуют на сравнительно большие расстояния, во всяком случае большие, чем размеры отдельных молекул адсорбтива, и поэтому можно говорить о существовании у поверхности адсорбента адсорбционного объема, который заполняется при адсорбции молекулами адсорбтива.
- Действие адсорбционных сил по мере удаления от поверхности уменьшается и на некотором расстоянии практически становится равным нулю.
- Притяжение данной молекулы поверхностью адсорбенга не зависит от наличия в адсорбционном пространстве других молекул, вследствие чего возможна полимолекулярная адсорбция.
- Адсорбционные силы не зависят от температуры, и, следовательно, с изменением температуры адсорбционный объем не изменяется. Это не противоречит тому, что с повышением температуры адсорбция уменьшается; в этом случае снижение адсорбции обусловливается не уменьшением адсорбционных сил, а увеличением в результате нагревания интенсивности теплового движения адсорбированных молекул, что приводит к увеличению десорбции.
Большинство изотерм физической адсорбции можно отнести к одному из пяти типов, от I до V, по классификации, впервые предложенной С. Брунауэром, Л. Демингом, У. Демингом. и Э. Теллером, иногда приписываемой Брунауэру, Эммету и Теллеру (БЭТ) или даже одному Брунауэру . Эти типы изотерм показаны на рис. 3.
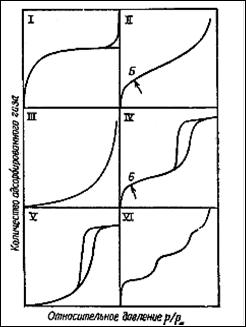
Рис. 3. Пять типов изотерм адсорбции (I—V) по классификации Брунауэра, Деминга, Деминга и Теллера (БДДТ) и ступенчатая изотерма (тип VI).
Как мы уже отмечали, полимолекулярная адсорбция характеризуетея S-образной изотермой адсорбции (тип II). Однако следует иметь в виду, что кривую аналогичной формы можно получить при адсорбции, осложненной капиллярной конденсацией (тип IV). Точка Б, которой соответствует начало прямолинейного участка, соответствует завершению образования монослоя, так что величина адсорбции в точке Б должна быть равна емкости монослоя. Возможность локализации точки Б зависит от формы изгиба изотермы. Если изгиб крутой, точка Б может быть локализована с хорошей точностью, даже если линейный участок изотермы короткий.
Существует много типов пористых систем. И в различных образцах, и в одном и том же образце отдельные поры могут значительно различаться как по форме, так и по размеру. Особый интерес во многих случаях может представлять поперечный размер пор, например диаметр цилиндрических пор или расстояние между стенками щелевидных пор. Удобная классификация пор по размерам принята Международным союзом по теоретической и прикладной химии (IUPAC) :
Таблица 1 ,
Дата: 2019-05-28, просмотров: 375.