Курсовая работа
На тему
«Развитие экологического мышления на уроках химии при изучении темы «Аминокислоты»»
СОДЕРЖАНИЕ
Введение
Глава 1 . Чистые продукты питания и здоровье человека
Глава 2. Состояние изучаемого вопроса в современной российской школе
2.1. Аминокислоты
2.2. Способы получения
2.3. Химические свойства
| |
2.4. Значение и применение аминокислот
Глава 3. Экологические особенности изучения темы «Аминокислоты»
Глава 4. Мои уроки
Литература
ВВЕДЕНИЕ
С первых шагов своего развития человек неразрывно связан с природой. Он всегда находился в тесной зависимости от растительного и животного мира, от их ресурсов и был вынужден повседневно считаться с особенностями распределения и образа жизни зверей, рыб, птиц. Представления древнего человека об окружающей среде не носили научного характера и были не всегда осознанными, но с течением времени они послужили источником накопления экологических знаний. Повсеместно растёт понимание того, что человечество разрушает окружающую среду и подрывает собственное будущее. Современная цивилизация осуществляет невиданное давление на природу. Планета земля как целое, включая воду, воздух, землю, недра, а также биологические объекты, не исключая и человека, является целостной системой. Экологические проблемы есть результат взаимодействия нашей цивилизации и окружающей среды в эпоху промышленного развития. Началом этой эпохи принято считать 1860 год, примерно в это время в результате бурного развития евроамериканского капитализма произошёл выход тогдашней промышленности на новый уровень.
Актуальность темы. Пища состоит из белков, жиров, углеводов, а белки в свою очередь состоят из аминокислот. Человек синтезирует некоторые аминокислоты, используя их в пищу и как добавка в корм животным. А как известно любой синтез сопровождается образованием отходов, и возникает проблема их вторичного использования или утилизации.
Цель моей работы заключалась в рассмотрении темы «Аминокислоты» и выявлении фактов, способствующих развитию экологического мышления на уроках химии при изучении данной темы. Для достижения цели были поставлены следующие задачи:
1. Рассмотреть как данная тема раскрывается в различных учебниках по химии.
2. Изучить прикладные и экологические аспекты данной темы.
3. Рассмотреть производство аминокислот и способы утилизации отходов.
4. Предложить конспект урока по данной теме.
5. Привести тесты и задачи общехимической и экологической направленности
Амины. Аминокислоты. Белки - 7 часов
Амины - органические основания
Анилин- представитель ароматических аминов, его практическое применение
Аминокислоты - амфотерные органические соединения. Строение, изомерия, свойства
Значение аминокислот. Синтез пептидов.
Белки - природные высокомолекулярные соединения. Химические функции белков.
Химические свойства белков. Проблема синтеза белка
Повторение и закрепление знаний по теме « Амины. Аминокислоты. Белки ».
Преподавание темы начинается с 11 класса, первого полугодия. При изучении этой темы пользуются учебником 11 класса химии под редакцией Г. Е. Рудзитис, Ф.Г. Фельдман, также учебником за 11 класс под редакцией Н. С. Ахметова. Дидактическим материалом служит книга по химии для 11классов под редакцией А. М. Радецкого, В. П. Горшкова; используются задания для самостоятельной работы по химии за 10-11 класса под редакцией Р. П. Суровцева, С. В. Софронова; используется сборник задач по химии для средней школы и для поступающих в вузы под редакцией Г. П. Хомченко, И. Г. Хомченко. В 11 классе на изучение темы «Аминокислоты» отводится 1 час [4].
Кратко рассмотрим как данная тема освещается в различных учебниках по химии
Аминокислоты
Аминокислотами называются соединения, в молекулах которых содержатся одновременно аминные и карбоксильные группы.В зависимости от положения аминогруппы по отношению к карбоксильной группе различают α-, β-, γ-аминокислоты. Наибольшее значение в процессах жизнедеятельности играют α-аминокислоты, из них как раз состоят белки.
Чаще используют тривиальные названия. Наиболее важные кислоты представлены в таблице.
Таблица"Важнейшие α-аминокислоты"
| Аминокислота | Формула | Условное обозначение | Тпл0C |
| Глицин | 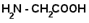
| Гли | 292 |
| Аланин | 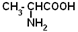
| Ала | 297 |
| Валин | 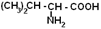
| Вал | 315 |
| Лейцин | 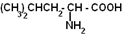
| Лей | 337 |
| Изолейцин | 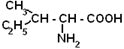
| Илей | 284 |
| Аспаргиновая кислота | 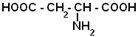
| Асп | 270 |
| Глутаминовая кислота | 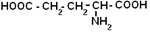
| Глу | 249 |
| Орнитин | 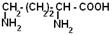
| Орн | 140 |
| Лизин | 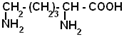
| Лиз | 224 |
| Серин | 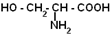
| Сер | 228 |
| Треонин | 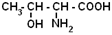
| Тре | 253 |
| Цистеин | 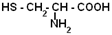
| цис-SH | 178 |
| Цистин | 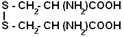
| цис-S | цис-S | 260 |
| Метионин | 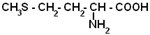
| Мет | 283 |
| Фенилаланин | 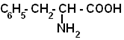
| Фен | 275 |
| Тирозин | 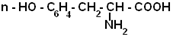
| Тир | 344 |
| Триптофан | 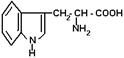
| Три | 382 |
| Пролин | 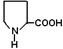
| Про | 299 |
| Оксипролин | 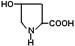
| Про-ОН | 270 |
| Гистидин | 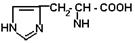
| Гис | 277 |
| Аргинин | 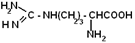
| Арг | 238 |
| Аспаргин | 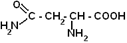
| Асн | 236 |
| Глутамин | 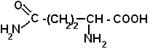
| Глн | 185 |
Физические свойства
Аминокислоты - бесцветные кристаллические вещества, хорошо растворяются в воде, температура плавления 230-300·С. Многие а-аминокислоты имеют сладкий вкус [5].
Способы получения
Для получения а-аминокислот в лабораторных условиях обычно используют два следующих способа.
1. Взаимодействие а-галогенкарбоновых кислот с избытком аммиака. В ходе этих реакций происходит замещение атома галогена в галогенкарбоновых кислотах (об их получении см. § 10.4) на аминогруппу. Выделяющийся при ЭТОМ хлороводород связывается избытком аммиака в хлорид аммония.
2. Гидролиз белков. При гидролизе белков обычно образуются сложные смеси аминокислот, однако с помощью специальных методов из этих смесей можно выделять отдельные чистые аминокислоты.
2.3 Химические свойства
| |
Основные свойства аминов 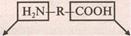 кислотные свойства карбоновых кислот
кислотные свойства карбоновых кислот
Амфотерные свойства
1. Взаимодействие с основаниями и с кислотами:
а) как кислота (участвует карбоксильная группа):
б) как основание (участвует аминогруппа)
2. Взаимодействие внутри молекулы- образование внутренних солей
3. Взаимодействие аминокислот друг с другом- образование пептидов
ГЛАВА 4. МОИ УРОКИ
Урок по теме: "Аминокислоты. Белки"
“Жизнь – это способ существования белковых тел, существенным моментом которого является постоянный обмен веществ с окружающей их внешней природой, причем с прекращением этого обмена веществ прекращается и жизнь, что приводит к разложению белка”.
Ф. ЭНГЕЛЬС
Цели:
1. обучающая: обеспечить сознательное усвоение учащимися важнейших химических законов, понятий, теорий в контексте изучения аминокислот и белков.
2. развивающая: формировать высокий уровень мыслительной деятельности, научить использовать в решении повседневных задач различные мыслительные приемы.
3. Воспитывающая: показать диалектическую взаимосвязь и взаимообусловленность химических фактов. Довести до учащихся мысль о том, что опровергаются только теории, факты опровергнуть нельзя. С помощью межпредметных связей способствовать формированию картины мира.
Оборудование:
1. Листы с заданиями экспресс теста, бланки ответа на тест (для каждого ученика по два листа, скрепленных скрепкой, между которыми вложена копировальная бумага). (Приложение 1)
2. Листы с текстом для изучения (по одному на парту). (Приложение 2)
3. Оформление доски:
На доске записана тема урока, на листах формулы и названия аминокислот, для изучения функций белков на листах: типы и примеры в центре записаны функции белков.
4. Оборудование для проведения лабораторного эксперимента:
Продукты питания: молоко, молочные продукты (простокваша, сметана, кефир, творог и др.), мука (смесь с водой), крупа (любая крупа, размоченная или разваренная до кашеобразного состояния), бобовые (горох, фасоль, бобы, соя), размельченные мясо и рыба, замоченные дрожжи, желатин.
Пробирки, 10%-ный раствор гидроксида натрия, 1%-ный раствор сульфата меди.
Методика проведения опыта: К 0,5 мл раствора белка добавляют столько же 10%-ного раствора гидроксида натрия (калия) и 6-10 капель 1%-ного раствора сульфата меди (II). Голубая окраска раствора, свойственная солям меди (II), по мере образования комплексного соединения переходит в сиреневую.
5. Листы с заданиями для работы в группах.
Этапы урока:
1. Вводное слово учителя. Постановка целей урока.
2. Экспресс – тест по темам «Аминокислоты. Белки». Проверка и обсуждение результатов.
3. Работа с текстом в парах по теме «История открытия и изучения белков».
4. «Типы белков и их функции в организме человека» дидактическая игра.
5. Лабораторный эксперимент по теме «Обнаружение белков в пищевых продуктах».
6. Рассказ учителя о превращениях белков в пищеварительной системе.
7. Решение познавательных задач с практическим содержанием (работа в группах).
8. Подведение итогов урока. Выставление оценок. Обозначение дальнейших тем.
ХОД УРОКА
Ход урока
I. Организационный момент.
II. Актуализация знаний.
(Ученикам заранее предлагается повторить тему “Аминокислоты”).
Два ученика работают у доски.
Задание 1. Напишите формулы 2-аминопропановой кислоты (аланина) и 3-метил-2-аминобутановой кислоты (валина). Какие еще названия этих кислот Вы можете предложить?
Задание 2. Напишите формулу 2-аминоэтановой кислоты. Какие еще названия этой кислоты Вам известны? Составьте дипептид из двух остатков этой кислоты. Укажите место пептидной связи.
Фронтальная беседа.
1. Какие две функциональные группы входят в состав аминокислот?
2. Чем являются аминокислоты с точки зрения кислотно-основных свойств? За счет каких функциональных групп?
3. Дать понятие пептидной связи.
4. Могут ли аминокислоты образовывать водородные связи? За счет каких атомов?
5. Какие вещества называются полимерами? Приведите примеры известных вам полимеров.
IV. Закрепление
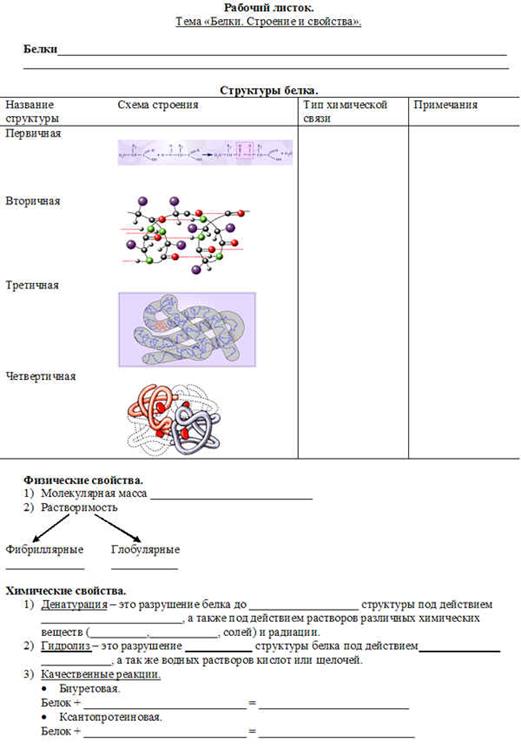
ТЕСТЫ
1. Выберите формулу аминокислоты:
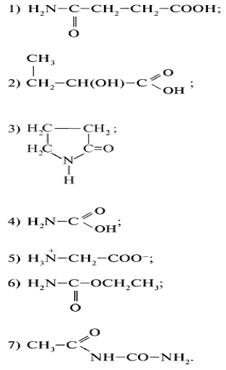
2. В задании 1 укажите химическую формулу амида.
3. В задании 1 укажите химическую формулу уреида.
4. Какая формула в задании 1 может принадлежать 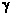 -бутиролактаму?
-бутиролактаму?
5. Среди приведенных ниже химических формул укажите формулу аминокислоты, содержащей ароматический заместитель.
6. Какое вещество в задании 5 имеет название «пролин»?
7. Какое вещество (см. задание 5) является изомером антраниловой кислоты?
8. Подберите второе название для 2-амино-3-меркаптопропановой кислоты.
1)Валин.
2)Серин.
3)Тирозин.
4)Метионин.
5) Цистеин. +
6)Треонин.
7) Аспарагин.
9. Какое вещество в задании 8 является амидом аминокислоты? 7)
10. Какое название получит данная аминокислота по номенклатуре ИЮПАК:
H2N–(CH2)4–CH(NH2)–COOH?
1) 2,6-Диаминогексановая кислота. +
2)2,6-Диаминокапроновая кислота.
3) 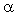 ,
, 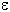 -Диаминокапроновая кислота.
-Диаминокапроновая кислота.
4) 1-Карбокси-1,5-диаминопентан.
11. В формуле аминоуксусной кислоты стрелками показано смещение электронной плотности по 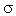 -связям:
-связям:
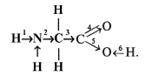
В каком месте направление смещения электронной плотности показано неправильно? В ответе укажите номер связи. (2)
12. Какой из пронумерованных атомов в молекуле глицина является объектом атаки электрофильных частиц? (1)
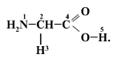
13. Известно, что аминокислоты представлены в водных растворах в виде биполярных ионов (цвиттер-ионов):
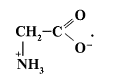
Определите ошибочное утверждение в описании строения и свойств цвиттер-иона.
1) Цвиттер-ион существует в растворах, у которых рН соответствует
зоэлектрической точке аминокислоты.
2) Биполярная частица не может проявлять кислотные свойства, т. к. в карбоксигруппе отсутствует ион Н+.
3) При добавлении в раствор более сильной кислоты карбоксигруппа приобретает свой обычный состав: –СООН.
4) В электрическом поле цвиттер-ион неподвижен.
5) Цвиттер-ионы образуют все аминокислоты независимо от строения радикала.
6) Водные растворы, содержащие указанные ионы, не изменяют окраски индикаторов. +
14. Выберите неверный пункт в описании строения и свойств аспарагиновой кислоты
НООС–СН2–СН(NН2)–СООН.
1) В водном растворе образует ионы, подвижные в электрическом поле.
2) Фиолетовый лакмус в растворе аспарагиновой кислоты приобретает красное окрашивание.
3) Ионы, образуемые аспарагиновой кислотой в водном растворе, в электрическом поле перемещаются к аноду.
4) Ионы аспарагиновой кислоты в электрическом поле неподвижны, т. к. представляют собой биполярные ионы. +
5) В водном растворе аспарагиновая кислота присутствует в следующей форме:
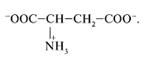
15. Все аминокислоты, образующие белки, – 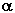 -аминокислоты. Их строение (за исключением пролина) может быть представлено следующими структурной и проекционной формулами:
-аминокислоты. Их строение (за исключением пролина) может быть представлено следующими структурной и проекционной формулами:
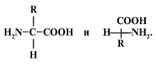
Определите неверное утверждение в описании проекционной формулы аминокислоты и свойств молекулы.
1) Это оптически активное соединение вращает плоскость поляризованного света влево или вправо.
2)Данная аминокислота относится к D-ряду.
3) Принадлежность к D-ряду определяется вращением плоскости поляризации света. В данном случае наблюдается вращение плоскости поляризации вправо. +
4) Принадлежность к D- или к L-ряду определяется относительным расположением атома Н и NH2-группы при С-2 в пространстве, группы –СООН и –R должны быть удалены от наблюдателя. При изображении на плоскости удаленность показана вертикальной линией связи; приближенность к наблюдателю демонстрирует горизонтальная линия.
5) Аминокислота приведенной оптической конфигурации не может быть обнаружена в белках.
16. Какое утверждение в описании строения и свойств лизина
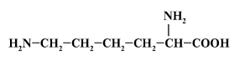
наиболее сомнительно?
1) Вещество может быть названо 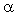 ,
, 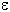 -диаминокапроновой кислотой.
-диаминокапроновой кислотой.
2) Это незаменимая аминокислота, т. к. в организме человека невозможен ее синтез из более простых веществ.
3) Водные растворы лизина имеют рН > 7 и изменяют цвет индикаторов фиолетового лакмуса и бесцветного фенолфталеина.
4) В образовании пептидной цепи белка у лизина участвуют карбоксильная группа и 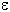 -аминогруппа. +
-аминогруппа. +
17. При каких условиях возможно такое превращение:
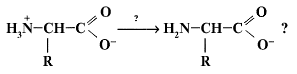
1) Достаточно растворения исходного вещества в воде. В водном растворе устанавливается равновесие между указанными формами.
2) При добавлении к исходному веществу раствора кислоты.
3) При добавлении к водному раствору вещества раствора основания. +
4) Подобный переход наблюдается при действии на цвиттерион сил электрического поля.
5) Переход возможен только при действии на исходное вещество окислителей.
18. В какой форме существует аминокислота валин в растворе при рН, соответствующем изоэлектрической точке для данной аминокислоты?
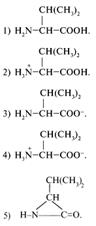
19. Одним из способов получения аминокислот является синтез галогенсодержащих карбоновых кислот с последующим действием избытка аммиака. Для каких аминокислот наиболее приемлем данный способ получения?
1) 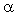 -Аминокислот. +
-Аминокислот. +
2) 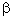 -аминокислот.
-аминокислот.
3) 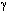 -Аминокислот.
-Аминокислот.
4) 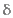 -Аминокислот.
-Аминокислот.
20. Какое исходное вещество необходимо взять для получения аминокислоты по приведенной схеме:
NН4CN + Х 
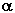 -аминомасляная кислота?
-аминомасляная кислота?
Вещество Х – это:
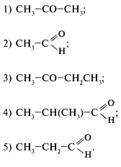
21. Укажите наиболее вероятный продукт реакции метакриловой кислоты с аммиаком:
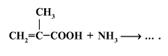
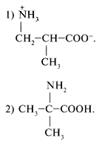
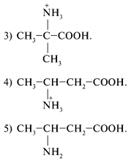
22. Какое вещество образуется в результате следующих превращений:
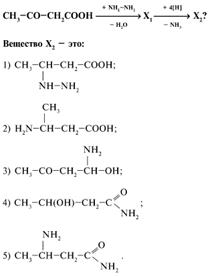
23. В данной схеме превращений определите вещество Х1:

24. В задании 23 определите конечный продукт цепочки превращений, вещество X4 (укажите основной продукт).
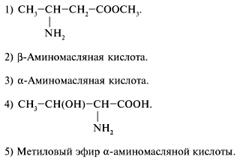
25. Какое вещество Х следует взять для получения 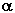 -аминоизовалериановой кислоты из метилового эфира нитроуксусной кислоты:
-аминоизовалериановой кислоты из метилового эфира нитроуксусной кислоты:
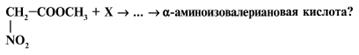
1) СН3–СНСl–CН3. +
2)СН3–СН2–CН2Сl.
3)(СН3)2СН–СН2Сl.
4)СН2Сl–СН2–СH3.
5) (СН3)3ССl.
26. Выберите правильное утверждение, описывающее приведенную ниже схему:
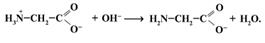
1) Аминокислота проявила специфическое свойство, которое следует рассматривать как результат присутствия в молекуле одновременно NН2- и СООН-групп.
2) Аминокислота проявила свойства основания, т. к. изменения произошли по 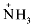 -группе, которая определяет основные свойства вещества.
-группе, которая определяет основные свойства вещества.
3) Аминокислота в таком состоянии не может проявлять свойства кислоты, т. к. в карбоксигруппе отсутствует атом водорода.
4) Аминокислота проявила свойство кислоты, т. к. в реакции отщепляются ионы Н+. +
5) Течение реакции по приведенной схеме невозможно.
27. Какое вещество вероятнее всего образуется в реакции
H2N–(СН2)2–СООН + РСl5  ... ?
... ?
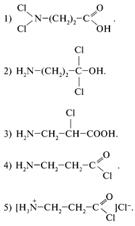
28. Аминокислоты могут быть проалкилированы с помощью ангидридов кислот. Вам предлагается определить продукт реакции, идущей по следующей схеме:
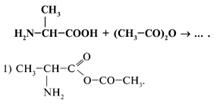
29. Какое условие будет способствовать реакции этерификации 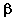 -аминопропионовой кислоты с этанолом:
-аминопропионовой кислоты с этанолом:
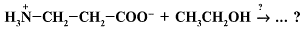
1)Добавление щелочи.
2) Аминокислота должна быть взята в виде водного раствора.
3)Повышение давления.
4) Добавление соляной кислоты. +
30. Какое вещество является продуктом реакции этерификации аланина с этанолом в присутствии бромоводорода?
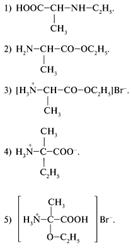
31. Каким веществом следует воспользоваться для получения
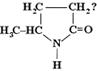
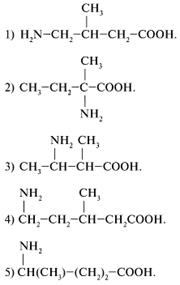
32. Какое вещество из предложенных в задании 31 при нагревании легко отщепляет аммиак и образует непредельную кислоту? (3)
33. Какая аминокислота из предложенных в задании 31 при нагревании отщепляет воду и может образовать производное дикетопиперазина? (1)
34. Какой из предложенных лактамов легче подвергается гидролизу?
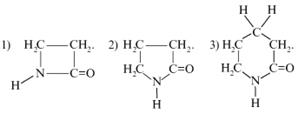
35. Какая из нижеприведенных химических реакций при указанных условиях приведет к дезаминированию аминокислоты?
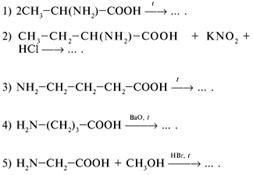
36. В ходе какой химической реакции (см. ответы к заданию 35) произойдет декарбоксилирование аминокислоты? (4)
37. Какая химическая реакция из приведенных в задании 35 приведет к образованию пропанамина? (4)
38. В какой реакции из приведенных в задании 35 образуется масляная кислота? (2)
39. Какое вещество образуется в результате полного гидролиза 3,6-диэтил-2,5-дикетопиперазина:
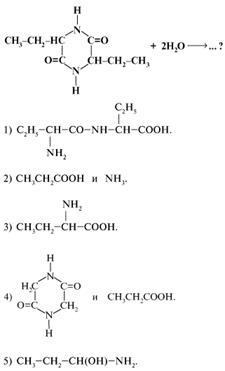
40. Возможно ли образование дипептида между указанными веществами при участии в химическом процессе атома Сl:
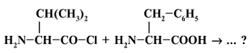
Выберите правильный ответ.
1) Да, возможно. Реакция сопровождается отщеплением НCl и образованием пептидной связи. +
2) Нет, пептидная связь образуется только при взаимодействии карбокси- и NН2-групп разных молекул аминокислот с отщеплением воды.
3) Нет, потому что атом Сl, имея свободные электронные пары, входит в сопряжение с р-орбиталями карбонильной группы. Вследствие этого cвязь С–Сl оказывается прочной. Дипептид не образуется.
4) Нет, дипептид по указанной схеме не образуется. Продуктом реакции является
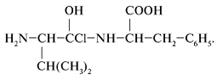
41.Сколько различных дипептидов можно получить, используя только глицин и фенилаланин?
а) 1
б) 2
в) 3
г) 4 +
42. Реагируя с какими веществами при определенных условиях аминоуксусная кислота образует соль?
а) хлороводород +
б) этанол
в) гидроксид натрия +
г) серная разбавленная кислота +
43. Реагируя с какими веществами при определенных условиях глицин формирует пептидную связь?
а) хлороводород
б) гидроксид калия
в) альфа- аланин +
г) глицилглицин +
44. При гидролизе каких веществ можно получить аминокислоту?
а) глицилфенилаланин +
б) крахмал
в) белок
г) твердый жир +
45. Аминокислоту можно получить при взаимодействии аммиака с:
а) хлорбензолом
б) этилбромидом
в) 2- пропанолом
г) β- хлорпропионовой кислотой +
46. В молекуле белка содержится один атом серы и массовая доля серы в белке 0,32%. Вычислите значение молярной массы (г/моль) белка:
а) 1000
б) 10000 +
в) 1* 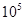
г) 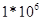
47. Укажите название веществ, которые реагируют с 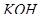 :
:
а) анилин
б) хлорид фениламмония +
в) глицин +
г) бромид триметиламмония +
48. С хлороводородом реагируют:
а) анилин +
б) хлорид метиламмония
в) глицин +
г) бромид триметиламмония +
49. Какие утверждения в отношении строения и свойств белков справедливы?
а) первичная структура- последовательность альфа- аминокислотных звеньев в линейной полипептидной цепи +
б) продукт реакции поликонденсации β—аминокислот
в) при гидролизе образует смесь различных альфа – аминокислот +
г) гемоглобин- белок с четвертичной структурой +
50. Какие из названных соединений обладают амфотерными свойствами?
а) метиламин
б) анилин
в) аминоуксусная кислота +
г) альфа- аланин +
51. Биполярный ион аминокислоты образуется в результате:
а) взаимодействия со щелочами
б) взаимодействия с галогеноводородами
в) образования полипептидов
г) внутренней нейтрализации +
52. Амин может образоваться в результате реакций:
а) гидролиза дипептида
б) взаимодействия бромида фениламмония с водным раствором щелочи+
в) внутренней нейтрализации аминокислоты
г) восстановления нитробензола водородом +
53. С какими веществами, перечисленными ниже реагирует гликокол:
а) бромоводород +
б) гидроксид калия +
в) 1- пропанол +
г) β- аланин +
54. Сколько пептидных связей входит в состав молекулы тетрапептида?
а) 1
б) 3 +
в) 2
г) 4
55. Реагируя с каким веществом глицин образует сложный эфир?
а) гидроксид натрия
б) этанол (кислая среда) +
в) бромоводород
г) аминоуксусная кислота
56. Реагируя с какими веществами хлороводород образует соль?
а) фенол
б) альфа- аланин +
в) анилин +
г) нитробензол
57. Чтобы выделить из бромида фениламмония фениламин нужно воспользоваться реактивом:
а) водой
б) водородом
в) водным раствором щелочи +
г) бромной водой
58. Процесс синтеза метионина включает:
а) 6 стадий
б) 2 стадии
в) 1 стадию
г) 5стадий +
59. Побочные продукты при синтезе метионина:
а) сероводород и циановодород +
б) серная кислота
в) формальдегид
г) фенол
60. Одним из промышленных способов метионина является:
а) синтез из метилового спирта +
б) синтез из ацетилена
в) синтез из азотной кислоты
г) синтез из элементарной серы [11].
| Количество выполненных заданий, в % | Оценка |
| 35-40 | неудовлетворительно |
| 40-60 | удовлетворительно |
| 60-95 | хорошо |
| 95-100 | отлично |
Литература
1.В.М.Комягин «Экология и промышленность».
2.Одум Ю. «Основы экологии» - М.:Мир, 1985г.
3.Никитин Д.П. Новиков Ю.В. Окружающая среда и человек. – М.: 1986г.
4. Горковенко М. Ю. Поурочные разработки по химии, Москва «ВАКО»,
5. Ахметов Н. С. Учебник для 11 класса общеобразовательных учреждений. М.: Просвещение, 1998 г.
6.Рудзитис Г. Е., Фельдман Р. Г. Учебник для 11 класса средней школы. М.: Просвещение, 1992
7. Котова Т.А., Волкова М.В. Успехи в области производства и применения аминокислот. - М.:ОНТИТЭ Имикробиопром, 2003.
8. Опытно-промышленный регламент № 254 производства L-триптофана микробиологическим синтезом. - М.; Бишкек, 1994. - 195 с.
9. Литовченко И.В., Макаренко К.В., Стручалина Т.И. Проблемы и перспективы анаэробной микробиологической конверсии аминокислот в биогаз. - Фрунзе: Илим, 1990. - 20с. .
10. Литовченко В.В., Таштаналиев А.С., Стручалина Т.И.., Прохоренко В.В. Биотрансформация органических отходов производства аминокислот // / Изв. НАН КР. - 2001. - № 1-2. - С. 31-35.
11. Габриелян О.С., Остроумов И.Г., Остроумова Е.Е. Органическая химия в тестах, задачах, упражнениях. 10 класс: Учеб. пособие для общеобразовательных учреждений. – М.: Дрофа, 2004. – С. 190–215.
12. Энциклопедия для детей. Т. 17. Химия / Под ред. В.А. Володина. – М.: Аванта+, 2001. – С. 370–393
13. Барковский Е. В., Врублевский А. И. Тесты по химии, Минск, Юнипресс, 2002
14. Химия: Большой справочник для школьников и поступающих в вузы / Е. А. Алферова, Н. С. Ахметов, Н. В. Богомолова и др. М.: Дрофа, 1999. 485-498
Курсовая работа
На тему
«Развитие экологического мышления на уроках химии при изучении темы «Аминокислоты»»
СОДЕРЖАНИЕ
Введение
Глава 1 . Чистые продукты питания и здоровье человека
Глава 2. Состояние изучаемого вопроса в современной российской школе
2.1. Аминокислоты
2.2. Способы получения
2.3. Химические свойства
| |
2.4. Значение и применение аминокислот
Глава 3. Экологические особенности изучения темы «Аминокислоты»
Глава 4. Мои уроки
Литература
ВВЕДЕНИЕ
С первых шагов своего развития человек неразрывно связан с природой. Он всегда находился в тесной зависимости от растительного и животного мира, от их ресурсов и был вынужден повседневно считаться с особенностями распределения и образа жизни зверей, рыб, птиц. Представления древнего человека об окружающей среде не носили научного характера и были не всегда осознанными, но с течением времени они послужили источником накопления экологических знаний. Повсеместно растёт понимание того, что человечество разрушает окружающую среду и подрывает собственное будущее. Современная цивилизация осуществляет невиданное давление на природу. Планета земля как целое, включая воду, воздух, землю, недра, а также биологические объекты, не исключая и человека, является целостной системой. Экологические проблемы есть результат взаимодействия нашей цивилизации и окружающей среды в эпоху промышленного развития. Началом этой эпохи принято считать 1860 год, примерно в это время в результате бурного развития евроамериканского капитализма произошёл выход тогдашней промышленности на новый уровень.
Актуальность темы. Пища состоит из белков, жиров, углеводов, а белки в свою очередь состоят из аминокислот. Человек синтезирует некоторые аминокислоты, используя их в пищу и как добавка в корм животным. А как известно любой синтез сопровождается образованием отходов, и возникает проблема их вторичного использования или утилизации.
Цель моей работы заключалась в рассмотрении темы «Аминокислоты» и выявлении фактов, способствующих развитию экологического мышления на уроках химии при изучении данной темы. Для достижения цели были поставлены следующие задачи:
1. Рассмотреть как данная тема раскрывается в различных учебниках по химии.
2. Изучить прикладные и экологические аспекты данной темы.
3. Рассмотреть производство аминокислот и способы утилизации отходов.
4. Предложить конспект урока по данной теме.
5. Привести тесты и задачи общехимической и экологической направленности
ГЛАВА 1. ЧИСТЫЕ ПРОДУКТЫ ПИТАНИЯ И ЗДОРОВЬЕ ЧЕЛОВЕКА
Каждый человек знает, что пища необходима для нормальной жизнедеятельности организма. Но мы часто употребляем в пищу то, что вкусно, что можно быстро приготовить, и не очень задумываемся о полезности и доброкачественности употребляемых продуктов. Врачи утверждают, что полноценное рациональное питание – важное условие сохранения здоровья и высокой работоспособности, а для детей ещё необходимое условие роста и развития. Для нормального развития и поддержки жизнедеятельности организму необходимы белки, жиры, углеводы, витамины и минеральные соли в нужном ему количестве. Нерациональное питание является одной из главных причин возникновения сердечно-сосудистых заболеваний, заболеваний органов пищеварения, болезней, связанных с нарушением обмена веществ. Регулярное переедание, потребление избыточного количества углеводов и жиров - причина развития таких болезней обмена веществ, как ожирение и сахарный диабет. Рациональное питание - важнейшие и непременное условие профилактики не только болезней обмена веществ, но и многих других. Пищевой фактор играет важную роль не только в профилактике, но и в лечении многих заболеваний. Специальным образом организованное питание, лечебное питание, обязательное условие лечения многих заболеваний. Лекарственные вещества синтетического происхождения в отличие от пищевых веществ, являются для организма чужеродными. Многие из них могут вызвать побочные реакции, например, аллергию. В продуктах питания многие биологически активные вещества обнаруживаются в равных, а иногда и в более высоких концентрациях, чем в применяемых лекарственных средствах. Вот почему продукты, в первую очередь овощи, фрукты, семена, зелень применяют при лечении различных болезней. Многие продукты питания оказывают бактерицидные действия, подавляя рост и развитие различных микроорганизмов (яблочный сок, сок граната, сок клюквы). Но теперь появилась новая опасность - химическое загрязнение продуктов питания. Появилось и новое понятие - экологически чистые продукты. Каждому из нас приходилось покупать на рынке или в магазине крупные, красивые овощи или фрукты. Но, попробовав их, с огорчением выясняешь, что они водянистые и совсем невкусные. Обычно это происходит, когда сельскохозяйственные культуры выращивают с применением большого количества удобрений и ядохимикатов. Такая сельскохозяйственная продукция может иметь не только плохие вкусовые качества, но быть опасной для здоровья. Азот – составная часть жизненно важных для растений, а также для животных организмов соединений, например белков. В растения азот поступает из почвы, а затем через продовольственные и кормовые культуры попадает в организмы животных и человека. Сейчас сельскохозяйственные культуры чуть ли не полностью получают минеральный азот из химических удобрений, так как навоза и других органических удобрений уже не хватает для обеднённых азотом почв. Однако в отличие от органических удобрений в химических удобрениях не происходит свободного выделения в природных условиях питательных веществ. Значит, не получается и «гармонического» питания сельскохозяйственных культур, удовлетворяющего требования их роста. В результате происходит избыточное азотное питание растений и вследствие этого накопление в нём нитратов. Излишек азотных удобрений ведёт к снижению качества растительной продукции, ухудшению её вкусовых свойств, снижению выносливости растений к болезням, что, в свою очередь, вынуждает земледельца увеличивать применение ядохимикатов. Они также накапливаются в растениях. Повышенное содержание нитратов приводит к образованию нитритов, вредных для здоровья человека. Употребление такой продукции может вызвать у человека серьёзные отравления, и даже смерть. Особенно резко проявляется отрицательное действие удобрений и ядохимикатов при выращивании овощей в закрытом грунте. Это происходит потому, что в теплицах вредные вещества не могут беспрепятственно испаряться и уноситься потоками воздуха. После испарения они оседают на растения. Растения способны накапливать в себе практически все вредные вещества. Вот почему особенно опасна сельхоз. продукция, выращиваемая вблизи промышленных предприятий и крупных автодорог [1,2].
ГЛАВА 2. СОСТОЯНИЕ ИЗУЧАЕМОГО ВОПРОСА В СОВРЕМЕННОЙ РОССИЙСКОЙ ШКОЛЕ
План изучения темы
Дата: 2019-04-23, просмотров: 355.