Начало созданию концепции стресса положил случайно обнаруженный в эксперименте Гансом Селье в 1936 г. "синдром ответа на повреждение как таковое", получивший название "триада": увеличение и повышение активности коркового слоя надпочечников, уменьшение (сморщивание) вилочковой железы (тимуса) и лимфатических желез, так называемого тимико-лимфатического аппарата, точечные кровоизлияния и кровоточащие язвочки в слизистой оболочке желудка и кишечника. Г. Селье сопоставил эти реакции с симптомами, характерными почти для любого заболевания, такими, как чувство недомогания, разлитые болевые ощущения и чувство ломоты в суставах и мышцах, желудочно-кишечные расстройства с потерей аппетита и уменьшением веса тела. Объединение их в единую систему было правомерно только при наличии единого механизма управления этими реакциями и общего совокупного процесса развития.
Вот как Селье описывает это управление стрессом: "Стрессор возбуждает гипоталамус (пути передачи этого возбуждения до конца не выяснены), продуцируется вещество, дающее сигнал гипофизу выделять в кровь адренокортикотропный гормон (АКТГ). Под влиянием же АКТГ внешняя корковая часть надпочечников выделяет кортикоиды. Это приводит к сморщиванию вилочковой железы и многим другим сопутствующим изменениям: атрофии лимфатических узлов, торможению воспалительных реакций и продуцированию сахара (легкодоступный источник энергии). Другая типичная черта стрессовой реакции – образование язвочек пищеварительного тракта (в желудке и кишечнике). Их возникновение облегчается высоким содержанием кортикоидов в крови, но автономная нервная система тоже играет роль в их появлении" [242, с. 37–38]. Возможность изменений, приводящих к увеличению коры надпочечников и уменьшению тимико-лимфатического аппарата, известна благодаря многочисленным экспериментальным исследованиям (см. далее). До настоящего времени не было определенного представления относительно биологической сущности изъязвлений слизистой желудка и кишечника – "штатного" симптома стресса. Нашу гипотезу, касающуюся этого феномена, мы изложим в главе 3.
Г. Селье предложил различать "поверхностную" и "глубокую" адаптационную энергию. Первая доступна "по первому требованию" и восполнима за счет второй – "глубокой". Последняя мобилизуется путем адаптационной перестройки гомеостатических механизмов организма. Ее истощение необратимо, как считает Г. Селье, и ведет к гибели или к старению и гибели. Предположение о существовании двух мобилизационных уровней адаптации поддерживается многими исследователями [129, 192, 241, 242, 271, 452–454]. Однако тезис об абсолютной необратимости затрат гипотетической "адаптационной энергии" в настоящее время является скорее символическим, чем экспериментально обоснованным.
При непрекращающемся действии стрессогенного фактора проявления "триады стресса" изменяются по интенсивности. Г. Селье выделяет три стадии этих изменений (см. рис. 2). Первая стадия развития стресса – мобилизация как бы по тревоге адаптационных возможностей организма – "стадия тревоги". Автор концепции стресса предположил ограниченность адаптационных возможностей организма. Она проявляется уже в первой стадии стресса. "Ни один организм не может постоянно находиться в состоянии тревоги. Если агент настолько силен, что значительное воздействие его становится несовместимым с жизнью, животное погибает еще в стадии тревоги, в течение первых часов или дней. Если оно выживает, за первоначальной реакцией обязательно следует "стадия резистентности"" [242, с. 35]. Эта вторая стадия – сбалансированное расходование адаптационных резервов. При этом поддерживается практически не отличающееся от нормы существование организма в условиях повышенного требования к его адаптационным системам. Ввиду того что "адаптационная энергия не беспредельна" (Там же), рано или поздно, если стрессор продолжает действовать, наступает третья – "стадия истощения". "Мы до сих пор не знаем, что именно истощается, но ясно, что только не запасы Калорий" (Там же), на этой стадии, так же как на первой, в организме возникают сигналы о несбалансированности стрессогенных требований среды и ответов организма на эти требования. В отличие от первой стадии, когда эти сигналы ведут к раскрытию кладовых резервов организма, в третьей стадии эти сигналы – призывы о помощи, которая может прийти только извне-либо в виде поддержки, либо в форме устранения стрессора, изнуряющего организм.
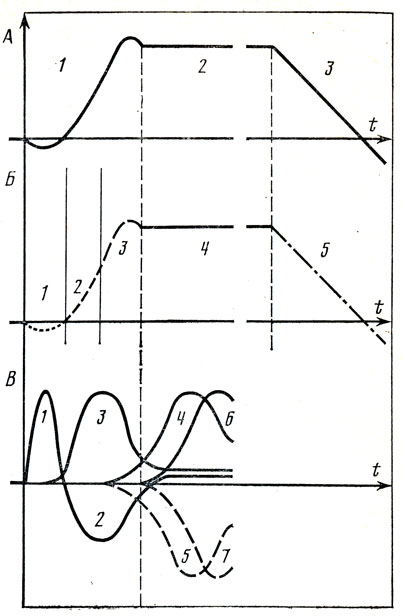
Рис. 2. Схемы развития стресса: А – Стадии развития стресса по Г. Селье: «аларм» – реакция (1); (1); фаза резистентности (2); истощение адаптационных резервов (3). Б – Фазы адаптации при стрессе: разрушение имевшейся «функциональной системности» (1); становление новой «функциональной системности» (2); (2); фаза неустойчивой адаптации (3); фаза устойчивой адаптации (4); фаза разрушения «функциональной системности» (истощения); (5). В – Динамика смены форм адаптационной активности при стрессе: эмоционально-поведенческая активность (1); эмоционально-поведенческая пассивность (2); превентивно-защитная вегетативная активность (3); усиление умственной активности «положительное» (4) и «отрицательное» (5); активизация общения – «положительная» (б) и «отрицательная» (7)
Экстремальные ситуации делят на кратковременные, когда актуализируются программы реагирования, которые в человеке всегда "наготове", и на длительные, которые требуют адаптационной перестройки функциональных систем человека, иногда субъективно крайне неприятной, а подчас неблагоприятной для его здоровья [124, 125, 191 и др.].
При кратковременных сильных экстремальных воздействиях ярко проявляются разные симптомы стресса. Кратковременный стресс – это как бы всестороннее проявление начала длительного стресса. При действии стрессоров, вызывающих длительный стресс (а длительно можно выдержать только сравнительно несильные нагрузки), начало развития стресса бывает стертым, с ограниченным числом заметных проявлений адаптационных процессов. Поэтому кратковременный стресс можно рассматривать как усиленную модель начала длительного стресса. И хотя по своим бросающимся в глаза проявлениям кратковременный и длительный стресс отличаются друг от друга, тем не менее в их основе лежат идентичные механизмы, но работающие в разных режимах (с разной интенсивностью). Кратковременный стресс – бурное расходование "поверхностных" адаптационных резервов и наряду с этим начало мобилизации "глубоких" [469]. Если "поверхностных" резервов недостаточно для ответа на экстремальные требования среды, а темп мобилизации "глубоких" недостаточен для возмещения расходуемых адаптационных резервов, то особь может погибнуть при совершенно неизрасходованных "глубоких" адаптационных резервах.
Длительный стресс – постепенные мобилизация и расходование и "поверхностных", и "глубоких" адаптационных резервов [500]. Его течение может быть скрытым, т. е. отражаться в изменении показателей адаптации, которые удается регистрировать только специальными методами. Максимально переносимые длительные стрессоры вызывают выраженную симптоматику стресса. Адаптация к таким факторам может быть при условии, что организм человека успевает, мобилизуя глубокие адаптационные резервы, "подстраиваться" к уровню длительных экстремальных требований среды. Симптоматика длительного стресса напоминает начальные общие симптомы соматических, а подчас психических болезненных состояний. Такой стресс может переходить в болезнь. Причиной длительного стресса может стать повторяющийся экстремальный фактор. В этой ситуации попеременно "включаются" процессы адаптации и реадаптации. Их проявления могут казаться слитными. В целях совершенствования диагностики и прогноза течения стрессогенных состояний предложено рассматривать как самостоятельную группу состояния, вызванные длительными прерывистыми стрессорами [332].
В настоящее время сравнительно хорошо изучена первая стадия развития стресса – стадия мобилизации адаптационных резервов ("тревога"), на протяжении которой в основном заканчивается формирование новой "функциональной системности" организма, адекватной новым экстремальным требованиям среды [54, 123 и др.]. Второй и третьей стадиям развития стресса, т. е. стадии устойчивого расходования адаптационных резервов и стадии их истощения, посвящены немногочисленные исследования, проводившиеся либо в натурных условиях, что затрудняло получение достоверных и сопоставимых данных, либо в экспериментах с животными [40, 248, 249 и др.].
При длительном пребывании в экстремальных условиях возникает сложная картина изменений физиологических, психологических и социально-психологических характеристик человека. Многообразие проявлений длительного стресса, а также трудности организации экспериментов с многосуточным, многомесячным и т. п. пребыванием человека в экстремальных условиях – основные причины недостаточной его изученности. Систематическое экспериментальное изучение длительного стресса было начато в связи с подготовкой длительных космических полетов [86, 109–111, 113, 114, 150–152, 157, 291–294, 390 и др.]. Исследования первоначально велись с целью определения пределов переносимости человеком тех или иных неблагоприятных условий. Внимание экспериментаторов при этом было привлечено к физиологическим и психофизиологическим показателям: когда в основном были определены физиологические пределы переносимости человеком различных экстремальных физических факторов 1 предметом исследования стали психические состояния и работоспособность человека в экстремальных условиях [124, 176, 277 и др.]. Это потребовало психологических и инженерно-психологических исследований длительного стресса 129–31, 277 и др.]. Важным направлением изучения длительного стресса явились социально-психологические его исследования, необходимые, в частности, для решения проблем групповой совместимости в экстремальных ситуациях, проблем управления массовыми психологическими процессами и т. п. [208 и др.].
Периоды мобилизации адаптационных резервов. Физиологические и психофизиологические исследования длительного стресса позволили выделить в первой стадии стресса три периода адаптации к устойчивым стрессогенным воздействиям (рис. 2).
Первый период – активизация адаптационных форм реагирования счет мобилизации в основном "поверхностных" резервов. Этот период во многом идентичен реакции организма на кратковременное воздействие. Его продолжительность при максимальной субъективно переносимой экстремальности стрессора исчисляется минутами, часами. Первый период стресса у большинства людей отличается стеническими эмоциями и повышением работоспособности.
Если мобилизованная "по тревоге" адаптационная защитная активность не прекращает стрессогенности воздействия, начинают действовать имеющиеся в организме "программы" перестройки существующей в неэкстремальных условиях "функциональной системности" и становления ее новой формы, адекватной экстремальному требованию среды. Эта перестройка рассматривается как второй период на первой стадии развития стресса. Для него часто характерно болезненное состояние человека со снижением работоспособности. Однако высокая мотивация в этом периоде стресса может поддерживать достаточно высокую работоспособность человека у несмотря на выраженную клиническую симптоматику. Более того, психологические факторы (мотивация, установка и т. п.) могут за счет временной "сверхмобилизации" резервов, в частности гипофиз-адреналовой системы, купировать неблагоприятные проявления второго периода [120, 121, 124, 125, 189, 191]. "Сверхмобилизация" может быть реализована безболезненно у здоровых, непереутомленных людей. При переутомлении, при болезнях (в том числе при компенсированных или неявно протекающих), а также в немолодом возрасте "сверхмобилизация" при стрессе за счет психологических побуждений может обострить имеющееся скрытое заболевание, а также вызвать другие болезни стресса (сосудистые, диспластические, воспалительные и психические).
Обращает внимание сходная суммарная продолжительность первых двух периодов стресса в различных экстремальных условиях. Если эти условия приближались к предельно переносимым для человека, то суммарная продолжительность этих периодов в совершенно разных стрессогенных условиях в среднем составляла около 11 суток [129, 277]. Авторы исследований жизнедеятельности человека в крайне неблагоприятных для него условиях описывают период неустойчивой адаптации к этим условиям. Этот период может рассматриваться как третий период первой стадии развития стресса. Его продолжительность варьирует в широких пределах (до 20–60 суток) [151, 248, 249, 256, 314, 354 и др.].
Физиологические компоненты стресса. С самого начала перед исследователями, развивающими теорию стресса, встали вопросы о нервной и эндокринной регуляции стресса, общего адаптационного синдрома. Эти вопросы далеки от исчерпывающего ответа на них, однако, полученные при их решении данные позволяют строить, пусть неполные, но тем не менее внушающие доверие схемы, иллюстрирующие возникновение и развитие стресса. Приведем схему стресса, разработанную Г.Н. Кассилем. "Каждое сильное и сверхсильное воздействие на организм, – пишет он, – возбуждая кору и лимбико-ретикулярную систему головного мозга, вызывает освобождение норадреналина из связанной клетками гипоталамуса формы. Действуя на адренореактивные элементы ретикулярной формации, норадреналин активирует симпатические центры головного мозга и тем самым возбуждает симпатоадреналовую систему. Мобилизация нервных элементов симпатоадреналовой системы ведет к нарастанию во внутренней среде норадреналина. Накопляясь в крови, адреналин через гемато – энцефалический барьер поступает в адренореактивные элементы заднего гипоталамуса… Поступление адреналина в гипоталамус ведет к активации системы гипоталамус – гипофиз – кора надпочечников через адренэргические элементы ретикулярной формации и стимулирует образование кортико – тропинреализующего фактора, следствием чего является образование в гипофизе адрено-кортико-тропного гормона и выброс кортикостероидов в кровь" [108, с. 183–184].
Г.Н. Кассиль подчеркивает, что регуляция описанной Г. Селье системы гипоталамус-гипофиз-кора надпочечников "осуществляется по цепи нейронов, имеющих различную медиаторную природу (адренергическую, холинэргическую, серотонинэргическую)… Различие гуморальных эффектов при стрессе можно объяснить дифференцированным поступлением различных медиаторов в разные отделы центральной нервной системы и действием их на те или другие звенья нейрогуморальной цепи, участвующей в реализации стресс-реакции" [108, с. 181].
Стадия декомпенсации при стрессе, приводящая к "болезням адаптации", по мнению Г.Н. Кассиля, формируется следующим образом. "При длительных и угрожающих жизни стресс-воздействиях кортикостероиды (КС) связываются с особым белком крови – транскортином (Т). Соединение КС + Т задерживается гемато – энцефалическим барьером. В мозг перестает поступать информация о содержании КС в крови, что приводит к нарушению обратной связи и расстройству регуляции функций. Непрерывное поступление КС в кровь приводит к истощению коры, а впоследствии и мозгового слоя надпочечников" [108, с. 180]. Как видно из цитируемой фразы, по мнению Г.Н. Кассиля, возникновение фазы истощепия при стрессе следует рассматривать, в частности, как нарушение механизма саморегуляции вследствие блокады гемато – энцефалическим барьером информации о переизбытке в организме кортикостероидов.
В заключительной стадии истощения "возникает стадия супер- и гиперкомпенсации, в которой уже необратимо подавлены защитные механизмы, истощены, сведены на нет эрготропные функции живой системы и начинают доминировать трофотропные факторы, неизбежно приводящие (если только не вмешиваются внешние силы) организм к коллапсу, шоку и гибели" [108, с. 184–185].
Эрготропные функциональные состояния, согласно теории Гесса-Моннье, характеризуются повышением реактивности (готовности к действию) всей системы чувствительных, двигательных и психических компонентов организма. Медиаторами эрготропного ряда являются катехоламины. Это дофамин, его производное – норадреналин и производное последнего – адреналин. С поступлением в кровь адреналина многие авторы связывают напряженно пассивное реагирование с задержкой внешних проявлений (страх, тревожность, чувство беззащитности и т. п.). Накопление в организме адреналина, видимо, связано со стеническими реакциями, требующими длительного умственного и физического напряжения (гнев, агрессия, аффект и т. д.). Переизбыток в некоторых структурах головного мозга дофамина бывает при паркинсонизме (дрожательном параличе).
М. Фрапкенхойзер называла адреналин "гормоном кролика" в отличие от норадреналина – "гормона льва" [271]. У. Кеннон характеризовал норадрепалин как гормон тревоги, как гормон гомеостаза [334].
Трофотропные функциональные состояния отличаются усилением в организме анаболических и ассимиляторных процессов, накоплением энергетических запасов. К медиаторам этого состояния относятся ацетилхолин – медиатор парасимпатического отдела вегетативной нервной системы, гистамин^ серотонин, принадлежащие к различным группам аминов.
Таким образом, эрготропные, трофотропные и описанные Г. Селье гипоталамо-гипофизарные механизмы функционируют взаимозависимо; тем не менее они могут быть выделены в некоторой степени в самостоятельные функциональные системы. В качестве элементов каждой такой системы выступают: количество данного медиатора (или взаимодействующих медиаторов) в крови* активность синтезирующих и расщепляющих это вещество ферментов, состояние связывающих его механизмов, возможности распространения этого вещества во внутренней среде и т. д. [108 и др.].
Реакция лимфоидной ткани при стрессе в виде сморщивания тимуса (вилочковой железы) и лимфатических узлов входит в "триаду" основных признаков стресс-реакции [242, 243]. Уменьшение тимуса обусловлено: а) деструкцией лимфоцитов; б) замедлением их воспроизводства в результате угнетения метаболических процессов. Наряду со значительным уменьшением количества лимфоцитов в корковом слое тимуса их число несколько увеличивается в мозговом слое этой железы, что Селье охарактеризовал как "инверсию" [242].
Каково физиологическое значение этих реакций в механизмах становления резистентности организма при стрессе, долгое время было неясно. Впоследствии обратили внимание на то, что указанные реакции характерны для стресса, приводящего животное к гибели. Такие реакции обнаруживались при моделировании стресса путем введения соответствующих гормонов в дозах, во много раз превышающих их физиологический уровень. Далее было установлено, что миграция лимфоцитов в мозговой слой, т. е. в ту его часть, в которой сосредоточены вены (артерии в корковом слое), связана с переходом лимфоцитов из тимуса в кровеносное русло [196 и др.]. Известно, что при многих неблагоприятных для организма воздействиях в кровеносное русло выбрасываются лимфоциты и другие клетки крови, продуцируемые селезенкой [68 и др.]. Именно такая реакция преобладала в экспериментах с использованием сравнительно слабых стресс-факторов, позволяющих моделировать начальные проявления стресса. Главной причиной уменьшения содержания клеток в тимусе и селезенке была их миграция, а не уменьшение их продукции или увеличенный их распад [68]. По мнению П.Д. Горизонтова и Ю.И. Зимина, "роль распада лимфоцитов в тимусе при увеличении силы и длительности экстремального воздействия может увеличиваться, особенно в условиях дефицита энергетических ресурсов, когда на восполнение их включаются механизмы неоглюкогенеза" [68, с. 76]. Таким образом, уменьшение лимфоидной ткани было связано с поддержанием некоторых форм энергетического баланса и с выходом лимфоцитов в кровяное русло.
Оставалось неясным, почему при стрессе наблюдается уменьшение числа лимфоцитов в крови (лимфопения). Это противоречие объяснялось тем, что через циркулирующую кровь осуществлялась только транспортировка лимфоцитов. Одним из мест, куда мигрирующие лимфоциты уходили, являлся костный мозг; возможно, таким местом была и рыхлая соединительная ткань, которая в результате этой миграции, вероятно, активирует свою способность поглощать и уничтожать инородные и патогенные элементы, проникающие в организм [68,69]. В условиях физиологической нормы так называемые тимусзависимые лимфоциты в костном мозге отсутствуют и появляются там при стрессе. Проникая в костный мозг, они участвуют в увеличении его иммунной активности [68].
В наших экспериментах (совместно с Елкиной Е.В. и Галле Р.) при тяжелой картине кинетоза была обнаружена реакция резкого "омоложения" крови с выходом в нее клеточных элементов, являющихся "зародышевыми" формами элементов крови, продуцируемыми костным мозгом и в норме не покидающими его до "созревания" и превращения в элементы крови [129].
Итак, в настоящее время становятся понятными первоначально казавшиеся парадоксальными механизмы реакции лимфоидной ткани при стрессе, являющиеся элементом "триады Селье".
Рассмотренные реакции лимфоидной ткани при стрессе, условно говоря, только эфферентное звено. Афферентным звеном включения этой реакции служат, как указывалось выше, не только гуморальные агенты, но и главным образом нервные механизмы. Известно влияние нервной регуляции на формирование иммунных реакций организма, осуществляющихся с участием тимико-лимфатического аппарата. Угнетение высшей нервной деятельности сопровождается угнетением поглотительной функции элементов соединительной ткани, возбуждение – стимуляцией этих функций. Такое регулирование, вероятно, осуществляется опосредованно, через описанные выше механизмы тимико-лимфатической системы.
А.Д. Адо на основании собственных данных и материалов Г.Н. Габричевского полагает, что напряжение нервных компенсаторных процессов в период предвестников ослабляет течение инфекционного процесса, а в некоторых случаях и совсем обрывает его развитие (абортивная форма инфекции или скрытая инфекция). Наоборот, ослабление компенсаторных процессов способствует переходу заражения в заболевание, увеличивая тяжесть инфекционной болезни.
Измерение содержания в крови ее форменных элементов используется (и в психологических экспериментах) как один из объективных показателей интенсивности стресса.
В первых публикациях Ганса Селье не рассматривалось участие нервных регуляционных механизмов в формировании стресса, что вызвало справедливую критику. "… Теория стресса Ганса Селье, исключающая участие нервной системы в активных реакциях организма на стрессор, является недостаточной для объяснения механизма возникновения патологических состояний" [16, с. 5].
В настоящее время накоплены обширные электрофизиологические данные о различных формах вовлечения кортико-лимбико-гипоталамической системы при разных формах стрессовой нагрузки на организм. Показано значение при стрессе афферентно-эфферентных связей гипоталамуса, таламуса, миндалевидного комплекса, гиппокампа и различных отделов коры больших полушарий головного мозга [25, 189, 191, 200, 254 и др.]. Разрозненность обширных экспериментальных данных в настоящее время не позволяет представить целостную картину нейрогормональных механизмов стресса, однако уже сейчас можно рассматривать многие ее элементы.
Были обнаружены две стадии изменений взаимодействия разных структур головного мозга при стрессе, вызванном у животных электрокожным раздражением [189, 191]. Первая характеризуется усилением функциональных связей заднего гипоталамуса с корой головного мозга и уменьшением фазовых сдвигов напряжения между задним гипоталамусом и ретикулярной формацией среднего мозга. На второй стадии снижаются функциональные связи коры полушарий и заднего гипоталамуса, в то же время отмечается фазовая синхронизация ритмической активности заднего гипоталамуса и ретикулярной формации среднего мозга. Поскольку эти стадийные изменения сопряжены с определенными соматовегетативными реакциями, они рассматриваются в рамках единой системы "церебровисцеральных" проявлений стресса [254].
Высказано предположение, что разные стадии стресса могут быть связаны с "чисто нервными механизмами" и с "вторичным включением гормональных механизмов" [254, с. 79]. При этом можно различать по крайней мере три круга циркуляции возбуждения в механизме формирования артериальных гипертензивных реакций при стрессе. Это циркуляция возбуждения внутри лимбико-ретикулярных структур, циркуляция возбуждений, идущих от гипоталамуса через гипофизарный аппарат и вегетативную систему к надпочечникам и от последних посредством гормональных механизмов к ретикулярной формации среднего мозга, наконец, циркуляция между прессорными и депрессорными аппаратами сосудов (Там же).
Приведенная схема может рассматриваться как иллюстрация сложности нейрогормональной регуляции стресса.
Известны различия стрессорных реакций в разных периодах созревания, взросления и старения организма. Эти различия связывают с возрастными изменениями как нервной, так и гормональной систем [21, 25, 156 и др.].
Многие индивидуальные различия стресс-реакции считают обусловленными генетическими особенностями периферической нервной системы, в частности с преобладанием либо симпатической нервной системы, либо системы блуждающего нерва (вагуса), в связи с чем широко распространено деление людей на "симпатикотоников" и "ваготоников". На основании такого разделения предписываются различные мероприятия для предотвращения и лечения "болезней стресса" [51, 91, 146,173 и др.]. В абсолютной правомочности такого разделения высказываются сомнения [108].
Во всей сложности стресс развивается при относительной целостности нервной регуляции организма животного или человека. Однако все основные физиологические проявления этого синдрома возможны у животных, лишенных коры больших полушарий головного мозга, при сохранности ретикулоталамических связей и гипоталамуса [25]. Описаны стрессорные реакции у низших позвоночных (рыб, амфибий) и у беспозвоночных (насекомых, ракообразных, моллюсков и червей) [цит. по 25, с. 3]. Предполагается, что в стрессорных реакциях участвуют нейрогормоны, обнаруженные в нервных узлах.
Различия стресса в зависимости от сложности биологической системы, ее эволюционного уровня используются при классификации форм стресса [25]. Это биологический стресс – главным образом у многих беспозвоночных животных при воздействии разнообразных физических и физико-химических факторов; физиологический стресс, проявляющийся в нарушении тех или иных физиологических процессов, и эмоциональный (психологический) стресс, когда на первый план по значимости или по заметности для исследователя выступают психические стресс-реакции.
Приведенные выше сведения лишь отчасти отражают сложность физиологических процессов при стрессе. Поток новых экспериментальных данных, касающихся стресса, рождает новые схематизированные представления о нем. Эти схемы еще далеки от завершающей обобщенности.
Дата: 2019-03-05, просмотров: 367.