В последние годы отмечено увеличение доли участия анаэробных неспорообразующих микроорганизмов в развитии гнойных заболеваний и осложнений - так называемая неклостридиальная анаэробная инфекция.
Этиология
Возбудителями неклостридиальной анаэробной инфекции часто становятся представители нормальной аутофлоры человека, находящиеся на коже, в полости рта, желудочно-кишечном тракте. Это такие микроорганизмы, как бактероиды, пептококки, пептострептококки, актиномицеты, микрококки и др.
Клиническая картина
Анаэробная неклостридиальная инфекция клинически протекает в виде флегмоны с обширным поражением подкожной жировой клетчатки, фасций и мышц (целлюлитом, фасцитом, миозитом). Особенность неклостридиальной анаэробной инфекции - разлитой, не склонный к ограничению характер процесса, его прогрессирование, несмотря на проводимые весьма радикальные лечебные мероприятия.
При целлюлите отмечают ограниченную, не соответствующую обширности поражения гиперемию кожи, умеренный отёк, выходящий за её пределы. В ране обнаруживают клетчатку грязно-серого цвета, пропитанную серозно-гнойной жидкостью бурого цвета.
При вовлечении в процесс фасций развивается фасцит. Для него характерны некроз и частичное расплавление фасций. При поражении мышц (миозит) они имеют вид «варёного мяса», пропитаны серозно-геморрагическим экссудатом.
Из общих явлений отмечают общую слабость, субфебрильную температуру тела, анемию. При прогрессировании местного процесса нарастают явления общей интоксикации: усиление болей, значительно повышается температура тела, появляются тахикардия, артериальная гипотензия, субиктеричность склер, олигурия, выраженный лейкоцитоз. Летальность при неклостридиальной анаэробной инфекции достигает 60%.
Лучший метод бактериальной диагностики - газожидкостная хроматография, позволяющая выявить анаэробные микроорганизмы, образующие летучие жирные кислоты.
Лечение
Основные компоненты комплексного лечения следующие.
Срочная радикальная хирургическая обработка, заключающаяся в широком рассечении всех поражённых тканей, максимальном иссечении нежизнеспособных тканей, а также тканей с сомнительной жизнеспособностью.
Антибактериальная терапия. Следует начинать лечение с внутривенного введения метронидазола, использования гидроксиметилхиноксилиндиоксида, клиндамицина. Дополнительно назначают антибиотики из группы аминогликозидов, цефалоспоринов, полусинтетических пенициллинов.
Массивная дезинтоксикационная терапия с применением средств экстракорпоральной детоксикации.
Иммунотерапия: переливание плазмы, введение препаратов вилочковой железы, полиоксидония, интерлейкинов, иммуноглобулинов, перфузия ксеноселезёнки.
Таким образом, для успешного лечения анаэробной неклостридиальной инфекции необходимо использовать весь комплекс современной патогенетической терапии при непременном адекватном хирургическом лечении.
Столбняк
Столбняк - специфическое инфекционное заболевание, осложняющее течение раневого процесса и проявляющееся судорожным синдромом и синдромом интоксикации.
На протяжении всей истории человечества столбняк был неизбежным спутником войн, что обусловлено обилием травматических повреждёний. Тем не менее его встречают и в мирное время. По данным ВОЗ, столбняком ежегодно заболевают более 1 млн человек. Летальность достигает 50%, а среди пожилых пациентов - 70-80%.
Этиопатогенез
Возбудитель столбняка - столбнячная палочка (Clostridium tetani). Это строго анаэробный, спорообразующий грамположительный микроорганизм. Споры его очень устойчивы к факторам внешней среды. Бактерии могут существовать в обычных условиях в течение многих лет.
Столбнячная палочка выделяет экзотоксин, состоящий из двух фракций: тетаноспазмина , повреждающего нервную систему, и тетаногемолизина , разрушающего эритроциты.
Тетаноинтоксикация развивается в связи со специфическим воздействием столбнячного токсина на ткани. Через гематоэнцефалический барьер и по нервным волокнам токсин поступает в ЦНС.
Основное его количество обнаруживают в мотонейронах. Токсин дезорганизует деятельность двигательных центров, что приводит к тоническому напряжению мышц и клонико-тоническим судорогам.
Столбняк - раневая инфекция. Столбнячная палочка поступает в организм только через повреждённые покровные ткани, поэтому профилактика и лечение столбняка - непременный удел хирургов.
Классификация
Выделяют несколько видов классификации столбняка.
• По виду повреждения:
- раневой;
- постинъекционный;
- послеожоговый;
- послеоперационный.
• По распространённости:
- общий (генерализованный);
- нисходящий;
- восходящий.
• По клиническому течению:
- острый;
- молниеносный;
- хронический;
- стёртая форма заболевания.
Клиническая картина
Инкубационный период
Клиническим проявлениям предшествует инкубационный период, длящийся от 4 до 14 дней. При этом чем короче инкубационный период, тем тяжелее протекает заболевание. Во время инкубационного периода больные жалуются на головную боль, бессонницу, раздражительность, чувство напряжения, общее недомогание, чрезмерную потливость, боли в области раны, подергивание тканей в ране, боли в спине.
Судорожный синдром
Ведущим симптомом столбняка становится развитие тонических и клонических судорог скелетных мышц. Спазм и судороги начинаются либо около места ранения, либо в жевательных мышцах (тризм жевательных мышц).
Существуют так называемые ранние симптомы столбняка, демонстрирующие судорожную готовность и позволяющие поставить диагноз ещё до клинических проявлений судорожного синдрома - симптомы Лори-Эпштейна:
• при сдавлении конечности проксимальнее зоны повреждения происходят подергивания мышечных волокон в ране;
• при постукивании молоточком (пальцем) по подбородку при полуоткрытом рте жевательные мышцы сокращаются, рот резко закрывается.
При нисходящем столбняке судороги начинаются с тризма жевательных мышц, а при прогрессировании появляются судорожные сокращения скелетной мускулатуры конечностей и туловища. При восходящем столбняке порядок вовлечения мышц в судорожный синдром обратный.
При развитии судорожных сокращений мимической мускулатуры лицо пациента перекашивается - так называемая «сардоническая улыбка». Распространение судорог на мышцы шеи приводит к запрокидыванию головы. Судорожные сокращения дыхательных мышц вызывают нарушение дыхания вплоть до асфиксии.
При генерализованном столбняке вследствие тонического сокращения всей скелетной мускулатуры развивается опистотонус - туловище и нижние конечности предельно выгнуты, пациент касается постели только затылком и пятками.
Частые судороги сочетаются с обильным потоотделением, высокой температурой тела и дыхательными расстройствами.
По степени выраженности и частоте возникновения судорожных приступов различают слабую, умеренно тяжёлую и тяжёлую формы заболевания.
Тяжесть заболевания определяется не только судорогами, но и интоксикацией, локализацией раны, характером и степенью разрушения тканей в области раны, количеством и вирулентностью возбудителя, реактивностью организма.
Осложнения
Стойкое сокращение мышц может привести к их разрыву, переломам костей, разрыву полых органов (мочевого пузыря, прямой кишки и др.). В момент судорог может возникнуть асфиксия или аспирация рвотными массами.
Вовлечение в судорожный синдром дыхательной мускулатуры приводит к нарушению дыхания и возможности развития пневмонии. Сокращения мышц шеи, спины, груди и конечностей вызывают нарушения функций сердечно-сосудистой системы. Регистрируют неустойчивость пульса и АД, изменение ритма сердечных сокращений.
Летальный исход обычно обусловлен развитием лёгочных осложнений.
Лечение
Лечение столбняка должно быть как местным, так и общим.
Местное лечение
Под местным воздействием подразумевают выполнение хирургических манипуляций в ране. Необходимо широко в пределах здоровых тканей удалить некротизированные ткани, содержащие возбудитель, создать неблагоприятные условия для жизнедеятельности анаэробного микроорганизма, т.е. обеспечить доступ к тканям воздуха, кислорода.
У больных со столбняком это касается и заживших к моменту появления первых признаков заболевания мелких ран: рубцы широко иссекают в пределах здоровых тканей, так как в них могут находиться инородные тела, содержащие столбнячные палочки. Рану после иссечения рубца оставляют открытой.
Для местного лечения целесообразно применение протеолитических ферментов, ускоряющих некролиз, очищающих рану, стимулирующих процессы регенерации.
Общее лечение
Общую терапию проводят по нескольким направлениям.
Специфическая серотерапия заключается во введении противостолбнячной сыворотки, связывающей циркулирующий в крови токсин. Специфического средства против токсина, фиксированного в ЦНС, пока нет. Поэтому сыворотку следует применять как можно раньше. В первые сутки лечения внутривенно вводят 200 000 ME сыворотки. Это очень большая доза чужеродного белка, поэтому введение проводят под наркозом для снижения вероятности иммунного конфликта. Такую дозу вводят в течение 2 сут. Затем её снижают до 140 000 ME и вводят ещё 2-3 дня.
В настоящее время лучшим антитоксическим средством считают противостолбнячный человеческий иммуноглобулин, полученный от людей-доноров, ревакцинированных очищенным сорбированным столбнячным анатоксином. Вводят его однократно внутримышечно в дозе 900 ME (6 мл).
В остром периоде для стимуляции активного иммунитета вводят 1,0 мл столбнячного анатоксина.
Противосудорожная терапия. Для борьбы с судорогами применяют препараты различных групп:
• препараты фенотиазинового ряда (хлорпромазин);
• нейролептики (дроперидол);
• транквилизаторы (диазепам);
• барбитураты (гексобарбитал, тиопентал натрий);
• хлоралгидрат (вводят в виде клизм, оказывает успокаивающее, снотворное и противосудорожное действия);
• литические коктейли в различных сочетаниях (хлорпромазин и дифенгидрамин; метамизол натрий, папаверин, дифенгидрамин и дроперидол и др.), оказывающие противосудорожное, снотворное и седативное действия.
Введение всех противосудорожных средств проводят по показаниям в зависимости от выраженности и частоты судорог, эффективности тех или иных средств и под постоянным контролем за функциями жизненно важных органов и систем.
Если не удаётся ликвидировать сильные и частые судороги указанными средствами, применяют миорелаксанты с обеспечением ИВЛ. Чаще используют антидеполяризующие миорелаксанты.
Гипербарическая оксигенация весьма эффективна в лечении заболевания. Воздействует как на сам микроорганизм и его токсин, так и на устойчивость клеток нервной системы к поражению.
Вспомогательная терапия в основном направлена на поддержание функций сердечно-сосудистой и дыхательной систем. В целях предупреждения и лечения осложнений, особенно пневмонии и сепсиса, назначают антибиотики широкого спектра действия.
Для компенсации потери жидкости и нормализации водно-электролитного баланса назначают инфузионную терапию.
Уход за больными. Необходимо уменьшить возможность влияния малейших раздражителей, способных спровоцировать судороги (пациентов помещают в отдельную палату с неярким светом, отсутствием шума и др.).
Тщательное наблюдение и уход, обеспечение полноценного зондового питания и инфузионной терапии, контроль диуреза и дефекации - важнейшие компоненты лечения столбняка.
Профилактика
Профилактика столбняка может быть плановой (когда нет повреждёний кожного покрова) и экстренной (проводят непосредственно после ранения).
Плановая профилактика
Плановая профилактика заключается в активной иммунизации. Её обычно проводят в детстве. Используют адсорбированную коклюшно-дифтерийно-столбнячную вакцину. Ревакцинации рекомендуют каждые 10 лет.
Кроме того, плановой профилактике подлежат лица, по роду деятельности имеющие высокий риск получения ран, особенно загрязнённых землёй. Это военнослужащие срочной службы, работники сельского хозяйства, строители в сельской местности и пр. Активную иммунизацию осуществляют введением 1,0 мл столбнячного анатоксина дважды с интервалом 1-1,5 мес.
Экстренная профилактика
Экстренную профилактику следует проводить сразу после ранения. Показанием к ней считают любые случайные раны, травмы с нарушением целостности кожных покровов, отморожения и ожоги II-IV степени, внебольничные аборты, роды вне больничных учреждений, гангрену или некроз тканей любого типа, укусы животными, проникающие ранения брюшной полости. Экстренная профилактика включает неспецифические и специфические мероприятия.
Неспецифическая профилактика
Неспецифическая профилактика столбняка прежде всего состоит в своевременно и правильно выполненной первичной хирургической обработке раны.
Определённое значение в более поздние сроки имеют также иссечение некротических тканей и удаление инородных тел.
Специфическая профилактика
При экстренной профилактике столбняка применяют средства пассивной иммунизации.
ПСС (противостолбнячная сыворотка) - в дозе 3 000 ME. Вводят по методу Безредко в три этапа:
• 0,1 мл внутрикожно;
• при отсутствии реакции через 20-30 мин - 0,1 мл подкожно;
• при отсутствии реакции через 20-30 мин - всю дозу внутримышечно.
ПСЧИ (противостолбнячный человеческий иммуноглобулин) - в дозе 400 ME, а также средства активной иммунизации - столбнячный анатоксин (1,0 мл внутримышечно).
Противопоказаниями к применению специфических средств экстренной профилактики столбняка признаны повышенная чувствительность к соответствующему препарату, беременность, существенно отягощённый аллергологический анамнез.
Общая гнойная инфекция (сепсис)
Термин «сепсис» был введён ещё в IV веке Аристотелем, понимающим под ним отравление организма продуктами гниения собственных тканей. В настоящее время определение сепсиса изменилось.
Сепсис - тяжёлое инфекционное заболевание, вызываемое разными возбудителями и их токсинами, проявляющееся своеобразной реакцией организма с однотипной, несмотря на различие возбудителей, клинической картиной.
Отличие сепсиса от других инфекционных заболеваний в том, что его не относят к заразным в эпидемиологическом отношении заболеваниям, он не имеет определённых сроков инкубационного периода.
Актуальность проблемы сепсиса определяется тремя факторами: частотой развития, высокой летальностью и значительной стоимостью лечения. В среднем сепсис развивается у одного-пяти больных на 1000 госпитализированных в зависимости от профиля лечебного учреждения. В гнойных отделениях частота сепсиса колеблется от 3 до 19%. В США ежегодно заболевает сепсисом 500000 человек с летальностью 35%. По данным различных авторов, летальность при сепсисе колеблется от 2 до 60%, а при септическом шоке доходит до 90%.
Терминология
В настоящее время используют стандартизированную терминологию, принятую на Всемирной «конференции согласия» сепсологов в 1991 г. Выделяют следующие термины.
Бактериемия - наличие жизнеспособных бактерий в крови пациента.
Синдром системной воспалительной реакции (ССВР) - системная воспалительная реакция на различные тяжёлые повреждения тканей, проявляющаяся двумя и более из указанных признаков:
• температура тела >38 ?С или <36 ?С;
• тахикардия >90 в минуту;
• частота дыхания >20 в минуту или раС02 32 мм рт.ст.;
• количество лейкоцитов >12х109/л, <4,0х109/л или наличие >10% палочкоядерных нейтрофилов.
Сепсис - системная реакция на инфекцию (ССВР при наличии соответствующего очага инфекции).
Тяжёлый сепсис (сепсис-синдром) - сепсис, сочетающийся с органной дисфункцией, гипоперфузией или артериальной гипотензией. Нарушения перфузии могут включать молочнокислый ацидоз, олигурию, острое нарушение сознания и др. Артериальная гипотензия подразумевает систолическое АД ниже 90 мм рт.ст или его снижение более чем на 40 мм рт.ст от обычного уровня при отсутствии других причин гипотензии.
Септический шок - сепсис с артериальной гипотензией, сохраняющейся, несмотря на адекватную коррекцию гиповолемии, и нарушением перфузии.
Синдром полиорганной дисфункции - нарушение функций органов у больного в тяжёлом состоянии (самостоятельное, без лечения, поддержание гомеостаза невозможно).
Теории сепсиса
К настоящему времени существует пять основных теорий сепсиса.
Бактериологическая теория (И.В. Давыдовский, 1928).
Все изменения, происходящие в организме, - результат развития гнойного очага. Они развиваются вследствие роста, размножения и попадания микроорганизмов в кровеносное русло.
Токсическая теория (В.С. Савельев и соавт., 1976).
Сторонники этой теории придают большое значение не самому микроорганизму, а продуктам его жизнедеятельности - экзо- и эндотоксинам.
Аллергическая теория (И.К. Ру, 1983).
Основана на данных, согласно которым бактериальные токсины вызывают в организме больного реакции аллергического характера. Нейротрофическая теория.
Построена на основании работ И.П. Павлова о роли нервной системы в регуляции нейро-сосудистных реакций организма. Цитокиновая теория (W. Ertel, 1991).
Занимает в настоящее время главенствующее положение. Была выдвинута на основании экспериментальных и клинических исследований. Инфекционный агент вызывает поступление в кровь значительного количества цитокинов. Процесс этот может быть прямым либо опосредованным. Цитокины - белки с низкой молекулярной массой, их синтезируют различные клетки (лимфоциты, лейкоциты, макрофаги, моноциты, эндотелий), эти белки регулируют специфический и неспецифический иммунитет.
Основная роль в активации цитокинового каскада принадлежит фактору некроза опухолей (TNF), выделяемому макрофагами. TNF индуцирует вторичную секрецию интерлейкинов (1, 6, 8), что ведёт к поражению эндотелия и формированию ССВР. После бурного начала септического процесса развивается иммунодепрессия, резко снижается синтез интерлейкина-2, служащего фактором роста Т-лимфоцитов, эффективным лимфокином для дифференциации В-клеток и синтеза иммуноглобулинов, ключевым фактором в развитии иммунного ответа.
Классификация сепсиса
• В зависимости от принципа, положенного в основу классификации сепсиса, существует несколько её вариантов: Различают первичный и вторичный сепсис.
- Первичный сепсис (криптогенный). Встречают относительно редко. Происхождение его не ясно. Предполагают связь с аутоинфекцией (хроническим тонзиллитом, кариозными зубами, дремлющей инфекцией).
- Вторичный сепсис развивается на фоне существования в организме гнойного очага: гнойной раны, острого гнойного хирургического заболевания, а также после оперативного вмешательства.
• По локализации первичного очага: хирургический, гинекологический, урологический, отогенный, одонтогенный сепсис и т.д.
• По виду возбудителя: стафилококковый, стрептококковый, колибациллярный, синегнойный, анаэробный. Иногда выделяют грамположительный и грамотрицательный сепсис.
• По источнику: раневой, послеоперационный, воспалительный сепсис (флегмона, абсцесс, остеомиелит и т.д.), сепсис при внутренних болезнях (ангина, пневмония и др.).
• По времени развития: ранний (до 14 дней с момента повреждения) и поздний (более 14 дней с момента повреждения).
• По типу клинического течения: молниеносный, острый, подострый, хронический сепсис.
- Молниеносный сепсис характеризуется быстрой генерализацией воспалительного процесса и уже в течение нескольких часов (12-24 ч) после повреждёния можно выявить его клинические симптомы. Длительность течения составляет 5-7 дней, чаще наступает летальный исход, даже при своевременном лечении.
- Острый сепсис характеризуется более благоприятным течением, клинические симптомы проявляются в течение нескольких дней. Длительность течения составляет 2-4 нед.
- Подострый сепсис продолжается 6-12 нед, исход благоприятный.
- Если не удаётся ликвидировать острый сепсис, процесс переходит в хроническую стадию. Хронический сепсис течёт годами с периодическими обострениями и ремиссиями.
• По характеру реакций организма: гиперергический, нормергический, гипергический сепсис.
• По клинико-анатомическим признакам: септицемия (без метастазов) и септикопиемия (со вторичными метастатическими гнойными очагами).
• По фазам клинического течения: фазы напряжения, катаболическая, анаболическая, реабилитационная.
- В фазе напряжения происходят включение функциональных систем и мобилизация защитных сил организма на внедрение микроорганизмов. Наступает стимуляция гипофизарной, а через неё - адреналовой системы.
- Катаболическая фаза характеризуется дальнейшими нарушениями обменных процессов, усиливается катаболизм белков, углеводов, жиров, происходят нарушения водно-электролитного обмена и кислотно-основного состояния.
- Анаболическая фаза начинается с 10-12-го дня, в этот период восстанавливаются, хотя и не полностью, все обменные процессы. Прежде всего идёт восстановление структурных протеинов.
- Реабилитационная фаза может быть длительной. В ней происходит полное восстановление всех обменных процессов.
Этиология
Возбудителями сепсиса могут быть почти все существующие патогенные и условно патогенные бактерии. Наиболее распространены стафилококки, стрептококки, синегнойная палочка, протей, анаэробная флора и бактероиды.
Следует обратить особое внимание на то, что в последние годы увеличилось количество mixt-инфекций, возникающих за счёт микробных ассоциаций. При этом микробный синергизм может быть направлен против лечебных препаратов и снижать резистентность организма.
Примерно в половине случаев, в которых удаётся микробиологическим методом диагностировать возбудителя при сепсисе, вызывающие его микроорганизмы оказываются грамотрицательными бактериями (Ps.Aeruginosa, E. coli, Klebsiella spp., Enterobacter, Proteus vulgaris).
При грамотрицательном возбудителе сепсиса центральную роль играет бактериальный эндотоксин (липополисахарид).
Если первичная микрофлора, вызвавшая сепсис, может быть разной, то начиная со 2-3-й недели происходит смена доминирующей микрофлоры. При этом ведущая роль переходит к эндогенной флоре, где абсолютно преобладают облигатные и необлигатные неклостридиальные анаэробы. Собственная эндогенная микрофлора обладает большей тропностью и резистентностью к тканям организма, поэтому постепенно вытесняет экзогенную в конкурентной борьбе за существование.
Помимо бактерий и их токсинов, на течение общей гнойной инфекции большое влияние оказывают продукты распада тканей первичного и вторичного очагов. Они, всасываясь в кровь, приводят к тяжёлой интоксикации и дегенеративным изменениям жизненно важных органов.
Патогенез
Патогенез общей гнойной инфекции определяется тремя следующими факторами:
• микробиологическим - видом, вирулентностью, количеством и длительностью воздействия попавших в организм бактерий;
• очагом внедрения инфекции - областью, характером и объёмом разрушения тканей, состоянием кровообращения в очаге;
• реактивностью организма - состоянием его иммунобиологических сил, наличием сопутствующих заболеваний основных органов и систем.
В зависимости от различных сочетаний перечисленных факторов сепсис может развиться через несколько часов после повреждения или через несколько недель и даже месяцев после появления воспалительного очага.
Развитие и течение сепсиса - результат сложного динамического процесса взаимодействия между внедрившейся микрофлорой и организмом больного.
Важную роль в генерализации гнойной инфекции играет порой бесконтрольное применение таких медикаментозных средств, как антибиотики и иммунодепрессанты.
Нарушение иммунитета - одна из основных причин возникновения сепсиса. Эти нарушения могут быть как врождёнными, так и приобретёнными, а также первичными, связанными с дефектами в самих иммуннокомпетентных клетках или цитокиновой сети, и вторичными, когда из-за других заболеваний снижается реактивность организма.
Важную роль в развитии гнойной инфекции играют такие факторы, как нарушение питания (истощение или избыточная масса тела) и гиповитаминоз.
Нельзя не брать в расчёт изменчивость и быструю адаптацию микрофлоры к антибиотикам и другим препаратам, их мутацию с образованием устойчивых штаммов, обмен информацией между микроорганизмами.
В частности, резкий рост послеоперационных гнойных осложнений может быть связан с появлением госпитальных штаммов микроорганизмов, чувствительных только к резервным антибиотикам.
Центральное место в патогенезе сепсиса в настоящее время в соответствии с положениями, принятыми на «конференции согласия» (1991), занимает вызванная бактериальным токсином чрезмерная воспалительная реакция организма.
В общем случае инфекция может проявляться, когда микроорганизмы проникают через барьеры (кожу, слизистые оболочки). Токсические бактериальные продукты активируют системные защитные механизмы. К ним относят систему комплемента и каскад системы свёртывания, а также клеточные компоненты: нейтрофилы, моноциты, макрофаги и клетки эндотелия.
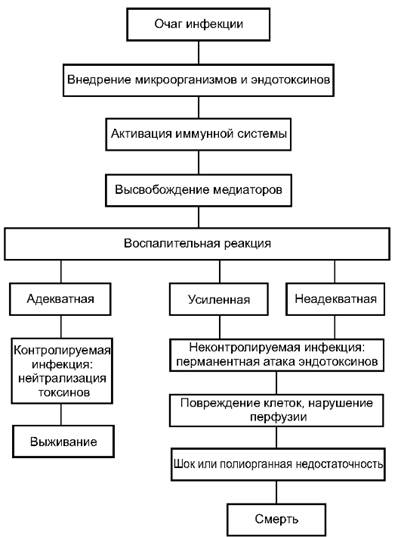
Рис. 12-14. Патогенез сепсиса
Активированные клетки синтезируют медиаторы, запускающие и поддерживающие воспалительную реакцию. К этим медиаторам относят цитокины (TNF, интерлейкины 1, 6, 8 и 10), фактор свёртывания Хагемана, кинины, липидные метаболиты (лейкотриены, простагландины), протеазы (эластазу, коллагеназу) и др.
Гипервоспалительная реакция организма может вместе с микробными токсинами привести к повреждению клеток, нарушению перфузии и в итоге к полиорганной недостаточности, шоку и смерти.
Патогенез сепсиса можно схематично представить следующим образом (рис. 12-14).
Дата: 2019-03-05, просмотров: 674.