Клиническая картина складывается из местных и общих проявлений.
Местные симптомы
Классические признаки воспаления
Местная реакция при острой гнойной инфекции проявляется симптомами, характеризующими развитие воспалительной реакции:
• ruber (краснота),
• color (местный жар),
• tumor (припухлость),
• dolor (боль),
• functio laesa (нарушение функции).
Красноту легко определить при осмотре. Она отражает расширение сосудов (артериол, венул и капилляров), при этом происходит замедление кровотока вплоть до его почти полной остановки - стаза. Такие изменения связаны с воздействием на сосуды гистамина и нарушениями обменных процессов в клетках в зоне воспаления. Иначе описанные изменения называют термином «гиперемия».
Местный жар связан с усилением катаболических реакций с высвобождением энергии. Определяют местное повышение температуры (обычно тыльной стороной ладони, сравнивая полученные при этом ощущения с ощущениями при пальпации вне болезненного очага).
Припухлость тканей обусловлена изменением проницаемости стенки сосудов для плазмы и форменных элементов крови, а также повышенным гидростатическим давлением в капиллярах. Повышенная проницаемость сосудистой стенки касается в основном капилляров и мелких вен. Пропотевающая из сосудов жидкая часть плазмы вместе с мигрирующими лейкоцитами, а нередко и вышедшими путём диапедеза эритроцитами, образуют воспалительный экссудат. Основную массу его составляют нейтрофильные лейкоциты. Обычно припухлость определяют визуально. В сомнительных случаях выполняют измерения (например, окружности конечности).
Боль. Наличие боли и болезненности при пальпации в зоне очага - характерный признак гнойных заболеваний. Следует помнить, что пальпацию нужно проводить достаточно осторожно, чтобы не вызывать у пациента негативных ощущений.
Нарушение функции связано как с развитием болевого синдрома, так и с отёком. В наибольшей степени оно выражено при локализации воспалительного процесса на конечности, особенно в области сустава.
Симптомы наличия скопления гноя
Для определения скопления гноя используют клинические симптомы (симптомы флюктуации и размягчения), данные дополнительных методов исследования и диагностическую пункцию.
Клинические симптомы
Важный метод выявления зоны скопления гноя - симптом флюктуации. Для его определения с одной стороны зоны патологического процесса врач кладёт свою ладонь (при очагах малого размера - один или несколько пальцев), а с противоположной стороны другой ладонью (или 1-3 пальцами) выполняет толчкообразные движения (рис.12-1).
Если между ладонями врача в патологическом очаге есть жидкость (в данном случае гной), эти толчки будут передаваться с одной кисти на другую. Обычно положительный симптом флюктуации, свидетельствующий о скоплении в тканях гнойного экссудата, становится определяющим в постановке показаний к операции (вскрытие и дренирование гнойника).
Сходное значение имеет и симптом размягчения: если на фоне воспалительного инфильтрата в центре появляется зона размягчения (ощущение пустоты, провала при пальпации), это также свидетельствует о гнойном расплавлении тканей и скоплении гноя.
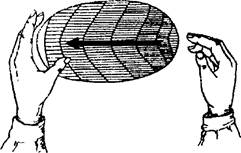
Рис. 12-1. Схема определения симптома флюктуации
Дополнительные методы исследования
Среди специальных методов исследования, способных определить скопление гнойного экссудата, на первом месте стоит УЗИ. Метод с большой точностью позволяет определить скопление жидкости, размеры и расположение полости.
В некоторых случаях диагностике помогает рентгеновское исследование. Существуют характерные рентгенологические признаки скопления гноя под диафрагмой, абсцесса лёгкого и т.д.
Для выявления гнойника и определения всех его параметров в сложных случаях можно выполнить КТ или МРТ.
Диагностическая пункция
Процедура производится при неясном диагнозе. Обычно тонкой иглой выполняют анестезию кожи, а затем толстой иглой (диаметром не менее 1,5 мм) выполняют пункцию, постоянно создавая разряжение в шприце.
Появление в нем хотя бы минимального количества гноя свидетельствует о наличии его скопления в соответствующей зоне, гнойного расплавления тканей, что чаще всего требует хирургического лечения. При глубоких гнойных процессах высокоэффективна пункция под контролем УЗИ.
Местные осложнения гнойных процессов
При развитии гнойных заболеваний возможны местные осложнения: некрозы, воспаление лимфатических сосудов (лимфангит) и узлов (лимфаденит), тромбофлебит.
Формирование некрозов связано с деятельностью микроорганизмов, а также с нарушением микроциркуляции вследствие воспалительного процесса. При этом в зоне воспаления появляются участки чёрного цвета.
Лимфангит - вторичное воспаление лимфатических сосудов, усугубляющее течение различных воспалительных заболеваний. При стволовом лимфангите отмечают гиперемию в виде отдельных полос, идущих от очага воспаления к зоне регионарных лимфатических узлов - подмышечной ямке или паховой складке. Наряду с гиперемией появляется отёчность кожи. При пальпации выявляют болезненные уплотнения в виде тяжей по ходу лимфатических сосудов. Довольно рано присоединяется лимфаденит. При воспалении внутрикожных лимфатических сосудов наблюдают гиперемию в виде сетчатого рисунка (множественные ярко-красные пересекающиеся полосы). Явления лимфангита могут быть скоротечными и продолжаться лишь в течение нескольких часов. В то же время возможно и развитие некротического лимфангита с формированием очагов некроза по ходу сосудов.
Лимфаденит - воспаление лимфатических узлов, возникающее как осложнение различных гнойно-воспалительных заболеваний и специфических инфекций (туберкулёза, чумы, актиномикоза). Таким образом, лимфаденит, как правило, бывает вторичным процессом.
Лимфаденит начинается с болезненности и увеличения лимфатических узлов. Иногда при стихании основного процесса лимфаденит доминирует в клинической картине заболевания. При прогрессировании заболевания и развитии периаденита указанные клинические признаки выражены в большей степени, четко пальпируемые ранее лимфатические узлы, сливаясь между собой и с окружающими тканями, становятся неподвижными. Процесс может перейти в деструктивную форму вплоть до развития аденофлегмоны.
Тромбофлебит - воспаление вен, обеспечивающих отток крови от зоны воспаления. Такой тромбофлебит называют восходящим. Обычно речь идёт о поверхностных венах. Клинически определяют болезненный инфильтрат по ходу вены, имеющий форму жгута, валика. Над ним кожа гиперемирована, может быть несколько приподнята. При тромбофлебите необходимо специальное лечение. Обычно воспалительные изменения нивелируются быстро, но достаточно долго после этого пальпируется тромбированная вена. В некоторых случаях тромбофлебит осложняется развитием абсцессов (абсцедирующий тромбофлебит), что приводит к необходимости хирургического лечения.
Следует отметить, что лимфангит, лимфаденит и тромбофлебит - первые признаки генерализации инфекционного процесса.
Общая (системная) реакция
Основные клинические проявления общей реакции при гнойных заболеваниях - симптомы интоксикации, выраженные в различной степени.
Клинические проявления интоксикации
Обычно больные жалуются на чувство жара, озноб, головную боль, общее недомогание, разбитость, слабость, плохой аппетит, иногда задержку стула.
У них отмечают повышение температуры тела (иногда до 40 С и выше), тахикардию, одышку. Больные часто покрыты потом, заторможены, сонливы.
Характерно изменение температуры тела в течение суток более чем на 1,5-2,0 градуса - температура утром нормальная или субфебрильная, а вечером достигает высоких цифр (до 39-40 °С).
Иногда у больных увеличиваются селезёнка и печень, появляется желтушная окраска склер. При сильно выраженной общей реакции организма на хирургическую инфекцию все перечисленные изменения проявляются в резкой форме. Если реакция средняя или слабая, изменения бывают умеренными или даже малозаметными, однако всякий местный процесс сопровождается общей реакцией, названной И.В. Давыдовским «гнойно-резорбтивной лихорадкой».
Описанная клиническая картина весьма сходна с сепсисом и некоторыми инфекционными заболеваниями (тифом, бруцеллёзом, паратифом и пр.). Поэтому такие больные нуждаются в тщательном клиническом обследовании. Основное отличие общей реакции организма на местный гнойный процесс от сепсиса заключается в том, что все симптомы её резко ослабевают или исчезают при вскрытии гнойного очага и создании адекватного оттока гнойного экссудата. При сепсисе этого не происходит.
Изменения лабораторных данных
Определение степени выраженности общей реакции организма на возникновение очага гнойной инфекции имеет большое значение для правильной оценки состояния больного, прогнозирования осложнений и выбора оптимальных способов лечения.
Изменения в клиническом анализе крови
Для всех гнойных хирургических заболеваний характерны лейкоцитоз, сдвиг лейкоцитарной формулы влево, повышение скорости оседания эритроцитов (СОЭ).
Под сдвигом лейкоцитарной формулы влево понимают нейтрофилёз (увеличение процентного содержания нейтрофилов), а также превышение нормального уровня палочкоядерных лейкоцитов (более 5- 7%) и появление в периферической крови незрелых (молодых) форм лейкоцитов (юные, миелоциты). При этом обычно отмечают относительное снижение количества лимфоцитов и моноцитов.
Абсолютное снижение содержания лимфоцитов и моноцитов - неблагоприятный признак, свидетельствующий об истощении защитных механизмов.
Повышение СОЭ обычно происходит через 1-2 суток от начала заболевания, а восстанавливается она через 7-10 дней после купирования острых воспалительных явлений. Нормализация СОЭ обычно свидетельствует о полной ликвидации активности воспалительного процесса. При длительных тяжёлых гнойных процессах развивается анемия.
Изменения в биохимическом анализе крови
Возможно повышение азотистых показателей (содержание креатинина, мочевины), свидетельствующее о преобладании катаболических процессов и недостаточности функций почек.
В сложных и тяжёлых случаях определяют в крови содержание белков острой фазы (С-реактивного белка, церулоплазмина, гаптоглобина и др.).
При длительных процессах отмечают изменения в составе белковых фракций (относительное увеличение количества глобулинов, в основном за счёт γ-глобулинов).
Важно также следить за концентрацией глюкозы крови, так как гнойные заболевания часто развиваются на фоне сахарного диабета.
Посев крови на микрофлору
Посев крови на микрофлору обычно выполняют на высоте лихорадки, он помогает диагностировать сепсис (бактериемию).
Изменения в анализах мочи
Изменения в анализах мочи развиваются лишь при крайне выраженной интоксикации, они получили название «токсическая почка». Отмечают протеинурию, цилиндрурию, иногда лейкоцитурию.
Интегральные показатели уровня интоксикации
Для определения уровня интоксикации и динамического наблюдения за больными с острой гнойной хирургической инфекцией используют интегральные показатели: лейкоцитарный индекс интоксикации (ЛИИ), гематологический показатель интоксикации (ГПИ), уровень средних молекул.
ЛИИ вычисляют по следующей формуле (по Я.Я. Кальф-Калифу, 1941).
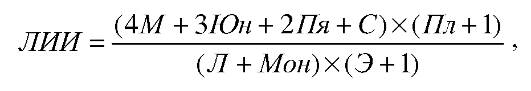
где:
М - миелоциты;
Юн - юные;
Пя - палочкоядерные нейтрофилы;
С - сегментоядерные;
Пл - плазматические клетки;
Л - лимфоциты;
Мон - моноциты;
Э - эозинфилы.
В норме ЛИИ = 1,0 0,6 усл. ед.
ГПИ дополнительно учитывает данные об общем лейкоцитозе и СОЭ.
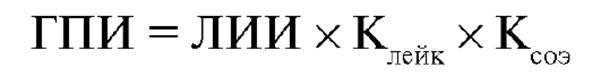
КЛЭЙК и КСОЭ - поправочные табличные коэффициенты, отражающие степень отклонения соответствующего показателя от нормального уровня (табл. 12-1).
В норме ГПИ = 0,69 ± 0,09 усл. ед.
Таблица 12-1. Значения Клейк и КСОЭ (по В.С. Васильеву и В.И. Комару, 1983)
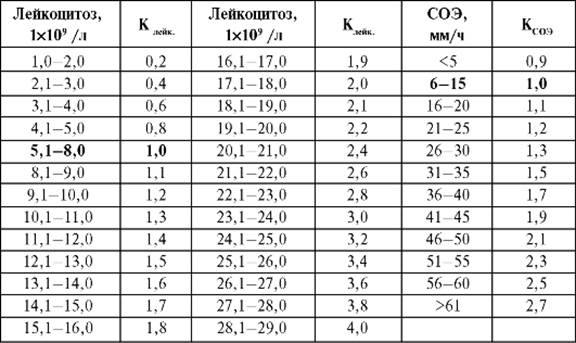
Средние молекулы - олигопептиды с молекулярной массой 500-5000. Да, их считают универсальным маркёром интоксикации. Прежде всего, их составляют продукты нарушенного метаболизма, гормоны и их фрагменты и биологически активные вещества. В норме уровень средних молекул равен 0,15-0,24 усл. ед. Повышение содержания средних молекул в сыворотке крови и моче коррелирует с тяжестью интоксикации.
Принципы лечения
Лечение острых гнойных хирургических заболеваний представляет трудную и сложную проблему, оно складывается из мероприятий местного и общего характера.
Местное лечение
Основные принципы местного лечения:
• вскрытие гнойного очага;
• адекватное дренирование гнойника;
• местное антисептическое воздействие;
• иммобилизация.
Вскрытие гнойного очага
Вскрытие гнойника обычно выполняют под проводниковой или общей анестезией (инфильтрационную анестезию используют редко, так как она может способствовать распространению инфекции, а эффективность действия анестетиков в воспалительном очаге снижается).
Разрез проводят на всю длину воспалительного инфильтрата. После вскрытия очага определяют наличие некротизированных тканей, затем их иссекают, определяют наличие гнойных затёков и дополнительно вскрывают, разделяют перемычки, определяют состояние соседних органов, ставших причиной или вовлечённых вторично в гнойный процесс.
Осмотр гнойной полости не всегда возможен. В таких случаях обязательно выполняют обследование полости пальцем.
Важный элемент интраоперационной санации - использование химических антисептиков для обильного промывания гнойной полости, образовавшейся при воспалении. Полость промывают раствором одного из антисептиков (пероксидом водорода, нитрофуралом, хлоргексидином), механическую некрэктомию можно дополнить одним из средств физической некрэктомии (ультразвуковой кавитацией, воздействием лучами углекислого лазера).
Следует отметить, что чем радикальнее выполнено хирургическое вмешательство, тем быстрее и с меньшим количеством осложнений пойдёт процесс выздоровления. Всегда проводят посев полученного гнойного экссудата на питательные среды для его бактериологического исследования и определения чувствительности к антибиотикам, что позволяет выбрать оптимальный вариант антибактериальной терапии.
Любую операцию по вскрытию гнойника завершают его дренированием.
Адекватное дренирование гнойника
Для адекватного дренирования применяют все возможные способы, относимые к физической антисептике: пассивное дренирование (используют перчаточную резину, дренажные трубки и др.), активную аспирацию и проточное дренирование (см. главу 2).
Важно правильно выполнять разрезы при вскрытии гнойника. Определённые направление и глубина разреза способствуют тому, чтобы края раны зияли и гнойный экссудат свободно оттекал наружу.
Местное антисептическое воздействие
Местное антисептическое воздействие заключается в ежедневной обработке ран 3% раствором перекиси водорода, применении влажновысыхающих повязок с 2-3% раствором борной кислоты, водным раствором хлоргексидина, нитрофурала и др.
Кроме того, необходимо использовать протеолитические ферменты, а также вспомогательные физиотерапевтические процедуры (УФО, УВЧ, электрофорез с антибиотиками и др.).
Иммобилизация
На время острого периода течения гнойного процесса необходимо создать покой поражённому сегменту, особенно в случае локализации гнойного процесса на конечностях, в зоне суставов. Для иммобилизации обычно применяют гипсовые лонгеты.
Общее лечение
Общие методы лечения можно разделить на четыре вида:
• антибактериальная терапия;
• дезинтоксикационная терапия;
• иммунокоррекция;
• симптоматическое лечение.
Антибактериальная терапия
Антибактериальную терапию проводят с учётом вида и чувствительности микрофлоры. Кроме антибиотиков, для общей антибактериальной терапии применяют бактериофаги, антисептики (гидроксиметилхиноксилиндиоксид, сульфаниламидные препараты, нитрофураны) и др.
Основные принципы антибактериальной терапии изложены в главе 2 в разделе «Биологическая антисептика». Дополнительно следует отметить, что возможно использование различных способов введения антибиотиков.
Существует поверхностная антибиотикотерапия (промывание ран), внутриполостная (введение в грудную, брюшную полости, полость сустава) и глубокая антибиотикотерапия (внутримышечное, внутривенное, внутриартериальное и эндолимфатическое введение), а также пероральный способ. Поверхностную и внутриполостную терапию относят к средствам местного лечения.
Пероральный способ введения
Показания к применению: лечение заболеваний внутренних органов и нетяжёлых инфекционных хирургических процессов.
Достоинства: простота, неинвазивность, возможно самостоятельное применение.
Недостатки: неприменим при заболеваниях брюшной полости, не- чётко дозирует концентрацию.
Особенности: частота приёма от 4 до 1 раза в сут. В последнее время наметилась тенденция введения препаратов 1 раз в сут (цефтриаксон).
Внутримышечный способ введения
Внутримышечный - основной (стандартный) способ введения антибиотиков при лечении гнойных заболеваний.
Достоинство метода - сочетание простоты применения с возможностью создания постоянной бактерицидной концентрации препарата в крови при соблюдении определённой для каждого антибиотика кратности введения.
Внутривенный способ введения
В связи с особенностями фармакодинамики (быстрое создание высокой концентрации в плазме и быстрое её снижение) не служит основным методом лечения острой хирургической инфекции. Используют при сепсисе как способ введения одного из двух антибиотиков. Применяют также как единственно возможный способ для введения антисептических средств (гидроксиметилхиноксилиндиоксида, метронидазола), а также некоторых видов антибиотиков (имипинем + целастатин натрия, пефлоксацина).
Внутривенное введение антибиотиков под жгутом
Показания: воспалительные процессы на пальце, кисти. Методика заключается в наложении на плечо манжетки от аппарата для измерения АД (создают давление 60-80 мм рт.ст), после чего пунктируют вену в области локтевого сгиба и вводят антибиотик. Манжетку снимают через 30 мин. При выборе антибиотика следует помнить об их тромбогенном эффекте. В связи с этим применение пенициллинов и цефалоспоринов нецелесообразно.
Внутриартериалъный способ введения
Особенность метода - создание высокой регионарной концентрации препарата в очаге воспаления. В то же время невозможно создать стойкую бактерицидную концентрацию в плазме крови. Метод показан при тяжёлых воспалительных заболеваниях органов грудной и брюшной полостей (внутриаортальная терапия) и воспалительных процессах на нижних конечностях (введение антибиотиков в бедренную артерию).
Эндолимфатическая терапия
В настоящее время существует два вида эндолимфатической терапии (ЭЛТ):
• прямая - введение препаратов непосредственно в лимфатическое сосуды или узлы (собственно ЭЛТ);
• непрямая - лимфотропная терапия - введение препаратов в различные клетчаточные пространства с последующей преимущественной резорбцией в лимфатическую систему.
ЭЛТ может быть антеградной и ретроградной. Ретроградная ЭЛТ через грудной лимфатический проток не нашла практического применения в связи со сложностью и травматичностью. Антеградную ЭЛТ обычно выполняют через лимфатические сосуды конечностей или лимфатические узлы.
Идею использования лимфатических сосудов для введения антибиотиков ещё в 50-е годы высказал Б.В. Огнев. Широкое внедрение ЭЛТ в клиническую практику при лечении различных, прежде всего хирургических заболеваний, стало возможным после выхода в свет в 1984 г. фундаментального труда Р.Т. Панченкова, Ю.Е. Выренкова, И.В. Яремы и Э.Г. Щербаковой «Эндолимфатическая антибиотикотерапия». В нём проведено детальное теоретическое, экспериментальное, микробиологическое и фармакологическое обоснование метода.
Преимущества ЭЛТ в лечении хирургической инфекции обусловлено следующими возможностями:
• Поддержание в течение длительного периода времени терапевтической концентрации антибиотика в лимфатических сосудах и централь-
ной лимфе, что крайне важно, учитывая токсичность лимфы при воспалительном процессе и нахождение в ней микроорганизмов.
• Обеспечение ещё более длительной бактерицидной концентрации антибиотика в регионарных лимфатических узлах, что способствует усилению их фильтрационно-барьерной функции и уменьшению вызванных воспалением морфофункциональных нарушений. Необходимо отметить, что ни при одном другом способе введения антибиотиков (внутримышечном, внутривенном, внутриартериальном и др.) не удаётся добиться столь значительной их концентрации в лимфатическом русле. В то же время именно насыщение антибиотиками лимфатической системы создаёт мощное препятствие для генерализации процесса.
• Возможность разового эндолимфатического введения антибиотика сохраняет его бактерицидную концентрацию в плазме в течение суток, что объясняется медленным, дозированным поступлением антибиотика в кровь из лимфатических узлов и грудного лимфатического протока.
• Достижение максимальной концентрации антибиотика в очаге воспаления. Отмечено повышение содержания цефалоспоринов и канамицина в очаге в 3-5 раз по сравнению с внутримышечным способом введения. Высокая концентрация антибиотика в зоне воспаления сохраняется в течение 24-48 ч после инфузии. Подобные данные объясняют тем, что лимфоциты больше, чем другие клетки крови, могут депонировать антибиотики. Именно в лимфатических узлах при длительном контакте с препаратами и происходит подобная «активация» клеток. «Активные» лимфоциты затем проникают в очаг воспаления, как бы принося на себе антибиотики. Определённое значение здесь имеют также вызванные воспалением изменения лимфообращения и микроциркуляции.
• Минимизация общей дозы антибиотика, что существенно не только с экономических позиций, но и с учётом токсичности и аллергогенности антибиотикотерапии.
• Иммуномодулирующее действие ЭЛТ. При эндолимфатическом введении антибиотиков отсутствует обычный для них иммунодепрессивный эффект. Иммуностимулирующее действие ЭЛТ объясняется повышением функциональной активности лимфоцитов, увеличением синтеза иммуноглобулинов и нормализацией иммунной функции лимфатических узлов вследствие санации лимфатического русла.
Методика ЭЛТ. Наиболее часто применяют внутрисосудистую ЭЛТ. Для этого необходимо выполнить катетеризацию лимфатического сосуда. Обычно катетеризируют лимфатические сосуды нижних конечностей (на тыле стопы и по медиальной или латеральной поверхности голени).
Для проведения процедуры используют обычные хирургические инструменты (скальпель, пинцет, ножницы), микрохирургические ножницы и пинцеты. Выполнение манипуляции облегчается использованием 3-10- кратного увеличения (бинокулярная лупа, операционный микроскоп).
Непосредственно перед катетеризацией в асептических условиях внутрикожно в первый и второй межпальцевые промежутки (или внутрикожно на 5-6 см дистальнее будущего разреза) вводят по 0,3-0,5 мл 0,4% раствора индигокармина. Этот краситель из тканей преимущественно поступает в лимфатические сосуды, окрашивает их в синий цвет и таким образом делает видимыми даже без увеличительной оптики.
Под местной инфильтрационной анестезией (10 мл 0,5% раствора прокаина) выполняют поперечный разрез в средней трети стопы (или в другом выбранном месте) примерно 2,0-3,0 см длиной. После выделения окрашенного индигокармином лимфатического сосуда микрохирургическими ножницами надсекают его переднюю стенку, вводят в образовавшееся отверстие катетер, продвигая его на 2,0-4,0 см и фиксируют лигатурами (аналогично методике венесекции).
Эндолимфатические инфузии осуществляют с помощью автоматического инъектора со скоростью 10 мл/ч.
Возможна также катетеризация или пункционное введение антибиотика в лимфатические узлы (в основном используют паховые лимфатические узлы).
Для создания максимальной регионарной концентрации антибиотика при ЭЛТ применяют временный фармакологический блок лимфооттока. Так как антибиотики блокируют сократительную активность лимфатических сосудов, применяют высокие их концентрации, а в качестве растворителя используют 0,5% раствор прокаина, также тормозящий сокращения лимфангионов - межклапанных сегментов лимфатических сосудов.
ЭЛТ - метод резерва в лечении гнойной хирургической инфекции. Показания к ней включают тяжёлые воспалительные заболевания органов брюшной полости, воспалительные заболевания забрюшинного пространства, нижних конечностей, сепсис, а также неэффективность предшествующей терапии.
Лимфотропная терапия
Лимфотропная терапия широко применяется в гнойной хирургии и имеет определённые преимущества по сравнению с традиционными способами введения препаратов. Безусловное достоинство метода - его техническая простота.
К основным вариантам метода относят однократное введение антибиотика в зону максимального расположения лимфатических капилляров (например, межпальцевой промежуток стопы или кисти), дозированное медленное введение (в том числе автоматическим инъектором со скоростью введения 10 мл/ч), предварительное введение ферментов (гиалуронидазы, террилитина, химотрипсина).
При лимфотропной терапии антибиотик вводят 1 раз в сут в разовой (или двойной разовой) дозе. Обычно достаточно 3-4 инфузий. Метод можно применять практически при всех местных гнойных процессах.
Дезинтоксикационная терапия
Комплекс методов, направленных на снижение интоксикации организма, получил название дезинтоксикационной терапии.
Дезинтоксикационную терапию можно проводить различными способами, что зависит от характера и тяжести интоксикации. Наиболее простые способы - обильное питьё, инфузионная терапия, форсированный диурез.
Значительно более сложными технически, более серьёзными для пациента, но в то же время более эффективными считают методы экстракорпоральной детоксикации, применяемые в самых тяжёлых и сложных случаях.
Обильное питьё
Обильное питьё способствует увеличению диуреза и соответственно возрастанию количества токсинов, удаляемых из организма с мочой.
Инфузионная терапия
Переливание кристаллоидных кровезаменителей (физиологического раствора, раствора Рингера, 5% раствора глюкозы и др.) вызывает эффект гемодилюции и также увеличивает диурез. Дополнительное использование кровезаменителей дезинтоксикационного действия, адсорбирующих на себе токсины и способствующих их выделению с мочой (гемодеза и пр.), существенно повышает эффективность метода. Возможно введение альбумина и плазмы, также обладающих мощным детоксикационным эффектом.
Форсированный диурез
Форсированный диурез представляет собой управляемую гемодилюцию. В течение 2-3 ч быстро вводят до 4-5 л кристаллоидных растворов под контролем гематокрита и концентрации гемоглобина. Скорость переливания 80-100 капель в минуту. Дополнительно диурез инициируют 40-200 мг фуросемида или 10% маннитолом (1 г/кг). Необходим тщательный контроль водно-электролитного баланса. Минимально эффективным считают диурез 100 мл/ч, возможно его увеличение до 600-800 мл/ч.
Методы экстракорпоральной детоксикации
При лечении гнойных заболеваний используют сорбционные, экстракционные методы, дренирование грудного лимфатического протока, электрохимическое окисление крови и методы квантовой терапии.
Сорбционные методы способствуют удалению гидрофильных и гидрофобных веществ средней и высокой молекулярной массы, связанных с альбумином.
Основные виды: гемосорбция, плазмосорбция, лимфосорбция.
Принцип: соответствующую жидкость пропускают через колонки с различными сорбентами (активированным углем, ионообменными смолами и специфическими сорбентами: иммунными, ферментными и пр.).
Один из методов биологической сорбции и иммунокоррекции - перфузия через ксеноселезёнку. Используют селезёнку свиньи, забранную с соблюдением мер асептики. Селезёнку промывают физиологическим раствором. Сама процедура заключается в пропускании крови, забираемой из вены больного, через канюлированную селезёночную артерию в селезёнку, а после прохождения органа кровь из селезёночной вены возвращается в вену пациента. Применяют модификацию способа: осуществляют перфузию крови через фрагментированную селезёнку или внутривенно вводят ксеноперфузат (физиологический раствор, пропущенный через фрагментированную селезёнку свиньи, хранящуюся в замороженном виде).
Экстракционные методы основаны на удалении из организма вместе с компонентами крови всех видов токсичных веществ. Основной метод - плазмаферез. Суть метода состоит в удалении из организма токсичной плазмы крови и замене её донорской свежезамороженной плазмой и кровезамещающими растворами. Используют ручной и автоматизированный (непрерывный) способы.
При ручном способе забирают кровь, добавляют стабилизатор и разделяют её на форменные элементы и плазму (отстаиванием или центрифугированием). Форменные элементы крови возвращают в сосудистое русло, а вместо изъятой плазмы вливают свежезамороженную плазму и плазмозамещающие растворы.
При непрерывном способе с помощью специальных мембранных фильтров кровь сразу разделяют на форменные элементы и плазму, при этом по тому же контуру форменные элементы поступают обратно в организм больного, а плазма удаляется. Вместо удалённой плазмы также вводят свежезамороженную плазму и плазмозамещающие растворы. Терапевтический эффект начинается с удаления 0,5-1,0 л плазмы.
Дренирование грудного протока позволяет удалить из организма лимфу, значительно более токсичную, чем кровь при многих гнойных заболеваниях (особенно при процессах в брюшной полости). Для этого под местной анестезией осуществляют доступ над левой ключицей, выделяют левый венозный угол (место соединения внутренней яремной и подключичной вен), обнаруживают устье грудного протока и катетеризируют его (используют стандартный катетер для катетеризации подключичной вены - диаметр протока обычно 2-4 мм). По катетеру за сутки поступает до 2-3 л лимфы, замещаемой свежезамороженной плазмой и кровезаменителями. Кроме того, можно очистить лимфу, пропустив её через специальные фильтры (лимфосорбция), и вернуть в организм пациента. Дренирование грудного лимфатического протока впервые выполнил Х. Вильмс в 1910 г.
Этот метод применяют по показаниям, в крайне тяжёлых случаях, так как он весьма сложен технически (часто наблюдают рассыпной тип строения грудного лимфатического протока), а также возникают проблемы с возмещением лимфопотери.
Электрохимическое окисление крови. Метод основан на использовании носителя активного кислорода. Существуют специальные аппараты (ЭДО-1, ЭДО-3), в которых при пропускании постоянного тока через физиологический раствор образуется гипохлорит натрия (малостойкое соединение, в присутствии органических веществ разлагающееся на активный кислород и хлорид натрия). Гипохлорит натрия при внутривенном введении выделяет активный кислород, способствующий окислению токсина и превращению последнего в водорастворимую форму, удаляемую через почки. Используют внутривенное введение 0,1% раствора гипохлорита натрия.
Методы квантовой терапии. Квантовое облучение крови вызывает образование свободных радикалов, функциональные изменения многих белков плазмы, изменяет заряд форменных элементов крови, способствует высвобождению биологически активных субстанций (гормонов, гепарина натрия, гистамина, простагландинов). Указанные механизмы обеспечивают активацию иммунных факторов, антигипоксическое и вазодилатационное действие, улучшение реологических свойств крови, стимуляцию регенерации и гемопоэза.
Наиболее распространены следующие методики.
Экстракорпоральное УФО крови. Используют аппараты типа «Изольда». С помощью обычной системы для переливания крови у пациента забирают кровь из расчёта 1,5-2,0 мл на 1 кг массы тела. Кровь (со стабилизатором) пропускают через аппарат с помощью роликового насоса, в аппарате кровь дважды при заборе и введении проходит через кварцевую кювету, где облучается ультрафиолетовыми лучами. После этого кровь вводят обратно в вену пациента. Процедура длится 20-30 мин, широко распространена как в стационарах, так и в амбулаторной практике. Обычно назначают три сеанса через день.
Внутрисосудистая методика облучения крови. Внутривенно вводят световод, соединённый с источником ультрафиолетовых лучей или лазера, и проводят облучение потока крови. Механизм действия аналогичен экстракорпоральной методике.
Иммунокоррекция
Для иммунокоррекции используют различные методы и вещества, а также средства заместительной терапии.
1. Иммунокорригирующим действием обладают общее УФО и лазерное облучение крови, ЭЛТ, перфузия крови через ксеноселезёнку.
2. Применяют лекарственные вещества химической природы (левамизол). Широко используют препараты вилочковой железы.
3. В качестве заместительной терапии можно использовать:
• кровь и её компоненты;
• гипериммунную плазму, γ-глобулины;
• интерлейкины;
• интерфероны и пр.
Симптоматическое лечение
Симптоматическое лечение направлено на восстановление нарушенных функций органов и систем.
Необходимым бывает применение жаропонижающих и противовоспалительных препаратов.
При развитии недостаточности системы кровообращения применяют кардиотонические средства, сердечные гликозиды, диуретики. При на- рушении функций дыхания используют специальные мероприятия вплоть до ИВЛ. Важны контроль функций желудочно-кишечного тракта и обеспечение полноценного питания (энтерального и/или парентерального).
Достаточно часто при инфекционных процессах развиваются нарушения свёртывающей системы крови, водно-электролитного баланса и т.д., в этом случае необходима их коррекция.
Гнойные заболевания кожи и подкожной клетчатки
Основные гнойные заболевания кожи и подкожной клетчатки - фурункул, карбункул, гидраденит, абсцесс, флегмона и рожа. Характерные для них зоны повреждения кожи, её дериватов и подкожной клетчатки представлены на рис. 12-2.
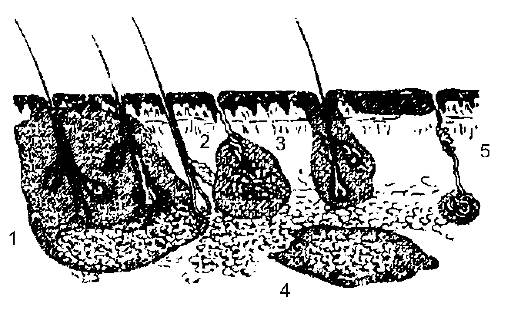
Рис. 12-2. Локализация основных гнойных процессов в коже и подкожной клетчатке: 1 - карбункул; 2 - гидраденит; 3 - фурункул; 4 - рожа; 5 - флегмона
Классификация гнойно-воспалительных процессов мягких тканей по Д. Аренхольцу (1991):
• I уровень - поражение собственно кожи (фурункул и другие пиодермии, рожа, эризипелоид).
• II уровень - поражение подкожной клетчатки (карбункул, гидраденит, абсцесс, мастит, лимфаденит, целлюлит и др.).
• III уровень - поражение поверхностной фасции тела (фасциты различной этиологии: стрептококковый некротизирующий, клостридиальный, неклостридиальный, синергичный некротизирующий, гангрена Фурнье).
• IV уровень - поражение мышц и глубоких фасциальных структур (пиомиозит, клостридиальный и неклостридиальный мионекроз и др.).
Фурункул
Фурункул - частая форма гнойных заболеваний кожного покрова преимущественно открытых частей тела. Большинство больных лечатся амбулаторно. При ухудшении состояния и появлении у пациентов осложнений показано направление их в стационар.
Фурункул - острое гнойно-некротическое воспаление волосяного фолликула и прилежащей сальной железы с окружающей соединительной тканью. В дальнейшем процесс переходит на близлежащую соединительную ткань.
Этиопатогенез
В подавляющем большинстве случаев возбудителем бывает золотистый стафилококк. Причинами, предрасполагающими к развитию заболевания, становятся нарушения обмена веществ (сахарный диабет, авитаминоз), тяжёлые сопутствующие заболевания, нарушение гигиенических требований. У мужчин фурункулы выявляют примерно в 10 раз чаще, чем у женщин.
Течение фурункула проходит три стадии:
• инфильтрация;
• формирование и отторжение гнойно-некротического стержня;
• рубцевание.
Особенность течения фурункула в том, что возникающий инфильтрат во много раз превышает зону развития некротического стержня. В инфильтрате тромбируются кожные капилляры и мелкие вены. Это замедляет выхождение лейкоцитов и процесс гнойного расплавления омертвевшего участка кожи (стержня). Преждевременная попытка механическим путём удалить стержень (выдавливание) может закончиться распространением инфицированных тромбов из очага по венам и генерализацией процесса.
Клиническая картина
Стадия инфильтрации
Процесс начинается с появления незначительного болезненного узелка и гиперемии над ним. В центре инфильтрата находится волос. Через 24-48 ч в области устья волосяного фолликула появляется маленький жёлтый пузырёк - пустула. Процесс может завершиться постепенным стиханием воспалительных изменений (рассасывание инфильтрата) или переходом к следующей стадии.
Стадия формирования и отторжения гнойно-некротического стержня
Волосяной фолликул и сальная железа подвергаются гнойному расплавлению. При этом увеличивается зона гиперемии и инфильтрата, он приподнимается над поверхностью кожи в виде пирамиды, в центре которой под истончённой кожей начинают просвечивать серо-зелёные массы (гнойно-некротический стержень). Увеличение воспалительных явлений сопровождается усилением болевого синдрома. Общие симптомы при фурункуле обычно представлены головной болью, слабостью и субфебрильной температурой тела.
Постепенно кожа в центре инфильтрата расплавляется, некротические массы начинают отторгаться наружу.
Рубцевание
После полного отторжения гнойно-некротических масс образуется небольшой тканевой дефект, замещающийся соединительной тканью и эпителизирующийся. После фурункулов остаются незначительные малозаметные рубцы.
Лечение
Местное лечение
Неосложнённый фурункул лечат только консервативно.
При лечении фурункула нельзя применять согревающий компресс, так как он разрыхляет кожу и создаёт благоприятные условия для развития инфекции.
В стадии инфильтрации кожу обрабатывают 70% спиртом, а пустулу прижигают 5% настойкой йода. Применяют сухое тепло, физиотерапию (УВЧ), лазеротерапию. Довольно эффективно выполнение короткого пенициллино-новокаинового блока (введение раствора вокруг фурункула).
При формировании гнойно-некротического стержня необходимо способствовать быстрейшему его отторжению. Для этого используют два метода.
• На кожицу в области зоны некроза накладывают кристаллы салициловой кислоты, кожу вокруг обрабатывают мазью для защиты от кератолитического действия кристаллов и накладывают сухую повязку. Через несколько часов кристаллы лизируют тонкую кожицу и начинается отторжение гнойно-некротического стержня.
• После обработки кожи антисептиком производят механическое удаление стержня пинцетом или тонким зажимом («москитом»). При этом нет необходимости в анестезии, но следует действовать очень аккуратно и исключить всякое давление на ткани в области инфильтрата. После того как некротические массы начали поступать наружу, для создания их непрерывного оттока в образовавшийся канал в качестве дренажа аккуратно вводят тонкую полоску перчаточной резины. Перевязки делают ежедневно. Перчаточный выпускник удаляют обычно на 3-и сутки после исчезновения инфильтрата и гнойного отделяемого. На рану накладывают сухие повязки или ведут её открытым способом, обрабатывая бриллиантовым зелёным или другими красителями.
Общее лечение
Как правило, в общем лечении нет необходимости. Исключение составляют фурункулы на лице, осложнённые фурункулы, а также фурункулы на фоне тяжёлых сопутствующих заболеваний (сахарного диабета, иммунодефицитных состояний и пр.). В этих случаях дополнительно проводят терапию антибиотиками, используют противовоспалительные средства, УФО крови.
Осложнения
Довольно часто фурункул осложняется лимфангитом и лимфаденитом. В этих случаях больные обязательно подлежат госпитализации, им необходимо проведение общей антибактериальной терапии.
При распространении процесса на подкожную клетчатку может сформироваться абсцесс (абсцедирующий фурункул). При этом необходимо оперативное лечение - вскрытие абсцесса.
Особенности фурункулов на лице
Следует отметить, что существует одна локализация фурункулов, с самого начала представляющая опасность для жизни больного. Это фурункулы лица, особенно верхней губы и носогубного треугольника. Процесс на лице быстро переходит на клетчатку, в которой находятся разветвления передней лицевой вены. Последняя через v.anguliaris имеет сообщение с v.ophtalmica , впадающей в sinus cavernosus. Распространение инфицированных тромбов из мелких вен в области инфильтрата при фурункуле может привести к тромбозу sinus cavernosus и гнойному менингиту. Летальность при этом осложнении достигает 80%. Наиболее опасны попытки выдавливания гноя при фурункуле, так как это способствует механическому распространению тромбов.
Существует правило, по которому все пациенты с локализацией фурункула на лице должны лечиться в стационаре. При этом кроме местного лечения назначают антибиотики, противовоспалительные средства, дезагреганты (ацетилсалициловая кислота, пентоксифиллин). Больные должны соблюдать постельный режим, ограничивают приём твёрдой пищи, разговоры.
Фурункулёз
Фурункулёзом называют состояние, при котором в разных местах тела образуются множественные фурункулы, которые часто находятся в разных стадиях процесса, а иногда последующие фурункулы развиваются после заживления предыдущих. Лечение каждого фурункула проводят по обычной методике. Кроме того, обязательны тщательная санация кожного покрова, общая антибактериальная терапия, а также иммунокоррекция. Наибольшее распространение получили такие методы, как УФО и лазерное облучение крови, использование левамизола, миелопида, эхинацеи, антистафилококкового иммуноглобулина, а в тяжёлых случаях при неэффективности других мероприятий - интерлейкин-2, интерферонов и др.
Карбункул
Карбункул - острое гнойно-некротическое воспаление нескольких волосяных фолликулов и сальных желёз с образованием единого воспалительного инфильтрата и переходом воспаления на подкожную клетчатку.
Этиопатогенез
Карбункул наиболее часто развивается у больных пожилого возраста, страдающих сахарным диабетом, на фоне истощения, авитаминоза и т.д. Как и при фурункуле, наиболее часто возбудителем бывает стафилококк.
Обычно выделяют две стадии: инфильтрации и гнойного расплавления.
Качественное и количественное отличие от фурункула заключается в массивном некрозе кожи и особенно подкожной клетчатки в зоне воспаления. Указанное заболевание может возникнуть при несвоевременном или неправильном лечении фурункула у больных, страдающих диабетом.
Так же как и при фурункуле, при карбункуле развитие воспалительного процесса сопровождается множественными тромбозами сосудов не только кожи, но и подкожной клетчатки, что существенно способствует некрозу и гнойному расплавлению.
Клиническая картина
В начальной стадии отмечают образование значительного (до 8-10 см) воспалительного инфильтрата. Он резко болезнен, кожа над ним гиперемирована, имеет синюшный оттенок. Карбункул практически всегда сопровождается лимфаденитом, а при локализации процесса на конечностях и лимфангитом.
Быстро нарастают общие явления: характерны высокая лихорадка до 39-40 ?С, озноб и другие признаки тяжёлой интоксикации.
Постепенно в центре инфильтрата образуется зона некроза кожи, она становится чёрного цвета, при этом через образовавшиеся в местах волосяных фолликулов отверстия начинают поступать гнойные массы (симптом «сита»).
Лечение
Местное лечение
При карбункуле в начальной стадии возможно назначение консервативной терапии (аналогично лечению стадии инфильтрации при фурункуле). Однако этот период очень короткий. Основной же метод лечения карбункула - хирургический, причём применять его нужно как можно раньше.
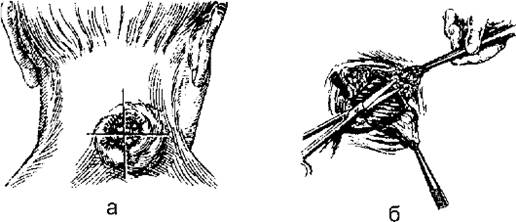
Рис. 12-3. Операция при карбункуле: а - крестообразный разрез; б - отсепаровка лоскутов и некрэктомия
Операцию при карбункуле называют «рассечение и иссечение карбункула». Её отличие от других операций в гнойной хирургии в том, что она прежде всего направлена на полное удаление некротизированных тканей.
Проводят крестообразный (или Н-образный) разрез (рис. 12-3). Кожные лоскуты отсепаровывают, иссекают всю некротизированную клетчатку в пределах здоровых тканей, вскрывают гнойные затёки, промывают рану 3% раствором перекиси водорода и вводят тампоны с антисептиками. В последующем проводят перевязки и лечение по принципам лечения гнойной раны.
Общее лечение
Применение общих методов лечения обязательно. Необходимо проводить антибиотикотерапию, дезинтоксикационную терапию (обычно достаточно инфузионной терапии с применением кровезаменителей дезинтоксикационного действия), иммунокоррекцию (УФО или лазерное облучение крови, антистафилококковый γ-глобулин и др.). Больным сахарным диабетом необходим контроль содержания глюкозы в крови и его коррекция.
Гидраденит
Гнойный процесс может изолированно поражать железы - придатки кожи, в частности потовые железы.
Гидраденитом называют гнойное воспаление потовых желёз.
Этиопатогенез
Гидраденит, как фурункул и карбункул, обычно бывает вызван золотистым стафилококком. Инфекция проникает через протоки желёз или небольшие повреждёния кожи (ссадины, расчёсы).
Клиническая картина
Гидраденит чаще локализуется в подмышечной впадине, реже - в паховой области. Предрасполагающие к его развитию факторы - повышенная потливость и несоблюдение норм личной гигиены. В глубине подкожной клетчатки появляется плотный болезненный узелок. Сначала он покрыт не- изменённой кожей, а затем его поверхность становится багрово-красной, неровной. При расплавлении инфильтрата появляется флюктуация; через образующееся небольшое отверстие выделяется сливкообразный гной.
Процесс развивается довольно длительно - 10-15 дней. Часто гидраденит имеет подострое течение, растягивающееся от нескольких недель до 1-2 мес. Нередко происходят рецидивы болезни.
Лечение
В начальных стадиях применяют сухое тепло, УВЧ, соллюкс, рентгенотерапию.
При наступлении гнойного расплавления необходима операция: вскрытие гнойника небольшим разрезом и дренирование (обычно полоской перчаточной резины). В последующем раз в 1-2 дня больных перевязывают; используют физиотерапию (УВЧ).
При лечении гидраденита необходимо принять меры для предотвращения инфицирования близлежащих от гнойника потовых желёз: тщательно обрабатывают кожу антисептиками с элементами дубления (96о этиловым спиртом, 2% борным спиртом, бриллиантовым зелёным и др.).
В подавляющем большинстве случаев общее лечение не показано. При подостром и рецидивирующем течении возможно применение антибиотиков и средств иммунокоррекции.
Абсцесс
Абсцессом, или гнойником, называют ограниченное скопление гноя в тканях и органах. Абсцесс - особая форма гнойной хирургической инфекции, способная развиться в различных тканях и органах.
Этиопатогенез
Причина возникновения абсцессов - проникновение в ткани гноеродных микробов через ссадины, уколы, раны, а также при осложнении воспалительных заболеваний (острого аппендицита, перитонита, пневмонии и др.). Микроорганизмы могут попадать в ткани и при лечебных манипуляциях (инъекциях), выполняемых без должного соблюдения правил асептики. Абсцессы могут возникать при сепсисе вследствие гематогенного метастазирования (метастатические абсцессы).
Особенность абсцесса как ограниченного гнойного процесса: наличие пиогенной оболочки - внутренней стенки гнойника, выстланной грануляционной тканью. Пиогенная оболочка отграничивает гнойно-некротический процесс и выделяет экссудат. Способность окружающих тканей создавать такую оболочку - проявление нормальной неспецифической защитной реакции организма, направленной на изолирование гнойного процесса.
Абсцессы могут образовываться в подкожной клетчатке, полостях тела (например, межпетельный абсцесс брюшной полости, поддиафрагмальный абсцесс и др.), органах (абсцесс мозга, печени, лёгкого). Они могут достигать значительных размеров.
Клиническая картина
Клиническая картина состоит из местных и общих проявлений.
Местные симптомы зависят от локализации абсцесса. Характерны болевой синдром и нарушение функций вовлечённых в воспалительный процесс органов и структур.
При поверхностном расположении над областью гнойника, как правило, отмечают явную припухлость и гиперемию кожи. Только при глубоком расположении абсцесса эти симптомы отсутствуют.
Важный признак - симптом флюктуации. Этот симптом отсутствует, когда стенка абсцесса очень толста, а полость небольшая и находится в глубине. Существенную помощь для диагностики могут оказать УЗИ и рентгеновское исследование, а также диагностическая пункция.
Выраженность симптомов интоксикации зависит от размеров и локализации абсцесса. При обширных абсцессах наблюдают выраженную общую реакцию: повышение температуры тела, общую слабость, потерю аппетита, бессонницу, изменение состава крови. Характерны колебания утренней и вечерней температуры тела с амплитудой до 1,5-3,0 градуса.
При метастатических абсцессах, как правило, тяжесть состояния обусловлена основными проявлениями сепсиса.
Лечение
Местное лечение
Диагноз абсцесса - показание для операции. Цель операции - вскрытие, опорожнение и дренирование его полости.
Пункцию абсцесса с аспирацией гноя и последующим введением в полость абсцесса антибиотиков, ферментных препаратов можно выполнять лишь по строгим показаниям, при определённых локализациях процесса, под контролем УЗИ.
При вскрытии абсцесса выбирают кратчайший оперативный доступ с учётом анатомо-топографических особенностей органа. Иногда абсцесс вскрывают по игле: первоначально пунктируют абсцесс, затем по игле рассекают ткани.
Во время операции по возможности подходят к нижнему полюсу гнойника, чтобы создать хорошие условия для дренирования. Если полость абсцесса обширна, её обследуют пальцем, разделяя перемычки и удаляя секвестры тканей. Полость абсцесса дренируют одним или несколькими резиновыми или полиэтиленовыми трубками и вводят в неё марлевые тампоны, смоченные раствором протеолитических ферментов, антисептиков, антибиотиков. При больших размерах абсцесса для адекватного дренирования делают дополнительные разрезы-контрапертуры.
После операции проводят лечение гнойной раны с учётом фазности течения раневого процесса.
Общее лечение
Общее лечение включает все компоненты лечения гнойной хирургической инфекции. Применяют антибиотики (с учётом чувствительности микрофлоры), дезинтоксикационную терапию (инфузионную терапию, переливание кровезаменителей, плазмы, а иногда и экстракорпоральные методы детоксикации) и иммунокоррекцию (по показаниям).
Флегмона
Флегмоной называют острое разлитое гнойное воспаление жировой клетчатки и клетчаточных пространств (подкожного, межмышечного, забрюшинного и др.).
В отличие от абсцесса при флегмоне процесс не отграничивается, а распространяется по рыхлым клетчаточным пространствам.
Этиопатогенез
Возбудителями флегмоны обычно бывают грамположительные и грамотрицательные кокки, но её могут вызывать и другие микроорганизмы, проникающие в клетчатку через случайные повреждения кожи, слизистые оболочки или гематогенным путём.
Флегмона - самостоятельное заболевание, но может быть и осложнением различных гнойных процессов (карбункула, абсцесса, рожи, остеомиелита, сепсиса и др.). Воспалительный экссудат распространяется по клетчатке, переходя из одного фасциального футляра в другой через отверстия для сосудисто-нервных пучков.
По характеру экссудата различают гнойную, гнойно-геморрагическую и гнилостную формы флегмоны.
По локализации флегмоны делят на поверхностные (поражение подкожной клетчатки до собственной фасции) и глубокие (поражение глубоких клетчаточных пространств). Глубокие флегмоны обычно носят специальные названия. Так, воспаление околопочечной клетчатки называют паранефритом, околокишечной - параколитом, околопрямокишечной - парапроктитом, клетчатки средостения - медиастинитом.
В особую группу выделяют постинъекционные флегмоны. Причиной развития постинъекционных флегмон становится нарушение правил асептики при введении лекарственных средств. В последнее время большое распространение получили постинъекционные флегмоны у наркоманов. Это связано как с грубыми нарушениями асептики, так и с резким снижением иммунитета на фоне наркомании. Особенно опасны такие флегмоны при попытках введения препаратов в глубокие вены (бедренную или плечевую). В таких случаях воспалительный процесс часто осложняется аррозивным кровотечением из крупных магистральных сосудов.
Клиническая картина
Обычно клиническая картина флегмоны характеризуется быстрым появлением и распространением болезненной припухлости, разлитым покраснением кожи над ней, болями, нарушением функций поражённой части тела, высокой температурой тела (до 40 ?С) и другими признаками интоксикации. Припухлость представляет собой плотный инфильтрат, со временем размягчающийся в центре. Появляется симптом флюктуации, или размягчения.
Клиническое течение флегмоны редко бывает благоприятным. Чаще встречают её злокачественные формы, когда процесс быстро прогрессирует, захватывая обширные участки подкожной, межмышечной клетчатки, и сопровождается тяжёлой интоксикацией. Температура обычно имеет постоянный характер. Отмечают высокий лейкоцитоз и сдвиг лейкоцитарной формулы влево.
При глубоких флегмонах наблюдают характерные симптомы, связанные с поражением близлежащих внутренних органов.
Лечение
Лечение больных всегда проводят в условиях стационара. Лишь в начальной стадии развития флегмоны (стадия инфильтрации) допустимо консервативное лечение: постельный режим, покой, внутримышечные инъекции антибиотиков, обильное питьё, молочно-растительная диета, сердечные средства. Местно применяют сухое тепло, УВЧ-терапию. При отграничении процесса и формировании гнойников (отграниченная флегмона) консервативное лечение сменяют их вскрытием и дренированием.
При прогрессирующей флегмоне отсрочка оперативного вмешательства недопустима. Под общим обезболиванием вскрывают флегмону с рассечением кожи и подкожной клетчатки на всю длину воспалительного инфильтрата, эвакуируют гной, забирают экссудат для бактериологического исследования, ревизуют гнойную полость, иссекают некротические ткани, при необходимости делают дополнительные разрезы и контрапертуры.
Следует отметить, что в ранних фазах развития стрептококковых флегмон гноя может и не быть. В этих случаях при вскрытии отмечают серозное или серозно-геморрагическое пропитывание тканей.
При завершении операции раны обрабатывают 3% раствором перекиси водорода, рыхло тампонируют марлей, смоченной растворами антисептиков, применяют протеолитические ферменты. После операции обычно быстро снижается температура тела, улучшается общее состояние, быстро стихают местные симптомы воспаления, что позволяет наложить ранний вторичный шов. В послеоперационном периоде проводят перевязки и лечение, как и при всех гнойных ранах, обязательно используя компоненты общего лечения гнойной хирургической инфекции. При флегмонах конечностей обязательна иммобилизация с помощью гипсовых лонгет.
В специализированных лечебных учреждениях можно применять активную хирургическую обработку раны, заключающуюся в иссечении всех нежизнеспособных тканей, эвакуации гнойного содержимого, дренировании несколькими дренажными трубками и наложении первичного шва. Через дренажные трубки в послеоперационном периоде производят активную аспирацию или применяют проточно-промывной метод с использованием антисептиков и протеолитических ферментов.
Лечение глубоких флегмон имеет особенности, связанные с локализацией патологического процесса; это предмет рассмотрения частной хирургии.
Рожа
Рожа (рожистое воспаление) - инфекционное заболевание, характеризующееся острым очаговым серозным или серозно-геморрагическим воспалением кожи или слизистых оболочек, лихорадкой и интоксикацией.
Этиопатогенез
Возбудитель рожи - β-гемолитический стрептококк группы А. Развитие заболевания может происходить и под воздействием некоторых других микроорганизмов. Микроорганизмы обычно проникают через мелкие раны, царапины, ссадины, инфицированные потёртости. В редких случаях рожа осложняет течение резаных и других инфицированных ран.
Частота заболевания возрастает, в то же время рожа малоконтагиозна, санитарно-эпидемиологическая служба не регистрирует её как инфекционное заболевание.
Рожа начинается с внедрения в кожу стрептококков (возможен также эндогенный путь инфицирования, особенно при рецидивирующем течении). Возникает серозное воспаление, при этом выделяется большое количество токсинов и ферментов, что приводит к токсикозу, гнойно-резорбтивной лихорадке. В кровеносное русло попадает большое количество биологически активных веществ, особенно гистамина. Это часто приводит к нарушению проницаемости сосудов, и воспаление может становиться серозно-геморрагическим. Поражение собственно кожи с выраженным её отёком, а также преимущественное распространение стрептококков по лимфатическим путям ведёт к местному нарушению лимфообращения. В последующем стрептококки способны формировать L-формы, длительное время находящиеся в коже, лимфатических сосудах и узлах и при определённых условиях вызывающие рецидивы заболевания (иммунитет к возбудителю кратковременный и нестойкий).
Определённое значение в этиопатогенезе имеют нарушения лимфатического и венозного оттока, трофические нарушения. В связи с этим наиболее часто рожа возникает на нижних конечностях (на голенях). Существуют данные об индивидуальной генетически детерминированной предрасположенности к заболеванию.
Воспалительные изменения собственно кожи обусловливают яркую гиперемию, что нашло отражение и в самом названии заболевания (rose - розовый, ярко-красный).
Классификация
Существует несколько классификаций рожи, в соответствии с которыми выделяют следующие формы этого заболевания.
По характеру местных проявлений:
• эритематозная;
• эритематозно-буллёзная;
• эритематозно-геморрагическая;
• буллёзно-геморагическая.
По тяжести течения:
• лёгкая;
• средней тяжести;
• тяжёлая.
По частоте возникновения:
• первичная;
• повторная;
• рецидивирующая.
Клиническая картина
Инкубационный период длится от нескольких часов до нескольких суток, обычно четко не регистрируется.
В течении рожи выделяют три периода: начальный, разгар заболевания и реконвалесценция.
Начальный период
В большинстве случаев заболевание начинается с общих симптомов тяжёлой интоксикации, предшествующих местным изменениям. Это отличительная черта рожи, часто становящаяся причиной диагностических ошибок (пациентам ставят диагноз острой респираторно-вирусной инфекции, пневмонии и пр.). Отмечают резкое повышение температуры тела (до 39-41 °С), выраженный озноб, тошноту, рвоту, головную боль, слабость. Параллельно с этим, а чаще к концу первых суток появляются умеренные боли в области регионарных лимфатических узлов (паховых), и только затем начинает проявляться характерная местная картина рожи.
Период разгара заболевания
Период разгара характеризуется яркими местными проявлениями. При этом, обычно в течение 4-5 сут, сохраняются общие симптомы интоксикации.
Местные проявления зависят от формы заболевания.
При эритематозной форме выявляют четко отграниченную яркую гиперемию, отёк и инфильтрацию кожи, местный жар. Граница зоны яркой гиперемии очень чёткая, а контуры неровные, поэтому воспалительные изменения кожи при роже сравнивают с «языками пламени», «географической картой».
При эритематозно-геморрагической форме на фоне описанной выше эритемы появляются мелкоточечные кровоизлияния, имеющие тенденцию к слиянию, что придает гиперемии синюшный оттенок. При этом сохраняются все местные воспалительные изменения, а синдром интоксикации бывает более длительным и выражен в большей степени.
При эритематозно-буллёзной форме на фоне эритемы появляются пузыри, заполненные серозным экссудатом, богатым стрептококками. Это более тяжёлая форма, при которой чаще развиваются осложнения, более выражена интоксикация.
Буллёзно-геморрагическая форма - наиболее тяжёлая из всех. На фоне эритемы появляются пузыри, заполненные геморрагическим экссудатом. Пузыри часто сливаются, кожа становится синюшно-чёрного цвета. Часто происходят обширные некрозы кожи, возможно развитие вторичной инфекции.
Период реконвалесценции
Исчезают общие признаки интоксикации, постепенно стихают местные воспалительные изменения, но ещё в течение 2-4 нед сохраняются отёк, утолщение, шелушение и пигментация кожи.
Лечение
Лечение рожи может быть местным и общим. Основной становится общая терапия.
Общее лечение
Основные компоненты общего лечения следующие.
• Антибактериальная терапия: используют полусинтетические пенициллины (ампициллин по 2,0-4,0 г/сут) в сочетании с сульфаниламидными препаратами (сульфаниламидом, сульфаленом). При тяжёлых геморрагических формах и рецидивах заболевания применяют цефалоспорины второго поколения. Методом выбора служит лимфотропное введение антибиотиков (ЭЛТ трудно осуществима из-за выраженного
отёка дистальных отделов конечности). Обычно 3-4 лимфотропных введения быстро купируют основные проявления заболевания.
• Дезинтоксикационная терапия необходима обычно в течение первых 4-5 дней. Применяют внутривенные инфузии кристаллоидных растворов (1,5-2,0 л/сут), а в тяжёлых случаях - кровезаменители дезинтоксикационного действия и препараты крови. Эффективным методом лечения служит УФО или лазерное облучение крови.
• Десенсибилизирующая терапия заключается во введении антигистаминных препаратов (клемастина, мебгидролина). При тяжёлых геморрагических формах используют глюкокортикоиды (преднизолон) в течение 3-5 сут.
• Укрепление сосудистой стенки необходимо при геморрагических формах. Применяют аскорбиновую кислоту, аскорбиновую кислоту + рутозид.
Местное лечение
При эритематозной и эритематозно-геморрагической формах местно применяют УФО в субэритемных дозах, конечности придают возвышенное положение и оставляют открытой или обрабатывают тонким слоем мази со сульфаниламидом (без влажных повязок).
При буллёзных формах крупные пузыри вскрывают, после чего накладывают влажно-высыхающие повязки с антисептиками (нитрофуралом, борной кислотой).
Профилактика рецидивов
Возможность развития рецидивов - отличительная черта рожи. При этом отмечают ту же локализацию или большую зону поражения. Иногда развиваются абортивные формы (без общих симптомов, быстро купирующиеся).
Основной профилактикой последующих рецидивов служит полноценное комплексное лечение первичной рожи. Кроме этого, при наличии частых рецидивов (до 4-5 рецидивов в год в течение многих лет) необходимо профилактическое лечение в холодный период. При этом используют такие методы.
• УФО или лазерное облучение крови.
• Курс лимфотропного (или эндолимфатического) введения антибиотиков. Препараты выбора - цефалоспорины и линкомицин (клиндамицин).
• Введение пролонгированных антибиотиков (бензатина бензилпенициллин + бензилпенициллин прокаина, 3-4 введения по 1,5 млн ЕД с интервалом 1 мес).
• Иммунотерапия (иммуноглобулины, интерлейкин-2).
• При развитии лимфедемы - коррекция лимфооттока, так как его нарушение способствует обострению заболевания.
Осложнения
Различают осложнения рожи в остром и отдалённом периодах.
Осложнения в остром периоде
В остром периоде при переходе воспалительного процесса на подкожную клетчатку развивается флегмона. Диагностика этого осложнения и определение показаний к операции затруднено в связи с маскирующим эффектом рожистого воспаления.
Геморрагические формы рожи часто осложняются обширными некрозами кожи, что в последующем требует выполнения кожной пластики.
При роже нередко развивается восходящий тромбофлебит и особенно - лимфангит и лимфаденит. Иногда возможна генерализация процесса с развитием сепсиса.
Все осложнения лечат в соответствии с принятыми для них принципами.
Осложнения в отдалённом периоде
В отдалённом периоде, особенно при рецидивирующей форме заболевания, возможно формирование лимфедемы конечностей - хронического заболевания, связанного с нарушением лимфооттока от конечности и сопровождающегося склерозирующими процессами в коже и подкожной клетчатке, вплоть до развития слоновости.
Лечение лимфедемы зависит от стадии заболевания и характера нарушения лимфооттока (выявляют методами рентгеноконтрастной и радиоизотопной лимфографии). Возможно оперативное лечение (формирование лимфовенозных анастомозов, а на поздних стадиях - операции резекционного характера: иссечение избыточных, склеротически изменённых кожи и подкожной клетчатки), а также комплекс консервативных мероприятий (физиотерапия, отводящий массаж, пневмомассаж; бинтование эластическими бинтами; применение препаратов, улучшающих венозный и лимфатический отток: диосмин + гесперидин и др.).
Аденофлегмона
Аденофлегмона - гнойное расплавление ткани лимфатического узла с переходом процесса на окружающую жировую клетчатку.
Этиопатогенез
В последнее время увеличилось количество больных с аденофлегмонами, особенно с аденофлегмонами шеи. Этому способствуют источники инфекции на волосистой части головы, в полости рта, носоглотке, а также в трахее и пищеводе. Развитая сеть лимфатических сосудов и узлов, а также особенности строения фасциальных листков и клетчатки шеи благоприятствуют развитию воспалительных процессов. Наличие в области шеи важнейших образований (крупных сосудов и нервов, гортани, трахеи, пищевода и щитовидной железы) создаёт известные опасности в течении этих процессов и затрудняет их оперативное лечение.
Большое значение в развитии аденофлегмон шеи имеют подбородочные лимфатические узлы, связанные с подчелюстными и глубоки- ми шейными лимфатическими узлами.
Таким образом, наличие многочисленных лимфатических узлов, щелей и пространств, ограниченных фасциями, определяет локализацию более или менее ограниченных или распространённых скоплений гноя на передней и боковой поверхностях шеи.
Обычно возбудителями флегмон шеи становятся стафилококки и стрептококки. Однако наличие в полости рта гнилостной инфекции, особенно кариозные зубы, влечёт за собой возможность развития и гнилостных флегмон, склонных к образованию весьма распространённых затёков.
Клиническая картина
Аденофлегмоны имеют особенности. Припухлость в начале заболевания плотная, иногда слегка бугристая, несколько подвижна. В связи с глубоким расположением очага под мышцей кожа над ним сначала не изменена и имеет обычную окраску. В начальных стадиях нет отёка.
При поверхностной подчелюстной аденофлегмоне есть местные признаки воспаления в подбородочной области: ограниченная краснота, припухлость, болезненность. При глубокой подчелюстной флегмоне (флегмона дна полости рта, ангина Людвига) заболевание начинается бурно, сопровождается выраженным диффузным отёком дна полости рта и подчелюстной области, резкой болезненностью, усиливающейся при жевании и глотании, слюнотечением, тризмом жевательной мускулатуры и затруднённым дыханием. При больших размерах гнойного очага и его поверхностном расположении отчётливо определяется симптом флюктуации.
Благодаря широкому и раннему применению антибиотиков многие воспалительные процессы, в том числе и в лимфатических узлах, не достигают стадии абсцедирования и претерпевают обратное развитие.
Гнойное расплавление, наступающее при дальнейшем прогрессировании процесса, сопровождается изменением конфигурации воспалительного инфильтрата - контуры его сглаживаются и становятся более расплывчатыми.
Лечение
Лечение с самого начала должно включать все современные методы борьбы с острой гнойной инфекцией. Прежде всего, следует создать покой - как общий, так и в области воспалительного очага, поэтому предписывают постельный режим. Назначают инъекции антибиотиков.
Местное применение холода целесообразно только в самых ранних стадиях заболевания. В ранних стадиях (стадия серозного отёка) можно применить диадинамофорез протеолитических ферментов.
Сочетание всех перечисленных мер может вызвать обратное развитие воспалительного процесса, о чём будут свидетельствовать падение температуры тела, исчезновение отёка, болей, улучшение самочувствия. Наоборот, нарастание указанных явлений - признак прогрессирования процесса, перехода его в стадию гнойного расплавления, что диктует необходимость оперативного вмешательства. При его выполнении нужно строго руководствоваться топографо-анатомическими соотношениями органов шеи и локализации гнойника.
Место разреза должно соответствовать участку наибольшей флюктуации. Осторожное послойное рассечение тканей предотвращает возможность повреждения важных образований, в первую очередь - сосудов.
Все операции вскрытия флегмон шеи необходимо заканчивать введением в полость гнойников резиновых или полихлорвиниловых дренажей. Возможно использование узких тампонов. Последние способствуют остановке капиллярного кровотечения в глубине раны, а также предохраняют полость гнойника от преждевременного (до отторжения некротических тканей и образования грануляций) спадения.
Гнойные заболевания железистых органов
Основные заболевания этой группы - гнойный паротит и мастит.
Гнойный паротит
Гнойный паротит - гнойное воспаление околоушной железы.
Этиопатогенез
Гнойный паротит возникает при проникновении микробов из полости рта в слюнную железу.
Ослабление защитных сил организма и нарушение выделения слюны приводят к развитию паротита у обезвоженных больных при инфекционных заболеваниях или после обширных операций.
Клиническая картина
В области околоушной железы появляется болезненность, увеличивающаяся припухлость, её пальпация вызывает усиление боли. Температура тела повышается до 39-40°С. Вследствие болей затрудняется процесс жевания. Напряжение тканей с каждым днём увеличивается, кожа над железой истончается, краснеет.
Общее состояние больного непрерывно ухудшается, отёчность тканей распространяется на шею, щеку, подчелюстную область, у тяжелобольных отмечают также отёчность мягкого нёба и боковой стенки глотки.
Лечение
В зависимости от формы паротита лечение может быть консервативным или оперативным.
При серозном паротите возможно выздоровление в результате консервативного лечения. Применяют антибиотики широкого спектра действия (полусинтетические пенициллины, цефалоспорины, аминогликозиды), назначают тепловые и физиотерапевтические процедуры (согревающие компрессы, УВЧ-терапию, соллюкс и др.). Если лечение начато рано, в большинстве наблюдений воспалительный процесс в околоушной железе подвергается обратному развитию.
При отсутствии успеха от консервативных мер и развитии гнойного паротита показано оперативное лечение. Цель операции - вскрытие всех гнойных очагов в железе и создание условий для хорошего оттока гноя.
Операция при паротите всегда серьёзна (опасность повреждения ветвей п. facialis). Большое значение имеет выбор места, направления и длины разреза. Производя разрез, необходимо учитывать направление основных ветвей лицевого нерва: он должен идти параллельно, а ни в коем случае не перпендикулярно к ним (рис. 12-4). Послойно рассекают кожу, подкожную клетчатку и обнажают капсулу околоушной железы. После надсечения капсулы пальцем или пинцетом осторожно проникают в гнойник и дренируют его.
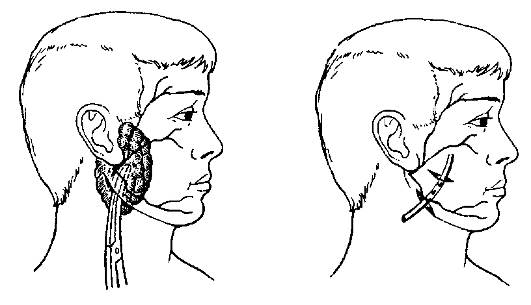
Рис. 12-4. Направление разрезов при вскрытии околоушной железы при паротите
После операции обычно наступает значительное облегчение. Припухлость уменьшается, уже на следующий день резко понижается температура тела, улучшается общее состояние больного, пульс становится менее частым, наполнение его улучшается. Из послеоперационной раны выделяются гной и участки омертвевших тканей, она очищается и активно гранулирует.
Из лечебных мероприятий в послеоперационном периоде необходимо продолжать антибактериальную и дезинтоксикационную терапию.
В профилактике развития паротита огромное значение имеют тщательный уход за полостью рта и борьба с обезвоживанием тяжелобольных, а также усиление саливации, чего достигают, например, сосанием лимона или жеванием жевательной резинки.
Осложнения
Возможны следующие осложнения паротита:
• опасные для жизни аррозивные кровотечения из сосудов, находящихся в паренхиме околоушной железы (или из сонной артерии при гнойных затёках);
• развитие флегмоны окологлоточного пространства, что обусловлено анатомическими соотношениями и особенностью сети лимфатических сосудов;
• глубокие флегмоны шеи вдоль сосудистого пучка и развитие медиастинита при запущенном гнойном паротите с образованием затёков по ходу сосудистого пучка шеи.
Мастит
Мастит - воспаление паренхимы и интерстициальной ткани молочной железы.
Этиопатогенез
Подавляющее большинство всех маститов (80-85%) развивается в послеродовом периоде у кормящих - лактационный мастит. Чаще возникает у первородящих, особенно в возрасте старше 30 лет.
Нелактационный мастит в последнее время стали выявлять чаще (10-15%).
Редко мастит возникает на фоне беременности - мастит беременных (0,5-1,0%).
Специальные названия получили достаточно редкие формы заболевания: воспаление млечных протоков (галактофорит) и воспаление околососкового кружка (ареолит).
По течению все маститы разделяют на острые и хронические.
С учётом характера воспаления острые маститы делят на следующие формы:
• серозный;
• инфильтративный;
• абсцедирующий;
• флегмонозный;
• гангренозный.
Хронические маститы бывают гнойными и негнойными.
Наиболее часто возбудителями мастита становится стафилококк (монокультура или в ассоциации с кишечной палочкой, палочкой сине-зелёного гноя или стрептококком). Большое значение имеет нозокомиальная инфекция, при этом мастит может развиваться непосредственно в родильном доме в течение ближайших дней после родов или сразу после выписки из стационара.
Входными воротами чаще всего бывают трещины сосков. Возможно и интраканаликулярное инфицирование при кормлении младенца и сцеживании молока.
Факторы, предрасполагающие к развитию мастита:
• трещины соска;
• недостаточное соблюдение правил гигиены;
• застой молока;
• ослабление иммунологической реактивности организма матери в первые недели после родов (особенно при патологических, осложнённых родах, сопровождающихся кровопотерей).
Особенность развития воспалительного процесса в молочной железе - слабо выраженная способность к его отграничению, что иногда приводит к прогрессированию заболевания, несмотря на предпринимаемые лечебные мероприятия.
Наиболее часто процесс начинается с застоя молока (лактостаза), переходящего в серозное воспаление железы, при неблагоприятном течении развиваются инфильтративные, а затем и деструктивные формы мастита.
Клиническая картина
Наиболее часто мастит развивается через 1-2 нед после родов, хотя возможно его развитие и в более поздние сроки.
Клиническая картина заболевания зависит от характера воспалительного процесса.
Лактостаз - ещё не стадия мастита. Происходят увеличение и напряжение молочной железы, появляется чувство тяжести в ней. При этом никаких изменений воспалительного характера и явлений интоксикации нет. Сцеживание приносит значительное облегчение, а регулярное его осуществление позволяет полностью нормализовать ситуацию.
Серозный мастит характеризуется тем, что на фоне лактостаза по- являются распирающие боли в молочной железе, незначительная гиперемия и местный жар, распространяющиеся на всю железу. Железа уплотняется, становится болезненной при пальпации, но каких-либо очаговых изменений в ней нет. Сцеживание молока резко болезненно и не приносит облегчения. Появляются симптомы общей интоксикации: лихорадка до 38-39 °С, озноб, слабость.
Переход серозного мастита в инфильтративный, а затем и в абсцедирующий, особенно при неправильном лечении, происходит быстро (в течение 3-4 дней) и характеризуется усилением общих и местных проявлений: температура тела держится постоянно на высоких цифрах или принимает гектический характер, нарастают все признаки интоксикации. Гиперемия кожи поражённой железы усиливается, в ней отчётливо пальпируется резко болезненный инфильтрат, а затем при его расплавлении в одном из участков появляется флюктуация.
В зависимости от локализации абсцессы в молочной железе могут быть субареолярными и интрамаммарными, при распространении гноя в ретромаммарную клетчатку может сформироваться ретромаммарный абсцесс (рис. 12-5).
При флегмонозном мастите молочная железа резко увеличивается, кожа её становится отёчной, блестящей, гиперемированной, с синюшным оттенком.
Возникает регионарный лимфаденит. Ухудшается общее состояние: температура тела достигает 40-41 °С, наблюдают потрясающий озноб, бледность, потливость, тошноту, рвоту.
Крайне тяжёлое состояние развивается при гангренозном мастите. Эта форма обычно развивается при позднем обращении за медицинской помощью или неадекватном лечении. Держится постоянная лихорадка до 40 °С и выше, пульс 110-120 в мин, слабого наполнения. Язык и губы сухие, кожные покровы бледные. Прогрессируют слабость, недомогание, головная боль, отсутствие аппетита и плохой сон. Молочная железа увеличена, отёчна, болезненная, пастозна. Кожа железы бледно-зелёного или сине-багрового цвета, местами покрыта пузырями, а иногда видны и зоны некроза. Сосок втянут, молоко отсутствует (причём часто его нет и в здоровой молочной железе). Регионарные лимфатические узлы увеличены и болезненны.
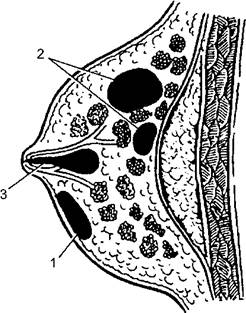
Рис. 12-5. Различные виды локализации гнойников при абсцедирующем мастите: 1 - субареолярный; 2 - интрамаммарный; 3 - ретромаммарный; 4 -галактоофорит
Диагноз мастита основывают на характерных данных клинического обследования. Дополнительно, кроме исследования крови (клинический анализ), проводят бактериологическое обследование молока из поражённой и здоровой молочных желёз.
В последние годы проводят экспресс-диагностику мастита с диагностикумом «Диана» и димастином. Метод основан на способности лейкоцитов молока вступать в реакцию с поверхностно-активными веществами, что приводит к изменению вязкости раствора. Смешивают в пробирке 1 мл молока с 1 мл реагента в течение 15-20 с. Образование желе - основной диагностический признак воспалительного процесса в молочной железе (свидетельствует о большом количестве лейкоцитов в молоке). У больных с начальными формами заболевания реакция слабо положительная, резко положительная реакция характерна для гнойных лактационных маститов.
В диагностически сложных случаях возможно применение термографии, УЗИ, маммографии.
Хронический мастит характеризуется наличием в железе длительно существующего ограниченного воспалительного инфильтрата (возможно и с абсцедированием) без явных признаков интоксикации (субфебрильная лихорадка, незначительная общая слабость).
Лечение
В зависимости от фазы развития мастита лечение может быть консервативным и оперативным.
Лечение серозной и инфильтративной форм мастита
При серозном и инфильтративном мастите лечение должно быть консервативным, оно включает следующие мероприятия.
• Возвышенное положение молочной железы. Достигают с помощью повязок или бюстгальтера, поддерживающего, но не сдавливающего железу.
• Сцеживание молока (при продолжении кормления грудью).
• Физиотерапевтические процедуры (УФО железы, УВЧ).
• Общая антибактериальная терапия (полусинтетические пенициллины, цефалоспорины).
• Ретромаммарная новокаиновая блокада (введение 150-200 мл 0,25% раствора прокаина с антибиотиками и химотрипсином в ретромаммарную клетчатку, рис. 12-6).
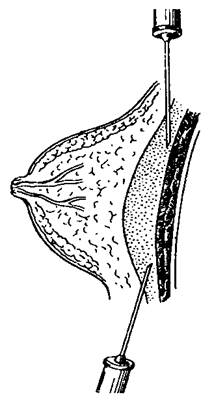
Рис. 12-6. Ретромаммарная новокаиновая блокада
Для регуляции лактации применяют парлодел - стимулятор дофаминовых рецепторов, подавляющий секрецию пролактина. Для пре- кращения лактации парлодел назначают по 1/2 таблетки 2 раза в сут в течение 2-3 дней, затем по 1 таблетке 2 раза в сут. После отмены препарата лактация может восстановиться.
Лечение абсцедирующей, флегмонозной и гангренозной форм мастита
При всех деструктивных формах показано хирургическое лечение.
При абсцедирующем мастите разрез длиной 5-6 см проводят в месте флюктуации или наибольшей болезненности в радиальном направлении, не доходя до ареолы по крайней мере на 1 см (в противном случае возможны галакторея, некрозы соска) - рис. 12-7.
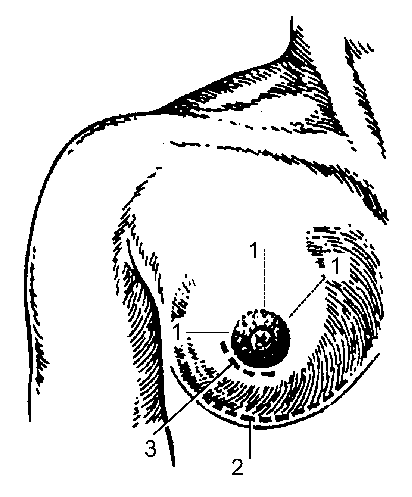
Рис. 12-7. Основные направления разрезов при вскрытии молочной железы при мастите: 1 - радиальные разрезы; 2 - разрез по Барденгейеру; 3 - параареолярный разрез
Рассекают кожу, подкожную клетчатку и вскрывают полость гнойника. Введённым в полость гнойника пальцем следует разделить все имеющиеся тяжи и перемычки. При затруднении опорожнения гнойника из одного разреза надо сделать второй радиальный разрез - контрапертуру. После освобождения от гноя в полость следует ввести резиновый или хлорвиниловый дренаж, тампоны. В послеоперационном периоде проводят местное и общее лечение в соответствии с принципами лечения гнойной раны.
При ретромаммарной локализации гнойника выполняют разрез под молочной железой по Барденгейеру, а при субареолярной - параареолярный разрез (см. рис. 12-7).
Склонность к рецидивам и прогрессированию гнойного процесса в молочной железе диктует необходимость тщательного выполнения операции, обязательного вскрытия всех гнойников и инфильтратов в железе, полной некрэктомии и проведения рационального дренирования.
При флегмонозном мастите разрезы выполняют по тем же правилам, но дополнительно необходимо выполнить широкую некрэктомию.
Гангрена молочной железы развивается достаточно редко; показана широкая некрэктомия, а иногда и ампутация железы, так как только эти вмешательства позволяют спасти жизнь пациентки.
Из общих методов лечения применяют антибиотикотерапию, дезинтоксикационную терапию (включая переливание плазмы и крови), а в особо тяжёлых случаях - методы экстракорпоральной детоксикации и иммунокоррекции.
Вопрос о прекращении лактации решают индивидуально в зависимости от характера воспаления в железе, степени инфицированности молока и состояния ребёнка.
Профилактика
Профилактика мастита направлена на устранение факторов, способствующих его развитию.
• Подготовка соска к кормлению во время беременности (уменьшает вероятность появления трещин).
• Гигиена молочной железы (мытьё железы с мылом перед кормлением, обработка трещин соска антисептиками).
• Рациональный режим кормления (регулярное кормление, сцеживание после кормления), что позволяет не допустить развития лактостаза.
• Уменьшение травматичности родов (полноценное обезболивание, возмещение кровопотери и пр.), повышение сопротивляемости организма в послеродовом периоде (полноценное питание, витаминотерапия, прогулки, режим дня). Профилактика госпитальной инфекции, санация очагов эндогенной инфекции.
Гнойные заболевания костей и суставов
В 1831 г. Рейно ввёл термин «остеомиелит». В переводе это слово означает воспаление костного мозга. Однако изолированное гнойное поражение костного мозга практически не встречается, поэтому определение несколько изменилось.
Остеомиелит - гнойно-воспалительное заболевание, поражающее все элементы кости как органа: костный мозг, собственно кость и надкостницу.
В подавляющем большинстве случаев в процесс в той или иной мере бывают вовлечены мягкие ткани, окружающие поражённую кость.
Все остеомиелиты делят на две большие группы, значительно различающиеся по способу проникновения инфекционных возбудителей в кость и по патогенезу. В случаях, когда инфекционные возбудители попадают в кость (костный мозг) гематогенным путём, остеомиелит называют гематогенным.
Если кость и её элементы инфицируются при открытой травме (открытом переломе), остеомиелит называют травматическим (при переломе вследствие огнестрельного ранения - огнестрельный остеомиелит, при развитии после оперативного лечения, например остеосинтеза, - послеоперационный остеомиелит).
Кроме того, в этом разделе будут рассмотрены вопросы диагностики и лечения острого гнойного артрита (воспаления сустава) и острого гнойного бурсита (воспаления синовиальной суставной сумки).
Гематогенный остеомиелит
Гематогенный остеомиелит - тяжёлое заболевание, преимущественно страдают дети и подростки, причём мальчики приблизительно втрое чаще девочек. По различным статистическим данным, больные гематогенным остеомиелитом составляют от 3 до 10% всех пациентов детских хирургических отделений. Поскольку в части случаев заболевание переходит в хроническую форму, тянется многие годы, а иногда и десятки лет, больных гематогенным остеомиелитом нередко встречают среди взрослых и даже пожилых людей.
Этиопатогенез
Этиология
Возбудителем гематогенного остеомиелита в подавляющем большинстве случаев бывает золотистый стафилококк, несколько реже - стрептококк, пневмококк и кишечная палочка. Для гематогенного остеомиелита характерна моноинфекция.
Патогенез
Как следует из названия, гематогенному остеомиелиту обязательно должна предшествовать бактериемия. Местом внедрения возбудителя в кровь может быть небольшой, иногда малозаметный гнойный очаг (на- пример, нагноившаяся ссадина, фурункул или гнойник в лимфоидном фолликуле при ангине), который к моменту возникновения клинически выраженного процесса в кости может быть излечен и забыт. В то же время бактериемия может быть и следствием тяжёлых гнойных процессов.
Гематогенный остеомиелит - заболевание периода роста, наиболее часто болеют дети в возрасте от 7 до 15 лет.
Возникновение гематогенного очага инфекции в кости связано с особенностями строения детской кости в зоне её роста, выявленными ещё Лексером в конце XIX века. Эти особенности следующие.
• У детей метафиз на границе с активно функционирующим эпифизарным хрящом имеет чрезвычайно обильную сеть сосудов, отличающуюся весьма широкими капиллярами с замедленным кровотоком. Сосудистая сеть метафиза не сообщается с сосудистой сетью эпифизарного хряща. Отчасти вследствие этого многие сосуды (артериолы) метафиза на границе с ростковым хрящом заканчиваются слепо. Они замкнуты, конечны и отходят под острым углом, вследствие чего создаются условия для задержки и фиксации в них микроорганизмов. В юношеском возрасте по мере редукции эпифизарного хряща устанавливаются сосудистые связи между эпифизом и метафизом, слепо оканчивающиеся сосуды исчезают, кровообращение в метафизе вообще становится более скудным, что, по-видимому, соответствует уменьшению вероятности фиксации здесь микроорганизмов.
• У детей в губчатой кости есть нежные, легко расплавляемые гноем костные балки, а также для детей характерна богато снабжённая сосудами и рыхло связанная с костью надкостница, что в совокупности способствует возникновению и прогрессированию остеомиелита.
Попавшие в капилляры метафиза ребёнка и зафиксировавшиеся там возбудители могут вызвать процесс не сразу или не вызывают его вообще. При соответствующем соотношении количества и патогенности возбудителей и состояния резистентности организма возможны следующие варианты течения процесса.
• Микроорганизмы погибают в костном мозге, будучи фагоцитированными макрофагами.
• Микроорганизмы немедленно вызывают вспышку гнойного процесса.
• Микроорганизмы остаются существовать в виде «дремлющей», клинически ничем не проявляющейся инфекции, дающей вспышку при том или ином снижении местной или общей резистентности макроорганизма, иногда через годы после внедрения.
Нередко фактором, ослабляющим местную резистентность к инфекции, становится травма (ушиб) кости, в которую, по-видимому, предварительно гематогенным путём были занесены гноеродные возбудители. Почти в половине случаев травма предшествует вспышке острого гематогенного остеомиелита.
К факторам, снижающим общую резистентность у детей, относят детские инфекции, грипп, переохлаждение.
Патоморфология
При развитии гематогенного остеомиелита происходят последовательные изменения (рис. 12-8).
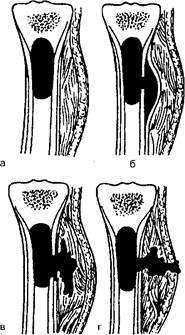
Рис. 12-8. Стадии развития гематогенного остеомиелита: а - абсцесс костного мозга; б - субпериостальный гнойник; в - межмышечная флегмона; г - образование свища
Небольшой гнойник, образовавшийся на границе эпифизарного хряща в метафизе, вызывает омертвение близлежащих костных балок и тромбоз сосудов. Эти изменения распространяются в направлении диафиза (эпифизарный хрящ довольно устойчив к нагноению). Костный мозг омертвевает и подвергается гнойному расплавлению (рис. 12-8, а), вследствие чего кортикальный слой кости лишается питания изнутри. Через систему гаверсовых каналов гной распространяется под надкостницу, отслаивая её от кости (у детей она связана рыхло) и образуя субпериостальный гнойник (рис. 12-8, б). Вследствие этого кость лишается питания и со стороны надкостницы и подвергается некрозу на большем или меньшем протяжении. Высокое давление гноя внутри замкнутой костномозговой полости ведёт к обильному всасыванию в кровь токсических продуктов и микроорганизмов, что обычно обусловливает тяжёлую гнойную интоксикацию и даже сепсис. Высокое давление внутри костномозгового канала вызывает к тому же жестокие боли. В конце концов гной, расплавляя надкостницу, прорывается в мягкие ткани, вызывая развитие межмышечной флегмоны (рис. 12-8, в). В последующем гной может прорваться и наружу с образованием свища (рис. 12-8, г).
Прорывом гноя или оперативным дренированием гнойного очага заканчивается острый период, характеризующийся тяжёлым гнойно- некротическим процессом, захватывающим все основные элементы кости и сопровождающимся тяжёлой интоксикацией.
При гематогенном остеомиелите чаще всего происходит поражение метафизов длинных трубчатых костей, наиболее часто - метафизов, прилежащих к коленному суставу. Диафизарные поражения наблюдают втрое реже метафизарных. Из плоских костей чаще всего страдают кости таза.
Клиническая картина
Острый гематогенный остеомиелит у детей и подростков начинается обычно как тяжёлое общее инфекционное заболевание, причём в первые дни общие симптомы несколько превалируют над местными.
Заболеванию нередко предшествуют ангина, местный гнойный процесс (нагноившаяся ссадина, фурункул) или ушиб конечности.
Болезнь начинается с внезапного подъема температуры тела до 39- 40 °С, сильного озноба, что сопровождается резким ухудшением общего самочувствия, иногда бредом. У детей младшего возраста нередко возникает обильная рвота, заставляющая думать о заболевании желудочно-кишечного тракта. В части случаев заболевание протекает чрезвычайно тяжело, злокачественно и заканчивается летальным исходом при явлениях молниеносного сепсиса в течение нескольких дней.
Одновременно с развитием тяжёлой интоксикации или несколько позже появляются жалобы на сильные распирающие, усиливающиеся при движении, перекладывании боли в соответствующей кости, однако ни припухлости, ни красноты в этой области в первые дни, как правило, нет. Отсутствует болезненность и при пальпации, особенно на бедре, где надкостница располагается глубоко под мышцами. Обнаружить местные симптомы в первые дни болезни особенно трудно. Правильной постановке диагноза помогают целенаправленное выявление местных симптомов, в частности мышечной контрактуры в близлежащих суставах, локальной болезненности, болей при нагрузке конечности по оси и др.
Лишь через 7-10 дней, когда гнойный процесс распространяется под надкостницу, начинают определяться более чёткая болезненность и припухлость. Через несколько суток после распространения процесса в мышечные пространства давление в очаге падает, вследствие чего боли несколько слабеют. Наблюдают клинические симптомы, характерные для глубокой флегмоны. В дальнейшем гной может прорваться наружу с образованием свища, после чего острые явления могут стихнуть.
Лабораторные данные свидетельствуют о наличии в организме очага гнойной инфекции (лейкоцитоз, сдвиг лейкоцитарной формулы влево и пр.).
Рентгенологические данные в первые 2 нед заболевания отрицательные (патологические изменения отсутствуют). В дальнейшем появляется сначала слабая тень отслоенной надкостницы, начинающей образовывать костное вещество (периостит). Ещё позже появляются зоны разрежения и смазывания структуры губчатой кости в области метафиза. Структура кости становится неравномерной. Отчётливое образование секвестров (отдельно лежащих участков некротизированной костной ткани) и секвестральной полости удаётся обнаружить лишь через 2-4 мес после начала заболевания, когда процесс уже перешёл в хроническую форму. В этот период в рентгенологической диагностике полостей и секвестров при наличии свищей помогает фистулография. Также позволяют уточнить диагноз КТ, радиоизотопное исследование, УЗИ, тепловидение, радиотермометрия.
Лечение
Лечение гематогенного остеомиелита включает общее и местное воздействие на очаг инфекции.
Общее лечение
Общие принципы лечения гнойной инфекции справедливы и в отношении остеомиелита.
Комплексная терапия при остром остеомиелите включает следующие элементы.
Антибиотикотерапия
С момента постановки диагноза больному внутримышечно вводят полусинтетические пенициллины, линкомицин или цефалоспорины, что обычно приводит к улучшению состояния больного, понижению температуры тела, уменьшению интоксикации и его выздоровлению. Если лечение антибиотиками начато рано, воспалительный процесс в костном мозге удаётся ликвидировать, а нарушенная гнойным процессом структура кости постепенно восстанавливается. Применение антибиотиков на ранних стадиях гематогенного остеомиелита в значительной степени изменяет его течение и улучшает исходы лечения. Хорошо зарекомендовало себя эндолимфатическое введение антибиотиков.
Дезинтоксикационная терапия
Начинают с первых дней, проводят переливание кристаллоидных растворов и кровезаменителей дезинтоксикационного действия, а также плазмы крови. В тяжёлых случаях возможно применение методов экстракорпоральной детоксикации.
Иммунокоррекция и симптоматическая терапия
Проводят по общим принципам лечения гнойной хирургической инфекции.
Местное лечение
С самого начала заболевания необходимы покой и иммобилизация больной конечности с помощью гипсовой лонгеты.
Благодаря эффективности лечения антибиотиками к операции приходится прибегать довольно редко.
Хирургическое лечение показано при запущенных процессах с развитием межмышечной флегмоны и в тех случаях, когда консервативное лечение не даёт успеха в течение нескольких суток при ухудшении общего состояния.
При операции на ранних стадиях (до прорыва гноя в мягкие ткани) рассекают мягкие ткани, формируют фрезевые отверстия через кость к полости абсцесса костного мозга и устанавливают дренажи для проточно-промывного дренирования.
При развитии межмышечной флегмоны её вскрывают широким разрезом, выполняемым с учётом расположения флегмоны, топографии сосудов, нервов и мышц. При этом рассекают надкостницу, тщательно ревизуют подлежащую кость, а при наличии костной полости осуществляют трепанацию кости и налаживают постоянное проточное дренирование.
В послеоперационном периоде проводят терапию по общим принципам лечения гнойных ран, обязательна иммобилизация до полного купирования воспалительного процесса.
Дата: 2019-03-05, просмотров: 556.