КАФЕДРА ОНКОЛОГИИ
Зав.кафедрой - доктор медицинских наук, доцент
Владислав Владимирович Семиглазов
РЕФЕРАТ НА ТЕМУ:
РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
Выполнила:
Студентка 632 группы
Топал Анастасия Андреевна
2019 г.
г.Санкт-Петербург
Содержание:
1. Введение
2. Этиология и патогенез
3. Клиническая картина
4. Диагностика
5. Регионарное метастазирование
6. Отдаленное метастазирование
7. Классификация TNM
8. Лечение
9. Прогноз
10. Заключение
11. Список использованной литературы
Введение.
Рак молочной железы (РМЖ) - одно из наиболее распространенных злокачественных новообразований у женщин. Заболеваемость РМЖ неуклонно растет и является одной из главных причин смертности женщин среднего возраста в экономически развитых странах. В России РМЖ занимает 1-е место в структуре онкологической заболеваемости у женщин, причем отмечается увеличение заболеваемости и смертности в трудоспособном возрасте.
В 2015 году зарегистрировано 66366 новых случаев, что составляет 20,8% от всей опухолевой патологии у женщин. Средний возраст заболевших составил 61,2 года. Ежегодный стандартизованный показатель прироста заболеваемости составил 1,8% за последние 10 лет. Кумулятивный риск развития РМЖ составляет 5,4% при продолжительности жизни 74 года. В последние годы увеличивается количество пациентов, у которых заболевание диагностировано в I-II стадиях. Так, в 2015 году этот показатель составил 69,5%, тогда как 10 лет назад равнялся 61,8%.
Летальность в течение первого года после установки диагноза снижается в течение десяти лет с 10,9% в 2005 году до 6,6 в 2015. Доля женщин, состоящих на учете 5 и более лет, составляет 59,8%. В структуре смертности женского населения РМЖ также находится на первом месте, составляя 17,0%.
РМЖ у мужчин составляет менее 1% опухолей этой локализации, занимая 0,3% в структуре заболеваемости.
Этиология и патогенез.
При выявлении групп повышенного риска по РМЖ учитывается ряд факторов, которые условно можно разделить на эндогенные (связанные с внутренней средой организма) и экзогенные.
Классификация факторов риска рака молочной железы (Семиглазов В.Ф. и др., 2001)
1. Факторы, характеризующие функционирование репродуктивной системы организма.
1.1. Менструальная, половая, детородная, лактационная функции.
1.2. Гиперпластические и воспалительные заболевания яичников и матки.
2. Эндокринно-метаболические факторы, обусловленные сопутствующими и предшествующими заболеваниями.
2.1. Ожирение.
2.2. Гипертоническая болезнь.
2.3. Сахарный диабет пожилых.
2.4. Атеросклероз.
2.5. Заболевания печени.
2.6. Заболевания щитовидной железы (гипотиреоз).
2.7. Дисгормональная гиперплазия молочных желез.
3.Генетические факторы (носители генов BRCA1 или BRCA2).
3.1. РМЖ у кровных родственников (наследственные и «семейные» случаи РМЖ).
3.2. Молочно-яичниковый синдром (РМЖ и рак яичников в семье).
3.3. Синдромы.
3.3.1. РМЖ + опухоль мозга.
3.3.2. РМЖ + саркома.
3.3.3. РМЖ + рак легкого + рак гортани + лейкоз.
3.3.4. SBLA-синдром + саркома + РМЖ + лейкоз + карцинома коры надпочечников.
3.4. Раковоассоциированные генодерматозы.
3.4.1. Болезнь Cowden - множественные трихолеммомы кожи + рак щитовидной железы, аденоматозный полипоз, рак толстой кишки + РМЖ.
3.4.2. Болезнь Bloom - аутосомальный наследственный генодерматоз + РМЖ.
4.Экзогенные факторы.
4.1. Ионизирующая радиация.
4.2. Курение.
4.3. Химические канцерогены, общие для всех локализаций опухолей.
4.4. Избыточное потребление животных жиров, высококалорийная диета.
Генетические факторы. Доказана наследственная предрасположенность к раку молочной железы. Исходя из этого, выделяют:
• спорадический рак (около 68%); нет случаев рака молочной железы у обоих родителей в 2 поколениях;
• семейный рак молочной железы (около 23%). Отмечают случаи рака молочной железы у одного или нескольких кровных родственников;
• генетическое предрасположение к раку в результате наличия мутаций генов BRCA1/BRCA2 (около 9%). Отмечают случаи рака молочной железы у кровных родственников, а также ассоциированный рак (первичная множественность — поражение яичников, толстой кишки).
Наследственный фактор является причиной рака молочной железы примерно у 5–10 % заболевших женщин. Речь идет о наследуемых мутациях генов BRCA-1, BRCA-2, TPS3, CDH1, pTEN, при которых опухоль развивается в несколько раз чаще, чем в среднем в популяции. Умеренный риск возникновения рака молочной железы обусловлен мутациями генов BRPIP, ATM, PA2B2, CHECK2. Кроме того, по наследству передается предрасположенность к злокачественной трансформации. Женщины, чьи кровные родственницы (мать, бабушка, сестра, тетя) болели раком молочной железы, имеют более высокий риск возникновения опухоли.
Гормональное влияние. Гормоны играют важную роль в развитии и функционировании молочной железы. Развитие ткани молочной железы начинается с появлением менструального цикла, а окончательная дифференцировка ткани происходит во время беременности, поэтому считают, что между этими событиями воздействие на ткань железы различных факторов (радиация, эстрогены) может оказывать наиболее повреждающее действие. Применение заместительной гормонотерапии с целью лечения патологического климакса и остеопороза также привело к увеличению риска развития рака молочной железы. Существуют также теории влияния избытка пролактина, дефицита мелатонина, надпочечниковых андрогенов, тиреоидной недостаточности на онкогенез рака молочной железы. К настоящему времени ни одна из них не доказана и не отвергнута.
Эстрогены не являются канцерогенами в классическом смысле этого слова — при присоединении этих гормонов к клеткам-мишеням опухоли происходит их активация и неконтролируемый рост. Более длительное и интенсивное воздействие эстрогенов на ткань органа происходит в следующих ситуациях: раннее менархе (до 13 лет), поздняя менопауза (более 55 лет), гинекологические заболевания (поликистоз яичников), позднее наступление 1-й беременности (после 30 лет), отсутствие беременности, количество детей менее 2. Такие факторы, как прерывание беременности, искусственное родоразрешение, отказ от естественного вскармливания вызывают дезадаптацию регуляторных процессов и создают условия для реализации действия условных канцерогенов.
Ионизирующая радиация. Женщины, которым многократно проводили рентгенологическое обследование грудной клетки в связи с туберкулёзом или проводили лучевую терапию на средостение, болели раком молочной железы значительно чаше. В Японии отмечали также увеличение частоты заболевания рак молочной железы среди выживших после атомных бомбардировок. Наибольший риск отмечен при облучении молочной железы в возрасте между 10 и 20 годами, что опять же указывает на высокую ≪уязвимость≫ к канцерогенным факторам не закончившей дифференцировку ткани железы.
Фактор питания. Многочисленные исследования установили связь между употреблением животных жиров и возникновением рака молочной железы, однако механизм влияния диеты на развитие рака неясен. Повышение риска возникновения рака молочной железы может быть обусловлено повышением синтеза эстрогенов в жировой клетчатке у женщин с избыточной массой тела. Включение в рацион продуктов с омега-3-полиненасыщенными жирными кислотами (льняное семя, орехи, рыба, ростки пшеницы, рапсовое масло и др.) способствует образованию продуктов, нейтрализующих токсины; профилактический эффект в отношении рака молочной железы доказан в опытах на животных. Овощи и фрукты содержат витамины и минералы, которые хорошо усваиваются, участвуют в метаболических процессах организма, выводят токсины. Эти продукты должны быть присутствовать в рационе ежедневно.
Учёт всех факторов, которые могут способствовать развитию рака молочной железы, вряд ли возможен и целесообразен, а отсутствие их не гарантирует от заболевания, поэтому в практической работе для оценки риска заболевания принято учитывать наиболее важные факторы:
• женский пол;
• раннее менархе (до 12 лет);
• позднее наступление менопаузы (после 55 лет);
• поздние первые роды (после 30 лет) и нерожавшие женщины;
• возраст старше 50 лет;
• атипическая гиперплазия ткани молочной железы;
• наличие семейного рака молочной железы (особенно рака у прямых родственниц в пременопаузе);
• мутации генов BRCA-1, BRCA-2;
• рак молочной железы в анамнезе.
Клиническая картина
По клинической картине РМЖ подразделяется на 3 основные формы: узловую, диффузную и атипические, характеризующиеся различным течением и прогнозом.
Клиническая классификация:
1. Узловая форма.
2. Диффузная форма:
2.1. Отечно-инфильтративная.
2.2. Маститоподобная.
2.3. Рожистоподобная.
2.4. Панцирная.
3. Атипические формы:
3.1. Рак Педжета.
3.2. Рак из придатков кожи.
3.3. Двусторонний рак.
3.4. Эктопированный рак.
3.5. Мультицентрический рак.
Узловая форма
Локальный рост в виде узла встречают наиболее часто. Пальпаторно выявляют плотное, округлое, бугристое безболезненное образование с нечёткими контурами, нередко ограниченно подвижное из-за инфильтрации окружающих тканей. В случае расположения под соском и малых размерах опухоли первыми симптомами могут быть отклонение соска в сторону, его фиксация или втяжение. Иногда над опухолевым узлом происходит фиксация кожи (симптом площадки) или её втяжение (симптом умбиликации). Указанные явления происходят за счёт вовлечения в процесс связок Купера. Лимфатический отёк кожи (≪лимонная корка≫) — поздний симптом заболевания. Увеличение или уплотнение подмышечных лимфатических узлов даже при небольшой подвижной опухоли с чёткими контурами должно вызвать подозрение на рак молочной железы. При УЗИ характерно превышение высоты образования над шириной, неровные края, наличие акустической тени, неоднородная внутренняя структура.
При маммографии выявляют солидное образование с неровными, лучистыми (спикулообразными) краями, часто содержащее микрокальцинаты. Можно определять ≪дорожку≫ к соску или грудной мышце, инфильтрацию кожи, увеличенные подмышечные лимфатические узлы повышенной плотности и округлой формы.
Выявление скоплений микрокальцинатов по ходу протоков к соску может свидетельствовать о продолженном внутрипротоковом росте опухоли.
Отёчная форма
Отёчную форму характеризует диффузное утолщение и гиперемия кожи. Эхографическим признаком отёка железы может быть утолщение кожи. Рентгенологически можно определить опухолевый узел и типичные изменения мягких тканей в виде поперечной тяжистости. скоплений микрокальцинатов. Если при биопсии кожи выявляют раковые эмболы и отсутствует локализованная опухолевая масса, то при клинической классификации применяют категорию T4d (воспалительный рак), а при наличии опухоли, отёка железы и отсутствии раковых эмболов в коже — Т4Ь.
Рожистоподобный рак
Эту форму рака молочной железы сопровождает выраженная гиперемия кожи с неровными языкообразными краями, внешне напоминающими рожистое воспаление. Гиперемия может распространяться на грудную стенку. Чаше всего заболевание протекает остро, с высокой (до 40 °С) температурой тела. Течение злокачественное, опухоль быстро метастазирует в лимфатические узлы и отдалённые органы.
УЗИ и маммография малоэффективны. Данные УЗИ могут быть интерпретированы как характерные и для воспалительного процесса, а маммография затруднена в связи с невозможностью проведения полноценной компрессии железы. При дифференциальной диагностике с воспалительными заболеваниями молочной железы в любом сомнительном случае необходима биопсия ткани образования (предпочтительнее трепан-биопсия).
Маститоподобная форма
Молочная железа увеличена в объёме за счёт быстро растущей опухоли без чётких контуров. Кожа железы над опухолью покрыта розовыми пятнами (раковый лимфангит) или гиперемирована. В глубине пальпируют инфильтрат без признаков размягчения. Железа ограничена в подвижности. Часто наблюдают повышение температуры тела, хотя и не обязательно до высоких цифр. Не бывает лейкоцитоза. При тонкоигольной аспирационной биопсии — гнойного отделяемого нет или получают гнойно-геморрагическое содержимое.
В дифференциальной диагностике наиболее эффективна сцинтимаммография. УЗИ не информативно, маммография затруднена из-за технических проблем (невозможность компрессии железы) и высокой плотности ткани.
При панцирной форме наблюдается опухолевая инфильтрация всей молочной железы и кожи с переходом на грудную стенку. Появляется множество внутрикожных опухолевых узлов. Молочная железа сморщивается, деформируется. Эта форма является IV стадией отечно-инфильтративного РМЖ.
Рак Педжета
Локализованный рак соска и ареолы считают наиболее благоприятной формой рака молочной железы. Клинически проявляется в виде явлений мацерапии (экземы) и изъязвления соска. Больных нередко длительно наблюдают дерматологи. При медицинских осмотрах наличие корочки ошибочно расценивают как высохший секрет из протоков. При прогрессировавший заболевания сосок разрушается и на его месте возникает язвенная поверхность.
Довольно часто рак Педжета сочетается с инвазивной протоковой формой рака. В такой ситуации больная выявляет узел в железе, но не обращает внимания на изменения соска.
При поражении соска и ареолы УЗИ неинформативно. При маммографии можно выявитв микрокалвцинаты или перестройку структуры ткани железы под соском.
Скрытый (оккультный) рак
Первый клинический признак — увеличение поражённых метастазами подмышечных лимфатических узлов без определяемой клинически опухоли в самой железе. Зачастую больных долго лечат от лимфаденита ≪инфекционной≫ природы и они попадают к онкологу уже при появлении отдалённых метастазов.
При наличии увеличения подмышечных лимфатических узлов показано проведение УЗИ и маммографии, тонкоиголвной аспирационной биопсии лимфатических узлов под контролем УЗИ. Использование маммографии, КТ. МРТ, сцинтимаммографии позволяет выявить локализацию первичной опухоли.
При отсутствии данных за первичную опухоль в молочной железе показано выполнение хирургической биопсии подмышечных лимфатических узлов для проведения гистологического и гистохимического анализов.
Диагностика
Анамнез
Учитывая, что многие заболевания молочной железы имеют дисгормональный характер и тесным образом связаны с деятельностью различных органов, участвующих в выработке и метаболизме гормонов, сбор анамнеза не следует ограничивать только длительностью и характеристикой процессов в самой железе. При опросе необходимо выяснить наличие в семейном анамнезе рака молочной железы, характер менструальной функции, акушерский анамнез, длительность лактации, наличие заболеваний матки и яичников, состояние нервной, пищеварительной систем, щитовидной железы, приём гормональных препаратов. Следует оценить изменение симптомов в зависимости от фазы менструального цикла, физической нагрузки или психологических стрессов.
Жалобы пациенток обычно сводятся к неприятным ощущениям в груди (боль, покалывание, распирание), обнаружению патологических очагов в ткани железы, изменению кожных покровов и консистенции железы. При раке Педжета могут ощущаться боль, зуд, жжение с области соска. При расспросе следует выяснить начало появления симптомов, последовательность их возникновения, взаимосвязь с лактацией, беременностью, фазами менструального цикла, травмами, другими заболеваниями. Необходимо отметить степень эффективности лечения, если оно проводилось. При расспросе врач должен попытаться составить впечатление о тенденции развития длительного заболевания: прогредиентное с постепенным усугублением симптоматики (характерно для злокачественных опухолей) или волнообразное с периодами ремиссий (неопухолевые заболевания). Информация о самообследовании пациенток принимается с учетом того, что регулярное и методически правильное самостоятельное обследование молочных желез порой позволяет обнаружить патологические очаги меньшего диаметра, чем доступные для выявления врачом, впервые пальпирующим конкретную женщину.
Осмотр
Перед осмотром необходимо снять всю одежду с верхней части тела и обеспечить хорошее равномерное освещение. Положение тела пациентки — сначала стоя с опущенными руками, затем — с поднятыми до горизонтального или вертикального уровня. Цель осмотра – выявление асимметрии молочных желез, патологических изменений кожи и сосковоареолярного комплекса. Используют следующие приемы: сравнение уровня нижнего края железы, сравнение симметрии наружного контура желез, сравнение цвета, ширины, рельефа, фактуры покрова сосковоареолярных комплексов слева и справа. Обязательно следует оценить рисунок подкожных вен. Их расширение и сгущение на определенном участке может быть вызвано патологическим процессом в подлежащих тканях. Патологические изменения на коже определяют с указанием их характера: узелок, пятно, трещина, эрозия, язва, корочка; описывают размеры, цвет, поверхность, очертания, консистенцию. Отмечают наличие рубцов после перенесенных заболеваний и операций. Отдельно оценивают наличие или отсутствие отека верхней конечности.
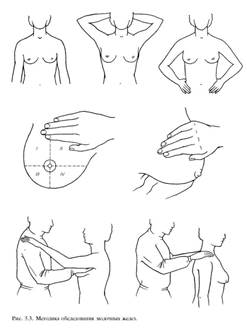 Пальпация
Пальпация
 Обязательное условие — отсутствие одежды на верхней половине тела. Положение пациентки — стоя с опущенными руками, затем — лежа на спине с приведенными руками. Для более детального обследования могут применяться другие положения рук. Ладонь врача образует единую плоскость с вытянутыми и сведенными 2–5 пальцами (рис.1). Ощупывание проводится кончиками пальцев. Цель пальпации — обнаружение участков ткани груди с измененной консистенцией. При этом ткань молочной железы прижимается к передней грудной стенке, перемещая одновременно соседние участки ткани между пальцами. Пальпацию лучше проводить с верхнее-наружного квадранта по часовой стрелке, заканчивая центральными квадрантами. После этого спине, с отведенными за голову руками, аналогично описанной ранее методике. При большом размере груди следует учитывать, что обследование нижних квадрантов более информативно в положении лежа. В случае значительного мастоптоза дистальную часть ощупывают, подкладывая ладонь врача к задней поверхности железы в качестве упора. Кроме молочной железы обязательно пальпируют лимфатические узлы подмышечной, подключичной и надключичной групп. Патологические очаги, обнаруженные при пальпации, описывают по следующим признакам: локализация, размер, консистенция, форма, очертания, смещаемость, состояние покрывающей кожи, болезненность. Например, в верхнее-наружном квадранте левой молочной железы имеется узловое образование 3 см в диаметре, плотноэластическое, неправильной формы, с нечеткими очертаниями, смещаемое относительно подлежащих тканей, покрытое неизмененной кожей, безболезненной, в левой подмышечной области у края большой грудной мышцы определяется лимфатический узел 1,5 см в диаметре, округлый, плотноэластический, безболезненный, смещаемый, с четкими очертаниями. Обязательный этап пальпации — попытка получения отделяемого из соска. Для этого как бы массируют ткань железы от периферии к центру, затем ареолу осторожно сдавливают 1 и 2 пальцами. Отмечается характер отделяемого: нативная или лизированная кровь, серозная жидкость, гной, молоко, мазеобразная субстанция.
Обязательное условие — отсутствие одежды на верхней половине тела. Положение пациентки — стоя с опущенными руками, затем — лежа на спине с приведенными руками. Для более детального обследования могут применяться другие положения рук. Ладонь врача образует единую плоскость с вытянутыми и сведенными 2–5 пальцами (рис.1). Ощупывание проводится кончиками пальцев. Цель пальпации — обнаружение участков ткани груди с измененной консистенцией. При этом ткань молочной железы прижимается к передней грудной стенке, перемещая одновременно соседние участки ткани между пальцами. Пальпацию лучше проводить с верхнее-наружного квадранта по часовой стрелке, заканчивая центральными квадрантами. После этого спине, с отведенными за голову руками, аналогично описанной ранее методике. При большом размере груди следует учитывать, что обследование нижних квадрантов более информативно в положении лежа. В случае значительного мастоптоза дистальную часть ощупывают, подкладывая ладонь врача к задней поверхности железы в качестве упора. Кроме молочной железы обязательно пальпируют лимфатические узлы подмышечной, подключичной и надключичной групп. Патологические очаги, обнаруженные при пальпации, описывают по следующим признакам: локализация, размер, консистенция, форма, очертания, смещаемость, состояние покрывающей кожи, болезненность. Например, в верхнее-наружном квадранте левой молочной железы имеется узловое образование 3 см в диаметре, плотноэластическое, неправильной формы, с нечеткими очертаниями, смещаемое относительно подлежащих тканей, покрытое неизмененной кожей, безболезненной, в левой подмышечной области у края большой грудной мышцы определяется лимфатический узел 1,5 см в диаметре, округлый, плотноэластический, безболезненный, смещаемый, с четкими очертаниями. Обязательный этап пальпации — попытка получения отделяемого из соска. Для этого как бы массируют ткань железы от периферии к центру, затем ареолу осторожно сдавливают 1 и 2 пальцами. Отмечается характер отделяемого: нативная или лизированная кровь, серозная жидкость, гной, молоко, мазеобразная субстанция.
Целесообразно провести пальпацию щитовидной железы, поскольку значительная часть дисгормональных состояний связана с нарушениями её функции.
Ультразвуковое исследование
Ультразвуковое исследование (УЗИ) ткани молочной железы позволяет обнаруживать патологические очаги более 3–4 мм. Метод относительно дешев, прост и неинвазивен. Эхоскопия более надежно выявляет образования в железистой части органа и в ткани с повышенной плотностью. УЗИ позволяет дифференцировать полостные и солидные очаги. Типичные эхоскопические признаки злокачественного роста: гипоэхогенное образование с нечеткими очертаниями, неоднородной эхо-структурой, включением микрокальцинатов. Под контролем эхо-датчика можно выполнять инвазивные процедуры: пункции, аспирации, введение препаратов и т.п. Кроме молочной железы этим методом обследуют органы-объекты регионарного и отдаленного метастазирования: лимфатические узлы подмышечной ямки, шеи, забрюшинного пространства, печень. Относительные недостатки метода: около 20 % узлов имеют изоэхогенную плотность и с трудом обнаруживаются при УЗИ, поле датчика не может охватить весь объем ткани при большом размере железы и поверхностные образования, получаемое изображение является плоскостным срезом, что затрудняет сравнительную диагностику.
Маммография
Рентгенологическое исследование на специально разработанных аппаратах — основной метод ранней диагностики рака молочной железы. Для повышения качества изображения и снижения лучевой нагрузки используют усиливающие экраны, компрессию железы. Стандартно выполняют снимки каждой железы в двух проекциях — вертикальной и косой (45°). При необходимости уточнения диагноза используют нестандартные укладки, местную компрессию, контрастные методы (дуктография).
В интерпретации маммограмм учитывают:
• асимметрию плотности и васкуляризации симметричных участков желёз;
• нарушения архитектоники железы;
• наличие опухолевидных образований: локализация, размер, плотность, форма, контуры;
• наличие микрокальцинатов;
• структуру и степень развития железистой ткани с учётом возраста и гормонального статуса;
• состояние кожи, соска и ретромаммарного пространства;
• наличие патологически изменённых лимфатических узлов.
Наиболее частая находка — микрокальцинаты и округлые образования различной плотности (чаще кисты, реже — солидные опухоли). Локальное скопление обызвествлений наиболее характерно для рака in siru, в то время как округлые образования и локальная перестройка структуры, асимметрия плотности и гиперваскуляризация характерны для инвазивного рака.
Другие методы
Дуктография (галактография) — метод введения в проток молочной железы контрастного вещества с последующими снимками с целью определения патологических образований. В клинической практике имеет значение в диагностике внутрипротоковых опухолей.
Компьютерная томография — позволяет выявлять патологические очаги в любой части железы, дифференцировать признаки злокачественного и доброкачественного роста, определять экстраорганное распространение опухоли, обнаруживать метастатические очаги в отдаленных анатомических зонах: головной мозг, кости, средостение.
Ультразвуковая компьютерная томография — способ диагностики опухолевого роста в молочной железе у молодых женщин, на фоне фиброзно-кистозной мастопатии, фиброаденоматоза, наличия имплантов или плотной ткани молочных желез.
Магниторезонансная томография — метод особенно перспективен в диагностике опухолевой патологии сосково-ареолярного комплекса, метастатического поражения головного мозга.
Радиоизотопное исследование — регистрация очагов накопления радиофармпрепарата в ткани железы (сцинтимаммография) или костях. В опухолевых очагах более интенсивно фиксируется 99Тс. Метод используется для топической диагностики первичной опухоли и выявления метастазов.
Термография — определение локальной температуры ткани молочной железы. В практической онкологии почти не используется.
Пневмоцистография — введение газа в просвет кисты с последующей рентгенографией. Позволяет выявлять внутрикистозные разрастания.
Трепан-биопсия
Использование специальной иглы позволяет получить необходимое количество ткани для гистологического изучения характера патологического процесса, включая дифференциальную диагностику инвазивного рака и поражений in situ, степень дифференпировки опухоли, наличие в ней рецепторов эстрогенов, прогестеронов. Этот метод также применяют амбулаторно, однако он уже требует местной анестезии. При непальпируемых опухолях, микрокальцинатах введение иглы проводят под контролем УЗИ или маммографии (стереотаксическая биопсия).
Биопсия
Хирургическую, или эксцизионную, биопсию следует выполнять при подозрении на рак молочной железы, если при тонкоигольной аспирапионной биопсии и трепан-биопсии не удалось подтвердить (исключить) ЗН. При непальпируемых патологических образованиях,
требующих биопсии, для ориентира хирурга участок, подлежащий удалению, маркируют, подводя к нему иглу с мандрен-фиксатором под контролем УЗИ или маммографии. В таких случаях чаше требуется госпитализация больной, как правило, общая анестезия, срочное гистологическое исследование удалённого препарата и при необходимости расширение объёма операции вплоть до мастэктомии. Возможное расширение объёма операции при раке требуется обсудить с больной и получить её письменное согласие до выполнения биопсии.
Опухолевые маркеры
Регулярное использование сывороточных опухолево-ассоциированных маркеров (РЭА, СА-15.3) оказалось малоинформативным. Однако определение СА-15.3 может быть целесообразным для мониторинга больных с установленным диагнозом. Повышение уровня этого маркёра в крови после проведённого комплексного лечения может свидетельствовать о прогрессировании заболевания.
Классификация TNM .
Американский объединенный комитет по изучению рака (AJCC) пересмотрел систему TNM классификации рака молочной железы. На территории США изменения вступили в силу 1 января 2018 года. Ниже приводится классификация рака молочной железы согласно AJCC 8-го пересмотра (2017).
Клиническая и патологическая классификации первичной опухоли (T) идентичны. Если измерения выполнены при физикальном осмотре, то клиницист может использовать параметры T1, T2 или T3. Если измерение опухоли выполнялось при маммографии или при микроскопическом исследовании препарата, то могут быть использованы параметры Т1а, Т1b и т.д. Размер шага при измерении опухоли не должен превышать 0,1 см.
Первичная опухоль (T)
· TX: Недостаточно данных для оценки опухоли;.
· T0: Признаки первичной опухоли отсутствуют.
· Tis (DCIS): протоковый рак in situ;
· Tis (Педжета): болезнь Педжета с поражением только соска НЕ ассоциирована с инвазивным раком и/или раком in situ (DCIS) в прилежащей паренхиме молочной железы. Рак в паренхиме молочной железы ассоциированый с болезнью Педжета оценивается основываясь на размере и характеристиках поражения паренхимы, однако наличие болезни Педжета должно быть отмечено.
Замечание: Tis (LCIS) - дольковый рак in situ имеет добракачественную природу и была удалена из TNM классификации AJCC 8-го пересмотра (2017).
· T1: Опухоль не менее 20 мм в наибольшем измерении
· T1mic: микроинвазия размером до 1 мм включительно в наибольшем измерении;
· T1a: размеры опухоли от более 1 мм до 5 мм включительно в наибольшем измерении;
· T1b: размеры опухоли от более 5 мм до 10 мм включительно в наибольшем измерении;
· T1c: размеры опухоли от более 10 мм до 20 мм включительно в наибольшем измерении.
· T2: размеры опухоли от более 20 мм до 50 мм включительно в наибольшем измерении.
· T3: размеры опухоли более 50 мм в наибольшем измерении.
· T4: опухоль любого размера с прямым распространением на грудную стенку и/или кожу (изъязвление или макроскопические узелки); инвазия в только дерму не классифицируется как T4
· T4a: распространение на грудную стенку; инвазия в грудные мышцы или прилегание к ним в отсутствии инвазии в структуры грудной стенки не классифицируется как T4;
· T4b: отек (включая «лимонную корку»), или изъязвление кожи молочной железы, или сателлитные узелки на коже пораженной молочной железы, не соответствующие критериям воспалительного (отечного) рака;
· T4c: сочетание признаков, характерных для T4a и T4b;
· T4d: воспалительный (отечный) рак.
Отдаленные метастазы (M)
· Mx: недостаточно данных для оценки отдаленных метастазов.
· M0: отдаленные метастазы отсутствуют.
· M1: отдаленные метастазы.
Лечение.
Хирургическое лечение. Операция — ведущий метод в лечении больных раком молочной железы. С развитием лучевой и химиотерапии, разработкой новых технологий диагностики опухоли на ранних стаднях удалось добиться улучшения отдалённых результатов лечения, и появились основания для пересмотра необходимого объёма операции при этом заболевании.
Мастэктомия
Мастэктомия остаётся методом выбора при лечении большого числа больных раком молочной железы из-за распространённости процесса или противопоказаний к органосохраняющим операциям.
Радикальную мастэктомию (операция Холстеда) в настоящее время выполняют только при прорастании опухоли в большую грудную мышцу. При этом используют различные виды разрезов кожи в зависимости от локализации и размеров опухоли, требований к закрытию раневого дефекта. Кожные лоскуты отсепаровывают кверху до ключицы, медиально до грудины, книзу до верхней трети прямой мышцы живота, латерально — до широчайшей мышцы спины. Удаляют единым блоком молочную железу, большую и малую грудные мышцы и жировую клетчатку подмышечно-подлопаточной области с лимфатическими узлами.
Модифицированная радикальная мастэктомия (операция Пейти) отличается сохранением большой грудной мышцы, но при этом удаляют малую грудную мышцу для облегчения доступа к лимфатическим узлам II —III уровней. Сохранение большой грудной мышцы снижает инвалидизацию больных, улучшает условия для последующего протезирования или реконструкции молочной железы.
Операция Маддена предусматривает сохранение как большой, так и малой грудной мышцы. При этом необходимо выполнение в полном объёме подключично-подмышечной лимфаденэктомии и удаление межмышечной клетчатки. Эту операцию в настоящее время считают оптимальным вариантом радикальной мастэктомии при узловых формах рака молочной железы, так как она носит щадящий характер и не увеличивает частоту местных рецидивов по сравнению с операциями Холстеда и Пейти.
Простая мастэктомия (абляция) показана при распространённом раке с распадом и кровотечением (санационная операция). Цель её — только улучшение качества жизни. В этом случае железу удаляют без фасции большой грудной мышцы. Подмышечную лимфодиссекцию не выполняют, так как это повышает риск осложнений.
Органосохраняющие резекции
Под туморэктомией (лампэктомией) понимают удаление только первичного очага без обширного иссечения неизменённых тканей с гистологическим подтверждением полного удаления опухоли (оценка краёв резекции). Остальные виды операций предполагают удаление не менее 2 см здоровой ткани по краям от опухоли.
Органосохраняющие операции обязательно дополняют лучевой терапией. Объём удаляемой ткани определяется размерами опухоли, её гистологической характеристикой и результатами интраоперационного исследования, подтверждающими отсутствие опухоли по краю резекции. В тех случаях, когда необходимо удалить более 1/3 части железы, большинство хирургов-онкологов считают целесообразным проводить мастэктомию и реконструкцию железы, особенно при локализации в верхневнутреннем квадранте, где нарушение формы наиболее заметно.
Как самостоятельный метод хирургического лечения лампэктомию применяют только у пожилых больных при карциномах in situ и небольших опухолях, выявленных при скрининговой маммографии.
Реконструктивные операции при раке молочной железы
Реконструкция молочной железы может быть проведена как одновременно с радикальной операцией на железе, так и в отсроченном варианте.
Общеизвестные методики одномоментной и отсроченной реконструкции после радикатьных мастэктомий заключаются в перемещении кожно-мышечного лоскута спины, передней брюшной стенки, ягодицы или имплантации протеза.
Возможность выполнения реконструктивных операций с хорошими результатами способствует быстрому восстановлению психосоматического статуса больных.
Радикальная секторальная резекция
Сам термин определяет, что удаляемый объём ткани соответствует сектору ткани молочной железы (как правило, несколько долей) с опухолью и магистральными протоками.
Подмышечная лимфодиссекция
При лимфодиссекции преследуют не только лечебные, но и диагностические цели — определение показаний к адъювантной химиотерапии и прогноза заболевания. Для исследования следует удалить и гистологически изучить не менее 10 лимфатических узлов.
Для уменьшения осложнений, связанных с лимфаденэктомией,
предложена методика выявления и удаления для анализа первого от опухоли лимфатического узла — ≪исследование сигнального лимфатического узла≫.
Клинические группы: первично операбельный рак молочной железы (0, I, IIA,IIB, IIIA стадии), местно-распространенный (первично не операбельный) рак молочной железы (IIIВ, IIIС стадии), метастатический рак молочной железы или рецидив болезни.
Алгоритм лечебно-диагностических мероприятий при различных стадиях рака молочной железы представлен на рис. 2.
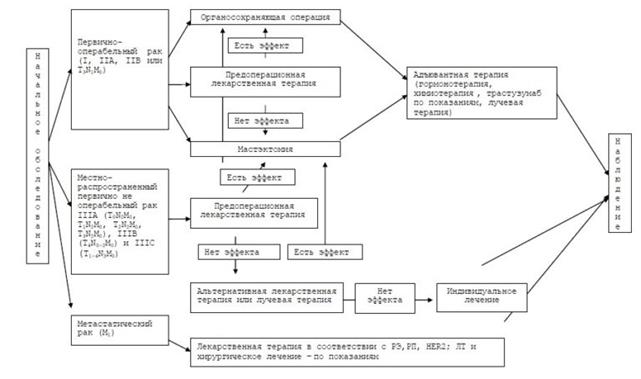 Рис.2. Алгоритм лечебно-диагностических мероприятий при различных стадиях рака молочной железы.
Рис.2. Алгоритм лечебно-диагностических мероприятий при различных стадиях рака молочной железы.
РАННИЙ (ПЕРВИЧНО ОПЕРАБЕЛЬНЫЙ) РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
Общие принципы адъювантной лекарственной терапии
Адъювантная лекарственная терапия проводится в дополнение к локальным (хирургическому и лучевому) методам лечения и позволяет снизить риск рецидива болезни и смерти. При планировании адъювантной лекарственной терапии необходимо оценить прогноз, ожидаемую пользу адъювантного лечения, возможные побочные эффекты и сопутствующую патологию, а также учесть предпочтения больной. Возраст сам по себе не является ограничением для лекарственной терапии при отсутствии сопутствующей патологии.
При опухолях небольших размеров (< 0,5 см) в сочетании c N0, являющихся прогностически благоприятными, адъювантная лекарственная терапия обладает минимальной эффективностью. Назначение адъювантной гормонотерапии (при гормонозависимых опухолях) в такой ситуации имеет целью профилактику вторых (контралатеральных) гормонозависимых опухолей.
План адъювантной лекарственной терапии основывается на принадлежности опухоли к одному из молекулярно-биологических подтипов (табл. 3). Адъювантная лекарственная терапия должна начинаться с химиотерапии, если таковая показана.
Химиотерапия (таксаны) может проводиться одновременно с анти-HER2-терапией, если таковая показана. Гормонотерапия, если таковая показана, должна начинаться после завершения химиотерапии и проводиться одновременно с анти-HER2-терапией. Лучевая терапия, если таковая показана, должна начинаться после завершения химиотерапии и может проводиться одновременно с гормонотерапией и анти-HER2-терапией.
| Молекулярно-биологический подтип | Клинико-патологическое (суррогатное) определение подтипа |
| Люминальный А | Наличие всех факторов: • РЭ положительные • HER2 отрицательный • Ki67 низкий (< 20 %) • РП высокие (> 20 %) |
| Люминальный В ( HER2 отрицательный) | • РЭ положительные • HER2 отрицательный и наличие одного из следующих факторов: • Ki67 высокий (> 30 %) • РП низкие (< 20 %) |
| Люминальный В ( HER2 положительный) | • РЭ положительные • HER2 положительный • Ki67 любой • РП любые |
| HER2 положительный (не люминальный) | • HER2 положительный • РЭ и РП отрицательные |
| Базальноподобный | • отрицательные РЭ, РП, HER2 (тройной негативный протоковый) |
| Молекулярно-биологический подтип | Рекомендуемая адъювантная системная терапия | Примечания |
| Люминальный тип А | Только гормонотерапия в большинстве случаев | Назначение адъювантной химиотерапии (в дополнение к гормонотерапии) должно быть рассмотрено при наличии одного из следующих факторов: • большая степень распространения болезни: - ≥ 4 пораженных метастазами регионарных лимфатических узлов; - ≥ Т3; • III степень злокачественности. Если принято решение о назначении химиотерапии (в дополнение к гормонотерапии), то в большин- стве случаев можно ограничиться режимами АС или CMF (без таксанов) |
| Люминальный тип В (HER2 отрицательный) | Гормонотерапия + химиотерапия в большинстве случаев | При T1a (≤ 5 мм) и N0: только адъювантная гормонотерапия. Остальные больные: химиотерапия антрациклинами и таксанами в дополнение к гормонотерапии |
| Люминальный тип В (HER2 положительный) | Химиотерапия + анти-HER2 терапия + гормонотерапия | При T1a (≤ 5 мм) и N0: только адъювантная гормонотерапия; химиотерапия и трастузумаб не показаны. При T1b, с (> 5 мм, но ≤ 20 мм) и N0: возможна химиотерапия паклитакселом (без антрациклинов) в сочетании с трастузумабом (с последующей гормонотерапией). При Т2-Т4 (> 20 мм) или N+: антрациклины → таксаны + трастузумаб (с последующей гормонотерапией). При противопоказаниях к назначению антрациклинов может быть рекомендован режим DСН. |
| HER2 положительный (не люминальный) | Химиотерапия + анти-HER2 терапия | При T1a (≤ 5 мм) и N0: системная терапия не показана. При T1b (> 5 мм, но ≤ 10 мм) и N0: возможна химиотерапия паклитакселом (без антрациклинов) в сочетании с трастузумабом. При Т1с-Т4 (> 10 мм) или N+: антрациклины → таксаны + трастузумаб. При противопоказаниях к назначению антрациклинов может быть рекомендован режим DСН. |
| Тройной негативный (протоковый) | Химиотерапия с включением антрациклинов и таксанов | При T1a (≤ 5 мм) и N0: системная терапия не показана; Производные платины могут быть включены в режим адъювантной химиотерапии у больных с доказанными мутациями гена BRCА. |
РМЖ относится к опухолям, для которых характерна высокая частота гематогенного и лимфогенного метастазирования. Использование адъювантной химиотерапии позволяет значительно сократить риск рецидива и смерти у больных операбельным РМЖ. Цели лекарственной терапии: излечение, продление жизни, уменьшение стадии опухолевого процесса, улучшение качества жизни и контроль симптомов болезни, повышение результатов хирургического и лучевого лечения, отказ от калечащих операций, уменьшение объема вмешательств. Каждый химиопрепарат действует только на те клетки, которые находятся в определенной фазе клеточного цикла. Поэтому монохимиотерапия менее эффективна, чем полихимиотерапия (ПХТ) - сочетание нескольких препаратов с различными фазовоспецифичностью и механизмом действия. Клинический опыт показал, что при РМЖ наиболее эффективны в качестве дополнения к операции (адъювантная терапия) химиопрепараты циклофофосфамид, тиотепа, фторурацил, метотрексат, доксорубицин и некоторые другие, противоопухолевое действие которых потенцируется при их сочетании.
Альтернативой хирургической или лучевой кастрации у менструирующих и находящихся в пременопаузе женщин является использование гонадотропин-рилизинггормона (ГтРГ) и агониста ГтРГ гозерелин или его отечественного аналога - бусерелина. Комбинация агониста ГтРГ и тамоксифена (метаанализ четырех рандомизированных исследований) превосходит по эффективности монотерапию агонистом ГтРГ у женщин в пременопаузальном периоде, больных распространенным РМЖ.
Все шире применяются физиологически неактивные антиэстрогенные препараты (нестероидные антигормоны), непосредственно воздействующие на опухолевую клетку и не затрагивающие центральные механизмы гормонообразования. Большую роль играет тамоксифен у больных в менопаузе при гормональнозависимых опухолях с метастазами в подмышечные лимфатические узлы.
Современные достижения в гормонотерапии РМЖ связаны с появлением новых препаратов, в том числе «чистых» антиэстрогенов, селективных модуляторов эстрогеновых рецепторов, включая ралоксифен, а также новых ингибиторов ароматазы 3-го поколения, включающих нестероидные препараты анастрозол, летрозол, фулвестрант (фазлодекс) и стероидный ингибитор экземестан.
Для уточнения показаний к гормонотерапии, в частности овариэктомии, следует пользоваться определением гормональных рецепторов удаленной опухоли или ее кусочка, взятого при трепанобиопсии до начала лечения. После овариэктомии больным назначают тамоксифен (по 20 мг в день на срок 2 года) для блокады надпочечниковых эстрогенов.
Иммунотерапия
Показанием для иммунотерапии является нарушенная реактивность организма, обусловленная наличием самой опухоли и иммунодепрессивными методами химиолучевого и хирургического лечения. До начала и в процессе лечения необходимо определение иммунологического статуса, в частности показателей клеточного и гуморального иммунитета. По данным Н.И. Переводчиковой (2000), к иммуномодуляторам относятся: цитокины (интерлейкины, интерфероны, колониестимулирующие факторы), моноклональные антитела, дифференцирующие агенты, антиангиогенезные факторы.
Прогноз.
На основании данных о стадии опухолевого процесса и с учетом биологических характеристик опухоли необходимо оценить прогноз заболевания и выработать оптимальный план лечения конкретной пациентки. Различают большое количество прогностических факторов: размер опухоли, состояние регионарных лимфатических узлов, степень дифференцировки опухоли, рецепторы эстрогенов, HER2/neu-статус. Предсказывающие факторы освещают связь между биологией опухоли и эффективностью лечения, коррелируют с частотой объективного ответа независимо от прогноза, разделяют больных по чувствительности к различным видам лечения. Таких факторов немного: рецепторы эстрогенов и оценка гормональной терапии, HER2/neu-статус и оценка ответа на трастузумаб и т.д.
Наиболее важными прогностическими признаками являются: распространенность процесса, количество метастазов в подмышечных лимфатических узлах, отек молочной железы, наличие инвазивных свойств протоковой карциномы, степень злокачественности опухоли.
Отдаленные результаты лечения принято оценивать по 5-летней выживаемости. Выживаемость больных во многом зависит от стадии заболевания, при которой начато лечение. Современные методы лечения позволяют достичь 5-летней выживаемости при I стадии рака у 96 %, IIA - у 90 %, IIB - у 80 %, IIIA - у 87 %, IIIB - у 67 % больных.
Заключение.
Рак молочной железы является одной из наиболее актуальных проблем современной онкологии с многовековой историей изучения. Это обусловлено клинической и социальной значимостью заболевания. Интересно отметить, что именно панцирная форма рака молочной железы породила термин «cancer — рак». В течение последних десятилетий проводятся разнообразные многоцентровые исследования биологических и клинических особенностей рака молочной железы. На основании полученных сведений совершенствуются диагностические и лечебные методы. В то же время динамика эпидемиологических показателей позволяет прогнозировать значительный рост заболеваемости. По данным специалистов в течение XXI в. каждая 10-я женщина заболеет раком молочной железы. Это определяет высокий уровень ответственности врачей клинических специальностей при выявлении опухолевой патологии молочных желез и соответствующие требования к теоретической подготовке.
Список использованной литературы.
1. Онкология : учебник с компакт-диском / под ред. В.И. Чиссова, С.Л. Дарьяловой. - М. : ГЭОТАР-Медиа, 2007. - 560 с.
2. Онкология [Электронный ресурс]: учебник / Давыдов М.И., Ганцев Ш.Х. - М. : ГЭОТАР-Медиа, 2013.
3. ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ЛЕКАРСТВЕННОМУ ЛЕЧЕНИЮ ИНВАЗИВНОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ. Коллектив авторов: Стенина М.Б., Жукова Л.Г., Королева И.А., Пароконная А.А., Семиглазова Т.Ю., Тюляндин С.А., Фролова М.А.
4. Клинические рекомендации по диагностике и лечению больных раком молочной железы. Утверждено на Заседании правления Ассоциации онкологов России. Москва, 2014 год.
5. Рак молочной железы: учеб.-метод. пособие для студентов старших курсов медицинских вузов, врачей-стажеров, клинических ординато- ров, практических врачей / С. А. Иванов, И. К. Кривенчук, В. А. Кри- венчук. — Гомель: учреждение образования «Гомельский государст- венный медицинский университет», 2012. — 36 с.
КАФЕДРА ОНКОЛОГИИ
Зав.кафедрой - доктор медицинских наук, доцент
Владислав Владимирович Семиглазов
РЕФЕРАТ НА ТЕМУ:
РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
Выполнила:
Студентка 632 группы
Топал Анастасия Андреевна
2019 г.
г.Санкт-Петербург
Содержание:
1. Введение
2. Этиология и патогенез
3. Клиническая картина
4. Диагностика
5. Регионарное метастазирование
6. Отдаленное метастазирование
7. Классификация TNM
8. Лечение
9. Прогноз
10. Заключение
11. Список использованной литературы
Введение.
Рак молочной железы (РМЖ) - одно из наиболее распространенных злокачественных новообразований у женщин. Заболеваемость РМЖ неуклонно растет и является одной из главных причин смертности женщин среднего возраста в экономически развитых странах. В России РМЖ занимает 1-е место в структуре онкологической заболеваемости у женщин, причем отмечается увеличение заболеваемости и смертности в трудоспособном возрасте.
В 2015 году зарегистрировано 66366 новых случаев, что составляет 20,8% от всей опухолевой патологии у женщин. Средний возраст заболевших составил 61,2 года. Ежегодный стандартизованный показатель прироста заболеваемости составил 1,8% за последние 10 лет. Кумулятивный риск развития РМЖ составляет 5,4% при продолжительности жизни 74 года. В последние годы увеличивается количество пациентов, у которых заболевание диагностировано в I-II стадиях. Так, в 2015 году этот показатель составил 69,5%, тогда как 10 лет назад равнялся 61,8%.
Летальность в течение первого года после установки диагноза снижается в течение десяти лет с 10,9% в 2005 году до 6,6 в 2015. Доля женщин, состоящих на учете 5 и более лет, составляет 59,8%. В структуре смертности женского населения РМЖ также находится на первом месте, составляя 17,0%.
РМЖ у мужчин составляет менее 1% опухолей этой локализации, занимая 0,3% в структуре заболеваемости.
Этиология и патогенез.
При выявлении групп повышенного риска по РМЖ учитывается ряд факторов, которые условно можно разделить на эндогенные (связанные с внутренней средой организма) и экзогенные.
Классификация факторов риска рака молочной железы (Семиглазов В.Ф. и др., 2001)
1. Факторы, характеризующие функционирование репродуктивной системы организма.
1.1. Менструальная, половая, детородная, лактационная функции.
1.2. Гиперпластические и воспалительные заболевания яичников и матки.
2. Эндокринно-метаболические факторы, обусловленные сопутствующими и предшествующими заболеваниями.
2.1. Ожирение.
2.2. Гипертоническая болезнь.
2.3. Сахарный диабет пожилых.
2.4. Атеросклероз.
2.5. Заболевания печени.
2.6. Заболевания щитовидной железы (гипотиреоз).
2.7. Дисгормональная гиперплазия молочных желез.
3.Генетические факторы (носители генов BRCA1 или BRCA2).
3.1. РМЖ у кровных родственников (наследственные и «семейные» случаи РМЖ).
3.2. Молочно-яичниковый синдром (РМЖ и рак яичников в семье).
3.3. Синдромы.
3.3.1. РМЖ + опухоль мозга.
3.3.2. РМЖ + саркома.
3.3.3. РМЖ + рак легкого + рак гортани + лейкоз.
3.3.4. SBLA-синдром + саркома + РМЖ + лейкоз + карцинома коры надпочечников.
3.4. Раковоассоциированные генодерматозы.
3.4.1. Болезнь Cowden - множественные трихолеммомы кожи + рак щитовидной железы, аденоматозный полипоз, рак толстой кишки + РМЖ.
3.4.2. Болезнь Bloom - аутосомальный наследственный генодерматоз + РМЖ.
4.Экзогенные факторы.
4.1. Ионизирующая радиация.
4.2. Курение.
4.3. Химические канцерогены, общие для всех локализаций опухолей.
4.4. Избыточное потребление животных жиров, высококалорийная диета.
Генетические факторы. Доказана наследственная предрасположенность к раку молочной железы. Исходя из этого, выделяют:
• спорадический рак (около 68%); нет случаев рака молочной железы у обоих родителей в 2 поколениях;
• семейный рак молочной железы (около 23%). Отмечают случаи рака молочной железы у одного или нескольких кровных родственников;
• генетическое предрасположение к раку в результате наличия мутаций генов BRCA1/BRCA2 (около 9%). Отмечают случаи рака молочной железы у кровных родственников, а также ассоциированный рак (первичная множественность — поражение яичников, толстой кишки).
Наследственный фактор является причиной рака молочной железы примерно у 5–10 % заболевших женщин. Речь идет о наследуемых мутациях генов BRCA-1, BRCA-2, TPS3, CDH1, pTEN, при которых опухоль развивается в несколько раз чаще, чем в среднем в популяции. Умеренный риск возникновения рака молочной железы обусловлен мутациями генов BRPIP, ATM, PA2B2, CHECK2. Кроме того, по наследству передается предрасположенность к злокачественной трансформации. Женщины, чьи кровные родственницы (мать, бабушка, сестра, тетя) болели раком молочной железы, имеют более высокий риск возникновения опухоли.
Гормональное влияние. Гормоны играют важную роль в развитии и функционировании молочной железы. Развитие ткани молочной железы начинается с появлением менструального цикла, а окончательная дифференцировка ткани происходит во время беременности, поэтому считают, что между этими событиями воздействие на ткань железы различных факторов (радиация, эстрогены) может оказывать наиболее повреждающее действие. Применение заместительной гормонотерапии с целью лечения патологического климакса и остеопороза также привело к увеличению риска развития рака молочной железы. Существуют также теории влияния избытка пролактина, дефицита мелатонина, надпочечниковых андрогенов, тиреоидной недостаточности на онкогенез рака молочной железы. К настоящему времени ни одна из них не доказана и не отвергнута.
Эстрогены не являются канцерогенами в классическом смысле этого слова — при присоединении этих гормонов к клеткам-мишеням опухоли происходит их активация и неконтролируемый рост. Более длительное и интенсивное воздействие эстрогенов на ткань органа происходит в следующих ситуациях: раннее менархе (до 13 лет), поздняя менопауза (более 55 лет), гинекологические заболевания (поликистоз яичников), позднее наступление 1-й беременности (после 30 лет), отсутствие беременности, количество детей менее 2. Такие факторы, как прерывание беременности, искусственное родоразрешение, отказ от естественного вскармливания вызывают дезадаптацию регуляторных процессов и создают условия для реализации действия условных канцерогенов.
Ионизирующая радиация. Женщины, которым многократно проводили рентгенологическое обследование грудной клетки в связи с туберкулёзом или проводили лучевую терапию на средостение, болели раком молочной железы значительно чаше. В Японии отмечали также увеличение частоты заболевания рак молочной железы среди выживших после атомных бомбардировок. Наибольший риск отмечен при облучении молочной железы в возрасте между 10 и 20 годами, что опять же указывает на высокую ≪уязвимость≫ к канцерогенным факторам не закончившей дифференцировку ткани железы.
Фактор питания. Многочисленные исследования установили связь между употреблением животных жиров и возникновением рака молочной железы, однако механизм влияния диеты на развитие рака неясен. Повышение риска возникновения рака молочной железы может быть обусловлено повышением синтеза эстрогенов в жировой клетчатке у женщин с избыточной массой тела. Включение в рацион продуктов с омега-3-полиненасыщенными жирными кислотами (льняное семя, орехи, рыба, ростки пшеницы, рапсовое масло и др.) способствует образованию продуктов, нейтрализующих токсины; профилактический эффект в отношении рака молочной железы доказан в опытах на животных. Овощи и фрукты содержат витамины и минералы, которые хорошо усваиваются, участвуют в метаболических процессах организма, выводят токсины. Эти продукты должны быть присутствовать в рационе ежедневно.
Учёт всех факторов, которые могут способствовать развитию рака молочной железы, вряд ли возможен и целесообразен, а отсутствие их не гарантирует от заболевания, поэтому в практической работе для оценки риска заболевания принято учитывать наиболее важные факторы:
• женский пол;
• раннее менархе (до 12 лет);
• позднее наступление менопаузы (после 55 лет);
• поздние первые роды (после 30 лет) и нерожавшие женщины;
• возраст старше 50 лет;
• атипическая гиперплазия ткани молочной железы;
• наличие семейного рака молочной железы (особенно рака у прямых родственниц в пременопаузе);
• мутации генов BRCA-1, BRCA-2;
• рак молочной железы в анамнезе.
Клиническая картина
По клинической картине РМЖ подразделяется на 3 основные формы: узловую, диффузную и атипические, характеризующиеся различным течением и прогнозом.
Клиническая классификация:
1. Узловая форма.
2. Диффузная форма:
2.1. Отечно-инфильтративная.
2.2. Маститоподобная.
2.3. Рожистоподобная.
2.4. Панцирная.
3. Атипические формы:
3.1. Рак Педжета.
3.2. Рак из придатков кожи.
3.3. Двусторонний рак.
3.4. Эктопированный рак.
3.5. Мультицентрический рак.
Узловая форма
Локальный рост в виде узла встречают наиболее часто. Пальпаторно выявляют плотное, округлое, бугристое безболезненное образование с нечёткими контурами, нередко ограниченно подвижное из-за инфильтрации окружающих тканей. В случае расположения под соском и малых размерах опухоли первыми симптомами могут быть отклонение соска в сторону, его фиксация или втяжение. Иногда над опухолевым узлом происходит фиксация кожи (симптом площадки) или её втяжение (симптом умбиликации). Указанные явления происходят за счёт вовлечения в процесс связок Купера. Лимфатический отёк кожи (≪лимонная корка≫) — поздний симптом заболевания. Увеличение или уплотнение подмышечных лимфатических узлов даже при небольшой подвижной опухоли с чёткими контурами должно вызвать подозрение на рак молочной железы. При УЗИ характерно превышение высоты образования над шириной, неровные края, наличие акустической тени, неоднородная внутренняя структура.
При маммографии выявляют солидное образование с неровными, лучистыми (спикулообразными) краями, часто содержащее микрокальцинаты. Можно определять ≪дорожку≫ к соску или грудной мышце, инфильтрацию кожи, увеличенные подмышечные лимфатические узлы повышенной плотности и округлой формы.
Выявление скоплений микрокальцинатов по ходу протоков к соску может свидетельствовать о продолженном внутрипротоковом росте опухоли.
Отёчная форма
Отёчную форму характеризует диффузное утолщение и гиперемия кожи. Эхографическим признаком отёка железы может быть утолщение кожи. Рентгенологически можно определить опухолевый узел и типичные изменения мягких тканей в виде поперечной тяжистости. скоплений микрокальцинатов. Если при биопсии кожи выявляют раковые эмболы и отсутствует локализованная опухолевая масса, то при клинической классификации применяют категорию T4d (воспалительный рак), а при наличии опухоли, отёка железы и отсутствии раковых эмболов в коже — Т4Ь.
Рожистоподобный рак
Эту форму рака молочной железы сопровождает выраженная гиперемия кожи с неровными языкообразными краями, внешне напоминающими рожистое воспаление. Гиперемия может распространяться на грудную стенку. Чаше всего заболевание протекает остро, с высокой (до 40 °С) температурой тела. Течение злокачественное, опухоль быстро метастазирует в лимфатические узлы и отдалённые органы.
УЗИ и маммография малоэффективны. Данные УЗИ могут быть интерпретированы как характерные и для воспалительного процесса, а маммография затруднена в связи с невозможностью проведения полноценной компрессии железы. При дифференциальной диагностике с воспалительными заболеваниями молочной железы в любом сомнительном случае необходима биопсия ткани образования (предпочтительнее трепан-биопсия).
Маститоподобная форма
Молочная железа увеличена в объёме за счёт быстро растущей опухоли без чётких контуров. Кожа железы над опухолью покрыта розовыми пятнами (раковый лимфангит) или гиперемирована. В глубине пальпируют инфильтрат без признаков размягчения. Железа ограничена в подвижности. Часто наблюдают повышение температуры тела, хотя и не обязательно до высоких цифр. Не бывает лейкоцитоза. При тонкоигольной аспирационной биопсии — гнойного отделяемого нет или получают гнойно-геморрагическое содержимое.
В дифференциальной диагностике наиболее эффективна сцинтимаммография. УЗИ не информативно, маммография затруднена из-за технических проблем (невозможность компрессии железы) и высокой плотности ткани.
При панцирной форме наблюдается опухолевая инфильтрация всей молочной железы и кожи с переходом на грудную стенку. Появляется множество внутрикожных опухолевых узлов. Молочная железа сморщивается, деформируется. Эта форма является IV стадией отечно-инфильтративного РМЖ.
Рак Педжета
Локализованный рак соска и ареолы считают наиболее благоприятной формой рака молочной железы. Клинически проявляется в виде явлений мацерапии (экземы) и изъязвления соска. Больных нередко длительно наблюдают дерматологи. При медицинских осмотрах наличие корочки ошибочно расценивают как высохший секрет из протоков. При прогрессировавший заболевания сосок разрушается и на его месте возникает язвенная поверхность.
Довольно часто рак Педжета сочетается с инвазивной протоковой формой рака. В такой ситуации больная выявляет узел в железе, но не обращает внимания на изменения соска.
При поражении соска и ареолы УЗИ неинформативно. При маммографии можно выявитв микрокалвцинаты или перестройку структуры ткани железы под соском.
Скрытый (оккультный) рак
Первый клинический признак — увеличение поражённых метастазами подмышечных лимфатических узлов без определяемой клинически опухоли в самой железе. Зачастую больных долго лечат от лимфаденита ≪инфекционной≫ природы и они попадают к онкологу уже при появлении отдалённых метастазов.
При наличии увеличения подмышечных лимфатических узлов показано проведение УЗИ и маммографии, тонкоиголвной аспирационной биопсии лимфатических узлов под контролем УЗИ. Использование маммографии, КТ. МРТ, сцинтимаммографии позволяет выявить локализацию первичной опухоли.
При отсутствии данных за первичную опухоль в молочной железе показано выполнение хирургической биопсии подмышечных лимфатических узлов для проведения гистологического и гистохимического анализов.
Диагностика
Анамнез
Учитывая, что многие заболевания молочной железы имеют дисгормональный характер и тесным образом связаны с деятельностью различных органов, участвующих в выработке и метаболизме гормонов, сбор анамнеза не следует ограничивать только длительностью и характеристикой процессов в самой железе. При опросе необходимо выяснить наличие в семейном анамнезе рака молочной железы, характер менструальной функции, акушерский анамнез, длительность лактации, наличие заболеваний матки и яичников, состояние нервной, пищеварительной систем, щитовидной железы, приём гормональных препаратов. Следует оценить изменение симптомов в зависимости от фазы менструального цикла, физической нагрузки или психологических стрессов.
Жалобы пациенток обычно сводятся к неприятным ощущениям в груди (боль, покалывание, распирание), обнаружению патологических очагов в ткани железы, изменению кожных покровов и консистенции железы. При раке Педжета могут ощущаться боль, зуд, жжение с области соска. При расспросе следует выяснить начало появления симптомов, последовательность их возникновения, взаимосвязь с лактацией, беременностью, фазами менструального цикла, травмами, другими заболеваниями. Необходимо отметить степень эффективности лечения, если оно проводилось. При расспросе врач должен попытаться составить впечатление о тенденции развития длительного заболевания: прогредиентное с постепенным усугублением симптоматики (характерно для злокачественных опухолей) или волнообразное с периодами ремиссий (неопухолевые заболевания). Информация о самообследовании пациенток принимается с учетом того, что регулярное и методически правильное самостоятельное обследование молочных желез порой позволяет обнаружить патологические очаги меньшего диаметра, чем доступные для выявления врачом, впервые пальпирующим конкретную женщину.
Осмотр
Перед осмотром необходимо снять всю одежду с верхней части тела и обеспечить хорошее равномерное освещение. Положение тела пациентки — сначала стоя с опущенными руками, затем — с поднятыми до горизонтального или вертикального уровня. Цель осмотра – выявление асимметрии молочных желез, патологических изменений кожи и сосковоареолярного комплекса. Используют следующие приемы: сравнение уровня нижнего края железы, сравнение симметрии наружного контура желез, сравнение цвета, ширины, рельефа, фактуры покрова сосковоареолярных комплексов слева и справа. Обязательно следует оценить рисунок подкожных вен. Их расширение и сгущение на определенном участке может быть вызвано патологическим процессом в подлежащих тканях. Патологические изменения на коже определяют с указанием их характера: узелок, пятно, трещина, эрозия, язва, корочка; описывают размеры, цвет, поверхность, очертания, консистенцию. Отмечают наличие рубцов после перенесенных заболеваний и операций. Отдельно оценивают наличие или отсутствие отека верхней конечности.
 Пальпация
Пальпация
 Обязательное условие — отсутствие одежды на верхней половине тела. Положение пациентки — стоя с опущенными руками, затем — лежа на спине с приведенными руками. Для более детального обследования могут применяться другие положения рук. Ладонь врача образует единую плоскость с вытянутыми и сведенными 2–5 пальцами (рис.1). Ощупывание проводится кончиками пальцев. Цель пальпации — обнаружение участков ткани груди с измененной консистенцией. При этом ткань молочной железы прижимается к передней грудной стенке, перемещая одновременно соседние участки ткани между пальцами. Пальпацию лучше проводить с верхнее-наружного квадранта по часовой стрелке, заканчивая центральными квадрантами. После этого спине, с отведенными за голову руками, аналогично описанной ранее методике. При большом размере груди следует учитывать, что обследование нижних квадрантов более информативно в положении лежа. В случае значительного мастоптоза дистальную часть ощупывают, подкладывая ладонь врача к задней поверхности железы в качестве упора. Кроме молочной железы обязательно пальпируют лимфатические узлы подмышечной, подключичной и надключичной групп. Патологические очаги, обнаруженные при пальпации, описывают по следующим признакам: локализация, размер, консистенция, форма, очертания, смещаемость, состояние покрывающей кожи, болезненность. Например, в верхнее-наружном квадранте левой молочной железы имеется узловое образование 3 см в диаметре, плотноэластическое, неправильной формы, с нечеткими очертаниями, смещаемое относительно подлежащих тканей, покрытое неизмененной кожей, безболезненной, в левой подмышечной области у края большой грудной мышцы определяется лимфатический узел 1,5 см в диаметре, округлый, плотноэластический, безболезненный, смещаемый, с четкими очертаниями. Обязательный этап пальпации — попытка получения отделяемого из соска. Для этого как бы массируют ткань железы от периферии к центру, затем ареолу осторожно сдавливают 1 и 2 пальцами. Отмечается характер отделяемого: нативная или лизированная кровь, серозная жидкость, гной, молоко, мазеобразная субстанция.
Обязательное условие — отсутствие одежды на верхней половине тела. Положение пациентки — стоя с опущенными руками, затем — лежа на спине с приведенными руками. Для более детального обследования могут применяться другие положения рук. Ладонь врача образует единую плоскость с вытянутыми и сведенными 2–5 пальцами (рис.1). Ощупывание проводится кончиками пальцев. Цель пальпации — обнаружение участков ткани груди с измененной консистенцией. При этом ткань молочной железы прижимается к передней грудной стенке, перемещая одновременно соседние участки ткани между пальцами. Пальпацию лучше проводить с верхнее-наружного квадранта по часовой стрелке, заканчивая центральными квадрантами. После этого спине, с отведенными за голову руками, аналогично описанной ранее методике. При большом размере груди следует учитывать, что обследование нижних квадрантов более информативно в положении лежа. В случае значительного мастоптоза дистальную часть ощупывают, подкладывая ладонь врача к задней поверхности железы в качестве упора. Кроме молочной железы обязательно пальпируют лимфатические узлы подмышечной, подключичной и надключичной групп. Патологические очаги, обнаруженные при пальпации, описывают по следующим признакам: локализация, размер, консистенция, форма, очертания, смещаемость, состояние покрывающей кожи, болезненность. Например, в верхнее-наружном квадранте левой молочной железы имеется узловое образование 3 см в диаметре, плотноэластическое, неправильной формы, с нечеткими очертаниями, смещаемое относительно подлежащих тканей, покрытое неизмененной кожей, безболезненной, в левой подмышечной области у края большой грудной мышцы определяется лимфатический узел 1,5 см в диаметре, округлый, плотноэластический, безболезненный, смещаемый, с четкими очертаниями. Обязательный этап пальпации — попытка получения отделяемого из соска. Для этого как бы массируют ткань железы от периферии к центру, затем ареолу осторожно сдавливают 1 и 2 пальцами. Отмечается характер отделяемого: нативная или лизированная кровь, серозная жидкость, гной, молоко, мазеобразная субстанция.
Целесообразно провести пальпацию щитовидной железы, поскольку значительная часть дисгормональных состояний связана с нарушениями её функции.
Ультразвуковое исследование
Ультразвуковое исследование (УЗИ) ткани молочной железы позволяет обнаруживать патологические очаги более 3–4 мм. Метод относительно дешев, прост и неинвазивен. Эхоскопия более надежно выявляет образования в железистой части органа и в ткани с повышенной плотностью. УЗИ позволяет дифференцировать полостные и солидные очаги. Типичные эхоскопические признаки злокачественного роста: гипоэхогенное образование с нечеткими очертаниями, неоднородной эхо-структурой, включением микрокальцинатов. Под контролем эхо-датчика можно выполнять инвазивные процедуры: пункции, аспирации, введение препаратов и т.п. Кроме молочной железы этим методом обследуют органы-объекты регионарного и отдаленного метастазирования: лимфатические узлы подмышечной ямки, шеи, забрюшинного пространства, печень. Относительные недостатки метода: около 20 % узлов имеют изоэхогенную плотность и с трудом обнаруживаются при УЗИ, поле датчика не может охватить весь объем ткани при большом размере железы и поверхностные образования, получаемое изображение является плоскостным срезом, что затрудняет сравнительную диагностику.
Маммография
Рентгенологическое исследование на специально разработанных аппаратах — основной метод ранней диагностики рака молочной железы. Для повышения качества изображения и снижения лучевой нагрузки используют усиливающие экраны, компрессию железы. Стандартно выполняют снимки каждой железы в двух проекциях — вертикальной и косой (45°). При необходимости уточнения диагноза используют нестандартные укладки, местную компрессию, контрастные методы (дуктография).
В интерпретации маммограмм учитывают:
• асимметрию плотности и васкуляризации симметричных участков желёз;
• нарушения архитектоники железы;
• наличие опухолевидных образований: локализация, размер, плотность, форма, контуры;
• наличие микрокальцинатов;
• структуру и степень развития железистой ткани с учётом возраста и гормонального статуса;
• состояние кожи, соска и ретромаммарного пространства;
• наличие патологически изменённых лимфатических узлов.
Наиболее частая находка — микрокальцинаты и округлые образования различной плотности (чаще кисты, реже — солидные опухоли). Локальное скопление обызвествлений наиболее характерно для рака in siru, в то время как округлые образования и локальная перестройка структуры, асимметрия плотности и гиперваскуляризация характерны для инвазивного рака.
Другие методы
Дуктография (галактография) — метод введения в проток молочной железы контрастного вещества с последующими снимками с целью определения патологических образований. В клинической практике имеет значение в диагностике внутрипротоковых опухолей.
Компьютерная томография — позволяет выявлять патологические очаги в любой части железы, дифференцировать признаки злокачественного и доброкачественного роста, определять экстраорганное распространение опухоли, обнаруживать метастатические очаги в отдаленных анатомических зонах: головной мозг, кости, средостение.
Ультразвуковая компьютерная томография — способ диагностики опухолевого роста в молочной железе у молодых женщин, на фоне фиброзно-кистозной мастопатии, фиброаденоматоза, наличия имплантов или плотной ткани молочных желез.
Магниторезонансная томография — метод особенно перспективен в диагностике опухолевой патологии сосково-ареолярного комплекса, метастатического поражения головного мозга.
Радиоизотопное исследование — регистрация очагов накопления радиофармпрепарата в ткани железы (сцинтимаммография) или костях. В опухолевых очагах более интенсивно фиксируется 99Тс. Метод используется для топической диагностики первичной опухоли и выявления метастазов.
Термография — определение локальной температуры ткани молочной железы. В практической онкологии почти не используется.
Пневмоцистография — введение газа в просвет кисты с последующей рентгенографией. Позволяет выявлять внутрикистозные разрастания.
Тонкоигольная аспирационная биопсия
Тонкоигольная аспирационная биопсия — наиболее простой способ получения материала для цитологического исследования в амбулаторных условиях, не требует анестезии. При наличии кист данная процедура может служить лечебным мероприятием.
Трепан-биопсия
Использование специальной иглы позволяет получить необходимое количество ткани для гистологического изучения характера патологического процесса, включая дифференциальную диагностику инвазивного рака и поражений in situ, степень дифференпировки опухоли, наличие в ней рецепторов эстрогенов, прогестеронов. Этот метод также применяют амбулаторно, однако он уже требует местной анестезии. При непальпируемых опухолях, микрокальцинатах введение иглы проводят под контролем УЗИ или маммографии (стереотаксическая биопсия).
Биопсия
Хирургическую, или эксцизионную, биопсию следует выполнять при подозрении на рак молочной железы, если при тонкоигольной аспирапионной биопсии и трепан-биопсии не удалось подтвердить (исключить) ЗН. При непальпируемых патологических образованиях,
требующих биопсии, для ориентира хирурга участок, подлежащий удалению, маркируют, подводя к нему иглу с мандрен-фиксатором под контролем УЗИ или маммографии. В таких случаях чаше требуется госпитализация больной, как правило, общая анестезия, срочное гистологическое исследование удалённого препарата и при необходимости расширение объёма операции вплоть до мастэктомии. Возможное расширение объёма операции при раке требуется обсудить с больной и получить её письменное согласие до выполнения биопсии.
Дата: 2019-03-05, просмотров: 364.