Сущность метода. При нагревании крахмала в концентрированной соляной кислоте он расщепляется по эфирным связям (связь между монозами) с образованием "осколков" разной величины – декстринов. Последние различаются между собой молекулярной массой и характером окраски при действии на них раствором йода.
Гидролиз идет по следующей схеме:
Крахмал + ]2 --- синее окрашивание
Амилодекстрины + ]2 ----- сине-фиолетовое окрашивание
Эритродекстрины + ]2 ---- красно-бурое окрашивание
Ахродекстрины----- не дают окраски
Мальтодекстрины----- не дают окраски
Мальтоза----- не дает окраски
Глюкоза----- не дает окраски
Опыт 1. Гидролиз крахмала в концентрированной соляной кислоте (контрольный опыт)
Реактивы: 1)Крахмал 1 % раствор
2)Реактив Фелинга
3)Соляная кислота, конц.
4)Раствор Люголя
5)Лакмусовая бумага
6)Гидроксид натрия 10 % раствор
Оборудование: 1)Пробирки
2)Пипетка
Порядок выполнения работы
В пробирку наливают 10 мл раствора крахмала и несколько капель концентрированной соляной кислоты. Перемешивают, кипятят на открытом огне. Через 1-2 мин после начала кипения берут пробу для реакции с йодом (несколько капель раствора пипеткой). Пробу выливают в пробирку, в которой налито 5-6 мл дистиллированной воды, а затем приливают 1-2 капли раствора Люголя.
Появившееся сине-фиолетовое окрашивание указывает на наличие в растворе амилодекстринов. Пробирку с раствором крахмала кипятят еще 1-2 минуты и снова проводят такую же пробу с йодом; появляется красно-бурое окрашивание от присутствия эритродекстринов. Пробирку с раствором снова кипятят и через 2-3 минуты повторяют опыт с йодом.
Крахмал через ахродекстрины, мальтодекстрины и мальтозу расщепляется до глюкозы. Реакция с йодом будет отрицательная – жидкость окрашивается в желтый цвет за счет окраски раствора Люгаля.
Гидролизат крахмала нейтрализуют по лакмусовой бумаге раствором гидроксида натрия, прибавляют реактив Фелинга и нагревают. Выпавший желтый осадок гидроксида меди (I) или красный оксида меди (I), укажет на присутствие в растворе продуктов гидролиза, обладающих восстановительными свойствами.
Сделайте выводы. Напишите уравнения реакций.
Опыт 2. Гидролиз крахмала в уксусной кислоте
Реактивы: 1) Крахмал 1 % раствор
2) Реактив Фелинга
3) Уксусная кислота, 6 % раствор
4) Универсальный индикатор
5) Лакмусовая бумага
6) Гидроксид натрия 10 % раствор
Оборудование: 1) Пробирки
2) Пипетка
Порядок выполнения работы
В пробирку наливают 10 мл раствора крахмала и добавляют 2 мл 6 % уксусной кислоты. Замеряют рН раствора универсальным индикатором.
Опыт проводят так же, как и опыт 1. Пробы на йод берут через 5-6 минут, т.к. гидролиз идет медленнее (слабая кислота).
Запишите наблюдения в лабораторный журнал. Сделайте выводы. Напишите уравнения реакции гидролиза и «цветной» реакции на глюкозу с реактивом Фелинга.
Опыт 3. Гидролиз крахмала пищевой содой
Реактивы: 1)Крахмал 1 % раствор
2)Реактив Фелинга
3)Гидрокарбонат натрия, кристаллический
4)Универсальный индикатор
5)Соляная кислота 0,1 н раствор
6)Гидроксид натрия 10 % раствор
Оборудование: 1)Пробирки
2)Пипетка
Порядок выполнения работы
В пробирку наливают 10 мл раствора крахмала и добавляют 0,2 г кристаллической пищевой соды. Соду растворяют встряхиванием, измеряют рН раствора. Далее гидролиз ведут как в опыте 1. Перед добавлением раствора йода пробу нейтрализуют несколькими каплями 0,1 н соляной кислоты.
Наблюдения занесите в журнал. Сделайте выводы. Напишите уравнения реакций.
1.6 КОНТРОЛЬНЫЕ ВОПРОСЫ:
1 При помощи каких реакций можно отличить альдозы от кетоз?
2 Что такое мутаротация? Каковы причины ее возникновения? Ответ иллюстрировать конкретными примерами.
3 Показать важнейшие способы получения производных аль-моноз (альдегидных форм).
4 На конкретных примерах показать способы, используемые для взаимопревращений альдоз в кетозы и обратно.
5 Написать общие формулы теоретически возможных дисахаридов, состоящих из остатков a-глюкозы.
6 Объяснить сущность инверсии сахарозы.
7 Написать схемы процессов окисления глюкозы: а) Аммиачным раствором оксида серебра, б) Реактивом Фелинга.
8 Написать структурные формулы целлобиозы по ее названию: 1–b–глюкозидо–4–b–глюкоза
9 Что такое эпимеризация моноз?
10 Превращения моноз в щелочной среде.
11 Вероятные реакции моноз с аминокислотами и белками при температуре больше 100°С.
12 Вероятные реакции моноз с пищевыми кислотами при температуре больше 100°С.
13 В чем заключается основное отличие животного крахмала от растительного?
14 Строение крахмала применение.
15 Вероятные реакции крахмала в кислой среде при температуре больше 100°С.
16 Строение клетчатки. Ее функции в пищеварении.
17 Что такое гемицеллюлоза, ее строение.
18 Пектиновые вещества. Строение. Их роль. Применение.
ВИТАМИНЫ
Общие сведения о витаминах
Витамины – низкомолекулярные органические вещества различной химической природы, объединяемых по признаку их строгой необходимости для питания животного и человеческого организма.
По сравнению с основными питательными веществами – белками, жирами и углеводами – витамины требуются в ничтожно малых количествах.
Слово “витамины” происходит от двух латинских слов: «vita», что означает «жизнь» и химического названия «amine», т.е. азотистые соединения. Основоположником учения о витаминах является русский ученый – врач Н.И. Лунин.
Основными поставщиками витаминов для человека является растительная и животная пища.
Установлено, что витамины входят в состав более 100 ферментов, тех могучих катализаторов химических превращений в организме. И, естественно ОТСУТСТВИЕ или НЕДОСТАТОК В ПИЩЕ ВИТАМИНОВ приводит к глубоким нарушениям обмена веществ и, в конечном счете, к заболеваниям, получившим название авитаминозы и гиповитаминозы.
Сейчас известно свыше тридцати соединений, относящихся к витаминам. Различают собственно витамины и витаминоподобные соединения.
К витаминоподобным относятся:
– биофлавоноиды (витамин Р),
– пангамовая кислота (витамин B 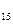 ),
),
– парааминобензойная кислота (витамин H 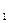 ),
),
– оротовая кислота (витамин B 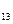 ),
),
– холин (витамин B 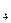 ),
),
– инозит (витамин B 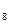 ),
),
– метилметионинсульфоний хлорид (витамин U),
– липоевая кислота, карнитин (витамин B 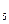 ).
).
Некоторые пищевые продукты содержат провитамины, т.е. соединения, способные в организме превращаться в витамины. Например, b-каротин (красящее вещество моркови) переходит в витамин А, эргостеролы (содержатся в дрожжах, в плесневых грибах, в пшеничном зерне) под действием ультрафиолетовых лучей превращаются в витамин Д в организме человека.
В процессе исследования химической природы и биологического действия витаминов был обнаружен ряд веществ, инактивирующих витамины и оказывающих на организм действие, противоположное действию витаминов. Такие вещества получили название антивитаминов. По своему строению они конкурируют с витаминами и могут занять их место в ферментных системах, но не в состоянии выполнять их функции. Например, стрептоцид – структурный аналог парааминобензойной кислоты; пантоилтаурин – аналог пантотеновой кислоты; пиритиамин – аналог тиамина, глюкоаскорбиновая кислота – аналог витамина С.
Так как химическая природа витаминов была открыта после установления их биологической роли, то их условное обозначение буквами латинского алфавита (А, В, С, Д и т.д.) сохранилось и до настоящего времени.
Рассмотрим строение и свойства наиболее важных витаминов.
Дата: 2019-03-05, просмотров: 550.