В современном тепловом оборудовании, связанном с превращениями вещества и энергии, важное место занимают объекты, создание и усовершенствование которых требуют термодинамического анализа.
Классический аппарат термодинамики часто оказывается недостаточным для решения задач повышения эффективности теплотехнического оборудования; необходимо не только его дальнейшее развитие, но и сопряжение с элементами системного подхода и экономики.
Под влиянием этих требований был разработан эксергетический метод.
Его основополагающая идея заключается во введении наряду с фундаментальным понятием энергии, дополнительного показателя эксергия, который позволяет учесть тот факт, что энергия в зависимости от внешних условий может иметь разную ценность для практического использования (например, одно и то же количество теплоты при различном температурном потенциале источников).
Расчеты балансов и различных характеристик технических систем с учетом эксергии дают возможность более просто и наглядно решать множество научных, технических и технико-экономических задач. Они помогают исключать ошибки, связянные с игнорированием качественной стороны энергетических превращений.
1.2 Физические основы понятия «эксергия»
1.2.1 Система и условия использования эксергетического метода
Под технической системой понимается теоретическая модель реального технического объекта, отражающая с той или иной степенью идеализации совокупность множества входящих в него элементов и связей между ними.
Эксергетические методы используют для анализа и оптимизации технических систем, работа которых происходит в условиях взаимодействия с независимым от системы окружением.
Эксергетический метод можно использовать для таких технических систем, в которых существенное место занимают энергетические превращения, изучаемые с применением ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ играет определяющую роль всегда. Т.е. в энергетических превращениях большое значение должны иметь такие, которые характеризуются отличной от нуля энтропией.
Поэтому механические, электрические технические системы, если процессы в них не соспровождаются существенными диссипативными эффектами, не изучаются методами термодинамического анализа, следовательно, и применение эксергетического метода для них не имеет смысла.
Эксергетический метод применяется для двух видов технических систем:
1) Предназначенных для пребразования энергии (теплосиловые, газотурбинные установки, ДВС, теплонасосные, холодильные, когенерационные установки, криогенные установки);
2) Предназначенные для преобразования вещества (химические, металлургические, пищевые производства).
Такое разделение условно, т.к. процессы преобразования вещества и энергии неразрвыно связяны друг с другом.
1.2.2 Виды энергии и их превращаемость
В процессах взаимного превращения энергии и вещества участвуют энергии разных видов.
Несмотря на их общность, отражаемую ПЕРВЫМ НАЧАЛОМ ТЕРМОДИНАМИКИ, существуют и ограничения превращаемости одного вида энергии в другой, определяемые ВТОРЫМ НАЧАЛОМ ТЕРМОДИНАМИКИ.
Поскольку эти ограничения имеют важнейшее значение для практики, все виды энергии делятся на 2 группы по признаку их превращаемости.
I группа энергий:
Виды энергий, которые полностью, без ограничений превращаются в любые другие виды энергии. Виды энергии I группы имеют энтропию, равную нулю: S = 0. Энергию таких видов наз. «организованной» или «безэнтропийной».
II группа энергий:
Виды энергий, которые не могут быть полностью преобразованы в любой др. вид энергии. Виды энергии II группы имеют энтропию отличную от нуля: S > 0. Энергию таких видов наз. «неорганизованной» или «энтропийной».
Согласно ВТОРОМУ НАЧАЛУ ТЕРМОДИНАМИКИ, в системе могут протекать только такие процессы преобразования энергии, в которых суммарная энтропия участвующих в нем тел или возрастает или (в обратимых процессах) остается постоянной (ΔS ≥ 0).
Следовательно, все виды «безэнтропийной» энергии (I группа) способны к любым превращениям, т.к. при любом превращении энергии энтропия будет либо возрастать либо оставаться постоянной.
Для видов энергии II группы однозначно невозможно превращение полностью в какой либо вид «безэнтропийной» энергии.
Любой вид «безэнтропийной» энергии, обладающий неограниченной превращаемостью, с технической точки зрения ценнее «качественнее», чем любой вид «энтропийной» энергии.
Это утверждение справедливо как для видов энергии, носителями которой являются транспортируемые тела (например, внутренняя энергия вещества – горячей воды), так и для видов энергии, находящихся в процессе перехода от одних тел к другим (тепло и работа любого вида).
Таблица 1.1 – Возможности взаимного преобразования видов энергии
| № п/п | 1. Механическая | 2. Электрическая | 3. Молекулярная | 4. Химическая | 6. Энергия в переходе - Теплота | 7. Энергия в переходе - Работа |
| ☺ | ☺ | ☺ | ☺ | ☺ | ☺ |
| ☺ | ☺ | ☺ | ☺ | ☺ | ☺ |
| ☻ | ☻ | ☺ | ☻ | ☺ | ☻ |
| ☻ | ☻ | ☺ | ☻ | ☺ | ☻ |
| ☺ | ☺ | ☺ | ☺ | ☺ | ☺ |
| ☻ | ☻ | ☺ | ☻ | ☻ | ☻ |
| ☺ | ☺ | ☺ | ☺ | ☺ | ☺ |
☺- Полное преобразование видов энергии I группы в энергию II группы;
☻- неполное преобразование.
Механическая, электрическая, ядерные (количество выделяющейся энергии при ядерных реакциях настолько велико, что энтропийной составляющей можно пренебречь) энергии и работа – относятся к I группе.
Молекулярная и химическая энергии, а также теплота – ко II группе. Все виды энергии I группы при взаимных преобразованиях полностью превращаются один в другой независимо от параметров окружающей среды.
В случае преобразования энергий II группы – чем меньше разность интенсивных параметров среды и рабочего тела технической системы – тем меньшая часть энергии может быть преобразована.
При равенстве параметров рабочего тела системы и окружающей среды – преобразование энергии невозможно.
1.2.3 Определение эксергии
Эксергия – является мерой, позволяющей оценить энергию (ее превращаемость) с учетом ее качественных характеристик.
Эксергия – это количество работы, которое может быть получено внешним приемником энергии при обратимом взаимодействии термодинамической системы или потока энергии с окружающей средой до установления полного равновесия.
Система, для анализа которой используется эксергетический метод, может быть простой (например, рабочее тело в замкнутом объеме) и сложной (энергетический агрегат, комплекс агрегатов, отрасль, регион).
Система может быть закрытой (без обмена веществ с внешней средой) и открытой (при существовании такого обмена).
Система может быть стационарной (с параметрами, не изменяющимися во времени) и нестационарной.
Эксергия системы определяется не только действием системы, но и одновременным действием окружающей среды (сосуд с газом, давление которого меньше атмосферного).
При полном равновесии системы и среды – эксергия равна нулю. Такое состояние системы наз. нулевым – в англояз. литературе мертвым состоянием.
Работа, которая согласно определению эксергии служит ее мерой, не обязательно является необходимым конечным результатом, т.е. целью действия анализируемой системы или потока энергии. Конечным результатом такого действия кроме работы могут быть преобразование и получение какого-либо вещества, теплоты, холода, излучения нужных параметров и т.д.
Поэтому в определении эксергии слово «работа» используется только как мера такой энергии, но не как обязательная конечная цель энергетических превращений.
Согласно ПЕРВОМУ и ВТОРОМУ НАЧАЛАМ ТЕРМОДИНАМИКИ в каждом данном сосотоянии эксергия системы, так же как и ее энергия, имеет определенное фиксированное значение, поскольку обратимый процесс выравнивания ее интенсивных параметров с параметрами окружающей среды однозначно характеризуется работой.
Взаимодействие системы с окружающей средой может проходить как обратимо (идеальный процесс), так и необратимо (реальный процесс).
В результате идеального процесса (по определению эксергии) получается работа, равная эксергии.
В реальном процессе работа меньше убыли эксергии (в пределе работа может быть равна нулю), т.к. часть ее не превращается в работу, а исчезает.
В этом сосотоит существенное отличие эксергии от энергии:
В любом процессе энергия подчинается закону сохранения.
Эксергия подчиняется закону сохранения только в обратимых процессах, в реальных процессах она может частично или полностью исчезать, теряться в результате диссипации энергии в необратимых процессах.
При прочих равных условиях чем меньше эта потеря эксергии, тем процесс более термодинамически совершенен, т.е. тем больше его термодинамическая эффективность.
Эксергетический баланс
Уравнение эксергетического баланса универсально и пригодно для любых термодинамических систем, независимо от видов энергии, участвующих в процессе:
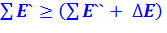 (1.1)
(1.1)
Или
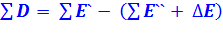 (1.1а)
(1.1а)
Здесь 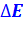 - приращение эксергии системы между начальной и конечной точками процесса;
- приращение эксергии системы между начальной и конечной точками процесса;
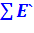 и
и 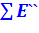 - суммарная эксергия в начальной и конечной точке процесса, соответственно;
- суммарная эксергия в начальной и конечной точке процесса, соответственно;
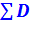 - суммарная потеря эксергии от необратимости процесса.
- суммарная потеря эксергии от необратимости процесса.
Для стационарного во времени процесса 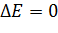 и
и 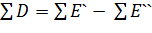 .
.
Соответствующее уравнение энергетического баланса:
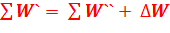 (1.2)
(1.2)
Здесь 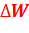 - приращение энергии системы между начальной и конечной точками процесса;
- приращение энергии системы между начальной и конечной точками процесса;
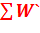 и
и 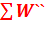 - суммарная энергия в начальной и конечной точке процесса, соответственно;
- суммарная энергия в начальной и конечной точке процесса, соответственно;
Принципиальная разница между уравнениями (1.1) и (1.2) состоит в том, что в (1.2) при любых условиях равенство правой и левой частей соблюдается, а в (1.1) левая часть в реальных процессах всегда больше правой.
Таким образом, энергетический балансне может отразить потери от необратимости процессов в рассматриваемой системе, т.к. независимо от степени ее совершенства уравнение (1.2) будет всегда справедливо.
Эксеретический баланс во всех случаях показывает потери от необратимости в системе. Степень ее термодинамического совершенства (эксергетический КПД) также определяется однозначно отношением:
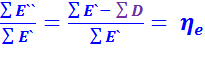 (1.3)
(1.3)
Термины «потери энергии» и «потери эксергии» имеют принципиально разное содержание.
«Потери энергии» - означает не потерю энергии вообще (Энергия не исчезает), а потерю ее для данной системы или данной цели, если часть энергии непригодна для нее по своей форме или параметрам.
«Потери эксергии» - означает полное исчезновение эксергии, т.е. ее уничтожение, связанное с диссипацией энергии.
В соответствии с методикой эксергетического анализа величины 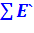 и
и 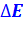 – включают эксергию тех видов вещества и энергии, которые входят в энергетический баланс рассматриваемой системы.
– включают эксергию тех видов вещества и энергии, которые входят в энергетический баланс рассматриваемой системы.
Как правило, это эксергия потока рабочего тела 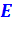 , эксергия теплового потока
, эксергия теплового потока 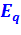 и работа L (равная энергии W для механической и электрической энергии).
и работа L (равная энергии W для механической и электрической энергии).
Дата: 2019-02-25, просмотров: 458.