Действием избытка триметилалюминия на диметилдигалогениды или монометилтригалогениды титана могут быть получены триметилхлорид и триметилбромид титана:
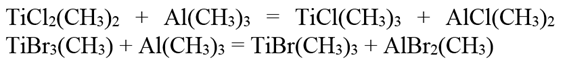
Триметилийодид титана образуется при реакции между тетраметилтитаном и йодтрифторидом углерода:
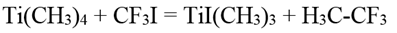
Триметилиодид титана представляет собой желтые иглообразные кристаллы; устойчив при низких температурах и в отсутствие кислорода.
Титантетраалкилы
Тетраметилтитан
Тетраметилтитан Ti(CH3)4 образуется при действии метиллития или метилгалогенида магния на тетрахлорид титана в эфирном растворе:
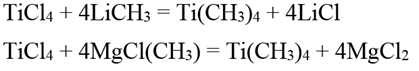
Тетраметилтитан представляет собой блестящие желтые иглообразные кристаллы. Может быть перегнан вместе с эфиром в вакууме при температуре ниже 0° С. Устойчив лишь при низких температурах; при температуре выше 0° С спонтанно разлагается с образованием черных пирофорных продуктов. При разложении тетраметилтитана в эфирном растворе первоначально желтая окраска переходит в зеленую, затем в черную; выделяется метан и, наконец, выпадает черный осадок, представляющий собой в основном диметилтитан Ti(CH3)2 с примесью элементарного титана и других продуктов. Диметилтитан диамагнитен. Термически он значительно более устойчив, чем тетраметилтитан: разлагается при нагревании до 250°С с выделением углеводородов (в основном метана) и образованием смеси (возможно, твердого раствора) элементарного титана с диметилтитаном. Соляной кислотой диметилтитан разлагается с выделением водорода, метана и образованием трихлорида титана. При действии воды гидролизуется с образованием ортотитановой кислоты и метана:
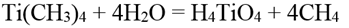
Кислородом тетраметилтитан легко окисляется. При действии галогенов, даже иода, легко разрушается с образованием тетрагалида титана и соответствующего галогенметана:
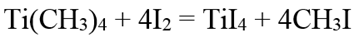
С тетрахлоридом титана дает метилтрихлорид титана:
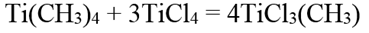
В предельных углеводородах тетраметилтитан растворяется без разложения и из гексана может быть перекристаллизован. В эфирном растворе со многими органическими соединениями азота и фосфора (амины, фосфины, гетероциклические соединения) тетраметилтитан образует нейтральные комплексы в виде кристаллов желтого или красного цвета. Все эти комплексы очень неустойчивы и разлагаются при температуре около 0°С.
Тетраэтилтитан
Тетраэтилтитан Ti(C2H5)4 образуется при действии этиллития на этилтрихлорид титана в эфирном или гексановом растворе:
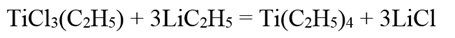
Тетраэтилтитан представляет собой оранжево-желтые кристаллы. Он чрезвычайно неустойчив и при выделении из раствора, даже при низкой температуре, моментально разлагается.
Тетрапропилтитан
Тетрапропилтитан Ti(C3H7)4 образуется при действии пропиллитня на пропилтрихлорид титана в гексановом растворе:
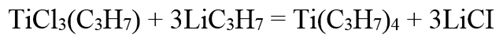
Титанциклоалкадиенилы
Для переходных элементов характерно образование π-комплексов. Не является исключением и титан. Он образует циклопентадиенильные, индиенильные и циклогептатриенильные соединения. Эти соединения построены по типу ферроцена, в них связь атома титана с лигандом осуществляется за счет взаимодействия π-электронов лиганда с 3d-орбиталями титана. Имеет место обобщенная связь металла с лигандом, например, циклопентадиенильным кольцом. Все кольцо циклопентадиена равномерно присоединено к атому титана, а не посредством связи металла с каким-то одним углеродом кольца. Такие структуры являются π-комплексами и получили название металлоценов (для титана — титаноценов). Эти соединения значительно устойчивее и менее реакционноспособны по сравнению с титанорганическими соединениями с σ-связью Ti—С.
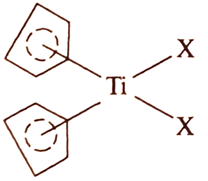
На рис. 1 представлена структура бис(циклопентадиенильного) производного титана.
Рис. 1. Структура бис-(циклопентадиенильного) производного титана, где X=Hal, OR; R=Alk, Аг
Дата: 2019-02-19, просмотров: 384.