4) CaCl2
Повышение температуры кипения раствора по сравнению с чистым растворителем является следствием
1) Понижения давления пара над раствором
64. Суть сольватной теории растворов состоит в том, что…
3) между частицами растворенного вещества и молекулами растворителя происходит взаимодействие с образованием сольватов
65. Изменение энергии Гиббса ( D G ) равно нулю при образовании ___
1) Разбавленных растворов
66. Согласно современным представлениям образование растворов является процессом
3) Физико-химическим
67. Раствор этилового спирта в воде не подчиняется закону Рауля, потому что спирт ___
2) летучая жидкость
68. Осмотическое давление раствора глюкозы с молярной концентрацией 0,1 моль/л при 25 ° С равно _____ кПа.
4) 247,6
69. Молярная масса неэлектролита, раствор 9,2 г которого в 400 г воды замерзает при –0,93 °С 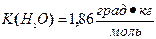 , равна _____ г/моль.
, равна _____ г/моль.
3) 46
70. Мольная доля растворенного вещества может быть выражена в …
Процентах
71. Молярная масса вещества, при растворении 2,3 г которого в 100г воды, температура кипения раствора относительно температуры кипения воды повышается на 0,26 градуса(k=0,52 град×кг/моль), составляет
3) 46
72. 500 см3 водного раствора, содержащего 106 г Na2CO3, разбавили дистилированной водой в 2 раза. Молярная концентрация карбоната натрия в полученном растворе составляет____ моль/л
3) 1
73. Водный раствор неэлектролита замерзает при -1,860С. Концентрация вещества в растворе составляет _____ моль/кг. (КН2О=1,86 град×кг/моль)
3) 1
74. В 500 см3 растворили 105 г фторида натрия. Моляльность раствора составляет_____ моль/кг
2) 5
75. После растворения нелетучего вещества в растворителе при температуре 200С давление насыщенного пара растворителя над раствором…
3) понижается
76. К 250 г раствора, содержащего 25 г сульфата калия, добавили 250 см3 дистиллированной воды. Массовая доля растворённого вещества в растворе…
2) уменьшилась в 2 раза
Что произойдёт с эритроцитами крови при помещении их в гипертонический раствор NaCl?
1) плазмолиз
78. Каким является по отношению к физиологическому раствору, раствор глюкозы с массовой долей 10%.
2) гипертоническим
При какой температуре замерзает раствор глюкозы по сравнению с водой?
4) ниже 00С
В основе, какой болезни лежит закон Генри?
2) кессонная болезнь
81) Растворимость газа в растворе с увеличением концентрации электролитов:
2) понижается
ПРОТОЛИТИЧЕСКИЕ ПРОЦЕССЫ. БУФЕРНЫЕ РАСТВОРЫ. ГИДРОЛИЗ.
1. Сокращенное молекулярно-ионное уравнение Ва+2+SO42-=BaSO4 соответствует реакции…
3) BaCl2+Na2SO4®
2. Полному гидролизу подвергаются соли…
2) Al2(SO4)3 3) Cr2S3
3. Нейтральную среду имеют растворы солей …
1) RbNO3 3) BaCl2
4. Кислую среду имеют растворы солей…
2) AlCl3 3) (NH4)2SO4
5. При разбавлении раствора степень диссоциации слабого электролита…
1) увеличивается 6. Сильными электролитами являются …
1) HI 2) СН3СООН 3) NH4OH 4) Ca3(PO4)2
7. Отношение числа молекул, диссоциирующих на ионы, к общему числу молекул растворенного вещества, называется _____ диссоциации.
2) степенью
8. В водном растворе гидролизу не подвергаются соли…
2) K2SO4 4) NaNO3
Среда водного раствора хлорида аммония
2) кислая
Диссоциация по трем ступеням возможна в растворе
4) ортофосфорной кислоты
11. Ионы I-образуются при диссоциации
2) KI
Лакмус краснеет в растворе соли
1) FeSO4
13. Вещество, при диссоциации которого образуются ионы Na+, H+, а также анионы SO42- является
4) кислой солью
Кислую среду имеет водный раствор
4) хлорида алюминия
15. Сокращенное ионное уравнение Fe2+ + 2OH- = Fe(OH)2 соответствует взаимодействию веществ:
2) FeSO4 и LiOH
16. Сокращенное ионное уравнение Ba2+ + SO42-- = BaSO4 соответствует взаимодействию веществ:
1) BaCI2 и K2SO4
Среда водного раствора сульфата алюминия
2) кислая
Наиболее слабым электролитом является
1) HF
19. В качестве анионов только ионы ОН- образуются при диссоциации
3) NaOH
Щелочную среду имеет водный раствор
4) сульфита натрия
Одновременно не могут находится в растворе все ионы ряда
4) Ba2+, Cu2+, OH-, F-
Дата: 2018-12-28, просмотров: 1023.