Лекция №23
Лечение лептоспироза, бруцеллеза. Противоэпидемические мероприятия в очаге инфекции
Бруцеллёз
Бруцеллёз (лихорадка мальтийская, лихорадка гибралтарская, лихорадка средиземноморская, лихорадка ундулирующая, болезнь Банга, болезнь Брюса, мелитококкоз, мелитококция) — зоонозная инфекционная болезнь с многообразными механизмами передачи возбудителя, характеризующаяся лихорадкой, поражением опорно-двигательного аппарата, нервной системы, половых органов.
Коды по МКБ -10
A23. Бруцеллёз.
A23.0. Бруцеллёз, вызванный Brucella melitensi.
A23.1. Бруцеллёз, вызванный Brucella abortus.
A23.2. Бруцеллёз, вызванный Brucella suis.
A23.3. Бруцеллёз, вызванный Brucella canis.
A23.8. Другие формы бруцеллёза.
A23.9. Бруцеллёз неуточнённый.
Этиология бруцеллеза
Возбудители — представители рода Brucella семейства Brucellaceae. Бруцеллёз человека может быть обусловлен четырьмя видами бруцелл: B. melitensis, В. abortus, В. suis и B. canis. Наиболее частая причина болезни — Brucella melitensis. Основные хозяева — овцы и козы. Несколько реже встречаются Brucella abortus; основной хозяин — крупный рогатый скот. У третьего вида бруцелл, Brucella suis, выделяют 4 биотипа. Основные хозяева — свиньи, зайцы и северный олень. Относительно редко диагностируют заболевание, обусловленное Brucella canis. Основной хозяин данного микроорганизма — собаки.
Они неподвижны, спор не образуют, жгутиков не имеют, грамотрицательны. Растут медленно на сложных питательных средах. Бруцеллы — внутриклеточные паразиты, они антигенно однородны, содержат эндотоксин.. Бруцеллы устойчивы в окружающей среде. В воде сохраняются свыше 2 мес, в молоке — 40 дней, в брынзе — 2 мес, в сыром мясе — 3 мес, в засоленном мясе — до 30 дней, в шерсти — до 4 мес. При кипячении погибают мгновенно, чувствительны к дезинфицирующим средствам, к антибиотикам тетрациклиновой группы, аминогликозидам, рифампицину, эритромицину.
Эпидемиология бруцеллеза
Резервуар и источник возбудителя — домашние животные. Хотя к бруцеллёзу чувствительны дикие животные, природных очагов инфекции нет.
Человек заражается от больных животных контактным, алиментарным, редко — аэрогенным путём. Заражение контактным путём носит профессиональный характер. Часто заражаются ветеринарные работники, телятницы, чабаны и др. Заражение может наступить и при контакте с мясом инфицированных животных. Алиментарное заражение часто происходит при употреблении непастеризованного молока или приготовленных из него продуктов .
Аэрогенное заражение возможно при попадании в дыхательные пути пыли, содержащей бруцеллы , а также в лабораториях при нарушении техники безопасности. Этот путь инфицирования наблюдают относительно редко. Чаще заболевают лица трудоспособного возраста (18–50 лет). Восприимчивость высокая. Инфицирующая доза составляет всего от 10 до 100 микробных тел. Постинфекционный иммунитет ненапряжённый, через 5–6 лет возможна реинфекция.
Патогенез бруцеллеза
Входные ворота инфекции — микротравмы кожи, слизистые оболочки органов пищеварения и респираторного тракта. В месте внедрения возбудителя изменений не наблюдают. По лимфатическим путям бруцеллы достигают регионарных лимфатических узлов, но и здесь выраженные изменения отсутствуют. Размножение и накопление бруцелл происходит преимущественно в лимфатических узлах, из которых они периодически поступают в кровь, а гибель сопровождается освобождением эндотоксина, вызывающего лихорадку, поражение вегетативной нервной системы. С кровотоком возбудитель разносится по всему организму, концентрируясь в органах и тканях, богатых макрофагами (печень, селезёнка, мышцы, фасции, суставные сумки, сухожилия), где вследствие незавершённого фагоцитоза длительно сохраняется, вызывает воспалительную реакцию с образованием специфических гранулём.
Для бруцеллёза характерна выраженная аллергическая перестройка организма, резко выражена ГЗТ, сохраняющаяся длительное время даже после освобождения организма от возбудителя. Аллергия играет большую роль в формировании вторичных очагов инфекции. Бруцеллёз отличается склонностью к хроническому течению, что связано с длительным персистированием бруцелл в организме. До введения в лечебную практику антибиотиков бруцеллы сохранялись в организме до двух лет, более длительное течение болезни связано с влиянием антибиотиков: часть бруцелл может переходить в L-формы и длительно сохраняется внутриклеточно.
Диагностика бруцеллеза
В соответствии с «Федеральными стандартами объёма медицинской помощи при диагностике бруцеллёза» используют следующие стандарты обследования: общий анализ крови, мочи (в динамике два раза), кал на яйца глистов, биохимическое исследование крови (концентрация билирубина, активность АЛТ, АСТ), кровь на Brucellae spp., анализ крови на реакцию Райта, Хеддлсона, РПГА с бруцеллёзным эритроцитарным диагностикумом, реакция Кумбса (в динамике два раза), проба Бюрне, ЭКГ, УЗИ внутренних органов, рентгенография позвоночника, суставов, консультация врача-офтальмолога, невролога (по показаниям).
При диагностике бруцеллёза учитывают эпидемиологические предпосылки. Во многих районах средней полосы и юго-запада России у животных бруцеллёз давно уже ликвидирован — следовательно, условия для заражения людей отсутствуют. В этих регионах бруцеллёз — «завозная» инфекция. Необходимо уточнить пребывание в местах, где бруцеллёз ещё встречают. Но иногда заражение происходит через продукты, инфицированные бруцеллами (брынза домашнего изготовления, молоко и др.).
Лабораторное подтверждение бруцеллёза ограничено, поскольку бруцеллы относятся к опасным возбудителям. Их выделение можно проводить только в специальных лабораториях, оборудованных в соответствии с требованиями профилактики. При серологических и аллергологических исследованиях необходимо учитывать, что у привитых против бруцеллёза (прививают группы риска, профессионально контактирующие с животными) довольно долго могут быть положительными результаты и серологических реакций, и особенно аллергических проб.
Из серологических реакций наиболее информативна РА (реакция Райта). Агглютинацию на стекле (реакция Хеддлсона) для диагностики не используют. Она предложена для выявления лиц, подлежащих обследованию на бруцеллёз, при массовых обследованиях по эпидемиологическим показаниям. Реакция Хеддлсона часто даёт ложноположительные результаты. В определённой степени это связано с перекрёстными реакциями с рядом антигенов (иерсинии, возбудитель туляремии, противохолерная вакцинация и др.). Следует учитывать, что В. melitensis и В. аbortus имеют перекрёстные реакции между собой, но не с В. canis, так что для выявления антител к этой бруцелле необходим специальный диагностикум, который пока ещё не выпускают. Возможно, это одна из причин того, что данную разновидность бруцеллёза выявляют редко.
При остросептической форме бруцеллёза антитела можно определить на 2-й неделе болезни, в дальнейшем титр их нарастает. Аллергическая проба становится положительной в конце первой и на 2-й неделе. При хронических формах нарастания титра антител часто не обнаруживают. Следует учитывать, что постановка аллергической пробы (проба Бюрне) может спровоцировать появление антител или нарастание их титра. Другие серологические реакции: РПГА, острофазовые реакции — менее информативны по сравнению с реакцией Райта и не имеют существенного значения. В последние годы применяют более чувствительный метод ИФА для определения IgG- и IgM-антител. Отрицательные результаты пробы Бюрне позволяют исключить бруцеллёз (кроме ВИЧ-инфицированных, у которых исчезают все реакции ГЗТ).
Примерная формулировка диагноза
А23.9. Хронический бруцеллёз, комбинированная форма (локомоторная + уро- генитальная), стадия субкомпенсации.
Лечение бруцеллеза
Принципы и методы терапии бруцеллёза зависят от его клинической формы. В соответствии с «Федеральными стандартами объема медицинской помощи, оказываемой больным бруцеллёзом» длительность госпитализации составляет 26 дней для больных острым бруцеллёзом и 30 дней — хроническим. Комплекс лечения включает антибактериальную терапию, нестероидные противовоспалительные средства (НПВС), глюкокортикоиды, десенсибилизирующую, дезинтоксикационную, вакцино-, иммуно-, физиотерапию и санаторно-курортное лечение.
Антибактериальную терапию проводят при остросептической и других формах болезни при наличии лихорадочной реакции. Продолжительность лечения составляет 1,5 мес.
Рекомендуют одну из схем:
Доксициклин внутрь по 100 мг два раза в сутки + стрептомицин в/м по 1 г/сут (первые 15 дней);
Доксициклин внутрь по 100 мг два раза в сутки + рифампицин внутрь по 600– 900 мг/сут в 1–2 приёма;
Ко-тримоксазол внутрь по 960 мг два раза в сутки + рифампицин внутрь по 600 мг 1–2 раза в сутки или стрептомицин в/м по 1 г один раз в сутки.
Эффективны также комбинации доксициклина с гентамицином и рифампицина с офлоксацином.
В связи с высокой эффективностью антибиотиков вакцинотерапию применяют редко. Используют лечебную бруцеллёзную вакцину.
Лечебная бруцеллёзная вакцина — взвесь бруцелл овечьего и бычьего вида, инактивированных (для внутрикожного введения) либо убитых нагреванием (для внутривенного введения), выпускается в ампулах с точным указанием количества микробных клеток в 1 мл. Стандартная концентрация лечебной бруцеллёзной вакцины — 1 млрд микробных клеток в 1 мл вакцины. Рабочая концентрация предусматривает 500 тыс. микробных клеток в 1 мл.
Наибольшее распространение получило подкожное и внутрикожное введение вакцины. Подкожно вакцину назначают при декомпенсации процесса и при выраженной клинической симптоматике. Важный принцип вакцинотерапии — индивидуальный подбор дозы препарата. О выраженности реакции судят по интенсивности пробы Бюрне. Подкожное введение чаще начинают с 10–50 млн микробных клеток. Если местная и общая реакция отсутствуют, то вакцину в увеличенной дозе вводят уже на следующий день. Для лечения подбирают такую дозу, которая вызывает умеренную реакцию. Следующую инъекцию вакцины делают лишь после того, как исчезнет реакция на предыдущее введение вакцины. Разовую дозу в конце курса доводят до 1–5 млрд микробных клеток.
Внутрикожная вакцинотерапия более щадящая. Этот метод используют в стадии компенсации, а также при переходе заболевания в латентную форму. По выраженности кожной реакции подбирают рабочее разведение вакцины (оно должно вызвать местную реакцию в виде гиперемии кожи диаметром 5–10 мм). Вакцину вводят внутрикожно в ладонную поверхность предплечья в первый день по 0,1 мл в три места, затем каждый день прибавляют по одной инъекции и доводят на 8-й день до 10 инъекций. Если реакция на вакцину уменьшается, используют меньшее разведение.
Следует учитывать, что даже при полном исчезновении всех клинических проявлений у 20–30% больных бруцеллёзом в дальнейшем может наступить обострение болезни.
С целью десенсибилизации при всех формах бруцеллёза применяют антигистаминные препараты (хлоропирамин, мебгидролин, прометазин). При поражении опорно-двигательного аппарата (артрит, полиартрит) показаны НПВС: диклофенак, ибупрофен, индометацин, мелоксикам, нимесулид и др. При неэффективности НПВС их сочетают с глюкокортикоидами (преднизолон, дексаметазон, триамцинолон) в средних терапевтических дозах (30–40 мг преднизолона перорально) со снижением дозы через 3–4 дня. Продолжительность курса лечения 2–3 нед. Глюкокортикоиды показаны также при поражении нервной системы, орхитах.
Хронические формы болезни, протекающие с обострением, при наличии изменений в иммунном статусе указывают на иммуносупрессию. Это показание к назначению иммуномодуляторов (имунофан, полиоксидоний и др.). При поражениях опорно-двигательного аппарата и периферической нервной системы рекомендуют физиотерапию (индуктотерапия, электрофорез новокаина, лидазы, димексида; ультравысокочастотная терапия, ионогальванотерапия, применение озокерита, парафиновых аппликаций, массаж, лечебная гимнастика и др.).
После того как признаки активности процесса изчезают, назначают бальнеотерапию. Преимущество отдают местным курортам. При нейровегетативных нарушениях показаны гидрокарбонатные, гидросульфатно-сероводородные, радоновые воды. При поражениях опорно-двигательного аппарата и периферической нервной системы эффективна грязетерапия.
Прогноз
Прогноз для жизни благоприятный. При адекватном лечении обычно наступает полное выздоровление. При остром неосложнённом бруцеллёзе клинические симптомы исчезают через 2–3 нед, однако лечение следует продолжать в течение 6 нед и более. Рецидивы заболевания возникают в 5% случаев. Летальные исходы редки. Возможна инвалидизация в результате тяжёлых поражений опорно-двигательного аппарата и ЦНС.
Профилактика бруцеллеза
Основное направление — профилактика бруцеллёза у сельскохозяйственных животных: предупреждение заноса в благополучные хозяйства, систематические обследования и выбраковка больных животных в неблагополучных хозяйствах, вакцинация животных, гигиеническое содержание и дезинфекция помещений, в которых находятся животные. Лица, ухаживающие за ними, должны носить спецодежду, систематически обследоваться на бруцеллёз. Обязательны пастеризация молока, выдерживание брынзы не менее 2 мес, а твёрдых сыров — 3 мес. Работникам животноводства (а по показаниям — населению неблагополучных районов) вводят бруцеллёзную сухую живую вакцину (надкожно в объёме 2 капель или подкожно — 5 мл). Ревакцинацию проводят в половинной дозе через 10–12 мес.
Лептоспироз
Лептоспироз (болезнь Васильева–Вейля, инфекционная желтуха, японская 7-дневная лихорадка,, водная лихорадка, иктерогеморрагическая лихорадка и др.) — острая зоонозная природно-очаговая инфекционная болезнь с преимущественно водным путём передачи возбудителя, характеризующаяся общей интоксикацией, лихорадкой, поражением почек, печени, ЦНС, геморрагическим диатезом и высокой летальностью.
Коды по МКБ -10
А27.0. Лептоспироз желтушно-геморрагический.
А27.8. Другие формы лептоспироза.
А27.9. Лептоспироз неуточнённый.
Этиология лептоспироза
Род Leptospira (лептоспира) семейства Leptospiraceae представлен двумя видами: паразитическим — L. interrogans и сапрофитным — L. biflexa. Оба вида подразделяют на многочисленные серотипы. В основу классификации лептоспир положено постоянство их антигенной структуры. На сегодняшний день известно 25 серо- групп, объединяющих около 200 патогенных серотипов лептоспир.
Возбудитель лептоспироза человека и животных относят к виду L. interrogans. Наибольшую роль в структуре заболеваемости имеют серогруппы L. interrogans icterohaemorragiae, поражающая серых крыс, L. interrogans pomona, поражающая свиней, L. interrogans canicola — собак, а также L. interrogans grippotyphosa, L. interrogans hebdomadis.
Лептоспиры — тонкие, подвижные микроорганизмы спиралевидной формы длиной от нескольких до 40 нм и более и диаметром от 0,3 до 0,5 нм.
Лептоспиры грамотрицательны. Это строгие аэробы. Факторы патогенности лептоспир — экзотоксиноподобные вещества, эндотоксин, ферменты (фибринолизин, коагулаза, липаза и др.), а также инвазивная и адгезивная способность.
Лептоспиры чувствительны к воздействию высоких температур: кипячение их убивает мгновенно, нагревание до 56–60 °С — в течение 20 мин. К действию низких температур лептоспиры более устойчивы. Так, при –30–70 °С и в замороженных органах они сохраняют жизнеспособность и вирулентность (способность к заражению) в течение многих месяцев. Жёлчь, желудочный сок и кислая моча человека губительно действуют на лептоспиры, а в слабощелочной моче травоядных они остаются жизнеспособными в течение нескольких суток. В воде открытых водоёмов при слабощелочной или нейтральной её реакции лептоспиры сохраняются в течение 1 мес, а в сырой и переувлажнённой почве они не теряют патогенность до 9 мес. На пищевых продуктах лептоспиры сохраняются до 1–2 сут, а под воздействием ультрафиолета и при высушивании погибают в течение 2 ч. Лептоспиры чувствительны к препаратам пенициллина, хлорамфениколу, тетрациклину и чрезвычайно чувствительны к действию обычных дезинфицирующих средств, кипячению, солению и маринованию. При этом низкие температуры не оказывают губительного воздействия на лептоспиры. Этим объясняют их способность зимовать в открытых водоёмах и влажной почве, полностью сохраняя вирулентность.
Эпидемиология лептоспироза
Лептоспироз — одна из самых распространённых природно-очаговых инфекционных болезней.
Источник возбудителя инфекции — дикие, сельскохозяйственные и домашние животные. Роль отдельных видов животных как источника лептоспироза далеко не одинакова в связи с различной степенью чувствительности их к этим микроорганизмам и с характером ответной реакции на заражение. Животные, у которых в результате инфицирования возникает хронический лептоспироз, а в ряде случаев и бессимптомный процесс, сопровождаемый длительным выделением лептоспир с мочой, имеют наибольшее эпидемиологическое и эпизоотологическое значение. Именно эти животные обеспечивают сохранение лептоспир как биологического вида. Наибольшее значение в природных очагах лептоспироза отводят представителям отряда грызунов, а также насекомоядным (ежи, землеройки). Носительство лептоспир доказано почти у 60 видов грызунов, из которых 53 относят к семейству мышеобразных и хомякообразных.
Биологическая пластичность лептоспир обусловливает возможность адаптации их к сельскохозяйственным и домашним животным (крупный рогатый скот, свиньи, лошади, собаки), а также к синантропным грызунам (серые крысы, мыши), которые формируют антропургические очаги инфекции, представляющие основную опасность для человека.
С эпидемиологической точки зрения важна заболеваемость крупного и мелкого рогатого скота, а также свиней. Болеют животные любого возраста, но у взрослых лептоспироз протекает чаще в скрытой форме, а у молодняка — с более выраженными симптомами.
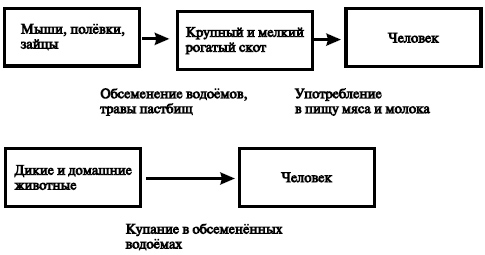
Человек не имеет значения в качестве источника инфекции.
Основной фактор передачи возбудителя лептоспироза — вода, загрязнённая выделениями (мочой) инфицированных животных. Непосредственными причинами заражения людей оказывается употребление сырой воды для питья, умывание из открытых водоёмов, купание в небольших слабопроточных прудах или переход их вброд.
Некоторое значение в передаче инфекции имеют и пищевые продукты, загрязнённые выделениями грызунов. Передача инфекции чаще всего происходит контактным путём, однако возможен и пищевой путь. Факторами передачи бывают и влажная почва, трава пастбищ, загрязнённые выделениями больных животных. Заражение может происходить при забое скота, разделке туш, а также при употреблении в пищу молока и термически не обработанного мяса. Зачастую лептоспирозом заболевают лица, имеющие профессиональный контакт с больными животными: ветеринары, дератизаторы и сельскохозяйственные работники. Для проникновения лептоспир достаточно малейших нарушений целостности кожного покрова.
Эпидемические вспышки лептоспироза происходят, как правило, в летне-осенний период. Пик заболеваемости приходится на август. Различают три основных типа вспышек: водный, сельскохозяйственный и животноводческий. Лептоспироз встречают и в виде спорадических случаев, которые могут регистрироваться в течение всего года.
Лептоспиры гидрофильны, поэтому для лептоспироза характерна высокая распространённость в областях, где много болотистых и сильно увлажнённых низменностей.
Естественная восприимчивость людей к лептоспирозной инфекции значительна. Постинфекционный иммунитет прочный, но типоспецифический, поэтому возможны повторные заболевания, вызванные другими сероварами возбудителя.
Патогенез лептоспироза
Возбудитель проникает в организм человека благодаря своей подвижности. Входными воротами служат микроповреждения кожных покровов и слизистых оболочек полости рта, пищевода, конъюнктивы глаз и др. Известны случаи лабораторного заражения лептоспирозом через повреждённую кожу. При внутрикожном проникновении в эксперименте на лабораторных животных лептоспиры проникают в кровь уже через 5–60 мин, очевидно, минуя лимфатические узлы, которые не выполняют барьерной функции при лептоспирозе. На месте внедрения возбудителя не возникает первичного аффекта. Дальнейшее распространение лептоспир происходит гематогенным путём, при этом лимфатические сосуды и регионарные лимфатические узлы также остаются интактными. С током крови лептоспиры попадают в различные органы и ткани: печень, селезёнку, почки, лёгкие, ЦНС, где происходят их размножение и накопление. Развивается первая фаза инфекции продолжительностью от 3 до 8 дней, что соответствует инкубационному периоду.
Вторая фаза патогенеза лептоспироза — вторичная бактериемия, когда количество лептоспир в крови достигает максимума и они ещё продолжают размножаться в печени и селезёнке, надпочечниках, обусловливая клиническое начало болезни. С током крови лептоспиры снова разносятся по всему организму, преодолевая даже ГЭБ. В этот период наряду с размножением лептоспир начинается их разрушение как следствие появления антител, агглютинирующих к четвёртому дню болезни и лизирующих лептоспиры. Накопление в организме продуктов метаболизма и распада лептоспир сопровождается лихорадкой и интоксикацией, что повышает сенсибилизацию организма и вызывает гиперергические реакции.
Эта фаза продолжается в течение 1 недели, однако может укорачиваться до нескольких дней. Максимальную концентрацию лептоспир к концу фазы лептоспиремии наблюдают в печени. Лептоспиры продуцируют гемолизин, который, оказывая влияние на мембрану эритроцитов, вызывает их гемолиз и высвобождение свободного билирубина. Кроме того, в печени развиваются деструктивные изменения с формированием воспаления и отёка ткани. При тяжёлом течении болезни основной фактор патологического процесса в печени — поражение мембран кровеносных капилляров, чем и объясняют наличие кровоизлияний и серозного отёка.
Патогенез желтухи при лептоспирозе носит двоякий характер: с одной стороны, распад эритроцитов вследствие токсического воздействия на мембраны гемолизина и гемолитического антигена, а также в результате эритрофагии клетками ретикулоэндотелиальной системы в селезёнке, печени и других органах, с другой — вследствие развивающегося паренхиматозного воспаления с нарушением желчеобразующей и выделительной функции печени.
Третья фаза патогенеза лептоспироза — токсическая. Лептоспиры гибнут вследствие бактерицидного действия крови и накопления антител, исчезают из крови и накапливаются в извитых канальцах почек. Накопленный вследствие гибели лептоспир токсин оказывает токсическое влияние на различные органы и системы. У части больных лептоспиры размножаются в извитых канальцах и выделяются из организма с мочой. В этом случае на первый план выступает поражение почек. Наиболее характерное поражение почек при лептоспирозе — дегенеративный процесс в эпителии канальцевого аппарата, поэтому их правильнее рассматривать как диффузный дистальный тубулярный нефроз. У больных появляются признаки ОПН с олигоанурией и уремической комой. Тяжёлое поражение почек — одна из наиболее частых причин смерти при лептоспирозе.
В фазе токсемии повреждение органов и тканей обусловлено действием не только токсина и продуктов жизнедеятельности лептоспир, но и аутоантител, образующихся в результате распада поражённых тканей и клеток макроорганизма. Этот период совпадает со второй неделей болезни, но может несколько затягиваться. Токсин оказывает повреждающее действие на эндотелий капилляров, что повышает их проницаемость с формированием тромбов и развитием ДВС-синдрома.
Центральная нервная система поражается вследствие преодоления ГЭБ лептоспирами. У части больных лептоспирозом развивается серозный или гнойный менингит, реже менингоэнцефалит. В отдельных случаях возникает специфический лептоспирозный миокардит. Патогномоничный симптом лептоспироза — развитие миозита с поражением скелетных, особенно икроножных мышц. Часто поражаются лёгкие (лептоспирозная пневмония), глаза (ириты, иридоциклиты), реже другие органы.
Классификация
Общепринятой классификации лептоспироза нет.
По клиническому течению выделяют лёгкую, среднетяжёлую и тяжёлую форму лептоспироза. Лёгкая форма может протекать с лихорадкой, но без выраженного поражения внутренних органов. Среднетяжёлую форму характеризуют выраженная лихорадка и развёрнутая клиническая картина лептоспироза, а для тяжёлой формы характерны развитие желтухи, появление признаков тромбогеморрагического синдрома, менингита и острой почечной недостаточности. По клиническим проявлениям выделяют желтушные, геморрагические, ренальные, менингеальные и смешанные формы. Лептоспироз может быть осложнённым и неосложнённым.
Осложнения лептоспироза
ИТШ, ОПН, острая печёночно-почечная недостаточность, ОДН (РДС), массивные кровотечения, кровоизлияния, миокардит, пневмония, в поздние сроки — увеит, ирит, иридоциклит.
Диагностика лептоспироза
Клиническая диагностика
Важную роль в диагностике лептоспироза играет эпиданамнез. Следует учитывать профессию больного (сельскохозяйственный рабочий, охотник, ветеринар, дератизатор), а также контакт с дикими и домашними животными. Следует обратить внимание на то, купался ли пациент в открытых водоёмах, поскольку обсеменение воды лептоспирами в отдельных регионах чрезвычайно велико.
Диагноз лептоспироза устанавливают на основании характерных клинических симптомов: острое начало, гипертермия, миалгия, гиперемия лица, сочетанное поражение печени и почек, геморрагический синдром, островоспалительные изменения в крови.
Лечение лептоспироза
Немедикаментозная терапиЯ
Режим. Диета
Лечение осуществляют в условиях стационара. Госпитализацию проводят по эпидемиологическим показаниям. Режим в остром периоде постельный. Диету определяют клинические особенности болезни. При доминировании почечного синдрома — стол № 7, печёночного — стол № 5, при сочетанных поражениях — стол № 5 с ограничением соли или стол № 7 с ограничением жиров.
Примерные сроки нетрудоспособности при лептоспирозе
Трудоспособность после заболевания восстанавливается медленно, но полностью. Неконтагиозность пациентов позволяет выписывать их через 10 дней после
нормализации температуры при полном клиническом выздоровлении, при наличии менингита — после санации СМЖ.
Примерные сроки восстановления трудоспособности 1–3 мес.
Диспансеризация
Диспансеризацию проводят в течение 6 мес с ежемесячным осмотром инфекциониста, по показаниям — нефролога, офтальмолога, невролога, кардиолога. Если
патология сохраняется в течение 6 мес, дальнейшее наблюдение проводят врачи соответствующего профиля (нефролог, офтальмолог, кардиолог) не менее 2 лет.
Профилактика лептоспироза
Лекция №23
Лечение лептоспироза, бруцеллеза. Противоэпидемические мероприятия в очаге инфекции
Бруцеллёз
Бруцеллёз (лихорадка мальтийская, лихорадка гибралтарская, лихорадка средиземноморская, лихорадка ундулирующая, болезнь Банга, болезнь Брюса, мелитококкоз, мелитококция) — зоонозная инфекционная болезнь с многообразными механизмами передачи возбудителя, характеризующаяся лихорадкой, поражением опорно-двигательного аппарата, нервной системы, половых органов.
Коды по МКБ -10
A23. Бруцеллёз.
A23.0. Бруцеллёз, вызванный Brucella melitensi.
A23.1. Бруцеллёз, вызванный Brucella abortus.
A23.2. Бруцеллёз, вызванный Brucella suis.
A23.3. Бруцеллёз, вызванный Brucella canis.
A23.8. Другие формы бруцеллёза.
A23.9. Бруцеллёз неуточнённый.
Этиология бруцеллеза
Возбудители — представители рода Brucella семейства Brucellaceae. Бруцеллёз человека может быть обусловлен четырьмя видами бруцелл: B. melitensis, В. abortus, В. suis и B. canis. Наиболее частая причина болезни — Brucella melitensis. Основные хозяева — овцы и козы. Несколько реже встречаются Brucella abortus; основной хозяин — крупный рогатый скот. У третьего вида бруцелл, Brucella suis, выделяют 4 биотипа. Основные хозяева — свиньи, зайцы и северный олень. Относительно редко диагностируют заболевание, обусловленное Brucella canis. Основной хозяин данного микроорганизма — собаки.
Они неподвижны, спор не образуют, жгутиков не имеют, грамотрицательны. Растут медленно на сложных питательных средах. Бруцеллы — внутриклеточные паразиты, они антигенно однородны, содержат эндотоксин.. Бруцеллы устойчивы в окружающей среде. В воде сохраняются свыше 2 мес, в молоке — 40 дней, в брынзе — 2 мес, в сыром мясе — 3 мес, в засоленном мясе — до 30 дней, в шерсти — до 4 мес. При кипячении погибают мгновенно, чувствительны к дезинфицирующим средствам, к антибиотикам тетрациклиновой группы, аминогликозидам, рифампицину, эритромицину.
Эпидемиология бруцеллеза
Резервуар и источник возбудителя — домашние животные. Хотя к бруцеллёзу чувствительны дикие животные, природных очагов инфекции нет.
Человек заражается от больных животных контактным, алиментарным, редко — аэрогенным путём. Заражение контактным путём носит профессиональный характер. Часто заражаются ветеринарные работники, телятницы, чабаны и др. Заражение может наступить и при контакте с мясом инфицированных животных. Алиментарное заражение часто происходит при употреблении непастеризованного молока или приготовленных из него продуктов .
Аэрогенное заражение возможно при попадании в дыхательные пути пыли, содержащей бруцеллы , а также в лабораториях при нарушении техники безопасности. Этот путь инфицирования наблюдают относительно редко. Чаще заболевают лица трудоспособного возраста (18–50 лет). Восприимчивость высокая. Инфицирующая доза составляет всего от 10 до 100 микробных тел. Постинфекционный иммунитет ненапряжённый, через 5–6 лет возможна реинфекция.
Патогенез бруцеллеза
Входные ворота инфекции — микротравмы кожи, слизистые оболочки органов пищеварения и респираторного тракта. В месте внедрения возбудителя изменений не наблюдают. По лимфатическим путям бруцеллы достигают регионарных лимфатических узлов, но и здесь выраженные изменения отсутствуют. Размножение и накопление бруцелл происходит преимущественно в лимфатических узлах, из которых они периодически поступают в кровь, а гибель сопровождается освобождением эндотоксина, вызывающего лихорадку, поражение вегетативной нервной системы. С кровотоком возбудитель разносится по всему организму, концентрируясь в органах и тканях, богатых макрофагами (печень, селезёнка, мышцы, фасции, суставные сумки, сухожилия), где вследствие незавершённого фагоцитоза длительно сохраняется, вызывает воспалительную реакцию с образованием специфических гранулём.
Для бруцеллёза характерна выраженная аллергическая перестройка организма, резко выражена ГЗТ, сохраняющаяся длительное время даже после освобождения организма от возбудителя. Аллергия играет большую роль в формировании вторичных очагов инфекции. Бруцеллёз отличается склонностью к хроническому течению, что связано с длительным персистированием бруцелл в организме. До введения в лечебную практику антибиотиков бруцеллы сохранялись в организме до двух лет, более длительное течение болезни связано с влиянием антибиотиков: часть бруцелл может переходить в L-формы и длительно сохраняется внутриклеточно.
Дата: 2019-02-02, просмотров: 481.