Т.П. Макарова, Г.Ф.Харисова
Технология переработки
Нефти и газа
Методические указания
по проведению практических занятий
по дисциплине «Технология переработки нефти и газа»
для студентов заочной формы обучения и студентов АЗЦ МРЦПК РТ
специальности 080502 «Экономика и управление на предприятиях нефтяной
и газовой промышленности»
Альметьевск 2009
УДК 54
М 15
Макарова Т.П.,Г.Ф.Харисова
М 15Технология переработки нефти и газа: Методические указания по проведению практических занятий по дисциплине «Технология переработки нефти и газа» для студентов заочной формы обучения и студентов АЗЦ МРЦПК РТ специальности 080502 «Экономика и управление на предприятиях нефтяной и газовой промышленности». – Альметьевск: Альметьевский государственный нефтяной институт, 2009. – 84 с.
Методические указания предназначены для работы студентов на практических занятиях и подготовки их к выполнению контрольной работы, лабораторных работ, экзамена по дисциплине «Технология переработки нефти и газа».
В методических указаниях приведены: теоретический материал, подлежащий изучению; примеры решения задач; задачи для самостоятельного решения; список рекомендованной литературы (основной и дополнительный).
Необходимый справочный материал для расчетов приведен в соответствующих приложениях, ссылка на которые дается в методических указаниях по их выполнению.
Печатается по решению учебно-методического совета АГНИ.
Рецензенты:
Доцент, к.т.н. кафедры ПТЭ Вахитова Р.И.
Доцент, к.т.н. кафедры ПХ Будкевич Р.Л.
© Альметьевский государственный
нефтяной институт, 2009
| |
СОДЕРЖАНИЕ
ВВЕДЕНИЕ…………………………………………………………………………..4
I. ОБЩАЯ ХАРАКТЕРИСТИКА НЕФТИ…………………………………………5
1. Фракционный состав нефти…………………………………………………..5
2. Классификация нефтей и нефтепродуктов……………………………..8
II. ПРИРОДНЫЕ И ПОПУТНЫЕ (НЕФТЯНЫЕ) ГАЗЫ…………………………9
1. Классификация и состав газов…………………………………………………9
2. Применение газа……………………………………………………………….11
III. ФИЗИЧЕСКИЕ СВОЙСТВА НЕФТИ И НЕФТЕПРОДУКТОВ……………12
1. Температуры кипения нефтяных фракций…………………………………...12
2. Характеристический фактор…………………………………………………..14
3. Плотность………………………………………………………………………14
4. Молекулярная масса…………………………………………………………...18
5. Массовый, объемный и мольный состав……………………………………..19
6. Давление насыщенных паров…………………………………………………25
7. Критические параметры и приведенные константы………………………...27
8. Коэффициент сжимаемости…………………………………………………...31
9. Фугитивность…………………………………………………………………..32
10. Вязкость……………………………………………………………………….35
11. Тепловые свойства…………………………………………………………...47
IV. НЕФТЯНЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ…………………………………...53
1.Классификация НДС…………………………………………………………...53
2. Водно-нефтяные эмульсии……………………………………………………61
3. Основные методы разрушения нефтяных эмульсий типа В/Н……………..63
V. ЛИТЕРАТУРА…………………………………………………………………..67
VI. ПРИЛОЖЕНИЯ………………………………………………………………...69
ВВЕДЕНИЕ
Нефть - это жидкий горючий минерал, распространенный в осадочной оболочке Земли. По составу нефть представляет собой сложную смесь углеводородов (алканов, циклоалканов, аренов, …) и соединений, содержащих помимо углерода и водорода гетероатомы - кислород, серу и азот.
По внешнему виду нефть - маслянистая жидкость, флуоресцирующая на свету. Цвет нефти зависит от содержания и строения содержащихся в ней смолистых веществ; известны темные (бурые, почти черные), светлые и даже бесцветные нефти. Нефть легче воды и почти нерастворима в ней. Вязкость нефти определяется ее составом, но во всех случаях она значительно выше, чем у воды.
Нефть представляет собой горючий материал, ее теплота сгорания выше, чем у твердых горючих полезных ископаемых (угля, сланца, торфа), и составляет около 42 МДж/кг. В отличие от твердых горючих ископаемых нефть содержит мало золы.
Свое название нефть получила от персидского слова нафата, означающего просачивающаяся, вытекающая.
Происхождение нефти является одной из наиболее сложных проблем современной науки. Значительное большинство геологов и химиков являются сторонниками теории органического происхождения нефти, однако отдельные ученые считают, что нефть образуется в природе абиогенным способом, за счет различных химических превращений неорганических веществ.
Одним из первых выдвинул теорию неорганического происхождения нефти Д. И. Менделеев (1877 г.). Согласно его гипотезе углеводороды нефти образовались в результате взаимодействия воды с находящимися в недрах земли карбидами металлов. Хотя, в принципе, такие реакции имеют место, с помощью карбидной теории невозможно объяснить появление в составе нефти огромного количества углеводородов разнообразного строения; непонятно также, как могла попасть вода из области низких давлений на поверхности Земли в область высоких давлений, существующих в недрах Земли. В последние годы были выдвинуты также гипотезы космического, магнетического, вулканического происхождения нефти, которые не получили широкой поддержки.
Большая часть геологических и геохимических наблюдений и фактов, накопленных в мировой науке о нефти на сегодняшний день, лучше подтверждает гипотезу органического происхождения нефти.
Сущность органической теории происхождения нефти заключается в том, что нефть и газ образуются из органического вещества, находящегося в рассеянном состоянии в осадочных породах. Считается, что основным органическим материалом, накапливающимся в осадочных породах, являются отмершие остатки микрофлоры и микрофауны (планктон, бентос и др.), развивающиеся в морской воде, к которым примешивались остатки животного и растительного мира.
В верхних слоях осадочной породы захороненный органический материал подвергается воздействию кислорода и бактерий и в значительной мере разлагается с образованием газов (СО2, N2, NH3, CH4 и др.) и растворимых в воде жидких продуктов. Наиболее устойчивая к химическому и бактериальному воздействию часть исходного органического материала остается в осадке.
В дальнейшем, по мере погружения в толщу осадочной породы, эти органические вещества в течение многих миллионов лет на глубине 1,5-3,0км и ниже подвергаются уже в восстановительной среде действию повышенных температур (примерно до 120-150, реже 200°С) и давления 10-30МПа, а также каталитическому влиянию вмещающих пород (в основном, глин). По современным воззрениям именно на этой стадии в результате термических и термокаталитических процессов органические вещества, и главным образом липиды (жиры, воска, масла), превращаются в углеводороды нефти.
Значение нефти для энергетики, транспорта, различных отраслей промышленности чрезвычайно велико. Из нефти вырабатываются всевозможные виды жидкого топлива (бензин, керосин, дизельное, газотурбинное, котельное топлива), смазочные и специальные масла, пластичные смазки, парафин, технический углерод (сажа), битумы, нефтяные коксы и другие товарные продукты.
Получаемые при переработке нефти легкие алканы и алкены, жидкий и твердый парафины, индивидуальные ароматические углеводороды представляют собой ценное сырье для дальнейшей химической переработки (нефтехимического синтеза). С помощью нефтехимического синтеза получают всевозможные пластические массы, синтетические смолы и каучуки, синтетические моющие средства, индивидуальные органические кислоты, спирты, альдегиды и кетоны.
Применение нефтяного сырья высвобождает большое количество пищевых продуктов (зерна, картофеля, жиров), которые ранее расходовались на технические цели.
Фракционный состав нефти
Для всех индивидуальных веществ температура кипения при данном давлении является физической константой. Так как нефть представляет собой смесь большого числа органических веществ, обладающих различным давлением насыщенных паров, то говорить о температуре кипения нефти нельзя.
Нефть и ее продукты характеризуются не температурами кипения, а температурными пределами начала и конца кипения и выходом отдельных фракций, перегоняющихся в определенных температурных интервалах. По результатам перегонки и судят о фракционном составе.
При исследовании новых нефтей фракционный состав определяют на стандартных перегонных аппаратах, снабженных ректификационными колонками. Это позволяет значительно улучшить четкость погоноразделения и построить по результатам фракционирования кривую истинных температур кипения (ИТК) в координатах температура - содержание фракций. Отбор фракций до 200°С проводится при атмосферном давлении, а остальных во избежание термического разложения - под различным вакуумом. По принятой методике от начала кипения до 300°С отбирают 10-градусные, а затем 50-градусные фракции до фракций с концом кипения 475-550°С.
Разгонку нефтепродуктов, перегоняющихся до 300°С, проводят в строго стандартных условиях на аппаратах без ректификации по ГОСТ 2177-82. По этой методике отмечают температуру начала кипения, температуры, при которых отгоняются 10, 50, 95 и 97,5% (об.), а также остаток и потери.
В условиях промышленной перегонки нефти для разделения ее на различные фракции применяют не постепенное испарение, как на лабораторных аппаратах, а однократное испарение с дальнейшей ректификацией. При этом отбирают следующие фракции, или дистилляты: бензин - фракция н. к.- 180°С, керосин - фракция 180-240°С; дизельное топливо - фракция 240-350°С. Из этих дистиллятов вырабатывают светлые нефтепродукты: авиационные и автомобильные бензины; бензины-растворители; авиационные и осветительные керосины; различные сорта дизельного топлива. Для всех этих нефтепродуктов соответствующими ГОСТами нормируется определенный фракционный состав.
Остаток после отбора светлых дистиллятов называется мазутом. Мазут разгоняют под вакуумом на фракции: 350-4200С - легкие дистиллятные масла; 420-500°С - тяжелые дистиллятные масла - или отгоняют фракцию 350-480°С - вакуумный газойль.
Остаток после разгонки мазута (выше 500°С) называется в зависимости от вязкости гудроном или полугудроном. Гудрон является сырьем для получения высоковязких смазочных масел и битумов.
Нефти различных месторождений сильно отличаются друг от друга по фракционному составу, а следовательно, по потенциальному содержанию бензиновых, керосиновых, дизельных и масляных дистиллятов. Фракционный состав той или иной нефти предопределяет пути ее промышленной переработки. Легкие нефти, содержащие небольшое количество масляных фракций, встречаются очень редко.
Задача 1. Составить структурные схемы веществ, названия которых указаны в условии задачи.
1. метан; этан; н-гептан; н-пентан; н-октан; 2,3-диметилгексан; 4,4-диэтилдекан
2. хлорэтан; 1,2-дихлорэтан; 1,3-дихлорпропан
3. циклопропан; трет-бутилциклобутан; 1,2-диметилциклопентан; 1,2-диэтилциклогексан; 1,1-метил-этилциклопентан; бициклооктан; бициклононан
4. бензол; толуол; 1,2,4-триметилбензол; фенол; о-этилфенол; нафталин
5.1-бутен; 2-бутен; 2-метил-2-бутен; 2-пентен; 2,3-диметилгексен
6. тиофан, тиофен, бензтиофен, тионафтен, дибензтиофен, дифенилсульфид
7. пиридин, хинолин, акридин, пиррол, индол, карбазол, пиррохинолин
Задача 2. Написать структурные формулы (не более пяти) изомеров следующих углеводородов, которые содержат n атомов углерода в главной цепи. Дать им названия.
| Варианты | |||||||||
| алканы | |||||||||
| С4Н10 | С5Н12 | С6Н14 | С7Н16 | С8Н18 | С9Н20 | С10Н22 | С11Н24 | С12Н26 | С13Н28 |
| n = 3 | n = 4 | n = 5 | n = 5 | n = 6 | n = 6 | n = 7 | n = 7 | n = 8 | n = 8 |
| алкены | |||||||||
| С13Н26 | С12Н24 | С11Н22 | С10Н20 | С9Н18 | С8Н16 | С7Н14 | С6Н12 | С5Н10 | С4Н8 |
| n = 8 | n = 8 | n = 7 | n = 7 | n = 6 | n = 6 | n = 5 | n = 5 | n = 4 | n = 3 |
| ароматические углеводороды | |||||||||
| С7Н9 | С8Н10 | С9Н12 | С10Н14 | С10Н13 | С6Н4Cl2 | С7Н8Cl | С8Н9 | С9Н11 | С10Н11 |
Задача 3. Написать уравнения реакций хлорирования и нитрования следующих углеводородов.
| Варианты | |||||||||
| ароматические | алканы | алкены | |||||||
| C6H4 | C5H3- CH3 | C6H4CH3 C2H5 | C3H8 | C4H10 | C5H12 | C6H14 | C3H6 | C4H8 | C5H10 |
Задача 4. Природный газ состава (метан + азот + оксид углерода (IV)) объемом v (н.у.) сожгли и затем всю газовую смесь пропустили через раствор гидроксида кальция. Рассчитайте массу образовавшегося осадка.
| Варианты | ||||||||||
| Объем смеси (л) | 5,48 | 5,68 | 6,35 | 5,72 | 6,56 | 7,36 | 8,46 | 4,48 | 6,65 | 8,68 |
| Состав, % (объемная доля) | ||||||||||
| Метан | ||||||||||
| Азот | ||||||||||
| Оксид углерода (IV) |
Задача 5. При сгорании алкана образовался оксид углерода (IV) объемом V при н.у. Определить объем кислорода (н.у.), израсходованный при горении, если потери кислорода составляют ω%.
| Варианты | |||||||||||||||||
| Алкан | метан | этан | про- пан | бутан | изобутан | 2-метил бутан | пен- тан | гек- сан | гептан | 2,2-диметил пентан | |||||||
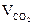 (л)
(л)
| 5,6 | 6,7 | 8,4 | ||||||||||||||
| ω% | 4,2 | 4,8 | 5,2 | 5,4 | 5,6 | 5,8 | 6,2 | 6,4 | 6,6 | ||||||||
Задача 6. Охарактеризовать физические и химические свойства следующих углеводородов.
| вариант | углеводород | вариант | углеводород |
| Этилен Пропилен Ацетилен Окись этилена Этиловый спирт | Этиленгликоль Глицерин Бензол Стирол Фенол |
Задача 7. Охарактеризовать получение и промышленное использование следующих углеводородов.
| вариант | углеводород | вариант | углеводород |
| Этилен Пропилен Ацетилен Окись этилена Этиловый спирт | Этиленгликоль Глицерин Бензол Стирол Фенол |
Применение газа
Одна из главных областей применения углеводородных газов - это использование их в качестве топлива. Высокая теплота сгорания, удобство и экономичность использования, ставят газ на одно из первых мест среди других видов энергетических ресурсов.
Другой важный вид использования попутного нефтяного газа - его отбензинивание, т.е. извлечение из него газового бензина на газоперерабатывающих заводах или установках. Газ с помощью мощных компрессоров сильно сжимается и охлаждается, при этом пары жидких углеводородов конденсируются, частично растворяя газообразные углеводороды (этан, пропан, бутан, изобутан). Образуется летучая жидкость - нестабильный газовый бензин, который легко отделяется от остальной неконденсирующейся массы газа в сепараторе. После фракционирования - отделения этана, пропана, части бутанов - получают стабильный газовый бензин, который используют как добавку к товарным бензинам, повышающую их испаряемость. Освобождающиеся при стабилизации газового бензина пропан, бутан, изобутан в виде сжиженных газов нагнетают в баллоны, применяют в качестве горючего. Метан, этан, пропан, бутан служат также сырьем для нефтехимической промышленности.
После отделения С2 - С4 из попутных газов оставшийся отработанный газ близок по составу сухому. Практически его можно рассматривать как чистый метан. Сухой и отработанный газы при сжигании в присутствии незначительных количеств воздуха в специальных установках образуют очень ценный промышленный продукт - газовую сажу:
СН4 + О2 ® С + 2Н2О.
газовая сажа
Ее используют главным образом в резиновой промышленности. Пропуская метан с водяным паром над никелевым катализатором при температуре 8500С, получают смесь водорода и окиси углерода - «синтез-газ».
[NI], 850ºС
СН4 + Н2О  СО + 3Н2.
СО + 3Н2.
При пропускании этой смеси над катализатором FeО при 4500С окись углерода превращается в двуокись и выделяется дополнительное количество водорода:
[FeO], 450ºС
СО + H2О  СО2 + Н2.
СО2 + Н2.
Полученный водород применяют для синтеза аммиака и других целей.
В пламени электрической дуги метан может быть разложен на углерод (сажу) и водород:
СН4  С + 2Н2.
С + 2Н2.
При обработке хлором и бромом (галогенирование) метана и других алканов получаются продукты замещения. Например, из метана и хлора можно получить следующие продукты:
СН4 + СI2 ® НСI + CН3СI (хлористый метил)
СН4 + 2СI2 ® 2НСI + CН2СI2 (хлористый метилен)
СН4 + 3СI2 ® 3НСI + СНСI3 (хлороформ)
СН4 + 4СI2 ® 4НСI + ССI4 (четыреххлористый углерод)
Аналогично при реакции с бромом получают бромзамещенные производные метана.
Метан служит также сырьем для получения синильной кислоты
[Pt - Ro], 1000-1100ºС.
2СН4 + 2NН3 + 3О2 ® 2НСN + 6Н2О,
а также для производства сероуглерода СS2, нитрометана СН3NО2, который используют как растворитель для лаков.
Этан служит сырьем для производства этилена путем пиролиза. Этилен, в свою очередь, является исходным сырьем для получения окиси этилена, этилового спирта, полиэтилена, стирола и др.
Пропан используют для выработки ацетона, уксусной кислоты, формальдегида и др., бутан - для получения - олефинов: этилена, пропилена, бутиленов, а также ацетилена и бутадиена (сырья для синтетического каучука). При окислении бутана образуются ацетальдегид, уксусная кислота, формальдегид, ацетон.
Характеристический фактор
Характеристический фактор К определяет химическую природу нефтепродукта, его парафинистость. Определяется в зависимости от двух параметров — плотности и температуры кипения, величина которых зависит от состава нефтепродуктов. Для парафинистых нефтепродуктов К = 12,5  13, для нафтено-ароматических К = 10
13, для нафтено-ароматических К = 10  11, для ароматизированных К ≤ 0, для крекинг-бензина К=11,54
11, для ароматизированных К ≤ 0, для крекинг-бензина К=11,54  11,8. Применяется характеристический фактор для корреляции при расчете физико-химических свойств нефтепродуктов. Характеристический фактор определяют по формуле
11,8. Применяется характеристический фактор для корреляции при расчете физико-химических свойств нефтепродуктов. Характеристический фактор определяют по формуле
 (5)
(5)
где Тср.уср - средне-усредненная температура кипения, К;  - относительная плотность нефтепродукта.
- относительная плотность нефтепродукта.
Можно определить величину К и по формуле
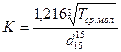 (6)
(6)
где Тср. мол - средне - молекулярная температура кипения, К;  - относительная плотность нефтепродукта.
- относительная плотность нефтепродукта.
Плотность
Плотностью вещества (ρ) называется масса его в единице объема. Плотность можно измерить в кг/м3, г/см3, кг/л, т/м3. В системе единиц СИ плотность измеряют в кг/м3.
В нефтепереработке при расчете физико-химических свойств нефтепродуктов принято пользоваться относительной плотностью, представляющей собой соотношение плотностей жидкого нефтепродукта и дистиллированной воды при определенных температурах. Обозначают относительную плотность  , где t1 - температура воды, °С; t2- температура нефтепродукта, °С. В России стандартными температурами при определении плотности являются для воды 4°С и для нефтепродуктов 20°С. В ряде зарубежных стран стандартной температурой воды и нефтепродукта является 15,6°С.
, где t1 - температура воды, °С; t2- температура нефтепродукта, °С. В России стандартными температурами при определении плотности являются для воды 4°С и для нефтепродуктов 20°С. В ряде зарубежных стран стандартной температурой воды и нефтепродукта является 15,6°С.
Относительная плотность узких фракций (10-20-градусных) может быть рассчитана по формуле
 (7)
(7)
Для нефтей парафинистых  = 0,736, n = 0,13; для нефтей сернистых
= 0,736, n = 0,13; для нефтей сернистых  = 0,722, n = 0,159.
= 0,722, n = 0,159.
Часто для технологических расчетов необходимо пересчитывать плотность нефтепродукта от одной температуры к другой. С этой целью можно пользоваться формулой Д. И. Менделеева в интервале температур от 0 до 150°С
 (8)
(8)
где  - относительная плотность нефтепродукта при 20°С;
- относительная плотность нефтепродукта при 20°С;  - относительная плотность нефтепродукта при заданной температуре; а - средняя температурная поправка на один градус.
- относительная плотность нефтепродукта при заданной температуре; а - средняя температурная поправка на один градус.
Значения температурной поправки представлены в Приложении 1.
Для определения плотности жидких нефтепродуктов при высоких температурах можно пользоваться графиками, приведенными на рис. 1 и в Приложениях 3 и 4.
На рис. 1 на оси абсцисс откладывают известное значение плотности; из определенной точки (А) восстанавливают перпендикуляр до пересечения с линией, соответствующей температуре, при которой определена эта плотность (точка В). Затем проводят линию, параллельную близлежащей наклонной кривой, до пересечения (в точке С) с линией температуры, при которой нужно определить плотность. Из точки С опускают перпендикуляр до пересечения с осью абсцисс и таким образом (в точке D) находят искомую плотность.
Графики Приложений 3 и 4 применимы при давлениях до 1,5 МПа. При большем давлении берется поправка (плотность под давлением минус плотность при атмосферном давлении) по графику Приложения 5.
Часто приходится пересчитывать  на
на  , а также
, а также  на
на  , и наоборот. С этой целью пользуются уравнениями
, и наоборот. С этой целью пользуются уравнениями
 (9)
(9)
где а - средняя температурная поправка (см. Приложение 1).
 (10)
(10)
Плотность смеси нефтепродуктов можно определять из равенства по известным
массовым процентам компонентов
 (11)
(11)
объемным процентам компонентов
 (12)
(12)
массам компонентов
 (13)
(13)

Рис. 1. График для определения относительной плотности жидких нефтепродуктов при температуре t (  ) пo известной их плотности
) пo известной их плотности  .
.
Пример 2. Определить плотность нефтепродукта при 150°С и давлении 20,0 МПа, если его плотность при 20°С равна 650 кг/м3 и К = 13,5.
Решение. Находим плотность нефтепродукта при 20°С и 20,0МПа. С этой целью воспользуемся Приложением 5, где находим поправку к плотности с учетом давления. Она равна 20 кг/м3. Тогда плотность при 20°С и Р = 20,0 МПа будет равна
 = 650 + 20 = 670 кг/м3
= 650 + 20 = 670 кг/м3
По Приложению 3 находим плотность при 150°С, зная плотность при 20°С и величину характеристического фактора К = 13,5. Плотность нефтепродукта при 150°С и 20,0 МПа будет равна 525 кг/м3.
Относительная плотность газа равна отношению массы m газа, занимающего объем V при некоторых температуре и давлении, к массе mв воздуха, занимающего тот же объем V при тех же температуре и давлении

Если считать газ идеальным, то при T = 273,16 К, Р = 0,1 МПа и V = 22,414 л масса m равна молекулярной массе М газа. В тех же условиях масса 22,414 л воздуха составляет 28,9 г, откуда относительная плотность газа или пара относительно воздуха равна
 (14)
(14)
Абсолютную плотность газов и паров (  , кг/м3) при нормальных условиях можно найти, зная массу М и объем 1 моль газа (22,414 л)
, кг/м3) при нормальных условиях можно найти, зная массу М и объем 1 моль газа (22,414 л)
 (15)
(15)
При абсолютной температуре Т (К) и давлении П (105 Па) плотность газа (в кг/м3) может быть найдена по формуле
 (16)
(16)
Используя формулу (15), можно написать

или
 (17)
(17)
Задача 11. Воспользовавшись формулой Д.И. Менделеева рассчитать плотность нефтепродукта при температуре tºС.
| вариант | ||||||||||
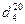
| 0,72 | 0,76 | 0,8 | 0,84 | 0,86 | 0,88 | 0,9 | 0,92 | 0,96 | 0,98 |
| t0С |
Задача 12. Используя рис. 1 определить относительную плотность жидкого нефтепродукта  при температуре tºС по известной их плотности
при температуре tºС по известной их плотности 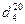 .
.
| вариант | ||||||||||
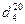
| 0,68 | 0,72 | 0,74 | 0,78 | 0,84 | 0,86 | 0,88 | 0,92 | 0,94 | 0,96 |
| t0С |
Задача 13. Определить плотность нефтепродукта при температуре t0С и давлении Р МПа, если известны при 200С его плотность 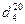 (кг/м3), давление Р1 (МПа) характеристический фактор К.
(кг/м3), давление Р1 (МПа) характеристический фактор К.
| вариант | ||||||||||
| Р1 МПа | ||||||||||
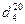
| ||||||||||
| t0С | -50 | |||||||||
| К | 12,5 | 12,5 | 10,5 |
Молекулярная масса
Молекулярная масса является одной из основных физико-химических характеристик нефтей и нефтепродуктов, величина, которая показывает, во сколько раз молекула данного вещества больше 1/12 части массы атома изотопа углерода  .
.
Между молекулярной массой и температурой кипения нефтяных фракций существует определенная зависимость; чем больше молекулярная масса нефтяной фракции, тем выше ее температура кипения. Учитывая эту зависимость, Б.М. Воинов предложил следующую общую формулу для определения молекулярной массы М нефтяной фракции:
 (18)
(18)
где t - средне-молекулярная температура кипения фракции, °С; а, b и с - коэффициенты.
В частности, для парафиновых углеводородов формула Б.М. Воинова имеет вид

или
 (19)
(19)
Данная формула применима и для узких бензиновых фракций.
Средняя температура кипения фракции 120°С. Ее молекулярная масса равна
М = 60 + 0,3 × 120 + 0,001(120)2 = 110,4
Формулу Б.М. Воинова уточнил А.С. Эйгенсон, введя характеризующий фактор К.
С введением характеризующего фактора формула (19) принимает вид
 (20)
(20)
Формулой (20) можно пользоваться для определения молекулярной массы фракций, выкипающих до 350°С (точность ±2  3%).
3%).
Молекулярную массу тяжелых, фракций можно определить по номограмме Приложения 6 в зависимости от вязкости при 50 и 100°С.
Пример 3. Определить молекулярную массу нефтепродукта с пределами выкипания 85-110°С, плотностью 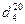 = 0,7609. Содержание узких фракций в этом продукте следующее (в мол. долях): (85 - 90°С) - 0,21; (90 - 95°С) - 0,10; (95 -100°С) - 0,35; (100 - 105°С) - 0,23; (105 - 110°С) - 0,11.
= 0,7609. Содержание узких фракций в этом продукте следующее (в мол. долях): (85 - 90°С) - 0,21; (90 - 95°С) - 0,10; (95 -100°С) - 0,35; (100 - 105°С) - 0,23; (105 - 110°С) - 0,11.
Решение. Определяем среднюю температуру кипения каждой узкой фракции в °С





Подставляя полученные данные в формулу (3), получаем

Определяем значение  по формуле (9)
по формуле (9)
 = 0,7609 + 5×0,000818 = 0,765
= 0,7609 + 5×0,000818 = 0,765
Определяем характеристический фактор К по формуле (6)
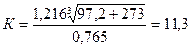
Молекулярную массу фракции определяем по формуле (20)
M = (7×11,3 - 21,5) + (0,76 - 0,04×11,3)×97,2 + (0,0003×11,3 - 0,00245)×(97,2)2 = 57,6 + 29,9 + 8,8 = 96,3
Молекулярная масса является свойством аддитивным.
Задача 14. Определить молекулярную массу нефтепродукта с пределами выкипания tн – tк, плотностью 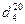 . Содержание узких фракций в этом продукте w (в долях единицы).
. Содержание узких фракций в этом продукте w (в долях единицы).
| вариант | ||||||||||
| tн0С | ||||||||||
| t10С | ||||||||||
| t20С | ||||||||||
| t30С | ||||||||||
| t4 0С | ||||||||||
| tк0С | ||||||||||
| w1 | 0,10 | 0,11 | 0,12 | 0,13 | 0,14 | 0,15 | 0,16 | 0,17 | 0,18 | 0,19 |
| w2 | 0,29 | 0,28 | 0,2 | 0,26 | 0,2 | 0,24 | 0,23 | 0,2 | 0,21 | 0,2 |
| w3 | 0,31 | 0,32 | 0,33 | 0,34 | 0,35 | 0,36 | 0,32 | 0,38 | 0,3 | 0,3 |
| w4 | 0,21 | 0,19 | 0,18 | 0,17 | 0,16 | 0,15 | 0,14 | 0,13 | 0,12 | 0,11 |
| w5 | 0,09 | 0,1 | 0,17 | 0,1 | 0,15 | 0,1 | 0,15 | 0,12 | 0,19 | 0,2 |
| d204 | 0,81 | 0,83 | 0,85 | 0,87 | 0,89 | 0,91 | 0,93 | 0,95 | 0,97 | 0,99 |
Давление насыщенных паров
Давление насыщенных паров - это давление, производимое паровой фазой, которая находится в равновесии с жидкостью при определенной температуре. Давление насыщенных паров индивидуального чистого вещества зависит только от температуры. Для смесей и таких продуктов, как нефть и нефтепродукты, давление насыщенных паров зависит не только от температуры, но и от состава паровой и жидкой фаз и их соотношения. Поэтому определение давления насыщенных паров нефтепродуктов представляет большие трудности. Однако для узких нефтяных фракций, выкипающих в узком интервале температур без заметного изменения состава фаз, можно с известной степенью приближения считать однозначной зависимость давления насыщенных паров от температуры. Единица давления в системе единиц СИ - паскаль (Па). Кратные единицы кПа, МПа. Паскаль - давление, вызываемое силой 1 ньютон (Н), равномерно распределенной по поверхности площадью 1м2 и нормально к ней направленной.
При изучении фракционного состава нефтей и проведении технологических расчетов аппаратуры приходится пересчитывать давление насыщенных паров нефтепродуктов при одной температуре на давление при другой, а также температуру кипения нефтяных фракций от одного давления к другому. Для осуществления таких пересчетов предложены формулы и номограммы (Приложения 7 и 8).
Пример 11. Узкая нефтяная фракция при атмосферном давлении имеет среднюю температуру кипения 149°С. Какова температура кипения этой фракции при 266,6 кПа?
Решение. По графику (Приложение 7) на оси координат находят точку, соответствующую температуре 149°С, и из этой точки проводят прямую, параллельную оси абсцисс, до пересечения с вертикальной линией, отвечающей давлению 101,3 кПа. Получают точку А, которая легла на искомый луч. Затем от точки, соответствующей давлению 266,6 кПа, проводят вертикаль до пересечения с найденным лучом в точке В. Из точки В проводят горизонтальную линию, параллельную оси абсцисс, до пересечения со шкалой температур в точке С. Эта точка дает значение искомой температуры кипения, равной 190°С.
Пример 12. При разгонке мазута из колбы Кляйзена температура паров в момент замера была равна 150°С, а остаточное давление 0,266 кПа. Какова температура паров при а<
Дата: 2016-10-02, просмотров: 440.