Нагнетаемые в продуктивные пласты пресные воды обладают различными физико-химическими и биолого-бактериологическими показателями (свойствами).
К физическим показателям поверхностных вод относятся температура воды, содержание в ней взвешенных веществ, запах, цветность (мутность).
К химическим показателям качества воды относятся рН, наличие азотсодержащих веществ, растворенных газов, хлоридов, сульфатов, железа, марганца, жесткость, щелочность, а также окисляемость воды.
К биологическим и бактериологическим показателям качества поверхностных вод относится наличие или отсутствие в них живых организмов и бактерий, тип которых зависит от химических показателей воды в водоеме.
Наибольшую значимость имеют следующие показатели: температура воды, размеры и количество взвешенных частиц, рН, количество и состав растворенных газов, жесткость, щелочность, окисляемость, биологические и бактериологические показатели качества воды.
Температура закачиваемой в пласт воды. Нагнетание больших объемов холодных поверхностных вод (особенно в зимний период) понижает температуру в пласте. С понижением температуры увеличивается вязкость нефти, повышаются показатели ее структурно-механических свойств. В нефтях, содержащих парафин и смолы, при понижении температуры в пласте могут образовываться и отлагаться кристаллы парафина, резко увеличивающие фильтрационные сопротивления и, как следствие этого - снижение нефтеизвлечения. Поэтому для каждого месторождения необходимо знать допустимые пределы изменения температуры закачиваемой в пласт воды и ее влияние на поведение флюидов в пласте.
Количество взвешенных частиц (КВЧ) в поверхностных водах, может колебаться в больших пределах и определяться фотоколориметрическим методом (при концентрации взвеси до 100 мг/л) с помощью бумажных фильтров (если эта концентрация выше 100 мг/л) или с применением культеров — электронных приборов, быстро дающих информацию о размерах частиц и их количестве.
Допустимые пределы изменения содержания механических примесей, содержащихся в поверхностных водах, как и для пластовых сточных вод, зависят от геолого-физических характеристик продуктивных горизонтов (проницаемости, трещиноватости, состава пород).
Концентрация водородных ионов. Важнейшей характеристикой ионного состава воды является содержание в них водородных ионов.
Известно, что молекула воды может диссоциировать на ионы:
Н2О → Н+ + ОНˉ
Состояние равновесия характеризуется константой
 (1.1.1)
(1.1.1)
где 
 - концентрация ионов Н+, ОНˉ в воде соответственно, моль/л;
- концентрация ионов Н+, ОНˉ в воде соответственно, моль/л;  - концентрация Н2О, моль/л.
- концентрация Н2О, моль/л.
Концентрация воды постоянна и равна 55,56 моль/л. Поэтому из (1.1.1) следует

где Кв – ионное произведение воды, значения которого при различных температурах представлены в таблице 1.1.1.
При нейтральной реакции концентрации ионов водорода Н+ и гидроксильной группы ОНˉ равны, следовательно

Так как при температуре 22°С ионное произведение воды равно 10-14, то  моль/л
моль/л
Таблица 1.1.1
Ионное произведение воды
| t, °С | Кв·1014 | t, °С | Кв·1014 | t, °С | Кв·1014 | t, °С | Кв·1014 |
| 0,112 | 1,01 | 9,61 | |||||
| 0,186 | 1,47 | ||||||
| 0,293 | 2,09 | ||||||
| 0,452 | 2,92 | ||||||
| 0,57 | 4,02 | ||||||
| 0,68 | 5,47 |
Отрицательное значение логарифма концентрации водородных ионов обозначается рН, т.е.
-lg СН+ = рН (1.1.2)
 (1.1.3)
(1.1.3)
При 22°С рН=7, следовательно, водный раствор с помощью рН – характеристики можно будет классифицировать следующим образом:
рН=7 – нейтральный;
рН>7 – щелочной;
рН<7 – кислый.
Растворенные в поверхностных водах газы - это могут быть кислород, углекислота, сероводород, азот и метан.
Углекислота встречается во всех водах и влияет на изменение солевого состава закачиваемой в пласт воды.
Н2S, O2, СO2 содержащиеся в поверхностных водах, вызывают коррозию трубопроводов и насосов, и поэтому количество их должно быть минимальным.
Жесткость природных вод. Жесткостью воды называется суммарная эквивалентная концентрация катионов кальция и магния в воде:
Сжо= (qСа2+ +qMg2+) (1.1.4)
Эквивалентом ионов Эи вещества называется их молекулярная масса или часть её, соответствующая единице валентности.
 (1.1.5)
(1.1.5)
Таким образом, чтобы выразить содержание ионов вещества в растворе [мг·экв/кг, мг·экв/л] нужно количество миллиграммов ионов вещества в килограмме или в литре разделить на эквивалент
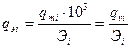 (1.1.6)
(1.1.6)
Таблица 1.1.2
Дата: 2016-10-02, просмотров: 353.