Физические свойства водорода.
При нормальной температуре водород представляет собой бесцветный газ без запаха. Газофазный водород состоит из 25% пароводорода и 75% ортоводорода. При сжижении водорода происходит самопроизвольная медленная орто – пара конверсия, поэтому жидкий водород практически на 100% состоит из параводорода.
Основные физические показатели водорода [ ]:
Температура кипения………………………………… -252,76єС (20,24 К)
Температура застывания…………………………….. -259,2єС (13,8 К)
Критическая температура…………………………….-239,97єС (32,9 К)
Критическое давление………………………………...1,27 МПА (12,87 кгс/см2 )
Плотность при НУ……………………………………...0,08987 кг/м3
» при температуре кипения……………….....0,07097 г/см3
» при температуре застывания………………0,0896 »
Коэффициент вязкости при температуре:……
застывания…………………………………………240·10-6 сП
кипения……………………………………………..131·10-6 сП
Жидкий водород представляет собой бесцветную жидкость без запаха, отличающуюся высокой степенью криогенности. Водород сжижается при 20 К, а при 14 К переходит в твердое состояние, т. е. в жидкофазном состоянии он находится в узком диапазоне температуры – около 6є. В этой области возможно образование промежуточной формы водорода – шугообразной, представляющей собой смесь жидкого водорода с твердым водородом в виде льда, плавающего в жидкости. Для образования шуги в жидком водороде требуется его небольшое – до 0,7єС переохлаждение. В шугообразной форме плотность водорода повышается до 0,08-0,087 г/см3 и становится максимальной при полном застывании.
Газообразный водород отличается высокой диффузионной способностью. На пример, коэффициент диффузии водорода в воздухе более чем в 3 раза выше по сравнению с такими компонентами, как метан, кислород и двуокись углерода. Среднее значение коэффициента Dо диффузии Н2 в различных средах представлены в таблице 1.
Таблица 1.
| Среда | О2 | N2 | СО2 | СО | СН4 | Воздух |
| D0·104, мІ/с | 0,69 | 0,7 | 0,54 | 0,6 | 0,625 | 0,61 |
Водород обладает способностью проникновения через толщу материала, в частности металлов. Это отрицательное явление ведущее к ухудшению свойств материала, получило название наводороживание. С повышением давления и температура диффузия водорода в металлы возрастает. Глубина наводораживания, т.е. проникновения молекул водорода в кристаллическую решетку металла, в большинстве случаев не превышает 4-6 мм, а при нагортовке материала может быть снижена до 2-1,5 мм. Для алюминия наводороживание достигает 15-30 мм, а при нагортовке уменьшается до 4-6 мм. В случае сталей водородная диффузия практически полностью устраняется путем легирования с помощью хрома, молибдена, вольфрама и других элементов.
Водородо – воздушные смеси характеризуются широкой областью воспламенения (4-75% по объему) и взрываемости (18,3-74% по объему), что повышает их пожаро- и взрывоопасность. В то же время водород отличается высокой температурой воспламенения (590єС) и способностью к быстрому рассеиванию в воздушной среде, благодаря чему по суммарным показателям безопасности он примерно равноценен природному газу. При загрязнении технологическими примесями взрывоопасность водорода увеличивается. Поэтому основным условием безопасной работы с водородом в закрытых помещениях является контроль за его содержанием в воздухе и возможными утечками.
Моторные характеристики.
Водород характеризуется наиболее высокими энерго-массовыми показателями среди химических топлив. Низшая теплота сгорания молекулярного водорода (с образованием водяного пара) составляет 241,9 МДж/моль (57740 ккал/моль), что соответствует 120 МДж/кг ( 28640 ккал/кг). С учетом диссоциации при 7,84 МПа расчетная теплота сгорания равняется 117,99 МДж/кг (28160 ккал/кг). Таким образом, водород по массовой энергоемкости превосходит традиционные углеводородные топлива примерно в 2,5-3., спирты-в 5-6 и аммиак-в 7 раз. Однако вследствие очень низкой плотности водорода его объемные энергетические характеристики невысоки даже в криогенной форме (см. таблицу 2.):
Таблица 2.
| Форма водорода | Газ (н.у.) | жидкий | шугообразный | твёрдый | |
| Теплота сгорания | МДж/мі | 10,501 | 8373,8 | 9439,2 | 10501,1 |
| ккал/л | 2,506 | 1998,5 | 2252,8 | 2506,2 | |
Массовая теплопроизводительность водорода – воздушных смесей также превышает теплопроизводительность остальных топлив и составляет 3,298 МДж/кг (787 ккал/кг) при б=1.
Однако из-за низкой энергоплотности водород по объемной теплопроизводительности уступает большинству жидких и газообразных топлив. Теплота сгорания 1м3 стехиометрической водородо-воздушной смеси составляет 3,1 МДж (740ккал), что меньше примерно на 15 и 10% по отношению соответственно к бензинам и спиртам.
Температура самовоспламенения водорода зависит от состава смеси и составляет для стехиометрических композиций 500-510єС [ ]. При этом период задержки воспламенения зависит от коэффициента избытка окислителя и в области Т>1100 К удовлетворительно описывается формулой:
фзд=(2•10‾8/Р)•е8600/Т,
где фзд выражено в секундах, а Р – в атмосферах.
Среди горючих газов водород характеризуется наиболее низкой энергией воспламенения (примерно в 70 раз меньше, чем у метана) и высокой скоростью сгорания. Максимальное значение нормальной скорости распространения пламени в водородо-воздушных смесях составляет по различным оценкам 240-270 см/с, причем сильно зависит от температуры (см. таблицу 3.) [ ]:
Таблица 3.
| Температура смеси, єС | 20 | 100 | 200 | 300 | 400 |
| Скорость распространения пламени, см/с | 250 | 400 | 600 | 900 | 1200 |
Максимум скорости не соответствует стехиометрическому соотношению, а довольно значительно сдвинут в область избытка содержания водорода, где соответственно кинетическому уравнению осуществляются оптимальные условия для выхода продуктов реакции. В условиях камеры сгорания двигателя скорость горения водородных смесях значительно выше нормальной скорости распространения пламени вследствие повышенных температур и давлений, а также значительной турбулизации горючей смеси. Согласно большинству данных водород начинает детонировать при степенях сжатия е≥6 в широком диапазоне б. В то же время очистка камеры сгорания (удаление нагара и выступающих кромок, шлифовка поверхности) позволяет осуществить работу на водороде при е близких 14 и стехиометрических смесях.
Зависимости концентрационных пределов детонации и воспламенения водорода воздушных смесей от степени сжатия приведены на рис.1.
Эти данные получены на стандартной установке CFR по моторному методу при температуре поступающей в двигатель смеси 38єС [ ]. Устойчивое воспламенение водорода обеспечивается в весьма широкой области б, причем богатая граница с увеличением е расширяется, в то время как бедная практически не изменяется. Однако вследствие высокой активности водорода его детонационное сгорание происходит уже при е=6 в области 0,2≤б≤1,82. Повышение степени сжатия расширяет концентрационные границы детонации до 0,12≤б≤2,85 при е=15. В данных условиях область отсутствия детонации, представляющая практический интерес, охватывает диапазон топливных смесей с б=2ч5.
Влияние добавок водорода на антидетонационную стойкость углеводородного топлива носит довольно сложный характер. На рис.2, при степени сжатия 12 увеличение концентрации водорода в метане до 60% практически не оказывает влияния на концентрационные пределы детонации [8]. Однако при дальнейшем повышении содержания водорода наблюдается тенденция к детонационному сгоранию, так что при концентрациях Н2 свыше 60% детонация имеет место уже при е=6, а при содержании водорода от 90 до 95 диапазон детонации расширяется почти в 2 раза. Отмечается, что для небольших добавок водорода (до 20%) детонация не наблюдается даже при степенях сжатия 15. при низком соотношении топлива к воздуху изменение пределов детонации при увеличении концентрации водорода в топливной смеси довольно умеренно, в то время как в богатой области предел детонации резко увеличивается с повышением содержания Н2.
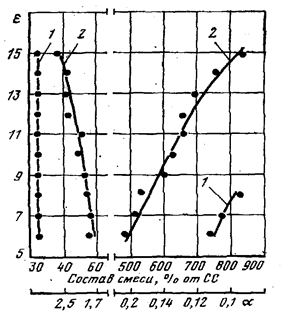
Рис.1. Концентрационные пределы водородо - воздушных смесей:
1-воспламенение; 2-детонация.
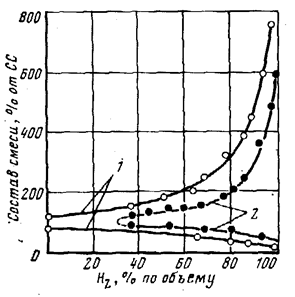
Рис.2. Концентрационные пределы детонации водородо – метановых смесей:b1-при температуре смеси 156єС; 2-при температуре смеси 38єС.
Водородные автомобили
Многочисленные схемы возможного применения водорода на автомобиле делятся на две группы: в качестве основного топлива и как добавки к современным моторным топливам. В рамках этих вариантов водород может использоваться в чистом виде (т.е. индивидуально) либо в составе вторичных энергоносителей. Водород как основное топливо является более далекой перспективной, связанной с переходом автомобильного транспорта на принципиально новую энергетическую базу. В то же время применение водородных добавок, позволяющих улучшить экономические и токсические показатели автомобильных двигателей, может быть реализовано в самое ближайшее время.
Америка поставила себе задачу: в ближайшие 10 – 15 лет избавиться от нефтяной зависимости. Единственный выход – как можно скорее запустить в серийное производство водородный автомобиль. Европа боится отстать, кроме того, европейцам приходится выполнять принятые у них нормы на выброс вредных веществ автотранспортом, которые все время ужесточаются. В 1993 году были введены нормы «Евро-1», в 1996 году - «Евро-2», в 1999 году - «Евро-3», а с 2005 года в Европе планируется ввести в действие еще более жесткие нормы - «Евро-4». В перспективе автомобилям совсем запретят выбрасывать вредные вещества, и тогда нельзя будет обойтись без машины, работающей на водороде. Автомобилестроение – это область, в которой как нигде перемешаны политика, интересы крупных корпораций, социология и экология. Но каковы бы ни были скрытые интересы сторон, гонка за водородным автомобилем началась.
Главное препятствие к внедрению водородного автомобиля на топливных элементах – отсутствие инфраструктуры промышленного получения водорода в нужных объемах, систем его хранения, транспортировки и заправки автомобилей. По мнению американских специалистов, такую инфраструктуру удастся создать не раньше чем в 2020 – 2030 гг. На переходный период ведущие автопроизводители предложат так называемые «гибридные автомобили»: в них экономичный двигатель внутреннего сгорания подзаряжает аккумуляторную батарею, которая питает электрический двигатель. Такие автомобили разрабатывают практически все ведущие автомобильные компании и уже серийно выпускают в Японии.
Россия в 1987 году присоединилась к Женевскому соглашению и теперь тоже обязана выполнять Европейские нормы выброса вредных веществ автотранспортом. И хотя у нас эти нормы вводят с некоторым опозданием («Евро-1» - с 1999 года, «Евро-2» - с 2001 года), «процесс пошел». В общем-то пора: в Москве и других крупных городах более 80% токсичных выбросов приходится на долю автотранспорта. Поэтому мы в гонке водородных автомобилей обязательно примем участие, тем более что когда – то наши разработки в этой области были на весьма высоком уровне: например, в 90-х годах прошлого столетия в ГНЦ РФ НАМИ сделали образец «Москвича», с двигателем, работающем на водороде, который получали прямо на борту из метанола. Более того, недавно на АвтоВАЗе сделали образец электромобиля, работающего на водородных топливных элементах. С 2001 года в странах Евросоюза для всех новых автомобилей вводятся нормы токсичности «Евро-3», см. табл. 6 [ ].
Классическая схема: двигатель внутреннего сгорания или дизельный двигатель приводят в движение колеса через механический привод. Нас окружают тысячи автомобилей, но мало кому приходит в голову, что их эффективность катастрофически мала. Если взять так называемые «условия городского цикла движения», то общий КПД автомобиля – 10-12% (за городом, где меньше светофоров, 15-17%)! Девять литров бензина из десяти попросту улетают в атмосферу [ ].
Таблица 6.
Требования к токсичности выхлопа.
| Нормы | СО, г/км | СН, г/км | NOx, г/км | Год введения |
| Евро-1 | 2,72 | сумма 0,97 | 992 | |
| Евро-2 | 2,20 | сумма 0,50 | 1996 | |
| Евро-3 | 2,30 | 0,2 | 0,15 | 2000 |
| Евро-3 (минус 7) | 15 | 1,8 | Не нормируется |
Автомобили на водородном топливе можно условно разделить на три класса: машины с обычным двигателем внутреннего сгорания, работающим на водороде или водородной смеси; машины с электрическим двигателем, питающимся от двигателя внутреннего сгорания, который работает на водороде (гибридные автомобили); с электрическим двигателем, питающимся от топливного элемента (электрохимического генератора).
Первый тип – это обычные карбюраторные или дизельные двигатели, у которых изменена система подачи топлива. Такие модели могут работать на чистом водороде, или 5 – 10% водорода добавляют к основному топливу. В обоих случаях КПД двигателя увеличивается (во втором случае примерно на 20%) и выхлоп становится гораздо чище (СО – уменьшается в полтора раза, СНх – в полтора раза, NOx – до пяти раз). Такие двигатели и автомобили были сделаны и прошли все испытания у нас и за рубежом примерно в 70 – 80-х годах. Дружный вывод учёных: учитывая все затраты и конструкционные сложности, это может быть только промежуточным, переходным этапом на пути к третьему типу.
Второй тип автомобилей – машины с двумя энергоносителями, или, как их называют, гибридные. Колёса приводят в движение электропривод, энергию ему поставляет буферный накопитель (это могут быть аккумуляторные батареи и механические или конденсаторные накопители) и высокоэкономичный двигатель внутреннего сгорания, работающий на водороде или на бензиновой или газовой смеси с водородом. У этого стратегического варианта развития автомобилестроения довольно много энтузиастов. Особенно привлекательным он становится, если отвлечься от водорода и просто скомбинировать электропривод с обычным двигателем внутреннего сгорания (или дизельным). Дело в том, что сам по себе электродвигатель – большой шаг вперед, поскольку его КПД (преобразование электрической энергии в механическую) равен примерно 90 – 95%, в отличие от двигателя внутреннего сгорания (35%) и дизеля (40%). В случае электропривода нет таких потерь энергии, как при сложной механической передаче, кроме того, благодаря промежуточному устройству – рекуператору энергии, электродвигатель экономит и накапливает энергию (до 10%) во время замедления автомобиля, чтобы использовать ее при ускорении.
Электромотор питается от буферного накопителя энергии, который ее тоже откуда – то должен получать. Идея подзарядки от общей сети потихоньку сошла на нет (по крайней мере, этот способ надо комбинировать с другими). Действительно, непрактично через каждые 100 км по нескольку часов заправляться. Инженеры пришли к тому, что на борту нужна маленькая электростанция. Электричество для подзарядки может, например, вырабатывать дизельный или обычный двигатель (на чём угодно: газе, бензине, водороде и пр.). Общий КПД такого гибридного автомобиля увеличивается примерно до 30% (соответственно снижается расход топлива), а объём вредных выбросов, при условии, что есть нейтрализатор, позволяет уложиться в европейские нормы, действующие с 2005 года, с десятикратным запасом. И всё же выхлоп «zero» можно получить только у третьего типа автомобилей.
Настоящий водородный автомобиль – это машина с электродвигателем, который питается от топливного элемента, расположенного на борту автомобиля. Пока самые эффективные и экологические топливные элементы - водородные (после окисления водород даёт только воду), на основе твердого полимерного электролита. Теоретически эффективность (КПД) топливного элемента, работающего на смеси водород – воздух, может быть больше 85%. Сейчас уже удалось получить около 75% - это более чем в два раза выше, нежели в лучших двигателях внутреннего сгорания. Кроме того, КПД таких машин, как и у всех электромобилей, увеличивается с уменьшением нагрузки ( при замедлении происходит возврат энергии), в отличие от обычных двигателей, у которых в эти моменты эффективность падает. Если сравнить эффективность обычных автомобилей и машин с топливным элементом в условиях города, то преимущество увеличится до пяти – шести раз, поскольку последние будут иметь максимальный КПД, в то время как эффективность первых в этих условиях уменьшается до 10 – 12%.
Топливный элемент, работающий на водороде, - одна из ключевых деталей в новом автомобиле. Топливный элемент, или электрохимический генератор, преобразует химическую энергию в электрическую. То же самое происходит в электрических аккумуляторах, но в топливных элементах есть два важных отличия: 1) они работают до тех пор, пока поступает топливо; 2) химический состав электролита в процессе работы не изменяется, то есть топливный элемент не нужно перезаряжать.
Топливная батарея состоит из многих десятков элементарных ячеек, каждая примерно в сантиметр толщиной. Только так можно получить необходимые силу тока и напряжение. Каждая ячейка состоит из двух электродов, разделённых электролитом. На один электрод (анод) подводится топливо (водород), на другой (катод) – окислитель (кислород воздуха), (см. рис. 8). Необходима также система удаления продуктов реакции (воды) и отработанного воздуха. Для ускорения химической реакции поверхность электродов покрывают катализатором. Катод и анод разделены электролитом (им может быть полимер или раствор), который пропускает ионы и не пропускает электроны. На аноде водород распадается на электроны и протоны. Последние проходят через электролит и достигают катода, где соединяются с кислородом – образуется вода. Электроны движутся к внешней части ячейки, где попадают в электрический контур, куда можно подсоединять нагрузку.
Существует много разных топливных элементов, в основном они различаются типом электролита и рабочей температурой. Их можно классифицировать, например, по используемому топливу, рабочему давлению и температуре, по характеру применения. Элементы на водородном топливе. В этом типичном описанном выше элементе водород и кислород переходят в электролит через микропористые углеродные или металлические электроды. Высокая плотность тока достигается в элементах, работающих при повышенной температуре (около 250° С) и высоком авлении. Элементы, использующие водородное топливо, получаемое при переработке углеводородного топлива, например природного газа или нефтепродуктов, по-видимому, найдут наиболее широкое коммерческое применение. Объединяя большое число элементов, можно создавать мощные энергетические установки. В этих установках постоянный ток, вырабатываемый элементами, преобразуется в переменный со стандартными параметрами. Новым типом элементов, способных работать на водороде и кислороде при нормальных температуре и давлении, являются элементы с ионообменными мембранами. В этих элементах вместо жидкого электролита между электродами располагается полимерная мембрана, через которую свободно проходят ионы. В таких элементах наряду с кислородом может использоваться воздух. Образующаяся при работе элемента вода не растворяет твердый электролит и может быть легко удалена.
Элементы на углеводородном и угольном топливах. Топливные элементы, которые могут превращать химическую энергию таких широко доступных и сравнительно недорогих топлив, как пропан, природный газ, метиловый спирт, керосин или бензин, непосредственно в электричество, являются предметом интенсивного исследования. Однако пока не достигнуто заметных успехов в создании топливных элементов, работающих на газах, получаемых из углеводородного топлива, при нормальной температуре.
Для повышения скорости реакции углеводородного и угольного топлива приходится повышать рабочую температуру топливного элемента. Электролитами служат расплавы карбонатов или других солей, которые заключаются в пористую керамическую матрицу. Топливо «расщепляется» внутри элемента с образованием водорода и оксида углерода, которые поддерживают протекание токообразующей реакции в элементе. Элементы, работающие на других видах топлива. В принципе реакции в топливных элементах не обязательно должны быть реакциями окисления обычных топлив. В перспективе могут быть найдены и другие химические реакции, которые позволят осуществить эффективное непосредственное получение электричества. В некоторых устройствах электроэнергия получается при окислении, например, цинка, натрия или магния, из которых изготавливаются расходуемые электроды.
Превращение энергии обычных топлив (угля, нефти, природного газа) в электричество было до сих пор многоступенчатым процессом. Сжигание топлива, позволяющее получить пар или газ, необходимые для работы турбины или двигателя внутреннего сгорания, которые, в свою очередь, вращают электрический генератор, – процесс не очень эффективный. Действительно, коэффициент использования энергии такого превращения ограничен по второму закону термодинамики, и его вряд ли можно существенно поднять выше существующего уровня. Коэффициент использования энергии топлива самых современных паротурбинных энергетических установок не превышает 40%. Для топливных элементов нет термодинамического ограничения коэффициента использования энергии. В существующих топливных элементах от 60 до 70% энергии топлива непосредственно превращается в электричество, и энергетические установки на топливных элементах, использующие водород из углеводородного топлива, проектируются на КПД 40–45%. назад дальше Самый перспективный топливный элемент, который предполагается использовать в новых автомобилях, - это элемент с твёрдой ионообменной мембраной (proton exchange membrane fuel cell, или сокращённо РЕМFC). Твёрдый электролит имеет множество преимуществ: его не растворяет образующаяся при работе элемента вода, его просто делать в промышленном масштабе. Более того, элемент на твёрдом электролите работает при относительно низких температурах (80єС) и соответственно не требует предварительного прогрева. С другой стороны, и КПД при таких температурах меньше, чем при повышенных.
Самая большая проблема с топливным элементом – его цена. Когда – то она была высокой в основном из – за платины (катализатора), покрывающей электроды. За последние двадцать лет её количество, необходимое для топливного элемента, уменьшилось в 100 раз, и учёные хотят сократить её ещё в два раза. Теперь самая дорогая часть – это электролит, мембрана «Nafion», Сейчас она стоит около 700 евро/мі, а на батарею для среднего автомобиля (объём 90 л и вес 60 кг – даёт примерно 60 кВт) нужно десятки квадратных метров такого полимера. Естественно, учёные пытаются всеми способами удешевить этот материал и заставить его работать при более высоких температурах (150 - 200єС).
У нас во многих институтах занимаются фундаментальными исследованиями, которые могли бы стать основой отечественного компактного топливного элемента.
В общем, топливный элемент на водороде вполне готов к применению. Остались мелочи – сделать его поменьше и подешевле.
Выводы.
На основании выполненного литературного обзора можно сделать следующие выводы:
• водород является экологически чистым топливом, так как при его сгорании образуется только вода;
• при работе на бедных смесях на водородном топливе можно добиться значительного снижения содержания NOх.;
• широкие возможности водорода как топлива благодаря его характеристикам сгорания позволяют разработать конструкцию двигателя, на котором можно было бы свести к минимуму эмиссии NOх.
• так как в основе топливных элементов лежит электрохимический процесс, то КПД топливных элементов на смеси водород – воздух, может быть более 85%.
Физические свойства водорода.
При нормальной температуре водород представляет собой бесцветный газ без запаха. Газофазный водород состоит из 25% пароводорода и 75% ортоводорода. При сжижении водорода происходит самопроизвольная медленная орто – пара конверсия, поэтому жидкий водород практически на 100% состоит из параводорода.
Основные физические показатели водорода [ ]:
Температура кипения………………………………… -252,76єС (20,24 К)
Температура застывания…………………………….. -259,2єС (13,8 К)
Критическая температура…………………………….-239,97єС (32,9 К)
Критическое давление………………………………...1,27 МПА (12,87 кгс/см2 )
Плотность при НУ……………………………………...0,08987 кг/м3
» при температуре кипения……………….....0,07097 г/см3
» при температуре застывания………………0,0896 »
Коэффициент вязкости при температуре:……
застывания…………………………………………240·10-6 сП
кипения……………………………………………..131·10-6 сП
Жидкий водород представляет собой бесцветную жидкость без запаха, отличающуюся высокой степенью криогенности. Водород сжижается при 20 К, а при 14 К переходит в твердое состояние, т. е. в жидкофазном состоянии он находится в узком диапазоне температуры – около 6є. В этой области возможно образование промежуточной формы водорода – шугообразной, представляющей собой смесь жидкого водорода с твердым водородом в виде льда, плавающего в жидкости. Для образования шуги в жидком водороде требуется его небольшое – до 0,7єС переохлаждение. В шугообразной форме плотность водорода повышается до 0,08-0,087 г/см3 и становится максимальной при полном застывании.
Газообразный водород отличается высокой диффузионной способностью. На пример, коэффициент диффузии водорода в воздухе более чем в 3 раза выше по сравнению с такими компонентами, как метан, кислород и двуокись углерода. Среднее значение коэффициента Dо диффузии Н2 в различных средах представлены в таблице 1.
Таблица 1.
| Среда | О2 | N2 | СО2 | СО | СН4 | Воздух |
| D0·104, мІ/с | 0,69 | 0,7 | 0,54 | 0,6 | 0,625 | 0,61 |
Водород обладает способностью проникновения через толщу материала, в частности металлов. Это отрицательное явление ведущее к ухудшению свойств материала, получило название наводороживание. С повышением давления и температура диффузия водорода в металлы возрастает. Глубина наводораживания, т.е. проникновения молекул водорода в кристаллическую решетку металла, в большинстве случаев не превышает 4-6 мм, а при нагортовке материала может быть снижена до 2-1,5 мм. Для алюминия наводороживание достигает 15-30 мм, а при нагортовке уменьшается до 4-6 мм. В случае сталей водородная диффузия практически полностью устраняется путем легирования с помощью хрома, молибдена, вольфрама и других элементов.
Водородо – воздушные смеси характеризуются широкой областью воспламенения (4-75% по объему) и взрываемости (18,3-74% по объему), что повышает их пожаро- и взрывоопасность. В то же время водород отличается высокой температурой воспламенения (590єС) и способностью к быстрому рассеиванию в воздушной среде, благодаря чему по суммарным показателям безопасности он примерно равноценен природному газу. При загрязнении технологическими примесями взрывоопасность водорода увеличивается. Поэтому основным условием безопасной работы с водородом в закрытых помещениях является контроль за его содержанием в воздухе и возможными утечками.
Моторные характеристики.
Водород характеризуется наиболее высокими энерго-массовыми показателями среди химических топлив. Низшая теплота сгорания молекулярного водорода (с образованием водяного пара) составляет 241,9 МДж/моль (57740 ккал/моль), что соответствует 120 МДж/кг ( 28640 ккал/кг). С учетом диссоциации при 7,84 МПа расчетная теплота сгорания равняется 117,99 МДж/кг (28160 ккал/кг). Таким образом, водород по массовой энергоемкости превосходит традиционные углеводородные топлива примерно в 2,5-3., спирты-в 5-6 и аммиак-в 7 раз. Однако вследствие очень низкой плотности водорода его объемные энергетические характеристики невысоки даже в криогенной форме (см. таблицу 2.):
Таблица 2.
| Форма водорода | Газ (н.у.) | жидкий | шугообразный | твёрдый | |
| Теплота сгорания | МДж/мі | 10,501 | 8373,8 | 9439,2 | 10501,1 |
| ккал/л | 2,506 | 1998,5 | 2252,8 | 2506,2 | |
Массовая теплопроизводительность водорода – воздушных смесей также превышает теплопроизводительность остальных топлив и составляет 3,298 МДж/кг (787 ккал/кг) при б=1.
Однако из-за низкой энергоплотности водород по объемной теплопроизводительности уступает большинству жидких и газообразных топлив. Теплота сгорания 1м3 стехиометрической водородо-воздушной смеси составляет 3,1 МДж (740ккал), что меньше примерно на 15 и 10% по отношению соответственно к бензинам и спиртам.
Температура самовоспламенения водорода зависит от состава смеси и составляет для стехиометрических композиций 500-510єС [ ]. При этом период задержки воспламенения зависит от коэффициента избытка окислителя и в области Т>1100 К удовлетворительно описывается формулой:
фзд=(2•10‾8/Р)•е8600/Т,
где фзд выражено в секундах, а Р – в атмосферах.
Среди горючих газов водород характеризуется наиболее низкой энергией воспламенения (примерно в 70 раз меньше, чем у метана) и высокой скоростью сгорания. Максимальное значение нормальной скорости распространения пламени в водородо-воздушных смесях составляет по различным оценкам 240-270 см/с, причем сильно зависит от температуры (см. таблицу 3.) [ ]:
Таблица 3.
| Температура смеси, єС | 20 | 100 | 200 | 300 | 400 |
| Скорость распространения пламени, см/с | 250 | 400 | 600 | 900 | 1200 |
Максимум скорости не соответствует стехиометрическому соотношению, а довольно значительно сдвинут в область избытка содержания водорода, где соответственно кинетическому уравнению осуществляются оптимальные условия для выхода продуктов реакции. В условиях камеры сгорания двигателя скорость горения водородных смесях значительно выше нормальной скорости распространения пламени вследствие повышенных температур и давлений, а также значительной турбулизации горючей смеси. Согласно большинству данных водород начинает детонировать при степенях сжатия е≥6 в широком диапазоне б. В то же время очистка камеры сгорания (удаление нагара и выступающих кромок, шлифовка поверхности) позволяет осуществить работу на водороде при е близких 14 и стехиометрических смесях.
Зависимости концентрационных пределов детонации и воспламенения водорода воздушных смесей от степени сжатия приведены на рис.1.
Эти данные получены на стандартной установке CFR по моторному методу при температуре поступающей в двигатель смеси 38єС [ ]. Устойчивое воспламенение водорода обеспечивается в весьма широкой области б, причем богатая граница с увеличением е расширяется, в то время как бедная практически не изменяется. Однако вследствие высокой активности водорода его детонационное сгорание происходит уже при е=6 в области 0,2≤б≤1,82. Повышение степени сжатия расширяет концентрационные границы детонации до 0,12≤б≤2,85 при е=15. В данных условиях область отсутствия детонации, представляющая практический интерес, охватывает диапазон топливных смесей с б=2ч5.
Влияние добавок водорода на антидетонационную стойкость углеводородного топлива носит довольно сложный характер. На рис.2, при степени сжатия 12 увеличение концентрации водорода в метане до 60% практически не оказывает влияния на концентрационные пределы детонации [8]. Однако при дальнейшем повышении содержания водорода наблюдается тенденция к детонационному сгоранию, так что при концентрациях Н2 свыше 60% детонация имеет место уже при е=6, а при содержании водорода от 90 до 95 диапазон детонации расширяется почти в 2 раза. Отмечается, что для небольших добавок водорода (до 20%) детонация не наблюдается даже при степенях сжатия 15. при низком соотношении топлива к воздуху изменение пределов детонации при увеличении концентрации водорода в топливной смеси довольно умеренно, в то время как в богатой области предел детонации резко увеличивается с повышением содержания Н2.

Рис.1. Концентрационные пределы водородо - воздушных смесей:
1-воспламенение; 2-детонация.

Рис.2. Концентрационные пределы детонации водородо – метановых смесей:b1-при температуре смеси 156єС; 2-при температуре смеси 38єС.
Дата: 2019-07-30, просмотров: 569.