СОДЕРЖАНИЕ
| Введение…………………………….……………………………… ………….….…. | 2 |
| 1. Структура и свойства эпоксидных смол…………………………….……….…. | 3 |
| 1.1. Получение эпоксидных смол ...…………….…………………………….…... | 3 |
| 1.2. Структура и свойства неотверждённых смол……….………………….……. | 7 |
| 2. Отверждение эпоксидных смол, их структура и свойства в отверждённом состоянии……………………………………………………………………………. | 10 |
| 2.1. Оверждение эпоксидных смол………………………………………………... | 10 |
| 2.2. Структура и свойства отверждённых эпоксидных смол……………………. | 16 |
| 3. Теоретические основы адгезии и экспериментальные методы определения адгезионной порочности……….……………………………......……….….…….. | 19 |
| 3.1. Теории адгезии……….………………………………...……….……….…….. | 19 |
| 3.2. Методы измерения адгезионной прочности………………………….……… | 23 |
| 3.3. Характер разрушения адгезионных соединений……………………………. | 30 |
| 4. Адгезионные свойства эпоксидных смол к субстратам различной природы | 32 |
| 4.1. Адгезия эпоксидных смол к металлам……………………………………….. | 32 |
| 4.2. Адгезия эпоксидных смол к стеклу…………………………………………... | 33 |
| 4.3. Адгезия эпоксидных смол к различным волокнам………………………….. | 34 |
| 5. Растровая электронная микроскопия как метод исследования поверхностей адгезионного контакта и разрушения……….…………………. | 42 |
| 5.1. Теоретические основы метода……….……………………………….…….… | 42 |
| 5.2. Устройство и работа растрового электронного микроскопа……………….. | 43 |
| 5.3. Применение растровой электронной микроскопии в исследованиях адгезионных соединений……………………………………………………… | 45 |
| Заключение ………………………………………………………………………….. | 47 |
| Литература…………………………………………………………………………… | 49 |
ВВЕДЕНИЕ
Целью данной работы- изучить структуру и адгезионные свойства отверждённых эпоксидных смол.
Эпоксидные смолы обладают высокой адгезией к различным материалам и поэтому используются в качестве клеёв, связующих в композиционных материалах и в качестве различных покрытий. Поэтому задача этой работы заключается в том, чтобы изучить получение эпоксидных смол, процесс их отверждения и адгезионные свойства к конкретным материалам различной природы.
Работа состоит из пяти основных разделов. В первом будут рассмотрены вопросы получения эпоксидных смол, их структура и свойства в неотверждённом состоянии.
Во втором разделе речь идёт о механизмах отверждения смол, структуре и свойствах после отверждения.
В третьем разделе рассмотрены основные теории адгезии полимеров, методы которые используются для измерения адгезионной прочности на практике, а также возможный характер разрушения адгезионной системы.
Эпоксидные смолы обладают разными адгезионными свойствами к материалам различной природы. Об этом и рассказывается в четвёртом разделе.
Пятый раздел рассказывает о растровой электронной микроскопии, о её роли при исследовании адгезии.
1. Структура и свойства эпоксидных смол
ОТЕЧЕСТВЕННЫЕ МАРКИ
ЭД-5
5-7
400
25
ЭД-6
3-5
550
18
ЭД-13
50-55
1500
8-10
ЭД-15
60-70
2200
5-7
ЗАРУБЕЖНЫЕ МАРКИ
Эпон 1064
40-45
-----
12,5
Эпон 1001
64-76
900
8,6
Эпон 1004
97-103
1400
5,2
Эпон 1007
127-133
2900
2,0
Эпон 1009
145-155
3750
1,3
При синтезе низкомолекулярных диановых эпоксидных смол ( мол. масса 350-450) обычно раствор дифенилолпропана (1 моль) в эпихлоргидрине (8-10 моль) нагревают до кипения и постепенно (5-8 часов) добавляют к нему 40%-ный водный раствор NaOH (2,2 моль). При этом непрерывно отгоняют воду в виде азеотропной смеси с эпихлоргидрином, который после отделения воды возвращают в реактор. После окончания процесса непрореагированный эпихлоргидрин отгоняют под вакуумом, эпоксидиановую смолу растворяют в толуоле, толуольный раствор промывают водой для удаления NaCl. Затем толуол отгоняют, сначала при атмосферном давлении, потом под вакуумом при температуре до 140-150 оС.
Смолы с молекулярной массой 500-1000 получают аналогичным способом, но при молярном соотношении дифенилолпропан : эпихлоргидрин, равном 1: (1,5-1,9), причём процесс ведут в среде растворителя (ксиол, толуол, их смеси с бутиловым спиртом или циклогексаном).
Смолы с молекулярной массой 1000-3500 синтезируют взаимодействием низкомолекулярной эпоксидиановой смолы с дифенилолпропаном в расплаве при 140-210 оС (катализаторы- третичные амины, мочевина, Na2CO3) или дифенилпропана с эпихлоргидрином в присутствии щёлочи в гетерогенных условиях в системах вода – органический растворитель (обычно изопропанол или бутанол) при 70-80 оС. Во втором случае в меньшей степени протекают побочные реакции, получаемые эпоксидиановые смолы имеют более узкое молекулярно-массовое распределение, сравнительно узкий интервал эпоксидных чисел, отличаются более светлым цветом.
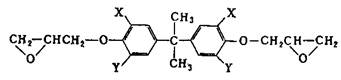
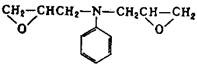
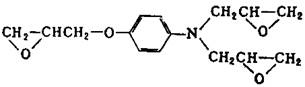
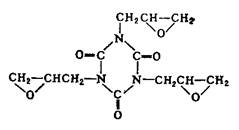
Из других эпоксидных смол, содержащих в молекуле глицидиловые группы, наибольшее практическое применение получили глицидиловые производные феноло-формальдегидных новолачных смол(II) (здесь и далее римскими цифрами указана нумерация эпоксидных смол в таблице 2), продуктов конденсации фенола с акролеином (III) и глиоксалем (IV), галогенированного дифенилолпропана (V), ароматических моноаминов (VI) и диаминов (VII), аминофенолов (VIII), циануровой кислоты (IX), резорцина (X), гликолей (XI). Промышленное значение получили также олигомерные диглицидилуретаны - продукты взаимодействия глицидола с олигомерными диизоцианатами, полученными на основе олигодиенидилов молекулярной массой 2000-4000, простых или сложных полиэфиров молекулярной массой 1000-2000. Эпоксидиановые смолы, содержащие эпоксидные группы в алифатических циклах или цепях, получают эпоксидированием (обычно надуксусной кислотой) двойных связей ненасыщенных соединений; практическое значение имеют диэпоксиды гексагидробензаль- 1,1-бис- (оксиметил) циклогексана (XIII), тетрагидробензилового эфира тетрагидробензойной кислоты (XIV), дициклопентенилового эфира (XV), дициклопентадиена (XVI), винилциклогексана(XVII), эпоксидированные олигомеры дивинила.
Таблица 2
Эпоксидные смолы [2].
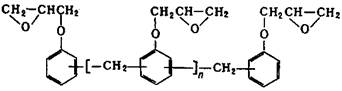 II II
|
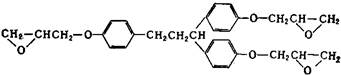 III III
|
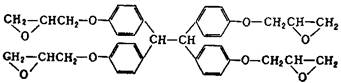 IV IV
|
 V V
|
 VI VI
|
 VII VII
|
 VIII VIII
|
 IX IX
|
 X X
|
 XI XI
|
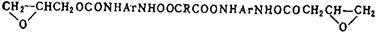 XII XII
|
 XIII XIII
|
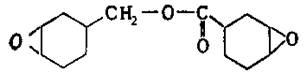 XIV XIV
|
 XV XV
|
 XVI XVI
|
 XVII XVII
|
Отверждение эпоксидных смол
Благодаря высокой реакционной способности эпоксидных и гидроксильных групп в качестве отвердителей эпоксидиановых смол можно использовать мономерные, олигомерные и полимерные соединения различных классов и таким образом, в широком диапазоне варьировать режимы отверждения (температура, время) и свойства получаемых трёхмерныx полимеров.
По механизму поликонденсации эпоксидиановые смолы отверждаются первичными и вторичными ди- и полиаминами, многоосновными кислотами и их ангидридами, феноло-формальдегидными смолами резольного и новолачного типов, многоатомными спиртами и фенолами в количестве 5—120% от массы эпоксидиановой смолы; по механизму полимеризации — третичными аминами, аминофенолами н их солями, кислотами Льюиса и их комплексами с основаниями в количестве обычно 5—15% от массы смолы.
Реакции поликонденсации и ионной полимеризации протекают одновременно при отверждении эпоксидиановой смолы дициандиамидом. Эпоксидиановые смолы способны отверждаться без подвода тепла (в том числе при температурах ниже О °С), в присутствии влаги и даже в воде.
Отверждение по механизму поликонденсации. Для холодного (без подвода тепла) отверждения эпоксидиановой смолы (мол. м. до 1000) в качестве отвердителей применяют алифатические полиамины (в том числе продукты их модификации), чаще всего полиэтиленполиамины Н2N(СН2СH2NH)nH где n=1-4, или гексаметилендиамин в количестве 5-15% от массы смолы. Жизнеспособность композиций с такими отвердителями при 15—25 °С составляет 1—3 ч (навеска 10-20 г), длительность отверждения около 24 часов (хотя степень отверждения продолжает увеличиваться ещё в течение 10-30 суток. Степень отверждения при комнатной температуре не превышает 65-70% . Для повышения ее и, следовательноo, улучшения и стабилизации и свойств продуктов отверждения проводят термообработку при 60—120°С в течение 12—2 ч.
Реакция смолы с алифатическими полиаминами экзотермична: в результате саморазогрева температура композиции (навеска 20 г, начальная температура 20 °С) может превысить 200 °С, что обычно приводит к деструкции полимера, возникновению больших напряжений (после охлаждения) и растрескиванию изделий. Поэтому отверждение чаще всего проводят в небольшой массе и тонких слоях для улучшения теплоотвода. Другие недостатки алифатических полиаминов - токсичность, сравнительно высокая хрупкость продуктов отверждения, необходимость строго соблюдать точность дозировки.
Модификации этих отвердителей окисями этилена или пропилена, a также акрилонитрилом позволяет избежать многих недостатков, однако при этом у продуктов отверждения ухудшаются водо- и химстойкость, уменьшается теплостойкость.
Для холодного отверждения эпоксидных смол используются также олигоаминоамиды - продукты конденсации полиэтиленполиаминов с полимеризованными кислотами растительных масел. Такие отвердители менее токсичны, чем полиамины, их удобнее дозировать (50—100% по отношению к массе эпоксидной смолы), при этом не требуется высокая точность дозировки, а получаемые полимеры более эластичны.
Для ускоренного отверждения эпоксидных смол при комнатной и более низких температурах (до —10 °С) отвердителями служат продукты конденсации полиэтиленполиаминов с фенолом и формальдегидом. Для получения сравнительно крупных отливок (массой до 5-10 кг) используют аминоэфиры - продукты модификации полиэтиленполиаминов эфирами метакриловой или акриловой кислоты.
Перечисленные алифатические полиамины применяют для отверждения эпоксидных клеев, герметиков, связующих, заливочных компаундов, лаков и эмалей. Для горячего (с подводом тепла) отверждения эпоксидных смол (мол. масса менее 1000) применяют обычно ароматические ди- и полиамины (м-фенилендиамин, 4,4-диаминодифенилметан, продукты конденсации анилина с формальдегидом, эвтептической смеси ароматических полиаминов). Отверждение проводят при 100—180 °С в течение 16—4 ч;
соотношение (по массе) эпоксидная смола : амин составляет обычно 100 : (15-50). Продукты отверждения отличаются повышенной механической прочностью, тепло- и химстойкостью. Такие отвердители применяют главным образом . в составе связующих для армированных пластиков и пресспорошков, ограниченно - в заливочных компаундах.
Для горячего отверждения эпоксидных смол используют также ангидриды дикарбоновых кислот, например фталевый, метилтетрагидрофталевый, гексагидрофталевый, малеиновый, эндометилентетрагидровталевый , метилендиковый. Отверждение проводят при 120—180 С в течение 24—12 ч. обычно в присутствии 0,1-2% катализатора отверждения, например диметилбензиламина, триэталонамина, диметиланилина или 2,4,6-трис (диметиламинометил) фенола. Соотношение ангидридных и эпоксидных групп близко к 1 при наличии катализатора и составляет около 0,8 , если он отсутствует. Обычно же ангидрид берут в количестве 50—100% от массы смолы. Продукты отверждения отличаются хорошими диэлектрическими свойствами, термо- и влагостойкостью. Композиции эпоксидных смол с ангидридными отвердителями используют главным образом для получения электроизоляционных компаундов, а также как связующие для армированных пластиков.
Для горячего отверждения эпоксидных смол (мол. масса больше 1000) применяют синтетические смолы - феноло-формальдегидные (резольные и новолачные), мочевино- и меламино-формальдегидные в количестве обычно 25-75% от массы эпоксидной смолы; температура отверждения 150-210'С, прoдолжнтельность от 12 ч до 10 мин.. Отвердители этого типа используют главным образом в составе лакокрасочных материалов, клеев и связующих.
Для этих же назначений в качестве отвердителей эпоксидных смол применяют мономерные и олигомерные изоцианаты, содержащие не менее двух изоцианатных групп в молекуле, элементоорганические мономеры и олигомеры, содержащие алкокси группы (например, тетраэтоксисилан, полибутилтитанат). Продукты отверждения высокомолекулярных эпоксидных смол указанными отвердителями отличаются высокой адгезией к металлам, эластичностью в сочетании с твердостью и химстоикостью.
Отверждение по механизму полимеризации. Из отвердителей этого типа наиболее широко используют триэтаноламин, триэтаноламинотитанат, 2,4,6-трис-(диметиламинометил)фенол н его соли с органическими одноосновными кислотами (олеиновой, 2-этилгексановой), 2-диэтиламиноэтанол, 2-этил-4-метилимидазол и другие кислоты Льюиса, особенно BF3, обычно используют в виде комплексов с аминами (например, с этиламином, анилином, бензиламином. пиперидином). Комплексы типа BF3*NH2 называют латентными отвердителями; их композиции с эпоксидными смолами стабильны в условиях хранения и быстро отверждаются при 120— l60 С (за 2,0—0,5 ч). Композиции эпоксидных смол с полимеризационными отвердителями отличаются повышенной адгезией к металлам и стеклу; их используют главным образом в качестве клеев и связующих для армированных пластиков.
Регулирование скорости и глубины отверждения. Для получения композиций, быстро отверждающихся в тонких слоях при сравнительно низких температурax, целесообразно использовать эпоксидиановые смолы повышенной реакционной способности (циануровая и резорцин) и отвердители следующих типов комплексы BF3 с гликолями, продукты конденсации алифатических полиаминов с фенолом и формальдегидом, а также вводить в композиции мономеры и олигомеры, содержащие группы ОН, SH или СООH (резорцино-формальдегидные смолы, тиоколы, салициловая кислота и др.). Для увеличения глубины отверждения композиций, предназначенных для холодного отверждения, когда невозможна последующая термообработка, применяют эпоксидиановые смолы и отвердители с возможно меньшей функциональностью, например бифункциональные диановые эпоксидные смолы в сочетании с трехфункциональным амином (N-алкилпропилендиамином. N-алкилгексаметилендиамином н др.), а также вводят в композиции соединения (гликоль или диглицидилуретаны), которые, участвуя в образовании трехмерной сетки полимера, способствуют увеличению его молекулярной подвижности.
Для получения композиции, быстро отверждающихся при повышенных температурах (60—120 °С), целесообразно использовать эпоксидиановые смолы ароматических моноаминов, циануровых кислот в сочетании с ангидридами дикарбоновых кислот (фталевым, малеиновьм) или высокоактивные эпоксидные смолы (резорцин) в сочетании с ароматическими полиаминами (например м-фенилендиамином).
Для получения композиций, стабильных при 15-25 °С и быстро отверждающихся при 120—200 °С, в качестве отвердителей используют дициандиамид, комплексы BF3 с алифатическими аминами, ароматические диамины пониженной основности и ароматические диамины, содержащие заместители в орто-положении к NH2-группе (например, 4,4-диаминодифенилсульфон, З,3-дихлор-4,4-диаминодифенилметан), гуанамины, дигидразиды дикарбоновых кислот, а также кансулированные отвердители и отвердители, нанесённые на цеолиты.
Если необходимо увеличить жизнеспособность композиции холодного отверждения (например, при пропитке или заливке изделий сложной формы), в состав композиции вводят соединения, содержащие протоноакцепторные группы, например сложные олигоэфиры, диалкилфталаты.
Для уменьшения экзотермического эффекта при отверждении применяют смолы с наименьшим эпоксидным числом и отвердители с меньшей функциональноcтью (например, аминоамид), а также вводят соединения с протоноакцепторными группами. Для повышения температуры саморазогрева композиции используют высокоактивные эпоксидиановые смолы (циануровая кислота и резорцин) и отвердители типа комплексов BF3 с гликолями[2].
Отверждение аминами
Способ отверждения эпоксидных смол с помощью полиаминов представляет особый интерес, так как путем их подбора удается получить композиции, отверждающиеся как при нагревании, так и на холоду. Основной особенностью отверждаемых эпоксидных смол является образование неплавких и нерастворимых продуктов без выделения каких-либо летучих веществ. Продукты реакции представляют собой полиоксиамины. Отверждение протекает по следующей схеме:
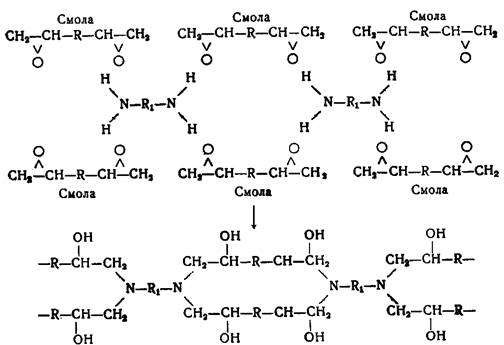
ВЫСОКОМОЛЕКУЛЯРНЫЙ ПОЛИАМИН
Из различных полиаминов наиболее пригодны те, которые содержат не менее двух первичных аминогрупп. При применении их достигаются лучшие результаты в отношении твердости, химической стойкости и скорости отверждения. Вторичные диамины образуют только линейные цепи, а третичные амины пригодны как катализаторы отверждения лишь при нагревании, вызывая реакцию полимеризации по эпоксигруппам.
При отверждении на каждую эпоксидную группу должен приходиться один активный атом водорода. Это позволяет определить необходимое стехиометрическое количество полиамина (в%) путем умножения эпоксидного числа смолы на эквивалентный вес полиамина в расчете на один активный атом водорода.
Применяемый амин оказывает значительное влияние на реакцию отверждения эпоксидных смол и свойства конечного продукта. Уже испытано более 150 различных полиаминов в качестве отвердителей. Проведено особенно много исследований по отверждению эпоксидных смол лакового назначения. В таблице 2 приведены условия отверждения жидкой ароматической смолы с эпоксидным числом 0,5 и вязкостью 480 сек. различными полиаминами.
В качестве новых отвердителей эпоксидных смол пригодны аминоэтилпиперазин, содержащий в одной молекуле первичную, вторичную и третичную аминогруппы, и смесь гетероциклических полиаминов, состоящая на 60—65% из аминоэтилпиперазина. Указанные амины придают отвержденным смолам повышенную стойкость к ударным нагрузкам.
Отверждение эпоксидных смол полиаминами может быть ускорено соединениями, содержащими гидроксильные группы. Вследствие того, что при отверждении наблюдается образование ОН-групп, этот процесс уже имеет автокаталитический характер. Но добавка посторонних веществ позволяет уменьшить время гелеобразования и регулировать степень изотермичности реакции. Было доказано, что вода наиболее эффективно ускоряет отверждение, а кислоты, фенолы, спирты, амиды и сульфамиды также способствуют более быстрому отверждению. Максимальный эффект наблюдается в присутствии 5—10% воды, но при содержании в смоле около 1% воды наблюдается вспенивание массы. Исследованные вещества по каталитической активности при добавлении 5,6% к смоле можно расположить в следующий ряд: вода>паратолуолсульфокислота> салициловая кислота > резорцин > муравьиная кислота > триэтаноламин > бензойная кислота > салициламид> молочная кислота > орта- и парааминофенолы > щавелевая кислота > уксусная кислота > фенол > масляная кислота > глицерин > ацетамид > диэтаноламин > метанол > маленновая кислота > мочевина > салициловый ангидрид > нитрометан > фталевая кислота.
Ускоряющее действие добавок, видимо, связано со способностью этих веществ образовывать водородные связи с эпоксидным кислородом. Т. е. вещества, являющиеся донорами водорода (—ОН. —СООН, —SO3H, —CONH2, —CONHR, —SO2NH2, —SО2NHR) ускоряют отверждение эпоксидных смол полиамидами.
Некоторые органические вещества заметно тормозят реакцию отверждения смол. К. ним относятся кетоны (этилметилкетон), сложные эфиры (этилацетаты), ароматические углеводороды (ксилол, толуол), диоксан, диметилформамид, ацетонитрил, нитробензол. В ряде случаев этот эффект можно объяснить легкостью их испарения, что способствует отводу теплоты реакции.
Отверждение ангидридами
Изучение отверждения эпоксидных смол ангидридами производится многими исследователями. Кроме химических методов применяются методы спектроскопии. В настоящее время твердо установлено, что процесс отверждения определяется в основном двумя реакциями. Сначала ангидрид реагирует с ОН-группой эпоксидной смолы; при этом раскрывается кольцо ангидрида и образуется карбоксильная группа:
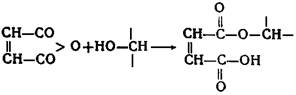
А затем карбоксильная группа раскрывает эпоксидное кольцо другой молекулы смолы:
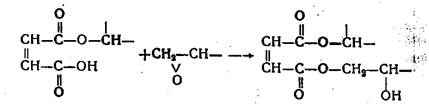
Вновь образовавшаяся гидроксильная группа взаимодействует с молекулой ангидрида и т. д. В результате таких реакций образуется твердая смола трехмерной структуры.
Недавно было найдено, что смола ЭД-5 при добавлении малеинового ангидрида до 35% полностью отверждается при 100° за 60 часов, все эпоксидные группы и весь малеиновый ангидрид вступают в реакцию (по инфракрасным спектрам). При более низких температурах даже за 200—300 час. не наблюдается полного исчезновения эпоксидных групп и малеинового ангидрида.
В пределах 50—100° не наблюдается взаимодействия гидроксильной и эпоксидной групп смолы по схеме:

Видимо, эта реакция может протекать при температурах, превышающих 100°. В последнее время было показано , что эпоксидные группы смолы могут реагировать непосредственно с ангидридом с образованием полиэфиров по следующей схеме:
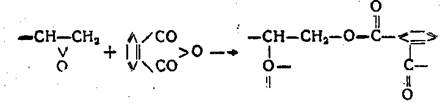
В присутствии третичного амина эпоксидные группы смолы реагируют с ангидридом уже при 70—100°. Указанная реакция лучше всего проходит с фталевым, гекса- и тетрагидрофталевым ангидридами. Малеиновый ангидрид в смеси с третичным амином темнеет, янтарный ангидрид реагирует медленно и также образует темные продукты.
В России наибольшее применение в качестве отвердителя нашли малеиновый или фталевый ангидриды. Фталевый ангидрид имеет высокую температуру плавления (130,8°), что затрудняет его смешение с эпоксидной смолой, а малеиновый ангидрид (Т пл. 53°) имеет сильную летучесть и токсичность. Поэтому в последнее время предложен метилтетрагидрофталевый ангидрид, легко получаемый из изопрена и малеинового ангидрида. Он плавиться при 64° и обладает гораздо меньшей летучестью, чем малеиновый ангидрид. Свойства эпоксидных композиций, отвержденных метилтетрагидрофталевым ангидридом, являются хорошими.
Повышение теплостойкости отвержденных эпоксидных смол достигается применением в качестве отвердителя пиромеллитового ангидрида, представляющего собой белый кристаллический порошок с температурой плавления 286° . Его строение выражается формулой:
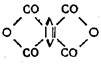
Введение пиромеллитового ангидрида в эпоксидную смолу может быть осуществлено тремя методами: а) растворением при повышенных температурах; б) добавлением в растворе ацетона; в) суспендированием в жидкой смоле при обычной температуре. Вследствие высокой химической активности пиромеллитовой ангидрид лучше всего смешивать с другими ангидридами (малеиновым или фталевым) и в виде смесей различного состава применять в качестве отвердителей эпоксидных смол. Но чем выше содержание пиромеллитового ангидрида в смеси, тем выше теплостойкость отвержденной смолы.
Литые изделия из эпоксидных смол, отвержденные пиромеллитовым ангидридом, сохраняют свою форму при 290°, а стеклопластики мало теряют прочность после 500 час. выдержки при 260° .
Можно применять для отверждения эпоксидных смол продукт реакции пиромеллитового ангидрида и гликоля, растворимый в обычных органических растворителях :
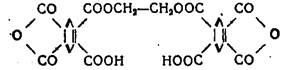
Указанный диангидрид придает клеям и стеклопластикам высокую теплостойкость, хорошие химические и диэлектрические свойства.
Теории адгезии
Адгезией (или прилипанием) называют сцепление двух приведенных в контакт поверхностей различных по своей природе материалов. При склеивании поверхностей различных полимерных тел возникают связи, природа которых может быть различной. Возникновение связей между склеиваемыми или свариваемыми поверхностями происходит во времени и определяется механизмом адгезии. В процессе склеивания двух полимерных поверхностей с течением времени происходит увеличение истинной поверхности контакта и числа связей, соединяющих контактируемые поверхности. Связи, обеспечивающие адгезию полимерного тела с другим (полимерным, металлическим и т. д.) телом, могут быть обусловлены как межмолекулярным взаимодействием, так и силами главных химических валентностей.
После приведения тела в контакт одновременно начинают развиваться три процесса: увеличение размеров истинной поверхности контакта, диффузия и возникновение адгезионных связей. Увеличение истинной поверхности контакта может происходить в силу ряда различных причин таких, как затекание одного тела, находящегося в жидком состоянии, в поры и микродефекты другого, развитие высокоэластической или вынужденноэластической деформации.
В общем виде адгезионная прочность Ad (оцениваемая удельной работой адгезионного разрушения склейки) выразится в виде:
 (1)
(1)
где Ui — энергия одной адгезионной связи i-го типа; nti — число связей i-гo типа на единицу поверхности, установившееся ко времени начала разрушения.
Предложено несколько теорий адгезии. Вокруг них было много споров, связанных, вероятно, с переоценкой их достоинств. В большинстве теорий рассматривается образование адгезионной связи. Хотя в каждой теории утверждается, что она объясняет явление адгезии, в действительности же любая из предложенных теорий имеет дело лишь с одним определенным аспектом сложного явления. Таким образом, объединенная теория была бы более корректной и полезной. В настоящее время известны механическая теория, адсорбционная, электрическая, диффузионная, химическая, электрорелаксационная теория адгезии, а также некоторые другие концепции, по-разному трактующие механизм адгезии.
Ниже буду рассмотрены некоторые наиболее обоснованные теории адгезии.
Химическая теория адгезии
Химическая теория адгезии исходит из того, что на границе раздела адгезив - субстрат возможно образование межфазных химических связей. Энергия химической связи обычно составляет около 80 ккал/моль, в то время как энергия вандерваальсова взаимодействия всего 2,5 ккал/моль, и поэтому естественно, что образование химических связей в поле межфазного контакта будет эффективно способствовать адгезии. Тот факт, что наличие химической связи в огромной степени увеличивает адгезионную прочность, был доказан экспериментально. Было установлено, что в результате образования химической связи адгезионная прочность возрастает примерно в 35 раз по сравнению с вандерваальсовым взаимодействием, что соответствует соотношению между энергиями этих связей. Функциональные группы с высокой реакционной способностью - карбоксильные, аминные, амидные, гидроксильные, эпоксидные и изоцианатные - способствуют адгезии на различных субстратах[7].
Диффузионная теория адгезии
Представления о взаимной диффузии полимеров и о связи этих процессов с явлениями адгезии и аутогезии существуют давно. Изучение явления срастания было начато с тел одинаковой природы, и для него был предложен термин «аутогезия».
Аутогезия связывалась с присутствием на поверхности полимеров свободных подвижных концов макромолекул, за счет которых происходило «сплавление» двух приведенных в контакт поверхностей. Общепризнано мнение, что в основе этих процессов лежит явление диффузии макромолекул или их участков.
Диффузия может иметь место также при склеивании разнородных полимеров. Адгезия полимеров сводится к диффузии макромолекул или их отдельных участков и к образованию вследствие этого между адгезивом и субстратом «спайки», представляющей собой постепенный переход от одного полимера к другому. Представления о решающей роли диффузии при установлении адгезионной связи, особенно в системах полимер — полимер, получили широкое распространение под названием диффузионной теории адгезии[6].
Роль взаимной или даже односторонней диффузии при образовании адгезионных соединений в некоторых случаях может оказаться весьма значительной. Диффузия — один из весьма эффективных способов достижения молекулярного контакта между адгезивом и субстратом. Чем глубже макромолекулы адгезива внедряются в субстрат, тем более благоприятны условия для реализации максимально возможного числа связей между молекулами адгезива и субстрата. Однако это не означает, что без диффузии макромолекул адгезива в субстрат нельзя достичь высокой адгезионной прочности. Но поскольку в реальных системах имеются факторы, снижающие величину адгезионной прочности, диффузия макромолекул адгезива в субстрат может оказаться весьма полезной. Если макромолекулы адгезива при образовании адгезионной связи продиффундируют в субстрат на значительную глубину, то суммарная величина межмолекулярных взаимодействий может превысить силы, необходимые для разрыва химических связей. Этот эффект связан с цепным строением молекул полимерных адгезивов[6].
Часто полагают, что движущей силой диффузии является градиент концентрации. Однако перемещение, вызванное градиентом концентрации и приводящее к постепенной гомогенизации системы, не исчерпывает все возможные проявления этого сложного процесса. Весьма часто при диффузии происходит не выравнивание концентраций, а наоборот, дальнейшее разделение компонентов системы. Поэтому более правильно считать, что движущей силой диффузии является разность термодинамических потенциалов. Выравнивание термодинамических потенциалов и приближение к термодинамическому равновесию достигается за счет теплового движения атомов (молекул)[6].
В основу молекулярно-кинетического диффузии в полимерах положены представления о тепловых флуктуациях в жидкостях. Молекулы диффундирующего вещества передвигаются в конденсированном теле отдельными импульсами через «дырки» — микрополости, которые возникают в результате тепловых флуктуаций кинетических единиц, атомов и молекул в массе конденсированного тела в непосредственной близости от диффундирующей молекулы.
Диффузия в полимерах неразрывно связана с гибкостью макромолекул. Чем выше гибкость макромолекулы, тем богаче набор ее конформаций и тем меньше размер сегмента. Чем меньше, размер сегмента, тем более независимо движутся отдельные части макромолекулы, тем чаще по соседству с молекулой диффундирующего вещества возникают флуктуации плотности и образуются микрополости и тем быстрее передвигается диффундирующее вещество в полимере. У эластомеров величина сегмента составляет несколько звеньев. У стеклообразных полимеров размеры сегментов соизмеримы с размерами макромолекул, т. е. практически независимое перемещение звеньев отсутствует. Сетка в пространственных полимерах оказывает существенное влияние на гибкость. Особенно заметно влияние сетки, когда длина участков цепей между узлами сетки оказывается одного порядка с размерами сегментов[6].
Диффузия в стеклообразных и кристаллических полимерах характеризуется очень низким коэффициентом диффузии. Однако часто в подобных материалах имеется система внутренних полостей, трещин и капилляров, что оказывает существенное влияние на диффузию.
В металлах и стеклах диффундирующее вещество внедряется в кристаллы и диффундирует в междоузлия решетки. Понятно, что таким образом могут диффундировать только атомы и молекулы очень небольших размеров. Объемная диффузия может осуществляться и путем обмена местами в кристаллической решетке, а также через вакансии («дырки»). Кроме того, имеется и другой вид активированной неспецифической диффузии — диффузия вдоль трещин молекулярных размеров, по границам зерен и т. д. При понижении температуры более чувствительная к ней диффузия в решетку уменьшается и начинает возрастать диффузия вдоль границ зерен. Вообще этот вид диффузии в металлах и стеклах является преобладающим.
Кроме диффузии макромолекул следует учитывать диффузию через границу раздела различных низкомолекулярных веществ — ингредиентов, входящих в состав адгезива и субстрата, примесей, непрореагировавших мономеров и т. п. В результате диффузии этих веществ могут измениться прочностные свойства адгезива и субстрата, что в свою очередь повлияет на величину адгезионной прочности[6].
Положительной стороной диффузионных представлений в адгезии является именно учет особенности полимерных адгезивов — цепное строение и гибкость их макромолекул. И хотя применимость диффузионных представлений в адгезии к реальным системам весьма ограничена и определяется выполнением по крайней мере двух условий: термодинамического (полимеры должны быть взаиморастворимы) и кинетического (макромолекулы и их звенья должны обладать достаточной подвижностью), — следует учитывать их роль при изучении условий формирования молекулярных контактов.
Электрической теории адгезии
Простой контакт с последующим разъединением двух разнородных металлов достаточен для их электризации. Контактная электризация обнаруживается также при разделении (без трения) пары металл—диэлектрик и двух диэлектриков. Электризация при трении двух диэлектриков известна с глубокой древности. Очевидно, электризация при трении и при отрыве (без трения) имеет одну и ту же природу, так как трение является последовательным установлением и нарушением контактов.
Процессы, лежащие в основе статической электризации, весьма сложны, многообразны по природе недостаточно изучены. Наиболее общий характер имеет идея Гельмгольца о двойном электрическом слое — молекулярном конденсаторе, возникающем в зоне контакта двух различных поверхностей. При нарушении контакта обкладки этого конденсатора разъединяются и на каждой из них обнаруживаются заряды противоположного знака. Следовательно, причина статической электризации лежит в разделении зарядов двойного электрического слоя. При установлении контакта адгезивов с субстратами различной природы в большинстве случаев также возникает двойной электрический слой[6].
Возможным механизмом образования двойных электрических слоев является поверхностная ориентация нейтральных молекул, содержащих, полярные группы. Этот случай электризации при контакте соответствует процессам, протекающим на границе субстрат—полимерный адгезив, независимо от того, является ли субстрат металлом, стеклом, полимером и т. д. Подавляющее большинство диэлектриков содержит полярные группы. В массе вещества их дипольные моменты взаимно компенсированы, а на поверхности — нет. При контакте с металлом или диэлектриком происходит ориентация поверхностных диполей, и поверхность приобретает заряд определенной величины и знака. Таким образом, возникновение зарядов на поверхностях при контакте металла и диэлектрика или двух диэлектриков связано с эффектом ориентации. При установлении контакта полимерных адгезивов с субстратами различной природы на границе раздела возникает двойной электрический слой. Этот процесс развивается в соответствии с описанными механизмами и является следствием химического взаимодействия адгезива и субстрата, образования водородных связей, донорно-акцепторного взаимодействия, ориентированной адсорбции дипольных молекул адгезива на поверхности субстрата, различного сродства к электрону адгезива и субстрата. Во всех этих случаях устанавливается такое распределение электронной плотности, что суммарный эффект приводит к образованию двойного слоя на границе раздела. При отрыве пленки полимера на одной поверхности преобладают положительные заряды, на другой — отрицательные. Все это легло в основу электрической теории адгезии[6].
Изучение электрических сил стимулировалось следующими обстоятельствами. Во-первых, некоторые аспекты адгезионных явлений не находили удовлетворительного разрешения в рамках существовавших представлений. В частности, недостаточно ясна была природа зависимости адгезионной прочности от скорости приложения разрушающего усилия. Поэтому возникло предположение, что прочность адгезионного соединения не может быть обусловлена действием только одних молекулярных сил. Было выдвинуто представление о дополнительном факторе — роли двойного электрического слоя, возникающего на границе адгезив — субстрат. Во-вторых, учет электрических сил впервые позволил объяснить различные электрические явления, происходящие при нарушении адгезионного взаимодействия поверхностей, образовавшихся при разрушении адгезионного соединения, возникновение электрических разрядов, сопровождающихся характерным треском и свечением, электронную эмиссию и, наконец, чрезмерно-высокие значения работы отслаивания[6].
Методы равномерного отрыва
Методом равномерного отрыва измеряют величину усилия, необходимого для отделения адгезива от субстрата одновременно по всей площади контакта. Усилие при этом прикладывается перпендикулярно плоскости клеевого шва, а величина адгезии характеризуется силой, отнесенной к единице площади контакта (в Г/см2 или кГ/см2). Некоторые из этих методов стандартизованы.
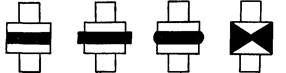
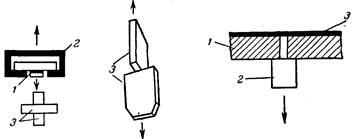
Рис. 3. Резино-металлические образцы для определения адгезии резины к металлам.
Чаще всего для измерения адгезии пользуются образцами грибкового типа, между торцовыми поверхностями которых находится адгезив. Таким способом измеряют, например, адгезию резины к металлам. Формы грибков и прослоечной резины весьма различны (рис. 3).
Чтобы избежать образования шейки при испытании, предложены образцы с диаметром резинового диска, превышающим диаметр металлического грибка. В последнее время рекомендованы грибки конической формы. Однако ценность такой модификации сомнительна: концентрация усилий у вершины конуса, а также сочетание сдвига с отрывом создают весьма сложное распределение напряжений. Образцы грибкового типа или просто склеенные торцами цилиндры используются также для определения адгезии клеев к металлам. Клеевая прослойка в этом случае имеет толщину нескольких сотен микрон (рис. 4).
Для измерения адгезии лакокрасочных покрытий два грибка или цилиндра, имеющие на торцовой части уже сформированное покрытие, склеивают специально подобранным клеем, адгезия которого к покрытию должна быть выше, чем адгезия покрытия к подложке. К поверхности покрытия, нанесенного на подложку, иногда приклеивают отрывающее приспособление, а затем прикладывают усилие, направленное перпендикулярно поверхности покрытия. Применение этого метода ограничено из-за трудности подбора соответствующего клея.
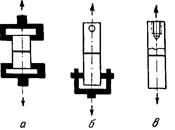
Рис. 4. Схемы измерений адгезии полимеров к металлам:
а—цилиндрические образцы—грибки; б—цилиндрические или призматические образцы с осевым креплением; 3—то же, с резьбовым креплением.
Адгезию резины к ткани также иногда определяют этим методом. Образцы приготавливают следующим образом. Ткань приклеивают к торцовым поверхностям деревянных цилиндров, выступающие края ткани загибают и крепят проволокой в выточке на цилиндре. Сырую резину накладывают на ткань и проводят вулканизацию. Подобным методом иногда измеряют адгезию заливочных компаундов к металлам, полимеров к стеклу, определяют прочность связи между слоями в стеклопластиках и т. д. На рис. 5. показаны некоторые схемы испытаний по этим методам. Иногда вместо склеенных встык цилиндров для измерения адгезии методом отрыва применяют образцы в виде крестовины (рис. 6). Таким методом измеряют адгезию клеев к металлам, дереву и стеклу[6].
В образцах типа грибков и крестовин под действием нагрузки возникают сложные и неоднородные напряжения. Адгезив растягивается сильнее, чем субстрат, и в большей степени подвергается поперечному сжатию. Вследствие этого возникают сдвиговые напряжения. Результирующие напряжения в слое адгезива оказываются неодинаковыми в различных местах площади контакта. Кроме того, растягивающее усилие не всегда прикладывается точно по оси образца. Все это вызывает наряду с отрывом появление расслаивания. Ускоренная киносъемка показала отсутствие параллельности поверхностей склейки непосредственно в момент отрыва.

Рис. 5. Схемы измерений адгезии полимеров к различным материалам методом отрыва:
а—резина к ткани (I — ткань, укрепленная на деревянном грибке; 2— резина);
б — смола к стеклу (1-металлические цилиндры; 2 - стеклянные пластинки;
3 — клей; 4 — слой смолы); в — заливочные компаунды к металлам (1— металлическая подложка; 2—компаунд; 3— держатели).
Более равномерного распределения напряжений можно добиться увеличением длины цилиндрического образца и уменьшением площади склеивания, что снижает влияние расслаивания при отрыве. В образцах типа крестовин особенно велика неоднородность напряжений. Так как нагрузка прикладывается к концам брусков, они стремятся изогнуться, поэтому приходится пользоваться массивными образцами. При переходе к более толстым блокам сопротивление отрыву возрастает, что объясняется снижением гибкости блоков и соответственно более равномерным распределением напряжений[6].
|
| |
| Рис. 6. Определение адгезии клеев к различным материалам на образцах в форме крестовины; 1 — клеевой шов; 2 — захват для крепления образца при испытании; 3— бруски. | Рис. 7. Принципиальная схема измерения адгезии методом штифтов: /—планка с отверстиями; 2—штифт; 3— пленка покрытия. |
Метод скрещенных нитей, в котором две кварцевые нити, покрытые пленками полимеров, приводятся в контакт, а затем отрываются друг от друга, позволяет измерить работу отрыва, по которой судят об адгезии. Этот метод оказался весьма эффективным для изучения кинетики прилипания тел в самых различных условиях. Метод скрещенных нитей основан на том предположении, что имеет место точечный контакт (поскольку применяются нити диаметром 20—100 мк) и нарушение контакта происходит мгновенно по всей площади путем равномерного отрыва. В действительности получить точечный контакт не удается, а определить истинную площадь контакта не представляется возможным. Это является одной из причин плохой воспроизводимости результатов. В тех случаях, когда адгезив и субстрат после приведения их в контакт подвергают полимеризации, вулканизации или какому-либо другому необратимому химическому превращению, этот метод вообще неприменим.
Интересный метод определения адгезии покрытий к подложкам основан на- отделении подложки от покрытия путем отрыва. Впервые он был разработан для определения сцепляемости электролитических осадков металлов с основой, а затем использован для определения адгезии полимерных покрытий к металлам. Сущность метода сводится к следующему. В планке-подложке прямоугольного сечения просверливаются отверстия, в которые вставляют цилиндрические или конические штифты по скользящей посадке. Торцы штифтов шлифуются вместе с планкой, затем на эту плоскость наносится покрытие. После формирования покрытия штифты выдергиваются (рис. 7). Однако метод штифтов может оказаться непригодным при использовании покрытий в виде растворов с низким поверхностным натяжением: трудно будет избежать затекания раствора в зазор между штифтом и стенкой отверстия. Кроме того, пленка покрытия должна обладать определенной механической прочностью, чтобы не произошло вместо отслаивания штифта разрушения пленки.
Имеется несколько методов отрыва адгезива от субстрата (или наоборот) путем сообщения адгезиву или субстрату ускорения[6].
Методы сдвига
Касательные напряжения создают в клеевых конструкциях различными путями, например растяжением соединенных внахлестку материалов. Этим методом измеряют адгезию металлов, древесины, пластмасс, а также резины к резине и металлам. Различные схемы испытаний на сдвиг при растяжении образцов показаны на рис. 8.
Установлено, что разрушающее напряжение не зависит от ширины образца, но линейно зависит от его длины до некоторого предела. При дальнейшем увеличении длины образца разрушающая нагрузка стремится к постоянной величине. Причина этого заключается в концентрации напряжений у концов образца, вызванной разностью деформаций склепных элементов и их изгибом.
Испытание клеевых соединений на сдвиг (срез) под действием сжимающих нагрузок (рис. 9) наиболее характерно для соединения материалов значительной толщины. Иногда этим методом испытывают и образцы из тонких слоев металла, но в таких случаях к ним подклеивают для устойчивости толстые деревянные бобышки.
| 
|
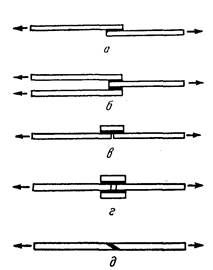
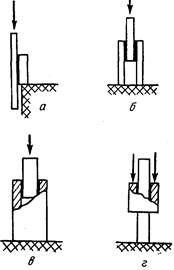
| Рис. 8. Схема испытаний клеевых соединений на сдвиг растягивающей нагрузкой: и—шов односторонний внахлестку; б—двусторонний внахлестку; в—односторонний внахлестку с накладкой; г — двусторонний внахлестку с накладкой; д — скошенный шов. | Рис. 9. Схемы испытаний клеевых соединений на сдвиг сжимающей нагрузкой': а—одностороннее соединение плиточных материалов; б—двустороннее соединение плиточных материалов; в, г— соединение цилиндра со стержнем, |
Испытание на сдвиг при кручении образцов имеет перед рассмотренными методами растяжения и сжатия одно важное преимущество: при кручении возникает чистый сдвиг без отрывающего усилия. В наиболее чистом виде сдвиг реализуется при скручивании двух тонкостенных цилиндров, склонных торцами. На рис. 10 приведены схемы испытаний клеевых соединений скручиванием. Описанный в предыдущем разделе метод штифтов также вполне пригоден для испытаний кручением. Получаемые при этом результаты не зависят от толщины покрытия. Известен также способ измерения адгезии покрытий путем скручивания приклеенных торцами к поверхности покрытия цилиндрических полых или сплошных стержней[6].
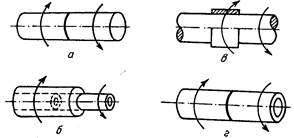
Рис. 10. Схемы испытаний клеевых соединений на сдвиг при кручении:
а— соединение прутков встык; б— соединение труб внахлестку; в—соединение прутка с трубой внахлестку; г— соединение труб встык.
Широкое распространение получили методы измерения адгезии путем выдергивания из блока полимера введенной туда заранее нити корда, металлической проволоки или стеклянной нити (волокна). Часто таким способом определяют адгезию кордной нити и металло- корда к резине. В настоящее время наиболее распространён Н-метод (Аш- метод), названный так из-за формы образца, напоминающего букву Н (рис.11). Этот метод используют и для определения адгезии стекловолокна к связующему (рис.12), а также для измерения адгезии в системе полимер—металл (рис.13).
|
| |
| Рис. 11. Схема измерения прочности связи корда (текстильного или металлического) с резиной: 1—держатели образца; 2— резиновые блоки; 3—нить. | Рис. 12. Схема измерения адгезии стекловолокна к связующему; /—волокно; 2— слой смолы, нанесенной на волокно. |
Сдвиговые усилия возникают на границе между адгезивом и субстратом и в случае деформации полимерного блока, внутри которого находится субстрат. На этом принципе основан метод измерения адгезии резины к текстилю. При испытании по методу отслоения при статическом сжатии нить корда располагают внутри образца по диаметру среднего сечения. Испытание заключается в определении усилия сжатия, при котором сдвиговые напряжения между резиной и кордом достигают величины, равной прочности связи между материалами. В тот момент, когда воронкообразное углубление, возникшее на поверхности образца при его сжатии, исчезает (рис. 14), измеряют нагрузку. Момент отслоения нити определяют визуально или с помощью тензодатчиков, контролируя величину внутренних напряжений[6].
При испытании по 1-методу (Аш- методу) кордная нить расположена внутри резинового образца по его длинной оси. Нагрузка при растяжении образца монотонно возрастает, а в момент начала отслоения нити наблюдается некоторое уменьшение напряжения. Отслоение второго конца нити приводит к повторному спаду напряжения, а сам образец при этом сильно вытягивается. Широкого распространения этот метод не получил.
Аналогичен описанному метод измерения адгезии покрытий к металлам. При формировании пленки в нее вводят отрезки металлической проволоки. Растяжение пленки приводит к отслоению проволоки от полимера.
Для определения адгезии связующего к стеклянным нитям иногда применяют цилиндрические образцы, изготовленные из ориентированных стеклянных нитей, пропитанных полиэфирной или эпоксидной смолой. Об адгезии судят по сопротивлению сжатию вдоль оси этих цилиндров.
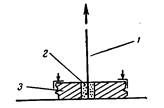
| 
|
| Рис. 13. Схема измерения адгезии клея к металлам: /—металлическая нить; 2—слой клея; 3— планка с отверстием. | Рис. 14. Схема измерения прочности связи резины с кордом при статическом сжатии: а—образец до испытания; б—сжатый образец; в—сжатый образец после отслоения нити. |
Некоторые из рассмотренных в этом разделе методов стандартизованы.
Динамические методы
Все рассмотренные методы измерения адгезии характеризуются кратковременным приложением нагрузки. Это так называемые статические методы. Но помимо обычных статических испытаний в некоторых случаях проводят измерения адгезии путем приложения знакопеременных циклически изменяющихся нагрузок, ударных и длительных статических нагрузок.
Практически многие методы, применяющиеся при статических кратковременных испытаниях, могут быть использованы и для испытаний на длительную статическую прочность. В первую очередь это относится к испытаниям клеевых соединений металлов других материалов.
Особую ценность представляют динамические испытания, с помощью которых устанавливается способность соединения адгезив — субстрат противостоять действию переменных нагрузок. Работоспособность изделия или модельного образца характеризуют числом циклов деформации до разрушения. Однако не всегда удается добиться разрушения образца по стыку. В таких случаях после приложения некоторого числа циклов деформации определяют адгезию одним из принятых статических методов и сравнивают прочность связи до и после утомления, определяя, таким образом, величину уменьшения адгезии в результате воздействия циклической нагрузки[6].
Велико значение динамических методов измерения адгезии в некоторых клеевых соединениях металлов, резин, резин с металлами и кордом. Динамические испытания клеевых соединений металлов проводят при сдвиге, неравномерном и равномерном отрыве.
При измерении усталостной прочности с помощью неравномерного отрыва для клеевых соединений рекомендуются образцы, показанные на рис.2,а. Усталостные испытания соединений металлов при сдвиге проводят на образцах, соединенных внахлестку (см. рис. 8, а), или на образцах, имеющих форму параллелепипеда, образованного двумя параллельными металлическими пластинками, промежуток между которыми заполнен резиной. Для усталостных испытаний соединений металлов при равномерном отрыве используют образцы, склеенные встык (см. рис. 4). Машины, применяемые для усталостных испытаний, должны обеспечивать нагружение с частотой 500—3000 циклов в 1 мин. Определение динамической прочности связи двух резин, а также резин со слоями корда может быть проведено на образцах различной формы. Можно осуществить при многократном сжатии и сдвиге различные синусоидальные динамические режимы: постоянство динамической нагрузки, постоянство деформации, постоянство произведения амплитуд силы и смещения. Во всех случаях на границе между резинами возникают касательные напряжения, достигающие максимума при расположении плоскости стыка под углом 45°. Применение цилиндрических образцов благоприятствует более равномерному распределению напряжений. Условия испытаний варьируются в зависимости от типов применяемых резин, размеров и формы образцов. Частота нагружений колеблется от 250 до 850 циклов в 1 мин[6].
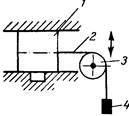
Рис. 15. Схема измерения динамической прочности связи единичной нити корда с резиной при многократном сжатии образца: 1— резина; 2—кордная нить; -3 — направляющий ролик; 4 -груз (1-2кГ).
Известны методы определения прочности связи единичной нити корда с резиной в динамических условиях. В этих случаях удается нагружать не только образец в целом, но и отдельную нить и точно задавать основные параметры режима. Описан, например, метод многократных деформаций изгиба на роликах резиновой пластины с завулканизованными в нее нитями корда. После утомления измеряли прочность связи выдергиванием нити (по типу Н-метода). Широкое распространение получил метод многократного изгиба цилиндрического образца, по оси которого проходит
кордная нить, выдергиваемая после утомления. Аналогичный метод испытания применяется и у нас: цилиндрические образцы с кордной нитью по диаметру среднего сечения подвергаются многократному сжатию до отслоения и выдергивания нити (рис.15). Динамическое разнашивание резины не наблюдается в гантелевидных образцах, укрепляемых в специальных держателях, так как в этих случаях образцы подвергаются знакопеременным деформациям растяжения — сжатия.
Теоретические основы метода
Большое разнообразие процессов взаимодействия электронов с веществом делает возможным использовать электроны для изучения разных характеристик вещества. Основной характеристикой электронов, которая определяет характер их взаимодействия с веществом и, следовательно, характер получаемой информации о веществе, является скорость электронов или, точнее, их кинетическая энергия.
С помощью электронных линз можно получить сфокусированный пучок электронов на поверхность объекта (электронный зонд). Получаемая при этом информация будет относиться к ограниченному участку поверхности (или объему) объекта. Электронно-зондовые приборы по существу могут давать микроскопические изображения, контраст которых обусловлен тем или иным эффектом взаимодействия электронов зонда с объектом (характеристическое рентгеновское излучение, упруго рассеянные или отраженные электроны и др.), а разрешающая способность обусловлена размером зонда и областью, в которой генерируется то или иное излучение[8].
На рис.20 показаны размеры областей объекта, относящихся к разным эффектам взаимодействия электронного луча с веществом.
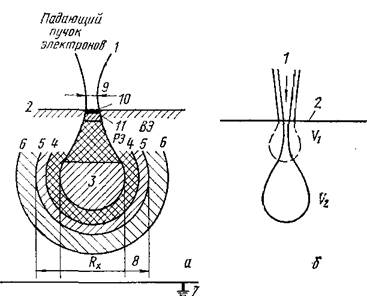
Рис. 20. Области возбуждения в объекте разных процессов взаимодействия электронов с веществом (металл), используемых в электронно-оптических приборах для анализа состава или микроструктуры (а), и те же области, но при разной энергии электронов зонда (б):
1—падающий пучок электронов; 2 — поверхность объекта (мишень); 3—первичное возбуждение рентгеновских лучей; 4 — граница возбуждения рентгеновских лучей торможения; 5—область возбуждения вторичного (флюоресцентного) рентгеновского излучения; 6 — область рассеяния рентгеновских лучей и дифракция Косселя; 7—ток образца; 8 — возможное разрешение для рентгеновского микроанализатора ( R х ); 9—диаметр зонда; 10 — область, от которой регистрируются ОЖЕ- электроны: 11 — ВЭ и РЭ- области, от которых регистрируются вторичные и упруго рассеянные электроны V1; V2 — области возбуждения при разном ускоряющем напряжении; V1> V2 [8]
Наиболее универсальное значение имеют регистрация вторичных электронов и регистрация отраженных (или «рассеянных обратно») электронов. Те и другие электроны улавливаются коллектором, установленным возле образца, преобразуются в электрический сигнал, который усиливается и затем направляется к электронно-лучевой трубке, где он модулирует яркость электронного луча, строящего изображения на экране этой трубки.
СОДЕРЖАНИЕ
| Введение…………………………….……………………………… ………….….…. | 2 |
| 1. Структура и свойства эпоксидных смол…………………………….……….…. | 3 |
| 1.1. Получение эпоксидных смол ...…………….…………………………….…... | 3 |
| 1.2. Структура и свойства неотверждённых смол……….………………….……. | 7 |
| 2. Отверждение эпоксидных смол, их структура и свойства в отверждённом состоянии……………………………………………………………………………. | 10 |
| 2.1. Оверждение эпоксидных смол………………………………………………... | 10 |
| 2.2. Структура и свойства отверждённых эпоксидных смол……………………. | 16 |
| 3. Теоретические основы адгезии и экспериментальные методы определения адгезионной порочности……….……………………………......……….….…….. | 19 |
| 3.1. Теории адгезии……….………………………………...……….……….…….. | 19 |
| 3.2. Методы измерения адгезионной прочности………………………….……… | 23 |
| 3.3. Характер разрушения адгезионных соединений……………………………. | 30 |
| 4. Адгезионные свойства эпоксидных смол к субстратам различной природы | 32 |
| 4.1. Адгезия эпоксидных смол к металлам……………………………………….. | 32 |
| 4.2. Адгезия эпоксидных смол к стеклу…………………………………………... | 33 |
| 4.3. Адгезия эпоксидных смол к различным волокнам………………………….. | 34 |
| 5. Растровая электронная микроскопия как метод исследования поверхностей адгезионного контакта и разрушения……….…………………. | 42 |
| 5.1. Теоретические основы метода……….……………………………….…….… | 42 |
| 5.2. Устройство и работа растрового электронного микроскопа……………….. | 43 |
| 5.3. Применение растровой электронной микроскопии в исследованиях адгезионных соединений……………………………………………………… | 45 |
| Заключение ………………………………………………………………………….. | 47 |
| Литература…………………………………………………………………………… | 49 |
ВВЕДЕНИЕ
Целью данной работы- изучить структуру и адгезионные свойства отверждённых эпоксидных смол.
Эпоксидные смолы обладают высокой адгезией к различным материалам и поэтому используются в качестве клеёв, связующих в композиционных материалах и в качестве различных покрытий. Поэтому задача этой работы заключается в том, чтобы изучить получение эпоксидных смол, процесс их отверждения и адгезионные свойства к конкретным материалам различной природы.
Работа состоит из пяти основных разделов. В первом будут рассмотрены вопросы получения эпоксидных смол, их структура и свойства в неотверждённом состоянии.
Во втором разделе речь идёт о механизмах отверждения смол, структуре и свойствах после отверждения.
В третьем разделе рассмотрены основные теории адгезии полимеров, методы которые используются для измерения адгезионной прочности на практике, а также возможный характер разрушения адгезионной системы.
Эпоксидные смолы обладают разными адгезионными свойствами к материалам различной природы. Об этом и рассказывается в четвёртом разделе.
Пятый раздел рассказывает о растровой электронной микроскопии, о её роли при исследовании адгезии.
1. Структура и свойства эпоксидных смол
Получение эпоксидиановых смол
Эпоксидиановые смолы получаются при взаимодействии дифенилпропана с веществами, содержащими эпоксидную группу 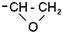 . Основным сырьём для производства смол являются эпихлоргидрин и 4,4' дигидроксидифенилпропан (диан).
. Основным сырьём для производства смол являются эпихлоргидрин и 4,4' дигидроксидифенилпропан (диан).
Эпихлоргидрин (3-хлор-1,2-эпоксипропан) представляет собой бесцветную жидкость с запахом хлороформа и кипит при 110 0С, плотность d=1,1807 г/см3. Получают его из аллихлорида по хлоргидринному методу:
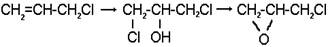
Молекула эпихлоргидрина содержит две активные группировки- эпоксидную и связь С-Сl. Эпоксидный цикл представляет собой почти правильный треугольник со значительно деформированными валентными углами (»600). Поэтому происходит только частичное перекрывание атомных орбиталей и энергия связей уменьшается:
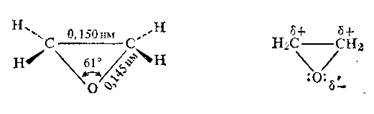
Эпоксидная группировка полярна и имеет дипольный момент m=6,28 10 -30 Кл м (1,88 D). Причинами этого являются полярность связей С—О и небольшой угол СОС, тогда как в обычных простых эфирах угол СОС равен 109 - 1120 и m==4-10-30...4,3-10-30 Кл м (1,2. . .1,3D).
Химические превращения эпоксидов определяются тем, что в молекуле имеются полярные связи С—О и атом кислорода с неподелёнными парами электронов. Связь С—О в эпоксидах разрывается легко, особенно в условиях кислотного катализа.
Дигидроксидифенилпропан (диан) представляет собой кристаллическое вещество с температурой плавления 156-157 оС:
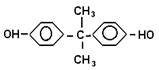
Его получают из фенола и ацетона в присутствии кислого катализатора.
Эпихлоргидрин взаимодействует по эпоксидной группе с активным атомом водорода. Образующийся хлоргидрин под действием основания подвергается дегидрохлорированию с образованием новой эпоксидной группы в глицидиловом производном, которая реагирует с активным атомом водорода другой молекулы и так далее; при дегидрохлорировании HCl связывается основанием (например, NaOH, давая в этом случае NaCl+H2O):
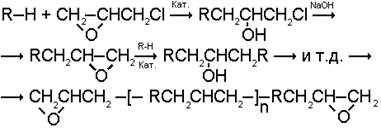
(Кат.- катализатор, в качестве которого используют основания, кислоты, соли металлов: n=0-3). Если реакцию проводят в присутствии кислот, то на концах молекул остаются хлоргидриновые группы; поэтому для осуществления дегидрохлорирования добавляют щёлочь.
Молекулярная масса эпоксидиановых смол определяется соотношением исходных соединений. Из-за протекания побочных реакций (гидролиз эпихлоргидрина до глицерина и эпоксигрупп глицидиловых производных до a-гликолевых групп, изомеризация эпоксидных групп в карбонильные и взаимодействие первых с образующимися гидроксильными, образование концевых 1,3-хлоргидриновых групп 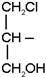 , не замыкающихся в эпоксидный цикл) и из-за обратимости дегидрохлорирования, обуславливающей наличие 1,2-хлоргидриновых групп, количество эпоксидных групп в молекуле эпоксидиановой (или эпоксидной) смолы всегда меньше теоретического (например, в случае бифункциональных исходных соединений 1,5 - 1,9).
, не замыкающихся в эпоксидный цикл) и из-за обратимости дегидрохлорирования, обуславливающей наличие 1,2-хлоргидриновых групп, количество эпоксидных групп в молекуле эпоксидиановой (или эпоксидной) смолы всегда меньше теоретического (например, в случае бифункциональных исходных соединений 1,5 - 1,9).
При взаимодействии дифенилпропана с эпихлоргидрином образуется полимер с прямой цепью, характеризующийся двумя функциональными группами- эпоксидной и гидроксильной. Строение неотверждённых ароматических эпоксидиановых смол может быть выражено следующей формулой :

Она содержит две конечные эпоксидные группы, и поэтому её рассматривают как диэпоксид.
Вдоль цепи имеются гидроксильные группы, число которых зависит от молекулярного веса смолы. Изменяя соотношение между количеством эпихлоргидрина и дифенилпропана, можно получить смолы с цепью различной длины и с различным процентным соотношением эпоксидных и гидроксильных групп. В зависимости от молекулярного веса и процентного содержания функциональных групп эти смолы могут быть как жидкими, так и твёрдыми продуктами. Чем выше молекулярный вес и меньше процентное содержание эпоксидных групп, тем выше температура плавления этих смол. Растворимость смол также обусловлена величиной их молекулярного веса. Характеристики некоторых эпоксидных смол отечественных и зарубежных марок приведены в таблице 1.
Таблица 1
Характеристики эпоксидиановых смол [3].
| Техническое наименование | Температура размягчения оС | Молекулярный вес | Содержание эпоксидных групп % |
ОТЕЧЕСТВЕННЫЕ МАРКИ
ЭД-5
5-7
400
25
ЭД-6
3-5
550
18
ЭД-13
50-55
1500
8-10
ЭД-15
60-70
2200
5-7
ЗАРУБЕЖНЫЕ МАРКИ
Эпон 1064
40-45
-----
12,5
Эпон 1001
64-76
900
8,6
Эпон 1004
97-103
1400
5,2
Эпон 1007
127-133
2900
2,0
Эпон 1009
145-155
3750
1,3
При синтезе низкомолекулярных диановых эпоксидных смол ( мол. масса 350-450) обычно раствор дифенилолпропана (1 моль) в эпихлоргидрине (8-10 моль) нагревают до кипения и постепенно (5-8 часов) добавляют к нему 40%-ный водный раствор NaOH (2,2 моль). При этом непрерывно отгоняют воду в виде азеотропной смеси с эпихлоргидрином, который после отделения воды возвращают в реактор. После окончания процесса непрореагированный эпихлоргидрин отгоняют под вакуумом, эпоксидиановую смолу растворяют в толуоле, толуольный раствор промывают водой для удаления NaCl. Затем толуол отгоняют, сначала при атмосферном давлении, потом под вакуумом при температуре до 140-150 оС.
Смолы с молекулярной массой 500-1000 получают аналогичным способом, но при молярном соотношении дифенилолпропан : эпихлоргидрин, равном 1: (1,5-1,9), причём процесс ведут в среде растворителя (ксиол, толуол, их смеси с бутиловым спиртом или циклогексаном).
Смолы с молекулярной массой 1000-3500 синтезируют взаимодействием низкомолекулярной эпоксидиановой смолы с дифенилолпропаном в расплаве при 140-210 оС (катализаторы- третичные амины, мочевина, Na2CO3) или дифенилпропана с эпихлоргидрином в присутствии щёлочи в гетерогенных условиях в системах вода – органический растворитель (обычно изопропанол или бутанол) при 70-80 оС. Во втором случае в меньшей степени протекают побочные реакции, получаемые эпоксидиановые смолы имеют более узкое молекулярно-массовое распределение, сравнительно узкий интервал эпоксидных чисел, отличаются более светлым цветом.
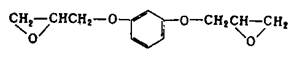
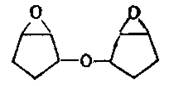
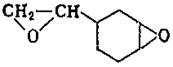
Из других эпоксидных смол, содержащих в молекуле глицидиловые группы, наибольшее практическое применение получили глицидиловые производные феноло-формальдегидных новолачных смол(II) (здесь и далее римскими цифрами указана нумерация эпоксидных смол в таблице 2), продуктов конденсации фенола с акролеином (III) и глиоксалем (IV), галогенированного дифенилолпропана (V), ароматических моноаминов (VI) и диаминов (VII), аминофенолов (VIII), циануровой кислоты (IX), резорцина (X), гликолей (XI). Промышленное значение получили также олигомерные диглицидилуретаны - продукты взаимодействия глицидола с олигомерными диизоцианатами, полученными на основе олигодиенидилов молекулярной массой 2000-4000, простых или сложных полиэфиров молекулярной массой 1000-2000. Эпоксидиановые смолы, содержащие эпоксидные группы в алифатических циклах или цепях, получают эпоксидированием (обычно надуксусной кислотой) двойных связей ненасыщенных соединений; практическое значение имеют диэпоксиды гексагидробензаль- 1,1-бис- (оксиметил) циклогексана (XIII), тетрагидробензилового эфира тетрагидробензойной кислоты (XIV), дициклопентенилового эфира (XV), дициклопентадиена (XVI), винилциклогексана(XVII), эпоксидированные олигомеры дивинила.
Таблица 2
Эпоксидные смолы [2].
 II II
|
 III III
|
 IV IV
|
 V V
|
 VI VI
|
 VII VII
|
 VIII VIII
|
 IX IX
|
 X X
|
 XI XI
|
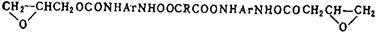 XII XII
|
 XIII XIII
|
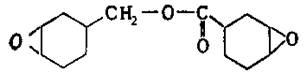 XIV XIV
|
 XV XV
|
 XVI XVI
|
 XVII XVII
|
Дата: 2019-07-30, просмотров: 309.