Синтезированы пептиды, соответствующие сигнальной последовательности дикого типа, а также мутантные сигнальные пептиды белка LamB наружной мембраны и исследовано их взаимодействие с модельными фосфолипидными мембранами и везикулами Е.coli. Показано, что пептид, соответствующий сигнальной последовательности дикого типа, эффективно ингибирует in vitro перенос предшественников как периплазматичекого белка, так и белка наружной мембраны, а пептид, соответствующий мутантной сигнальной последовательности, дефектной по экспорту, не ингибирует перенос в бесклеточной системе. Это означает, что сигнальные пептиды узнают какой-то общий рецептор в цитозольной или мембранной фракции. Кроме того, эффективность связывания этих пептидов с модельными мембранами (монослоем и бислоем) коррелирует с их способностью служить сигналом переноса. Корреляция между гидрофобностью сигнальной последовательности и способностью инициировать транслокацию обнаруживается и при использовании предшественника мальтозосвязывающего белка.
Эти данные согласуются с моделью, согласно которой первичная сигнальная последовательность определяет локализацию полипептидного предшественника в мембране путем неспецифических взаимодействий с липидным бислоем, после чего осуществляется более специфическое связывание с белковым рецептором. Сходная модель была предложена для амфифильных пептидных гормонов. Но сигнальный пептид в животных клетках до его связывания с мембраной взаимодействует с каким-то растворимым рецептором. Какое значение для сигнального пептида имеет его способность связываться с липидами – остается неясным.
Сигнальные пептидазы
Для удаления временных N-концевых сигнальных пептидов необходимы специфические белки. Наиболее полно охарактеризованы сигнальные протеазы из Е.coli. Большинство экспортируемых белков Е.coli содержат сигнальный пептид, который отщепляется на периплазматической поверхности внутренней мембраны с помощью лидер-пептидазы; ее структура представлена на рис.2.
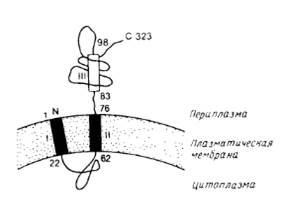
Рис.2. Предполагаемая топология лидер-пептидазы из Е.coli.
Аминокислотные остатки пронумерованы. Прямоугольниками обозначены гидрофобные сегменты. Первый гидрофобный участок не был обнаружен экспериментально, вывод о его существовании был сделан исходя из его гидрофобности. Наличие и ориентация второго гидрофобного участка установлены экспериментально и, по-видимому, он функционирует как внутренняя сигнальная последовательность. Третий гидрофобный сегмент имеет слабо выраженный гидрофобный характер и является частью периплазматического домена.
Для переноса белков через внутреннюю мембрану эта пептидаза не нужна, но она необходима для высвобождения экспортируемого белка из цитоплазматической мембраны. In vitro очищенный фермент мог функционировать, будучи включенным в липосомы. Специфичность расщепления весьма высока, но не определяется исключительно аминокислотной последовательностью вблизи сайта расщепления. Сигнальная пептидаза, функционирующая в эндоплазматическом ретикулуме, имеет ту же специфичность, что и соответствующий фермент Е.coli, что неудивительно, если учесть сходство сигнальных последовательностей. Была очищена сигнальная пептидаза из микросом эукариот. Показано, что она ассоциирована с другими полипептидами, возможно имеющими отношение к механизму переноса.
У Е.coli имеется вторая сигнальная пептидаза, участвующая в процессинге пролипопротеинов. Эти полипептидные компоненты оболочки Е.coli замечательны тем, что при созревании их N-конец модифицируется с помощью глицерида. Пролипопротеиновая сигнальная пептидаза также находится в цитоплазматической мембране. После отщепления сигнальный пептид остается в цитоплазматической мембране и разрушается с помощью мембраносвязанного фермента протеазы ΙV.
В митохондриях и хлоропластах должно присутствовать несколько сигнальных пептидаз, поскольку процессинг происходит более чем в одном компартменте. Растворимую пептидазу из митохондриального матрикса удалось частично очистить, но охарактеризована она не полностью.
Дата: 2019-07-30, просмотров: 298.