Нефтяной газ при нормальных условиях содержит неполярные углеводороды – - смесь углеводородовв от С1 до С4 (метан, этан, пропан, изо-бутан и н-бутан). С точки зрения физики к ним можно применять законы для идеальных систем. С точки зрения математики - это аддитивная система. Аддитивность - (свойство) значение величины, соответствующее целому объекту, равно сумме значений величин, соответствующих его частям. Т.о., для оценки свойств нефтяного газа (при нормальных условиях) применимы аддитивные методы расчётов физико-химических и технологических параметров (Псмеси): 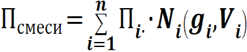 где Пi - параметр i-го углеводорода или неуглеводородного компонента; Ni - мольная доля; gi - весовая доля; Vi - объёмная доля; Например, плотность смеси газов рассчитывается следующим образом:
где Пi - параметр i-го углеводорода или неуглеводородного компонента; Ni - мольная доля; gi - весовая доля; Vi - объёмная доля; Например, плотность смеси газов рассчитывается следующим образом:
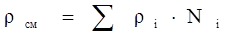 ρi – плотность i- того компонента; Ni – мольная доля i- того компонента. Плотность газа можно рассчитать через отношение молекулярной массы газа (Mi) к мольному объему (Vм). Например, для нормальных условиях (н. у.): rг = Mi / 22,414 Способы выражения состава. Нефтяной газ представлен в виде смеси углеводородов, поэтому для оценки его физико-химических свойств по формуле (Псмеси= ) необходимо знать, как выражается состав смеси. 1.Массовая (весовая) доля (gi) – величина (нормированная на 1 или 100%) характеризует отношение массы i-го компонента (mi), содержащегося в системе к общей массе системы:
ρi – плотность i- того компонента; Ni – мольная доля i- того компонента. Плотность газа можно рассчитать через отношение молекулярной массы газа (Mi) к мольному объему (Vм). Например, для нормальных условиях (н. у.): rг = Mi / 22,414 Способы выражения состава. Нефтяной газ представлен в виде смеси углеводородов, поэтому для оценки его физико-химических свойств по формуле (Псмеси= ) необходимо знать, как выражается состав смеси. 1.Массовая (весовая) доля (gi) – величина (нормированная на 1 или 100%) характеризует отношение массы i-го компонента (mi), содержащегося в системе к общей массе системы: 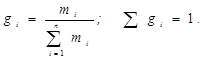 2.Молярная (мольная) доля (Ni) - отношение числа молей i-го компонента (ni) к общему числу молей в системе:
2.Молярная (мольная) доля (Ni) - отношение числа молей i-го компонента (ni) к общему числу молей в системе:
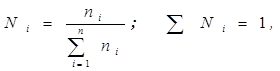
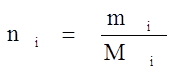
где mi - масса i-го компонента; Мi - молекулярный вес i-го компонента.
Из последних формул находим выражения для пересчетов массового и мольного составов: 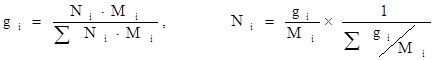
3.Объёмная доля - это доля (Vi), которую занимает компонент в объёме системы и с учетом предыдущих формул можно найти взаимосвязь ее с массовым и мольным составами:
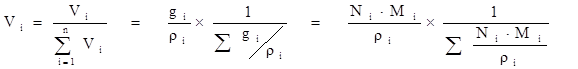
Для идеального газа соблюдается соотношение: объемная доля компонента (Vi) равна мольной доли компонента (Ni), т.е.Vi = Ni, как следствие закона Авогадро. Для идеальной системы, как нефтяной газ, состав его можно рассчитать на основе любых данных: масс компонентов, объемов, плотностей, парциальных давлений и др. 4.Молекулярная масса смеси рассчитывается по принципу аддитивности для смесей, состав которых выражен в мольных или объемных долях:
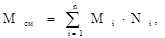 Для смесей, состав которых выражен в массовых процентах:
Для смесей, состав которых выражен в массовых процентах:
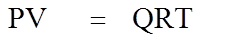
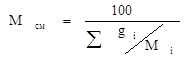
уравнением состояния Менделеева-Клайперона:
где Р - абсолютное давление, Па; V - объём, м3; Q - количество вещества, кмоль; Т - абсолютная температура, К; R - универсальная газовая постоянная, Па×м3/ (кмоль×град). Уравнение справедливо для идеальных газов при нормальном и близких к нормальному давлениях. При повышенном давлении газ сжимается.
Дата: 2019-07-24, просмотров: 355.