Содержание
1. Железоуглеродистые сплавы. Производство чугуна и доменный процесс
1.1 Железоуглеродистые сплавы
1.1.1 Фазовые состояния
1.1.2 Строение железоуглеродистых сплавов
1.1.3 Полиморфные превращения железоуглеродистых сплавов
1.2 Производство чугуна и доменный процесс
1.2.1 Доменный процесс
1.2.2 Продукты доменной плавки
2. Термическая обработка железоуглеродистых сплавов
2.1 Превращения в стали при нагревании
2.2 Превращения в стали при охлаждении
2.3 Основные виды термической обработки стали
2.3.1 Отжиг стали
2.3.2 Закалка стали
2.3.3 Отпуск стали
3. Медь и её сплавы. Область применения
3.1 Физические свойства
3.2 Химические свойства
3.2.1 Отношение к кислороду
3.2.2 Взаимодействие с водой
3.2.3 Взаимодействие с кислотами
3.2.4 Отношение к галогенам и некоторым другим неметаллам
3.2.5 Оксид меди
3.2.6 Гидроксиды меди
3.2.7 Сульфаты
3.2.8 Карбонаты
3.2.9 Качественные реакции на ионы меди
3.3 Сплавы
3.3.1 Латуни
3.3.2 Бронзы
3.3.3 Медноникелевые сплавы
3.4 Применение меди
Список использованных источников
Железоуглеродистые сплавы. Производство чугуна и Доменный процесс
Железоуглеродистые сплавы
Железоуглеродистые сплавы, сплавы железа с углеродом на основе железа. Варьируя состав и структуру, получают железоуглеродистые сплавы с разнообразными свойствами, что делает их универсальными материалами.
Различают: чистые железоуглеродистые сплавы (со следами примесей), получаемые в небольших количествах для исследовательских целей и технические железоуглеродистые сплавы — стали (до 2%С) и чугуны (св. 2% С), мировое производство которых измеряется сотнями млн. т.
Технические железоуглеродистые сплавы содержат примеси. Их делят на обычные (фосфор Р, сера S, марганец Mn, кремний Si, водород Н, азот N, кислород О), легирующие (хром Cr, никель Ni, молибден Mo, вольфрам W, ванадий V, титан Ti, кобальт Со, медь Cu и др.) и модифицирующие (магний Mg, церий Ce, кальций Ca и др.).
В большинстве случаев основой, определяющей строение и свойства сталей и чугунов, является система Fe — С. Начало научному изучению этой системы положили русские металлурги П. П. Аносов (1831) и Д. К. Чернов (1868).
Аносов впервые применил микроскоп при исследовании железоуглеродистые сплавы, а Чернов установил их кристаллическую природу, обнаружил дендритную кристаллизацию и открыл в них превращения в твёрдом состоянии.
Из зарубежных учёных, способствовавших созданию диаграммы состояния Fe — С сплавов, следует отметить Ф. Осмонда (Франция), У. Ч. Робертса-Остена (Англия), Б. Розебома (Голландия) и П. Геренса (Германия).
Фазовые состояния.
Железоуглеродистые сплавы при разных составах и температурах описываются диаграммами стабильного (рис. 1, а) и метастабильного (рис. 1, б) равновесий. В стабильном состоянии в железоуглеродистые сплавы встречаются жидкий раствор углерода в железе (Ж), три твёрдых раствора углерода в полиморфных модификациях железа (табл. 1)
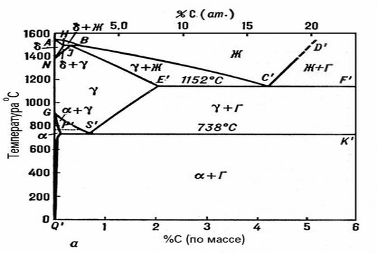
Рис. 1a. Диаграммы состояния железоуглеродистых сплавов: состояние стабильных равновесий.
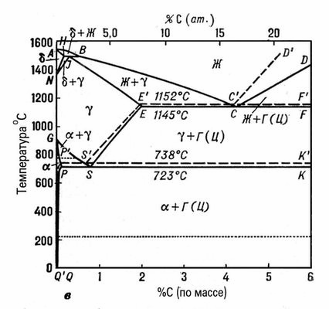
Рис. 1в. Диаграммы состояния железоуглеродистых сплавов: состояния с двойными линиями.
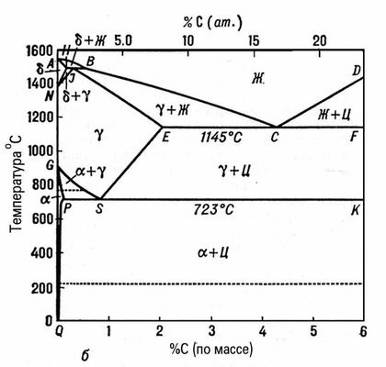
Рис. 1б. Диаграммы состояния железоуглеродистых сплавов: состояние метастабильных равновесий.
Таблица 1.— Кристаллические фазы железоуглеродистых сплавов.
| Название фазы | Природа фазы | Структура |
| a-феррит | Твердый раствор внедрения углерода в a-Fe | Объемноцен трированная кубическая |
| Аустенит | Твердый раствор внедрения углерода в g-Fe | Гранецентри рованная кубическая |
| d-феррит | Твердый раствор внедрения углерода в d-Fe | Объемноцен трированная кубическая |
| Графит | Полиморфная модификация углерода | Гексогональная слоистая |
| Цементит | Карбид железа Fe2C | Ромбическая |
a-раствор (a-феррит), g-раствор (аустенит) и d-раствор (d-феррит), и графит (Г).
В метастабильном состоянии в железоуглеродистые сплавы встречаются a-, g-, d-растворы и карбид железа Fe3C — цементит (Ц). Области устойчивости железоуглеродистых сплавов в однофазных и двухфазных состояниях указаны на диаграммах. При некоторых условиях в железоуглеродистых сплавах могут существовать в равновесии и три фазы. При температурах НВ возможно перитектическое равновесие d + g + Ж, E’C’F’ — эвтектическое стабильное равновесие g + Ж + Г; при ECF — эвтектическое метастабильное равновесие g + Ж + Ц; при P'S'K' — эвтектоидное стабильное равновесие a + g + Г', при PSK — эвтектоидное метастабильное равновесие a + g + Ц.
Диаграммы а и б вычерчиваю и в одной координатной системе (рис. 1, в). Такая сдвоенная диаграмма наглядно характеризует относительное смещение однотипных линий равновесия и облегчает анализ железоуглеродистых сплавов, содержащих стабильные и метастабильные фазы одновременно.
Основной причиной появления в железоуглеродистых сплавах высокоуглеродистой метастабильной фазы в виде цементита являются трудности формирования графита.
Образование графита в жидком растворе Ж и твёрдых растворах a и g связано с практически полным удалением атомов железа из участков сплава, где зарождается и растет графит. Оно требует значительных атомных передвижений. Если железоуглеродистые сплавы охлаждаются медленно или длительно выдерживаются при повышенных температурах, атомы железа успевают удалиться из мест, где формируется графит, и тогда возникают стабильные состояния.
При ускоренном охлаждении и недостаточных выдержках удаление малоподвижных атомов железа задерживается, почти все они остаются на месте, и тогда в жидких и твёрдых растворах зарождается и растет цементит. Необходимая для этого диффузия легкоподвижных при повышенных температурах атомов углерода, не требующая больших выдержек, успевает происходить и при ускоренном охлаждении.
Помимо основных фаз, указанных на диаграммах, в технических железоуглеродистые сплавы встречаются небольшие количества и др. фаз, появление которых обусловлено наличием примесей. Часто встречаются сульфиды (FeS, MnS), фосфиды (Fe3P), окислы железа и примесей (FeO, MnO, Al2O3, Cr2O3, TiO2 и др.), нитриды (FeN, AlN) и др. неметаллические фазы. Точечными линиями на диаграммах отмечены точки Кюри, наблюдающиеся в железоуглеродистых сплавах в связи с магнитными превращениями феррита (768°С) и цементита (210°С).
Доменный процесс
Для успешного ведения доменного процесса необходимо соблюдать два основных условия:
1. количество тепла и температура по высоте печи должны быть распределены так, чтобы все реакции протекали в определённом месте и в определённое время;
2. образование шлака должно происходить только после окончания восстановления из руды железа и необходимых примесей.
Первое условие обеспечивается непрерывным движением в печи 2-х встречных потоков, поднимающих снизу вверх горячих газов от сгорания в горне топлива и опускающихся сверху вниз шихтовых материалов, нагревающихся под действием тепла газов.
Второе условие обеспечивается подбором по тугоплавкости шлаков соответственно сортам выплавляемого чугуна, чтобы образовавшийся шлак не сплавил руду до восстановления железа и др. примесей, не изменил заданного состава чугуна и не вызвал расстройство в ходе процесса.
Доменный процесс начинается с горения топлива.
Горячий воздух, вдуваемый через фурмы, сжигает углерод кокса по реакции:
C+O 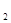 =CO
=CO 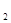 +Q (1)
+Q (1)
Двуокись углерода (CO 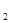 ) встречает углерод раскаленного кокса и почти полностью разлагается:
) встречает углерод раскаленного кокса и почти полностью разлагается:
CO 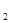 +C=2CO-Q
+C=2CO-Q 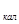 (2)
(2)
Одновременно с этим идёт реакция восстановления водорода из пара, содержащегося в дутье:
H 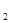 O
O 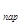 +C = H
+C = H 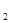 +CO-Q (3)
+CO-Q (3)
В результате этих реакций вверх из горна идут газы, состоящие из CO, H 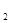 .
.
Подготовительные процессы в загруженных шихтовых материалах начинают происходить в верхних горизонтах печи немедленно под влиянием температуры поднимающихся газов. Сначала при температуре 100…200ºС испаряется гигроскопическая вода, а при 300…500ºС кристаллизационная, при соприкосновении которой с окисью углерода газов и углеродом кокса колошниковые газы получают дополнительно CO 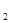 , CO и H
, CO и H 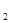 .
.
Восстановление железа из руды начинает происходить при помощи окиси углерода (непрямое восстановление) в верхних горизонтах печи, где температура не высока, и постепенно усиливается при опускании вниз по мере повышения температуры примерно до 900°C. Обычно в доменных газах содержится небольшое количество водорода, поэтому основное восстановление идёт за счёт окиси углерода и углерода кокса.
Восстановление окисью углерода начинается в шахте и происходит ступенчато от высшего окисла железа к низшему в следующем порядке:
Fe2O3 ® Fe3O4 ® FeO ® Fe.
Протекают следующие реакции восстановления:
3Fe2O3 + CO = 2Fe3O4 + CO2 (4)
Fe3O4 + CO = 3FeO CO2 (5)
FeO + CO = Fe + CO2 (6)
Основной реакцией считается реакция (6), т.к. конечным продуктом является металлическое железо и она называется реакцией косвенного восстановления железа, протекает при умеренных температурах (500…900°C) с выделением тепла.
При более высоких температурах (выше 1000…1100°C) в присутствии раскалённого кокса в доменной печи идёт восстановление железа при помощи углерода по реакции:
FeO + C = Fe + CO (7)
Эта реакция называется прямым восстановлением железа. Считается, что в доменной печи около 60…50% железа образуется по реакции (6), т.е. с помощью окиси углерода и 50…40% с помощью твёрдого углерода. Прямое восстановление железа происходит в районе распара доменной печи. Образующееся в доменной печи металлическое железо находится в твёрдом виде (губчатое железо), поскольку оно имеет температуру плавления 1535°C. В присутствии окиси углерода губчатое металлическое железо постепенно науглероживается по реакции:
3Fe + 2CO = Fe3C + CO2 (8)
Температура его плавления понижается вплоть до 1150…1200°C. Вследствие этого науглероженное железо (от 1,8 до 2 % C) переходит в жидкое состояние (расплавляется) и стекает по каплям между кусками раскалённого кокса на лещадь горна доменной печи.
Во время перемещения капелек металла происходит дополнительное насыщение железа углеродом примерно до 3,5…4 %, т.е. до обычного содержания углерода в жидком чугуне. Параллельно с процессом восстановления железа в доменной печи наблюдается восстановление из шихты марганца, кремния и фосфора, которые переходят в чугун.
Восстановление высших и средних окислов марганца до низшего окисла происходит ступенчато за счёт окиси углерода по схеме:
MnO2 ® Mn2O3 ® Mn3O4 ® MnO ® Mn
Закись марганца MnO трудно восстановимый низший окисел марганца, восстанавливается твёрдым углеродом по реакции:
MnO + C = Mn + CO (9)
Реакция сопровождается поглощением тепла и происходит при температурах выше 1100…1200°C. Восстановление кремния из пустой породы происходит при температуре 1450°C при помощи твёрдого углерода по реакции:
SiO2+ 2C = Si + 2CO – Q (10)
В присутствии железа эта реакция начинается при температуре 1050°C и требует поглощения меньшего количества тепла.
Фосфор содержится в руде в виде соединений (FeO)3P2O5 и (CaO)3P2O5 и восстановление его в присутствии пустой породы железной руды совершается за счёт твёрдого углерода:
P2O5(CaO)4 + 5C + 2SiO2 = 2P + 2(CaO)2*SiO2 + 5CO (11)
и фосфат железа восстанавливается окисью углерода:
2Fe3(PO4)2 +16CO = 2Fe3P + 2P + 16CO2 (12)
Сера поступает в плавку с рудой, флюсом и коксом в виде сульфида железа. Часть серы улетучивается (от 10 до 60%), оставшаяся часть серы руды и кокса переходит в шлак и в металл. Для удаления серы в шлак необходимо иметь избыточное количество извести:
FeS + CaO = FeO +CAS + Q (13)
Образующееся сернистое железо вступает в реакцию с известью. Другой путь удаления серы из чугуна – это после выпуска из печи выдержке и при перевозках в ковшах наличие реакции взаимодействия сернистого железа с марганцем:
FeS + Mn = MnS + Fe +Q (14)
Никель подобно железу восстанавливается окисью углерода, твёрдым углеродом и водородом. Процесс восстановления начинается и заканчивается раньше восстановления железа.
Хром, никель, титан и ванадий принадлежат к числу трудно восстанавливаемых элементов и восстанавливаются только твёрдым углеродом при температуре выше 1250…1300°C.
Шлакообразование, т.е. сплавление пустой породы руды с флюсом, начинается с образования наиболее лёгкоплавкого соединения из кремнезёма, глинозёма и извести. Это происходит в распаре при температуре около 1200°C. При более высоких температурах он изменяет свой химический состав в связи с растворением в нём золы кокса, флюсов и остатков пустой породы железной руды. Окончательный состав шлака находится в заплечиках и горне.
Продукты доменной плавки
Основным продуктом доменной плавки является чугун.
Расплавленный чугун через одну – две лётки по 10 – 18 раз в сутки выпускают из доменной печи. В ковшах – чугуновозах ёмкостью, 80…100 т, везут его по железнодорожным путам, попадают либо в сталеплавильный цех для передела в сталь, либо на разливочную машину. В первом случае чугун сливают в миксеры (копильники), ёмкостью до 2000 т, отапливаемые газом. При выдержке в миксере выравниваются химический состав и температура чугуна, происходит дополнительное удаление серы.
Разливочная машина представляет собой конвейер с укреплёнными на нём формами (мульдами); в них получают небольшие слитки – чугунные чушки (до 55 кг), которые направляют на другие заводы.
В доменных печах выплавляют передельные и литейные чугуны, а также некоторые ферросплавы.
Передельные чугуны по ГОСТ 805–69 3-х видов:
1. коксовый М1, М2, М3, Б1, Б2;
2. фосфористый МФ1, МФ2, МФ3;
3. высококачественный ПВК1, ПВК2, ПВК3.
Отжиг стали
Отжиг стали - термическая обработка, включающая при полном отжиге нагрев до температуры выше верхних критических точек на 30...50°С, выдержку при такой температуре до полного прогрева металла и последующее очень медленное охлаждение (вместе с охлаждаемой печью). При неполном отжиге нагрев стали производится до температур выше нижних критических точек на 30...50°С, а при низкотемпературном отжиге - до температур, лежащих ниже нижних критических точек. При неполном и низкотемпературном отжигах происходит только частичная перекристаллизация. Структура стали после отжига образуется в полном соответствии с диаграммой состояния железоуглеродистых сплавов.
Отжиг стали производится в тех случаях, когда необходимо уменьшить твердость, повысить пластичность и вязкость, ликвидировать последствия перегрева, получить равновесное состояние, улучшить обрабатываемость при резании.
Разновидностями отжига сталей являются нормализационный и изотермический отжиги.
Нормализационный отжиг (нормализация) - вид термической обработки стали, заключающийся в нагреве до температуры на 30...50°С выше верхних, критических точек, выдержке и охлаждении на спокойном воздухе. В результате нормализации стали с содержанием углерода менее 0,3% приобретают ферритно-перлитную структуру, а стали с содержанием углерода 0,3...0,7% - сорбитную.
Нормализация применяется в тех случаях, когда необходимо получить мелкозернистую однородную структуру с более высокой твердостью и прочностью, но с несколько меньшей пластичностью, чем после отжига. При нормализации в заэвтектоидных сталях устраняется цементитная сетка, поэтому ею часто заменяют полный или неполный отжиг при подготовке углеродистых сталей к механической обработке. Нормализация более производительный и экономичный процесс, чем отжиг.
Изотермический отжиг - вид термической обработки стали, заключающийся в нагреве стали до температуры, на 30...50°С превышающей верхнюю критическую точку, выдержке при этой температуре, а затем переносят детали в другую печь с заданной температурой (ниже верхней критической точки) и изотермическую выдержку ее до полного распада аустенита. Изотермический отжиг улучшает обрабатываемость резанием и применяется для деталей и заготовок небольших размеров.
Закалка стали
Закалка стали - термическая обработка, включающая нагрев до температур выше верхних критических точек на 30...50°С, выдержку при этих температурах до полного прогрева металла и последующее очень быстрое его охлаждение. В результате закалки в стали из аустенита образуется мартенсит.
Стали с малым содержанием углерода закалить на мартенсит очень трудно, так как начало и конец процесса образования мартенсита происходит в области высоких температур, соответствующих образованию других, более устойчивых структур (троостит, сорбит). Прокаливаемость обыкновенной углеродистой стали распространяется на 5...7 мм.
Микроструктура закаленной стали зависит от ее химического состава и условий закалки (температуры нагрева и режима охлаждения). Закалка стали с содержанием углерода до 0,025...0,03% задерживает выделение третичного цементита по границам зерен и не меняет структуру феррита. Такая закалка повышает пластичность и почти не изменяет прочностных характеристик.
Микроструктура стали с 0,08...0,15% С (с нагревом выше верхних критических точек и охлаждением в воде) представляет собой низкоуглеродистый мартенсит с выделениями феррита. Дальнейшее увеличение содержания углерода (0,15...0,25%) при тех же условиях закалки приводит к повышению твердости с 110...130 НВ до 140...180 НВ, а предел текучести возрастает на 30...50%. Наиболее значительное изменение свойств происходит при содержании углерода более 0,30...0,35%.
Микроструктура доэвтектоидных сталей представляет собой мартенсит, кристаллы которого имеют характерную форму пластин (игл). При содержании углерода более 0,5...0,6% в микроструктуре сталей наблюдается незначительное (2...3%) количество аустенита.
Микроструктура заэвтектоидных сталей состоит из мартенсита, зерен вторичного цементита (не растворившегося при нагреве) и остаточного аустенита. Кристаллы (иглы) мартенсита очень небольших размеров. Повышение температуры закалки вызывает растворение вторичного цементита и способствует росту зерна.
В тех случаях, когда требуются высокая твердость и повышенная износостойкость поверхности при сохранении вязкой и достаточно прочной сердцевины изделия, применяется поверхностная закалка, то есть закалка не на полную глубину. Поверхностной закалке подвергаются стали при содержании углерода более 0,3%. Выбор оптимальной толщины упрочняемого слоя определяется условиями работы детали и составляет от 1,5 до 15 мм (и выше). Площадь сечения закаленного слоя не должна превышать 20% площади всего сечения. В практике наиболее часто используют поверхностную закалку с индукционным нагревом током высокой частоты (ТВЧ).
Мартенситная структура стали после закалки метастабильна и для ее превращения в более устойчивую производят отпуск.
Отпуск стали
Отпуск стали - термическая обработка, включающая нагрев закаленной стали до температуры ниже критических точек, выдержка при этой температуре и охлаждение. В результате отпуска в зависимости от температуры нагрева неустойчивая структура мартенсита закалки в результате диффузионного перераспределения углерода превращается в более устойчивые структуры - мартенсит отпуска, троостит, сорбит и перлит.
Мартенсит отпуска имеет измененную кристаллическую решетку и его образование сопровождается объемными изменениями, выделением теплоты и частичным снятием внутренних напряжении. При более высокой температуре нагрева образуются троостит, сорбит и перлит отпуска, которые в отличие от получаемых из аустенита при непрерывном охлаждении имеют зернистую, а не пластинчатую микроструктуру. Стали с зернистой микроструктурой отпуска характеризуются более высокой пластичностью и лучшей обрабатываемостью резанием.
В зависимости от температуры отпуска различают низкотемпературный (низкий), среднетемпературный (средний) и высокотемпературный (высокий) виды отпуска. Закалка на мартенсит с последующим высоким отпуском называется улучшением стали. Улучшение обеспечивает хороший комплекс свойств (прочность, ударная вязкость, твердость) и применяется для ответственных изделий из среднеуглеродистых сталей (коленчатые валы, шатуны и др. детали).
К основным дефектам, которые могут возникнуть при закалке стали относят трещины и деформацию. Трещины - неисправимый дефект, предупредить который можно конструктивном решением (избегать в изделии конструктивных элементов, которые могут стать концентраторами напряжений) и тщательным соблюдением режимов термообработки. Деформация, то есть изменение размеров и формы изделий, всегда сопровождает процессы термической обработки, особенно закалки. Несимметричную деформацию изделий в практике часто называют короблением (поводкой). Деформацию можно уменьшить подбором соответствующего состава стали и условий термической обработки, а избежать коробления - обеспечив равномерность нагрева под закалку и правильное положение детали при погружении в закалочную среду.
Физические свойства
Металлы подгруппы меди, как и щелочные металлы, имеют по одному свободному электрону на один ион-атом металла. Казалось бы, эти металлы не должны особенно сильно отличатся от щелочных. Но они, в отличие от щелочных металлов, обладают довольно высокими температурами плавления. Большое различие в температурах плавления между металлами этих подгрупп объясняется тем, что между ион-атомами металлов подгруппы меди почти нет “зазоров” и они расположены более близко. Вследствие этого количество свободных электронов в единице объема, электронная плотность, у них больше. Следовательно, и прочность химической связи у них больше. Поэтому металлы подгруппы меди плавятся и кипят при более высоких температурах.
Металлы подгруппы меди обладают, по сравнению с щелочными металлами, обладают большей твердостью. Объясняется это увеличением электронной плотностью и отсутствием “зазоров” между ион-атомами.
Необходимо отметить, что твердость и прочность металлов зависят от правильности расположения ион-атомов в кристаллической решетке. В металлах, с которыми мы практически сталкиваемся, имеются различного рода нарушения правильного расположения ион-атомов, например пустоты в узлах кристаллической решетки. К тому же металл состоит из мелких кристалликов (кристаллитов), между которыми связь ослаблена. В Академии Наук СССР была получена медь без нарушения в кристаллической решетке. Для этого очень чистую медь возгоняли при высокой температуре в глубоком вакууме на глубокую подложку. Медь получалась в виде небольших ниточек – “усов”. Как оказалось такая медь в сто раз прочнее, чем обычная.
Чистая медь обладает и другой интересной особенностью. Красный цвет обусловлен следами растворенного в ней кислорода. Оказалось, что медь, многократно возогнанная в вакууме (при отсутствии кислорода), имеет желтоватый цвет. Медь в полированном состоянии обладает сильным блеском.
При повышении валентности понижается окраска меди, например CuCl – белый, Cu2O – красный, CuCl + H2O – голубой, CuO – черный. Карбонаты характеризуются синим и зеленым цветом при условии содержания воды, чем обусловлен интересный практический признак для поисков.
Медь обладает наибольшей (после серебра) электропроводимостью, чем и обусловлено её применение в электронике.
Медь кристаллизируется по типу централизованного куба (рис 3).
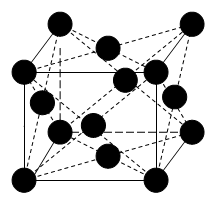
Рисунок 3. Кристаллическая решетка меди.
Химические свойства
Строение атома.
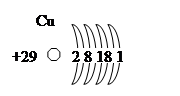
Рисунок 4. Схема строения атома меди.
Отношение к кислороду
Медь проявляет к кислороду незначительную активность, но во влажном воздухе постепенно окисляется и покрывается пленкой зеленоватого цвета, состоящей из основных карбонатов меди:
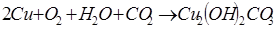 (15)
(15)
В сухом воздухе окисление идет очень медленно, на поверхности меди образуется тончайший слой оксида меди:
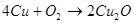 (16)
(16)
Внешне медь при этом не меняется, так как оксид меди (I) как и сама медь, розового цвета. К тому же слой оксида настолько тонок, что пропускает свет, т.е. просвечивает. По-иному медь окисляется при нагревании, например при 600-800 0C. В первые секунды окисление идет до оксида меди (I), которая с поверхности переходит в оксид меди (II) черного цвета. Образуется двухслойное окисное покрытие.
Qобразования (Cu2O) = 84935 кДж.

Рисунок 5. Строение оксидной пленки меди.
Взаимодействие с водой
Металлы подгруппы меди стоят в конце электрохимического ряда напряжений, после иона водорода. Следовательно, эти металлы не могут вытеснять водород из воды. В то же время водород и другие металлы могут вытеснять металлы подгруппы меди из растворов их солей, например:
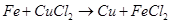 (17)
(17)
Эта реакция окислительно-восстановительная, так как происходит переход электронов:
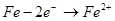 (18)
(18)
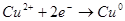 (19)
(19)
Молекулярный водород вытесняет металлы подгруппы меди с большим трудом. Объясняется это тем, что связь между атомами водорода прочная и на ее разрыв затрачивается много энергии. Реакция же идет только с атомами водорода.
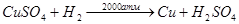 (20)
(20)
Медь при отсутствии кислорода с водой практически не взаимодействует. В присутствии кислорода медь медленно взаимодействует с водой и покрывается зеленой пленкой гидроксида меди и основного карбоната:
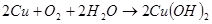 (21)
(21)
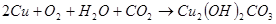 (22)
(22)
Взаимодействие с кислотами
Находясь в ряду напряжений после водорода, медь не вытесняет его из кислот. Поэтому соляная и разбавленная серная кислота на медь не действуют. Однако в присутствии кислорода медь растворяется в этих кислотах с образованием соответствующих солей:
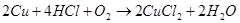 (23)
(23)
Оксид меди
При прокаливании меди на воздухе она покрывается черным налетом, состоящим из оксида меди
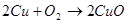 (26)
(26)
Его также легко можно получить прокаливанием гидроксокарбоната меди (II) (CuOH)2CO3 или нитрата меди (II) Cu(NO3)2. При нагревании с различными органическими веществами CuO окисляет их, превращая углерод в диоксид углерода, а водород – в воду восстанавливаясь при этом в металлическую медь. Этой реакцией пользуются при элементарном анализе органических веществ для определения содержания в них углерода и водорода.
Под слоем меди расположен окисел розового цвета – закись меди Cu2O. Этот же окисел получается при совместном прокаливании эквивалентных количеств меди и окиси меди, взятых в виде порошков:
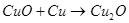 (27)
(27)
Закись меди используют при устройстве выпрямителей переменного тока, называемых купроксными. Для их приготовления пластинки меди нагревают до 1020-1050 0C. При этом на поверхности образуется двухслойная окалина, состоящая из закиси меди и окиси меди. Окись меди удаляют, выдерживая пластинки некоторое время в азотной кислоте:
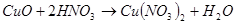 (28)
(28)
Пластинку промывают, высушивают и прокаливают при невысокой температуре – и выпрямитель готов. Электроны могут проходить только от меди через закись меди. В обратном направлении электроны проходить не могут. Это объясняется тем, что закись меди обладает различной проводимостью. В слое закиси меди, который примыкает непосредственно к меди, имеется избыток электронов, и электрический ток проходит за счет электронов, т.е. существует электронная проводимость. В наружном слое закиси меди наблюдается нехватка электронов, что равноценно появлению положительных зарядов. Поэтому, когда к меди подводят положительный плюс источника тока, а к закиси меди – отрицательный, то электроны через систему не проходят. Электроны при таком положении полюсов движутся к положительному электроду, а положительные заряды – к отрицательному. Внутри слоя закиси возникает тончайший слой, лишенный носителей электрического тока, - запирающий слой. Когда же медь подключена к отрицательному полюсу, а закись меди к положительному, то движение электронов и положительных зарядов изменяется на обратное, и через систему проходит электрический ток.
Гидроксиды меди
Гидроксид меди малорастворимое и нестойкое соединение. Получают его при действии щелочи на раствор соли:
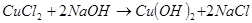 (29)
(29)
Это ионная реакция и протекает она потому, что образуется плохо диссоциированное соединение, выпадающее в осадок:
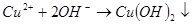 (30)
(30)
Медь, помимо гидроксида меди (II) голубого цвета, дает еще гидроксид меди (I) белого цвета:
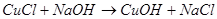 (31)
(31)
Это нестойкое соединение, которое легко окисляется до гидроксида меди (II):
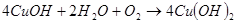 (32)
(32)
Оба гидроксида меди обладают амфотерными свойствами. Например, гидроксид меди (II) хорошо растворим не только в кислотах, но и в концентрированных растворах щелочей:
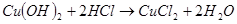 (33)
(33)
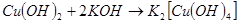 (34)
(34)
Таким образом, гидроксид меди (II) может диссоциировать и как основание:
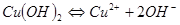 (35)
(35)
и как кислота. Этот тип диссоциации связан с присоединением меди гидроксильных групп воды:
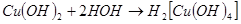 (36)
(36)
Сульфаты
Наибольшее практическое значение имеет CuSO4*5H2O, называемый медным купоросом. Его готовят растворением меди в концентрированной серной кислоте. Поскольку медь относится к малоактивным металлам и расположена в ряду напряжений после водорода, водород при этом не выделяется:
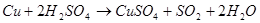 (37)
(37)
Медный купорос применяют при электролитическом получении меди, в сельском хозяйстве для борьбы с вредителями и болезнями растений, для получения других соединений меди.
Карбонаты
Карбонаты для металлов подгруппы меди не характерны и в практике почти не применяются. Некоторое значение для получения меди имеет лишь основной карбонат меди, который встречается в природе.
Сплавы
Латуни
Это двойные и многокомпонентные медные сплавы, в которых основной легирующий компонент — цинк (содержание не превышает 45 %). Среди медных сплавов латуни получили наибольшее распространение в промышленности благодаря сочетанию высоких механических и технологических свойств. По сравнению с медью латуни обладают более высокой прочностью, коррозионной стойкостью, лучшими литейными свойствами, имеют более высокую температуру рекристаллизации. Латуни — наиболее дешевые медные сплавы.
Двойные (простые) латуни относятся к системе Cu—Zn (рис. 19.3). Медь с цинком образует кроме a -твердого раствора на основе меди ряд промежуточных фаз b, g и т. д.
Фаза b — это твердый раствор на основе электронного соединения CuZn (фаза Юм—Розери) с решеткой ОЦК. При охлаждении при температуре около 450 ° С b -фаза переходит в упорядоченное состояние (b ® b ¢), причем b ¢ -фаза в отличие от b -фазы является более твердой и хрупкой.
Фаза g — твердый раствор на основе электрон-ного соединения Cu5Zn8 отличается очень высокой хрупкостью и ее присутствие в промышленных конструкционных сплавах исключается.
Механические свойства латуни определяются свойствами фаз. По мере увеличения содержания цинка в латунях их прочность возрастает (рис. 19.4). Максимум прочности достигается в двухфазной области (a + b) при содержании цинка около 45 %. При большем содержании цинка прочность резко уменьшается из-за высокой хрупкости b ¢ -фазы. Поэтому в промышленности применяют преимущественно a - и (a + b)-латуни. Представляют интерес как основа сплавов с эффектом памяти формы b -латуни.
Все латуни, содержащие более 20 % Zn, склонны к коррозионному растрескиванию. Это растрескивание проявляется при хранении и эксплуатации изделий, в которых имеются остаточные растягивающие напряжения, во влажной атмосфере с небольшим количеством аммиака или сернистого газа. Установлена определенная связь между данным явлением и временем года, что объясняется закономерными изменениями состава атмосферы. В связи с этим это явление было названо «сезонным растрескиванием» («сезонная болезнь»). Другой формой коррозии латуни является обесцинкование, которое характерно для латуней с повышенным содержанием цинка (Л68, ЛС59-1 и др.). Высокомедистые латуни практически не подвергаются обесцинкованию. Для уменьшения обесцинкования в латуни вводят небольшое количество мышьяка (0,02–0,06 %).
В России принята буквенно-цифровая маркировка латуней, в которой буквы обозначают основные компоненты сплава, числа — их примерное содержание в процентах. Марка латуни начинается с буквы «Л». В двойных (простых) латунях число после буквы «Л» определяет среднее содержание меди. В марках многокомпонентных латуней после буквы «Л» указаны легирующие элементы, которым даны следующие обозначения: О — олово; А — алюминий; Н — никель; К — кремний; Ж — железо и т. д. Порядок букв и чисел в деформируемых и литейных латунях различен. В деформируемой латуни первое число после букв указывает среднее содержание меди, последующие числа, отделенные через тире, указывают среднее содержание легирующих элементов. Например, латунь ЛА77-2 имеет следующий состав: 77 % Cu, 2 % Al, остальное Zn. В литейных латунях среднее содержание компонентов сплава указывается сразу после буквы, обозначающей его название; цинк обозначается буквой «Ц». Например, литейная латунь ЛЦ30А3 содержит 30 % Zn, 3 % AL, Cu — основа.
Бронзы
Бронзами называют медные сплавы, в которых основными легирующими элементами являются различные металлы, кроме цинка. В особую группу выделяют медноникелевые сплавы.
По химическому составу бронзы подразделяются на оловянные и безоловянные, и в каждой из этих групп по технологии производства бронзы делятся на обрабатываемые давлением и литейные.
В марке обрабатываемых давлением оловянных (ГОСТ 5017–74) и безоловянных бронз (18175–78) после букв «Бр» стоят буквенные обозначения названий легирующих элементов в порядке убывания их концентрации, а в конце марки в той же последовательности указаны средние концентрации соотвествующих элементов (например, БрОЦС4-4-2,5). В марке литейных оловянных (ГОСТ 613–79) и безоловянных бронз (ГОСТ 493–79) после каждого обозначения легирующего элемента указано его содержание. Если составы литейной и деформируемой бронз перекрываются, то в конце марки литейной бронзы ставится буква «Л» (например, БрА9Ж3Л).
Свойства бронз определяются содержанием в них легирующих элементов. Для бронз, в которых легирующие элементы входят в основном в твердый раствор, характерно твердорастворное упрочнение. Дополнительно они могут быть упрочнены путем пластической деформации. Бронзы, содержащие бериллий, хром, цирконий и некоторые другие элементы с переменной растворимостью в твердом растворе, упрочняются путем закалки и последующего дисперсионного твердения. К классу термически упрочняемых сплавов относится также алюминиевая бронза БрАЖН10-4-4, в которой упрочнение при термообработке связано с мартенситным превращением.
Бронзы по сравнению с латунью обладают более высокой прочностью, коррозионной стойкостью и антифрикционными свойствами. Они достаточно коррозионностойки в морской воде, в растворах большинства органических кислот, углекислых растворах.
Медноникелевые сплавы
Никель — металл серебристо-белого цвета, кристаллизующийся в решетку ГЦК с параметром а = 0,352 нм (при 20 ° С) и полиморфных превращений не имеет. При температуре ниже 358 ° С (точка Кюри) никель является слабым ферромагнетиком. Никель — прочный, высокопластичный металл, отличающийся высокой коррозионной стойкостью, повышенной температурой плавления и высокой каталитической способностью. Это обусловило его широкое применение в металлургии, машиностроении, электронике, медицине и других отраслях техники.
Сплавы меди с никелем отличаются хорошими механическими свойствами, коррозионной стойкостью, технологичностью и особыми электрическими свойствами, что обусловливает широкое применение их в технике.
Медь образует с никелем непрерывные твердые растворы. Никель существенно упроч-няет медь, причем максимальную прочность и твердость имеют сплавы примерно эквиатомного состава. Важно отметить, что при этом характеристики пластичности и ударной вязкости практически не меняются. Никель повышает характеристики жаропрочности, модуль упругости и понижает температурный коэффициент электросопротивления меди.
По назначению медноникелевые сплавы делятся на две группы: конструкционные и электротехнические. К первой группе относятся высокопрочные и коррозионностойкие сплавы типа мельхиор, нейзильбер и куниаль, ко второй — константан, манганин и копель, обладающие высоким электрическим сопротивлением и определенными термоэлектрическими свойствами.
Применение меди
Примерно половина производимой меди в настоящее время используется в радиотехнике и электротехнической промышленности. Это связано с ее хорошей проводимостью и относительно высокой коррозионной стойкостью. К меди, идущей на изготовление электрических проводов, часто добавляют в небольшом количестве кадмий, который не снижает электропроводимость меди, но повышает ее прочность на разрыв.
Древнейший сплав меди с цинком – латунь и в настоящее время производится в больших количествах. Содержание цинка в латуни составляет 30-45%. Она применяется для изготовления различной арматуры, соприкасающейся с водой (краны, вентили и т.д.), а также для производства различных труб. Из латуни прокатывают полосы и листы, идущие для выработки самых разнообразных изделий (проволока, произведения искусств, предметы быта и т.д.).
Латунь хорошо прокатывается, штампуется и несколько дешевле меди, так как цинк более дешевый металл по сравнению с медью.
Другие сплавы меди называются бронзами. Наиболее распространенная бронза – оловянная. Она содержит от 5 до 80% олова. В зависимости от содержания олова свойства и назначение меняется. При содержании олова 10-13% ее цвет красновато-желтый, а более 27-30% - белый. Подшипниковая бронза содержит 81-87% меди. Для изготовления подшипников, различных тормозных устройств, где происходит скольжение металла, применяют бронзы, содержащие до 45% свинца. В часовых и других точных механизмах, где нужна высокая механическая прочность и коррозионная стойкость, применяется бериллиевая бронза, содержащая 1-2% бериллия. Ее прочность равна прочности стали.
В быту и особенно в химической промышленности применяют сплавы меди с никелем, например монель-металл, в котором отношение меди к никелю равно 2:1, и мельхиор, в котором это соотношение равно 4:1. Мельхиор по внешнему виду похож на серебро, из него приготовляют предметы домашнего обихода: ложки, вилки, подносы и т.д. Монель-металл применяют для изготовления монет, различных реакторов для химической промышленности, так как это сплав коррозионно-стоек.
Гидроксокарбонат меди (II) – (CuOH)2CO3 – применяют для получения хлорида меди (II), для приготовления синих и зеленых минеральных красок, а также в пиротехнике.
Сульфат меди (II) – CuSO4 – в безводном состоянии представляет собой белый порошок, который при поглощении воды синеет. Поэтому он применяется для обнаружения следов влаги в органических жидкостях.
Смешанный ацетат-арсенит меди (II) – Cu(CH3COO)2*Cu3(AsO3)2 – применяют под названием “парижская зелень” для уничтожения вредителей растений.
Из солее меди вырабатывают большое количество минеральных красок, разнообразных по цвету: зеленых, синих, коричневых, фиолетовых и черных. Все соли меди ядовиты, поэтому медную посуду лудят – покрывают внутри слоем олова, чтобы предотвратить возможность образования медных солей.
Содержание
1. Железоуглеродистые сплавы. Производство чугуна и доменный процесс
1.1 Железоуглеродистые сплавы
1.1.1 Фазовые состояния
1.1.2 Строение железоуглеродистых сплавов
1.1.3 Полиморфные превращения железоуглеродистых сплавов
1.2 Производство чугуна и доменный процесс
1.2.1 Доменный процесс
1.2.2 Продукты доменной плавки
2. Термическая обработка железоуглеродистых сплавов
2.1 Превращения в стали при нагревании
2.2 Превращения в стали при охлаждении
2.3 Основные виды термической обработки стали
2.3.1 Отжиг стали
2.3.2 Закалка стали
2.3.3 Отпуск стали
3. Медь и её сплавы. Область применения
3.1 Физические свойства
3.2 Химические свойства
3.2.1 Отношение к кислороду
3.2.2 Взаимодействие с водой
3.2.3 Взаимодействие с кислотами
3.2.4 Отношение к галогенам и некоторым другим неметаллам
3.2.5 Оксид меди
3.2.6 Гидроксиды меди
3.2.7 Сульфаты
3.2.8 Карбонаты
3.2.9 Качественные реакции на ионы меди
3.3 Сплавы
3.3.1 Латуни
3.3.2 Бронзы
3.3.3 Медноникелевые сплавы
3.4 Применение меди
Список использованных источников
Железоуглеродистые сплавы. Производство чугуна и Доменный процесс
Железоуглеродистые сплавы
Железоуглеродистые сплавы, сплавы железа с углеродом на основе железа. Варьируя состав и структуру, получают железоуглеродистые сплавы с разнообразными свойствами, что делает их универсальными материалами.
Различают: чистые железоуглеродистые сплавы (со следами примесей), получаемые в небольших количествах для исследовательских целей и технические железоуглеродистые сплавы — стали (до 2%С) и чугуны (св. 2% С), мировое производство которых измеряется сотнями млн. т.
Технические железоуглеродистые сплавы содержат примеси. Их делят на обычные (фосфор Р, сера S, марганец Mn, кремний Si, водород Н, азот N, кислород О), легирующие (хром Cr, никель Ni, молибден Mo, вольфрам W, ванадий V, титан Ti, кобальт Со, медь Cu и др.) и модифицирующие (магний Mg, церий Ce, кальций Ca и др.).
В большинстве случаев основой, определяющей строение и свойства сталей и чугунов, является система Fe — С. Начало научному изучению этой системы положили русские металлурги П. П. Аносов (1831) и Д. К. Чернов (1868).
Аносов впервые применил микроскоп при исследовании железоуглеродистые сплавы, а Чернов установил их кристаллическую природу, обнаружил дендритную кристаллизацию и открыл в них превращения в твёрдом состоянии.
Из зарубежных учёных, способствовавших созданию диаграммы состояния Fe — С сплавов, следует отметить Ф. Осмонда (Франция), У. Ч. Робертса-Остена (Англия), Б. Розебома (Голландия) и П. Геренса (Германия).
Фазовые состояния.
Железоуглеродистые сплавы при разных составах и температурах описываются диаграммами стабильного (рис. 1, а) и метастабильного (рис. 1, б) равновесий. В стабильном состоянии в железоуглеродистые сплавы встречаются жидкий раствор углерода в железе (Ж), три твёрдых раствора углерода в полиморфных модификациях железа (табл. 1)

Рис. 1a. Диаграммы состояния железоуглеродистых сплавов: состояние стабильных равновесий.

Рис. 1в. Диаграммы состояния железоуглеродистых сплавов: состояния с двойными линиями.

Рис. 1б. Диаграммы состояния железоуглеродистых сплавов: состояние метастабильных равновесий.
Таблица 1.— Кристаллические фазы железоуглеродистых сплавов.
| Название фазы | Природа фазы | Структура |
| a-феррит | Твердый раствор внедрения углерода в a-Fe | Объемноцен трированная кубическая |
| Аустенит | Твердый раствор внедрения углерода в g-Fe | Гранецентри рованная кубическая |
| d-феррит | Твердый раствор внедрения углерода в d-Fe | Объемноцен трированная кубическая |
| Графит | Полиморфная модификация углерода | Гексогональная слоистая |
| Цементит | Карбид железа Fe2C | Ромбическая |
a-раствор (a-феррит), g-раствор (аустенит) и d-раствор (d-феррит), и графит (Г).
В метастабильном состоянии в железоуглеродистые сплавы встречаются a-, g-, d-растворы и карбид железа Fe3C — цементит (Ц). Области устойчивости железоуглеродистых сплавов в однофазных и двухфазных состояниях указаны на диаграммах. При некоторых условиях в железоуглеродистых сплавах могут существовать в равновесии и три фазы. При температурах НВ возможно перитектическое равновесие d + g + Ж, E’C’F’ — эвтектическое стабильное равновесие g + Ж + Г; при ECF — эвтектическое метастабильное равновесие g + Ж + Ц; при P'S'K' — эвтектоидное стабильное равновесие a + g + Г', при PSK — эвтектоидное метастабильное равновесие a + g + Ц.
Диаграммы а и б вычерчиваю и в одной координатной системе (рис. 1, в). Такая сдвоенная диаграмма наглядно характеризует относительное смещение однотипных линий равновесия и облегчает анализ железоуглеродистых сплавов, содержащих стабильные и метастабильные фазы одновременно.
Основной причиной появления в железоуглеродистых сплавах высокоуглеродистой метастабильной фазы в виде цементита являются трудности формирования графита.
Образование графита в жидком растворе Ж и твёрдых растворах a и g связано с практически полным удалением атомов железа из участков сплава, где зарождается и растет графит. Оно требует значительных атомных передвижений. Если железоуглеродистые сплавы охлаждаются медленно или длительно выдерживаются при повышенных температурах, атомы железа успевают удалиться из мест, где формируется графит, и тогда возникают стабильные состояния.
При ускоренном охлаждении и недостаточных выдержках удаление малоподвижных атомов железа задерживается, почти все они остаются на месте, и тогда в жидких и твёрдых растворах зарождается и растет цементит. Необходимая для этого диффузия легкоподвижных при повышенных температурах атомов углерода, не требующая больших выдержек, успевает происходить и при ускоренном охлаждении.
Помимо основных фаз, указанных на диаграммах, в технических железоуглеродистые сплавы встречаются небольшие количества и др. фаз, появление которых обусловлено наличием примесей. Часто встречаются сульфиды (FeS, MnS), фосфиды (Fe3P), окислы железа и примесей (FeO, MnO, Al2O3, Cr2O3, TiO2 и др.), нитриды (FeN, AlN) и др. неметаллические фазы. Точечными линиями на диаграммах отмечены точки Кюри, наблюдающиеся в железоуглеродистых сплавах в связи с магнитными превращениями феррита (768°С) и цементита (210°С).
Дата: 2019-05-29, просмотров: 410.