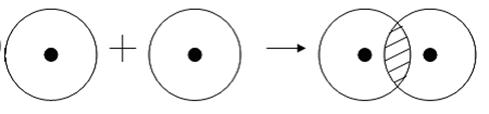
10. Ионная связь — сильная химическая связь , возникающая в результате электростатического притяжения катионов и анионов. Возникает между атомами с большой разностью (>1,7 по шкале Полинга) электроотрицательностей, при которой общая электронная пара переходит преимущественно к атому с большей электроотрицательностью. Это притяжение ионов как разноимённо заряженных тел. Примером может служить соединение CsF, в котором «степень ионности» составляет 97 %. Ионная связь — крайний случай поляризации ковалентной полярной связи . Образуется между типичными металлом и неметаллом . При этом электроны у металла полностью переходят к неметаллу, образуются ионы.
Если химическая связь образуется между атомами , которые имеют очень большую разность электроотрицательностей (ЭО > 1,7 по Полингу), то общая электронная пара полностью переходит к атому с большей ЭО. Результатом этого является образование соединения противоположно заряженных ионов :
11.
| Тип кристаллической решетки | Характеристика |
| Ионные | Состоят из ионов. Образуют вещества с ионной связью. Обладают высокой твердостью, хрупкостью, тугоплавки и малолетучи, легко растворяются в полярных жидкостях, являются диэлектриками. Плавление ионных кристаллов приводит к нарушению геометрически правильной ориентации ионов относительно друг друга и ослаблению прочности связи между ними. Поэтому их расплавы (растворы) проводят электрический ток. Ионные кристаллические решетки образуют многие соли, оксиды, основания. |
| Атомные (ковалентные) | В узлах находятся атомы, которые соединены между собой ковалентными связями. Атомных кристаллов много. Все они имеют высокую температуру плавления, не растворимы в жидкостях, обладают высокой прочностью, твердостью, имеют широкий диапазон электропроводимости. Атомные кристаллические решетки образуют элементы III и IV групп главных подгрупп (Si, Ge, B, C). |
Продолжение табл. З4
| Молекулярные | Состоят из молекул (полярных и неполярных), которые соединены между собой слабыми водородными, межмолекулярными и электростатическими силами. Поэтому молекулярные кристаллы имеют малую твердость, низкие температуры плавления, малорастворимы в воде, не проводят электрический ток и обладают высокой летучестью. Молекулярную решетку образует лед, твердый углекислый газ («сухой лед»), твердые галогенводороды, твердые простые вещества, образованные одно- (благородные газы), двух- (F2, Cl2, Br2, J2, H2, N2, O2), трех- (O3), четырех- (P4), восьми- (S8) атомными молекулами, многие кристаллические органические соединения. |
| Металлические | Состоят из атомов или ионов металлов, соединенных металлической связью. Узлы металлических решеток заняты положительными ионами, между которыми перемещаются валентные электроны, находящиеся в свободном состоянии (электронный газ). Металлическая решетка является прочной. Этим объясняются свойственные большинству металлов твердость, малая летучесть, высокая температура плавления и кипения. Она же обусловливает такие характерные свойства металлов как электро- и теплопроводность, блеск, ковкость, пластичность, непрозрачность, фотоэффект. Металлической кристаллической решеткой обладают чистые металлы и сплавы. |
Кристаллы по величине электропроводности делятся на три класса:
Проводники I рода – электропроводность 104 - 106 (Ом × см)-1–вещества с металлической кристаллической решеткой, характеризующиеся наличием «переносчиков тока» - свободно перемещающихся электронов (металлы, сплавы).
Диэлектрики (изоляторы) – электропроводность 10-10-10-22 (Ом × см)-1 – вещества с атомной, молекулярной и реже ионной решеткой, обладающие большой энергией связи между частицами (алмаз, слюда, органические полимеры и др.).
Полупроводники – электропроводность 104-10-10 (Ом × см)-1 – вещества с атомной или ионной кристаллической решеткой, обладающие более слабой энергией связи между частицами, чем изоляторы. С ростом температуры электропроводность у полупроводников возрастает (серое олово, бор, кремний и др.)
12. Окисли́тельно-восстанови́тельные реа́кции (ОВР), также редокс (сокр. англ. redox, от reduction-oxidation — восстановление-окисление) — это встречно-параллельные химические реакции , протекающие с изменением степеней окисления и не более 2 атомов, входящих в состав реагирующих веществ (или ионов веществ ), реализующимся путём перераспределения электронов между атомом-окислителем ( акцептором ) и атомом-восстановителем (донором).
Среди оксидов также имеются твердые при обычных условиях вещества – SiO2, Fe2O3, жидкие – H2O и, конечно, газообразные – CO, CO2.
Дата: 2019-05-29, просмотров: 314.