Органическая химия.
3.1.Тема: «Теория строения органических соединений. Классификация и номенклатура»
1. Немного из истории органической химии. Природные и синтетические органические вещества. Общие свойства органических веществ (состав, тип химической связи, кристаллическое строение, растворимость, отношение к нагреванию в присутствии кислорода и без него).
2. Теория строения органических соединений А.М. Бутлерова. Развитие теории и ее значение.
3. Классификация органических веществ.
4. Особенности строение органических соединений.
5. Номенклатура органических соединений.
Свое название органические вещества получили потому, что первые из изученных веществ этой группы входили в состав живых организмов. Большинство известных сейчас органических веществ не встречаются в живых организмах, они получены (синтезированы) в лаборатории. Поэтому различают природные (натуральные) органические вещества (хотя большинство из них может быть сейчас получено в лаборатории), а органические вещества, не существующие в природе – синтетические органические веществами. Т.е. название «органические вещества» историческое и особого смысла не имеет. Все органические соединения являются соединениями углерода. К органическим веществам относятся соединения углерода, кроме изучаемых в курсе неорганической химии простых веществ, образованных Карбоном, его оксидов, угольной кислоты и ее солей. Другими словами, органическая химия – это химия соединений углерода.
Краткая история развития органической химии:
Первый учебник органической химии. Берцелиус, 1827, Виталисты. Учение о «жизненной силе».
Первые органические синтезы. Велер, 1824, синтез щавелевой кислоты и мочевины. Кольбе,1845, уксусная кислота. Бертло,1845, жир. Бутлеров,1861, сахаристое вещество.
Создания теории строения органических соединений. Существенный вклад в нее внесли немецкий ученый Ф.А.Кекуле и шотландец А.С.Купер. Но решающий вклад несомненно принадлежит русскому химику А.М.Бутлерову.
Все органические соединения – это соединения углерода. Среди всех элементов углерод выделяется своей способностью образовывать устойчивые соединения, в которых его атомы связаны друг с другом в длинные цепи различной конфигурации (линейные, разветвленные, замкнутые). Причина этой уникальной способности: примерно одинаковая энергия связи С-С и С-О (для других элементов энергия второй связи – намного больше). Кроме того, атом углерода может находиться в одном из трех видов гибридизации, образуя соответственно одинарные, двойные или тройные связи, причем не только между собой, но и с атомами кислорода или азота. Правда, гораздо чаще (практически всегда) атомы углерода соединены с атомами водорода. Если в состав органического соединения входит только углерод и водород, то соединения называются углеводородами. Все остальные соединения можно рассматривать как производные углеводородов, в которых некоторые атомы водорода замещены на другие атомы или группы атомов. Поэтому можно дать такое определение: Органические соединения – это углеводороды и их производные. Органических соединений очень много - более 10 млн. (неорганических около 500 тыс.).
Правила номенклатуры:
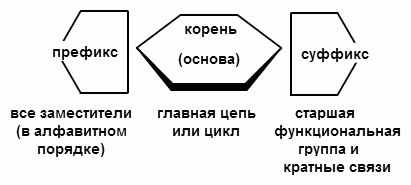
1) В молекуле выбирают главную углеродную цепь. Название предельного углеводорода, соответствующее этой цепи и будет корнем (основой) названия. Цепь должна быть самой длинной и содержать максимальное число заместителей и кратных связей. Если соединение циклическое –то главная цепь циклическая.
2) Атомы углерода нумеруются в главной цепи так, чтобы атом, к которому присоединена функциональная группа (кратная связь, заместитель, углеводородный радикал) получил наименьший номер. Цифра (или буква), указывающая положение атома или группы атомов в молекуле называется локантом (или адресом), она указывается перед префиксом и после суффикса.
3) В суффиксе указывается главная функциональная группа. Для этого к корню добавляют соответствующий суффикс и после него цифрой указывают номер атома углерода, к которому он присоединен). Если в цепи есть кратная связь, она тоже указывается в суффиксе. Если есть двойная связь, то суффикс –ан в названии предельного углеводорода заменяют на –ен; если есть тройная связь, то заменяют на –ин. Двойная связь считается старше тройной. Кратная связь образуется между двумя атомами, но названии указывается меньший номер. Если есть несколько одинаковых кратных связей или функциональных групп, то пользуются множительными приставками: ди-, три-, тетра-…
4) В приставке указываются младшие функциональные группы, галогены, нитрогруппа и углеводородные радикалы. Если в молекуле несколько одинаковых заместителей, то используют приставки ди-, три-, тетра-… Если заместители разные - их перечисляют в алфавитном порядке. Перед приставкой цифрой указывают положение заместителя (номер атома углерода, к которому он присоединен).
Органическая химия.
3.1.Тема: «Теория строения органических соединений. Классификация и номенклатура»
1. Немного из истории органической химии. Природные и синтетические органические вещества. Общие свойства органических веществ (состав, тип химической связи, кристаллическое строение, растворимость, отношение к нагреванию в присутствии кислорода и без него).
2. Теория строения органических соединений А.М. Бутлерова. Развитие теории и ее значение.
3. Классификация органических веществ.
4. Особенности строение органических соединений.
5. Номенклатура органических соединений.
Свое название органические вещества получили потому, что первые из изученных веществ этой группы входили в состав живых организмов. Большинство известных сейчас органических веществ не встречаются в живых организмах, они получены (синтезированы) в лаборатории. Поэтому различают природные (натуральные) органические вещества (хотя большинство из них может быть сейчас получено в лаборатории), а органические вещества, не существующие в природе – синтетические органические веществами. Т.е. название «органические вещества» историческое и особого смысла не имеет. Все органические соединения являются соединениями углерода. К органическим веществам относятся соединения углерода, кроме изучаемых в курсе неорганической химии простых веществ, образованных Карбоном, его оксидов, угольной кислоты и ее солей. Другими словами, органическая химия – это химия соединений углерода.
Краткая история развития органической химии:
Первый учебник органической химии. Берцелиус, 1827, Виталисты. Учение о «жизненной силе».
Первые органические синтезы. Велер, 1824, синтез щавелевой кислоты и мочевины. Кольбе,1845, уксусная кислота. Бертло,1845, жир. Бутлеров,1861, сахаристое вещество.
Создания теории строения органических соединений. Существенный вклад в нее внесли немецкий ученый Ф.А.Кекуле и шотландец А.С.Купер. Но решающий вклад несомненно принадлежит русскому химику А.М.Бутлерову.
Все органические соединения – это соединения углерода. Среди всех элементов углерод выделяется своей способностью образовывать устойчивые соединения, в которых его атомы связаны друг с другом в длинные цепи различной конфигурации (линейные, разветвленные, замкнутые). Причина этой уникальной способности: примерно одинаковая энергия связи С-С и С-О (для других элементов энергия второй связи – намного больше). Кроме того, атом углерода может находиться в одном из трех видов гибридизации, образуя соответственно одинарные, двойные или тройные связи, причем не только между собой, но и с атомами кислорода или азота. Правда, гораздо чаще (практически всегда) атомы углерода соединены с атомами водорода. Если в состав органического соединения входит только углерод и водород, то соединения называются углеводородами. Все остальные соединения можно рассматривать как производные углеводородов, в которых некоторые атомы водорода замещены на другие атомы или группы атомов. Поэтому можно дать такое определение: Органические соединения – это углеводороды и их производные. Органических соединений очень много - более 10 млн. (неорганических около 500 тыс.).
Состав, строение и свойства всех органических веществ имеют много общего.
Органические вещества имеют ограниченный качественный состав и неограниченный количественный состав. Обязательно входят элементы С и Н, часто О или N, реже галогены, фосфор, сера. Другие элементы входят в состав органических веществ очень редко. А вот число атомов в молекуле может достигать млн, и молекулярная масса может быть очень большая.
Строение органических соединений. Т.к. состав – неметаллы. => Химическая связь: ковалентная. Неполярная и полярная. Ионная очень редко. => Кристаллическая решетка чаще всего молекулярная.
Общие физические свойства: невысокая температура кипения и плавления. Среди органических веществ есть газы, жидкости и легкоплавкие твердые вещества. Часто летучи, могут иметь запах. Обычно бесцветные. Большинство органических веществ нерастворимо в воде.
Общие химические свойства:
1) при нагревании без доступа воздуха все органические вещества «обугливаются», т.е. при этом образуется уголь (точнее сажа) и некоторые другие неорганические вещества. Происходит разрыв ковалентных связей, сначала полярных, потом и неполярных.
2) При нагревании в присутствии кислорода все органические вещества легко окисляются, и при этом конечными продуктами окисления являются углекислый газ и вода.
Дата: 2019-04-23, просмотров: 357.