По способу получения нуклиды подразделяют на: реакторные, циклотронные и генераторные.
Например, у нас, в ОКБ ХМАО, в настоящее время используется генераторный изотоп 99mTc.
Такой нуклид является короткоживущим. Образуется из изотопа с длительным перио-
дом полураспада, помещенного в свинцовый контейнер(генератор). Генератор можно транспортировать на большие расстояния. В последующем получают дочерний нуклид 99mTc непосредственно в диагностической лаборатории, ex tempore.
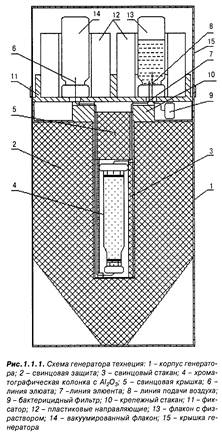
Радионуклидный генератор 99Мо – 99mTc представляет собой стальной цилиндрический контейнер со съемной крышкой. В середине находится стеклянная или пластмассовая колонка, окруженная свинцовой защитой от y- излучения. Внутри колонки содержится сорбент (оксид алюминия или силикагель), на котором прочно адсорбирован материнский радионуклид 99Мо.
При промывании колонки физиологическим раствором (элюентом) происходит обмен ионами Cl – и 99mTc04-, давая на выходе элюат 99mTc в виде пертехнетата натрия Na +(99mTc04-).
Для элюирования на иглу входного канала помещают флакон с элюентом, а на иглу выходного канала- вакуумированный пустой флакон. В него поступает элюат под избыточным давлением из колонки, промываемый поступающим элюентом. Через 10-12 часов в генераторе снова накапливается 99mTc, и тогда снова можно повторять процесс элюирования («дойка» генератора на радиологическом жаргоне).
Стоимость одного такого генератора примерно 100 тыс. рублей
Срок его работы-две недели
Всего за время работы одного генератора можно обследовать примерно 200 пациентов.
Кроме того, для ОКБ ХМАО-Югры приобретен и установлен циклотрон. На нём получают ультракороткоживущие изотопы, для проведения ПЭТ- исследований. В настоящее время уже завершены т многочисленные подготовительные и разрешительные мероприятия, а также подготовка специалистов. Проводят обследование пациентов, онкопрофиля, и кардиологических.
Активность примененного радионуклида в организме уменьшается вследствие двух факторов: распада его атомов, то есть физического процесса, и выведения его из организма, то есть биологического процесса.
Физический период полураспада – время, в течение которого активность радиоактивного нуклида уменьшается вдвое за счет его распада.
Эффективный период полувыведения – время, в течение которого активность РФП, введенного в организм, уменьшается вдвое за счёт его распада, так и за счет выведения его из организма.
Требования к радионуклидам и РФП:
*Для визуализации предпочитают изотопы, распад которых сопровождается гамма- или рентгеновским излучением, так как альфа и бета частицы плохо проходят через ткани организма.
*Энергия квантов в диапазоне 70-200 кэв;
*Небольшой физический период полураспада и небольшой период эффективного полувыведения;
* минимальная лучевая нагрузка при введении
*органотропность РПФ- то есть свойство препарата накапливаться в определенном органе.
* Физиологическая фармакодинамика без фармакологического воздействия;
*Атоксичность;
*Апирогенность.
Единицей активности радионуклида в системе единиц СИ является беккерель (Бк): 1 Бк равен 1 ядерному превращению за 1 с.
На практике еще используют внесистемную единицу кюри (Ки): 1 Ки=3,7х10-10 ядерных превращений за 1 с, кратную единицу мегакюри (МКи) и дольные - милликюри; микрокюри (мкКи),нанокюри(nKu)
Подсчитано, что 1 Бк равен 0,027 нКи.
Объект исследования- человек или его среды, животное.
Методы РД условно можно разделить на две группы: in vitro и in vivo .
РД in vitro основана на способности химического вещества присоединять изотопы. Тем самым по уровню гамма-излучения можно измерить количество активного вещества в определенном обьеме. Например, уровень гормонов, ферментов, витаминов, лекарственных препаратов в периферической крови. Метод выполняется без введения РФП в организм. Чаще применяется радиоиммунологический анализ.
РД in vivo –основан на способности органов человека избирательно накапливать РФП. Радионуклид соединен с молекулой-носителем, определяющей их распределение в организме. Можно изучать метаболические процессы, то есть получать информацию о физиологических функциях органов. Эта способность –главное преимущество РД в сравнении с другими методами лучевой диагностики.
Приемник (детектор) излучения – при всех способах регистрации излучения всегда один и тот же во всех приборах (радиометр, радиограф, сканер, гамма-камера) – сцинтиляционный датчик. Меняются только размеры сцинтиляционного кристалла.
На рисунке видны составляющие сцинтиляционного датчика:
-коллиматор, расположенный перед сцинтиляционным кристаллом. Представляет собой свинцовую пластину с мелкими параллельными отверстиями. Гамма- кванты, перпендикулярно направленные датчику, свободно проходят. Кванты, имеющие косое направление, поглощаются свинцом.
-сцинтиляционный кристалл ( чаще йодит натрия), способный испускать свет (сцинтиляцию) при поглощении гамма-квантов,
-фотоумножители, улавливающие свет, и генерирующие электрический сигнал. Анализом сигналов со всех фотоумножителей определяется интенсивность и расположение каждой сцинтиляции. Далее идет обработка данных.
-блок обработки информации.
Регистрация уровня излучения включает пять способов: радиометрия клиническая или лабораторная, радиография, сканирование, сцинтиграфия, а также эмиссионная томография, одно- или двух фотонная. Три последних способа могут называть радиоактивной визуализацией.Потому что при этом видна картина пространственного распределения РФП в органах.
Методы радионуклидной диагностики (краткий обзор):
Радиометрия клиническая - детектор расположен над интересующей областью. Измеряется уровень гамма-излучения в импульсах\ мин. По уровню излучения определяют скорость захвата органом РФП, то есть о функциональной активности. В основном определяют медленно протекающие процессы. Например, йодпоглотительная функция щитовидной железы.
Радиометрия лабораторная: группа лабораторных исследований, при которых происходит взаимодействие РФП с биологическими средами в пробирке по механизму взаимодействия антиген-антитело.
Радиография - в отличие от радиометрии здесь измерение уровня излучения производится через определенные промежутки времени. Это позволяет построить график накопления, перераспределения и выведения РФП в органе или органах. Метод применяют для относительно быстро протекающих процессов: радиоренографии, радиопульмонографии, радиогепатографии.
Пример проведения радиоренографии. Иногда бывает, кроме двух датчиков над почками, третий датчик - над сердцем.
Радионуклидная визуализация. Методика создания картины пространственного распределения в органах РФП, введенного в организм. Радионуклидная визуализация включает в себя следующие виды:
Сканирование – прибор регистрации- сканер. Детектор сканера движется над исследуемой зоной, измеряя активность «по строчкам». Например, сканирование печени. Одновременно по бумаге движется печатающая головка. На получающемся изображении густота штриховки и ее цвет отображают уровень зарегистрированной активности.
Сцинтиграфия – прибор регистрации- гамма-камера. Детектор гамма- камеры имеет большие размеры (0,5 метра) и регистрирует активность сразу над большой площадью. С компьютера изображение органона идет на экран монитора, или на бумагу или на пленку. Или сохраняется файл.
Сцинтиграмма это функционально-анатомическое изображение. В этом заключается уникальность метода, отличающая его от УЗИ, КТ, МРТ. Поэтому обязательное условие для назначения сцинтиграфии – исследуемый орган должен быть хоть в ограниченной степени функционально активным, в противном случае изображение не получится.
Различают сцинтиграфию:
Статическая сцинтиграфия – получение небольшого количества изображений органа с преимущественной задачей изучения морфологии органа и выявления в нем участков повышенного или пониженного накопления РФП.
Динамическая сцинтиграфия – информация записывается непрерывно или через короткие промежутки времени с отражением на серии кадров.
В целом сцинтиграфия метод морфо-функциональный.
Дата: 2019-03-05, просмотров: 490.