СОДЕРЖАНИЕ
1. Предисловие………………………………………………………………5
2. Краткая история…………………………………………………………….6
3. Черепно-мозговая травма………………………………………………33
- Эпидемиология ЧМТ…………………………………………………..33
- Классификация ЧМТ……………………………………………………35
4. Основные клинические синдромы при нейрохирургической
патологии…………………………………………………………………40
- Синдром ВЧГ……………………………………………………………40
- Нарушение сознания……………………………………………………42
- Эпилептический синдром………………………………………………51
- Очаговый неврологический синдром…………………………………54
- Менингеальный синдром………………………………………………61
- Травматическое субарахноидальное кровоизлияние…………………63
- Гипертензионно-дислокационный синдром…………………………66
5. Клиническая характеристика поражений головного мозга
при ЧМТ…………………………………………………………………73
- Сотрясение головного мозга……………………………………………74
- Ушиб головного мозга легкой степени………………………………74
- Ушиб головного мозга средней степени………………………………76
- Ушиб головного мозга тяжелой степени………………………………78
- Сдавление головного мозга……………………………………………80
· Эпидуральная гематома……………………………………………81
· Субдуральная гематома……………………………………………83
· Внутримозговая гематома…………………………………………86
· «Светлый промежуток»……………………………………………89
6. Построение нейрохирургического диагноза……………………………92
- Классификация переломов черепа……………………………………94
- Формулировка диагноза………………………………………………101
- Переломы основания черепа…………………………………………..102
7. Дополнительные методы исследования……………………………….104
- Люмбальная пункция…………………………………………………104
- ЭХО-энцефалоскопия (ЭЭС)…………………………………………105
- Протокол обследования пациента с ЧМТ……………………………108
8. Хирургическое лечение ЧМТ…………………………………………109
- Шкала исходов ЧМТ…………………………………………………116
9. Заключение………………………………………………………………119
10. Список принятых сокращений…………………………………………119
11. Дидактический материал………………………………………………121
12. Список рекомендуемой литературы………………………………….125
ПРЕДИСЛОВИЕ
Вопрос о необходимости преподавания нейрохирургии в медицинских институтах поставил еще в 1937 г. академик Н. Н. Бурденко. Молодые врачи различных специальностей после окончания института должны быть знакомы с основами диагностики и лечения повреждений и заболеваний нервной системы, требующих своевременного распознавания, а иногда и неотложной нейрохирургической помощи. Нейрохирургия, как предмет преподавания в медицинских вузах СССР, был включен в учебную программу с 1972 года. Первое издание учебника «Нейрохирургия», написанного профессором И.М.Иргером, вышло в 1971 году, учебник был переиздан в 1982 году. В течение многих лет он оставался единственным учебным пособием по нейрохирургии для студентов в нашей стране. Многие современные нейрохирурги начали свой путь в нейрохирургию со знакомства с ним. Неплохо зарекомендовал себя учебник «Основы нейрохирургии» венгерского профессора Э. Пастора, переведенный на русский язык в 1985 году. Следующий учебник «Нейрохирургия» для студентов медицинских вузов, написанный С.В. Можаевым, А.А. Скоромцом, Т.А. Скоромцом был издан в 2001 г. В нем были обобщены достижения нейрохирургии и смежных наук за последние два десятилетия ХХ века.
Процесс преподавания нейрохирургии в нашем Университете совершенствуется и существенно изменился за последние 10 лет, возникла необходимость публикации нового учебного пособия по нейрохирургии. В данном пособии освещены основные разделы нейрохирургии, приводятся базовые аспекты предмета, необходимые студенческой аудитории. При его составлении мы следовали мудрому принципу Аристотеля «docendo discimus» (обучая, мы обучаемся сами).
ЧЕРЕПНО-МОЗГОВАЯ ТРАВМА
Эпидемиология ЧМТ. Черепно-мозговая травма (ЧМТ) – это русскоязычный термин, который не совсем правильно отражает суть явлений. Дело в том, что повреждения черепа, в виде его переломов, встречаются только при ушибах головного мозга и то менее, чем в 50 – 60% случаев, а при сотрясении головного мозга, на долю которого приходится 80% всех ЧМТ, повреждений черепа не бывает. Наверное, правы англоязычные авторы, называя ЧМТ- «head injury» (повреждение головы). Тем не менее, в России исторически сложилась такая ситуация, что этот вид травмы характеризуют, как черепно-мозговую травму.
ЧМТ занимает первое место среди всех травм (40%) и встречается во всех возрастах, но наиболее часто в трудоспособном возрасте (15 – 44 года).
ЧМТ в 2 раза чаще встречается среди мужчин, по сравнению с женщинами, а смертность от ЧМТ среди мужчин в 3 раза выше, чем среди женщин, что свидетельствует о более тяжелом характере травмы у «сильной» части человечества. Ежегодный общий ущерб от ЧМТ в государственном масштабе по данным американских исследователей составляет до 100 миллиардов $. Для того, чтобы наглядно охарактеризовать ущерб, наносимый ЧМТ, достаточно сказать, что на эти средства можно было бы построить 7 гидроэлектростанций. Поэтому ЧМТ является не только серьезной медицинской, но и социальной проблемой.
В популяции около 250 миллионов человек (население США) ЧМТ встречается у 500.000 человек ежегодно (2:1000), а в крупных городах частота ее встречаемости возрастает до 7 случаев на 1000 населения. 50.000 (10%) погибают на догоспитальном этапе и 450.000 поступают в стационары.
То есть мы видим, что речь идет только о засвидетельствованной травме. Если учесть, что до 20% лиц, получивших легкую ЧМТ за медицинской помощью не обращаются, то количество пострадавших увеличится на 100000 человек.
Из поступивших в стационар у 80% (360.000) имеется легкая ЧМТ, у 10% (45.000) - средней тяжести и 10% (45.000) – тяжелая травма. Обшая смертность от ЧМТ составляет 4 – 5 %.
Перманентные последствия в виде инвалидизации имеются у 10% перенесших легкую ЧМТ, у 66% после травмы средней степени тяжести и у 100% с тяжелой ЧМТ. Общий государственный ущерб за счет больных с последствиями ЧМТ составляет в США около 25 миллиардов $.
В мирное время по механизму получения на первом месте находится автодорожная травма (водитель, пассажиры салона во время аварии, сбитые автомобилем пешеходы).
На втором месте стоит бытовая травма. Это случайные падения с ударом головой о твердое покрытие, удары головой о стену и т.д. К бытовой травме относится и травма вследствие криминальных действий (нападения, избиения, драки).
Третье место принадлежит производственной травме и четвертое место отводится спортивной травме.
Классификация ЧМТ. Первая классификация ЧМТ принадлежит Жану-Луи Пти (рис.1) – французскому хирургу и анатому.
Пти предлагал выделять при ЧМТ три основных нозологических формы: сотрясение головного мозга (commotio cerebri) , ушиб головного мозга (contusio cerebri) и сдавление головного мозга (compressio cerebri). Сдавление головного мозга Ж.Л. Пти относил к одной из самостоятельных нозологических форм наравне с сотрясением и ушибом головного мозга.
В основе любой медицинской классификации лежит диагностический принцип - на основании классификации формулируется развернутый диагноз и в соответствии с поставленным диагнозом назначается лечение. Так как медицинские знания совершенствуются и углубляются, то медицинские классификации время от времени подвергаются пересмотру. Не является исключением и классификация черепно-мозговой травмы. Современная классификация ЧМТ выглядит следующим образом (рис. 2)
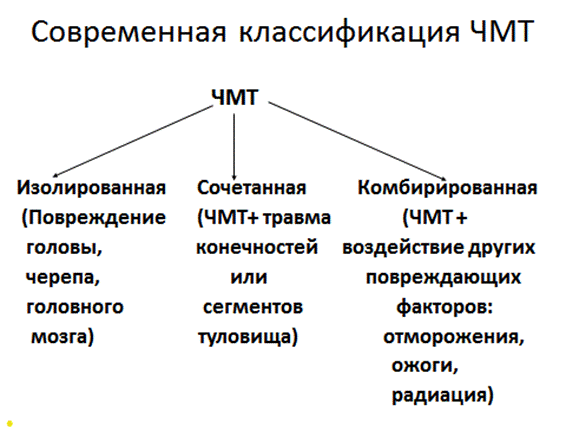
Рис. 2. Изолированная, сочетанная, комбинированная ЧМТ
Изолированная ЧМТ – это травма, при которой имеются повреждения кожных покровов головы, черепа и головного мозга. Сочетанная ЧМТ – травма, при которой ЧМТ сочетается с травмой конечностей (например: переломы) или сегментов туловища (грудной клетки, брюшной полости). При комбинированной ЧМТ имеет место комбинация различных по своей сути повреждающих факторов (травматический, вследствие воздействия, которого возникает ЧМТ, плюс, например, термический фактор – отморожение, ожоги, или радиационное воздействие). Неврологов и нейрохирургов в большей степени интересует изолированная ЧМТ, классификация которой приведена на рисунке 3.
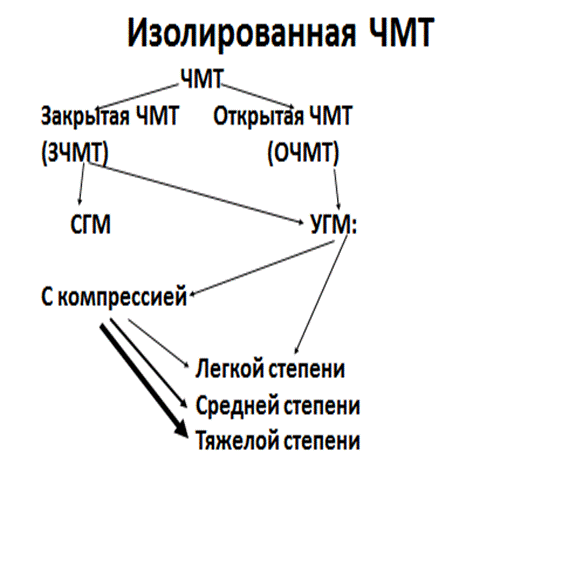
Рис. 3. Классификация изолированной черепно-мозговой травмы
В данной схеме следует уделить внимание следующим моментам. Во-первых, при ЗЧМТ может быть как сотрясение головного мозга (СГМ), так и ушиб головного мозга (УГМ), но если у пострадавшего имеется ОЧМТ, то речь всегда идет о УГМ. Во-вторых, СГМ является монолитным диагнозом и не подлежит градации, а ушиб головного мозга делится на ушиб легкой, средней и тяжелой степени. В-третьих, компрессия головного мозга встречается только при УГМ. В-четвертых, по современной классификации, в отличие от классификации Ж.-Л. Пти, компрессия головного мозга не является самостоятельной нозологической формой и рассматривается как внутричерепное негнойное осложнение острого периода тяжелой ЧМТ.
ОЧМТ это травма, при которой возникает сообщение полости черепа с внешней средой. Такая ситуация возникает при открытых переломах костей свода черепа (ситуация, при которой имеется рана кожных покровов головы, на дне которой определяется перелом кости черепа), а также при переломах средней (СЧЯ) и передней черепных ямок (ПЧЯ) (рис. 4). При переломах ПЧЯ часто повреждается lamina cribrosa, являющаяся верхней стенкой носовой полости, сообщение полости черепа с внешней средой происходит за счет носовых ходов. В этом случае у пострадавшего имеется такой абсолютный признак перелома ПЧЯ, как истечение ликвора с примесью крови из носа. Этот симптом называется назоликворея. При переломах СЧЯ, когда повреждается пирамида височной кости, вглубь которой вдается наружный слуховой проход, сообщение внешней среды с полостью черепа происходит именно через него. В данном случае при осмотре у пострадавшего выявляется истечение ликвора с примесью крови из наружного слухового прохода. Этот клинический признак перелома СЧЯ является абсолютным и называется отоликвореей.
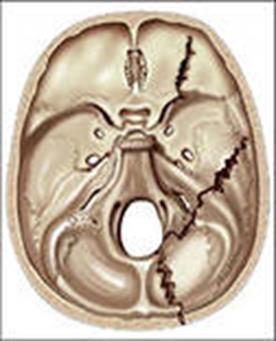
Рис. 4. Переломы основания черепа
Почему важно выделять ОЧМТ в отдельную нозологическую форму? Если при ОЧМТ, как было сказано выше, имеется сообщение полости черепа с внешней средой, то существует вероятность развития внутричерепной гнойной инфекции – это:
- гнойный менингоэнцефалит
- абсцесс головного мозга
- остеомиелит костей черепа
Поэтому пациент с диагнозом ОЧМТ с первого дня поступления в стационар должен получать антибактериальную терапию, направленную на профилактику этих весьма серьезных гнойных осложнений.
Все другие варианты травмы относятся к закрытой черепно-мозговой травме. Это – ушибленные раны кожи головы, закрытые переломы костей черепа, травмы, при которых кожные и костные повреждения разнесены по поверхности головы, например, кожная рана имеется в лобной области, а перелом локализуется в затылочной кости.
ОСНОВНЫЕ КЛИНИЧЕСКИЕ СИНДРОМЫ ПРИ НЕЙРОХИРУРГИЧЕСКОЙ ПАТОЛОГИИ.
Для того чтобы охарактеризовать тяжесть поражения головного мозга, необходимо представлять, что любое нейрохирургическое заболевание головного мозга (травма, опухоль, сосудистое или воспалительное заболевание) может быть охарактеризовано 4 основными синдромами. Это синдром внутричерепной гипертензии (ВЧГ), синдром очаговой неврологической симптоматики, менингеальный синдром и гипертензионно-дислокационный синдром. Коротко остановимся на этих 4 синдромах.
Синдром внутричерепной гипертензии (ВЧГ).
Синдром ВЧГ относится к общемозговым синдромам. Чтобы представить за счет чего повышается внутричерепное давление при заболеваниях головного мозга, необходимо знать доктрину Монро-Келли, предложенную этими двумя авторами более 200 лет назад. Суть доктрины заключается в следующем. Внутричерепные объемы (рис. 5) заключены в ригидном костном образовании – полости черепа и суммарный объём внутричерепных компонентов (кровь, ликвор и мозговое вещество) остается постоянным.
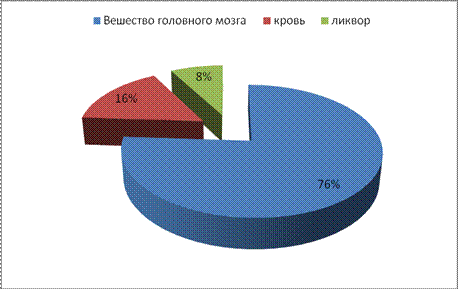
Рис. 5. Соотношение внутричерепных объемов
Основное место в соотношении внутричерепных объемов принадлежит головному мозгу, на долю которого приходится 76%. 8% объема внутричерепного содержимого (ОВЧС) занимает ликвор. Оставшиеся 16% - это артериальная и венозная кровь, протекающая по сосудам головного мозга и синусам полости черепа. В норме объем полости черепа больше, чем ОВЧС, т.е. в полости черепа имеются так называемые резервные пространства, объем которых увеличивается с возрастом в силу атрофических процессов головного мозга. При появлении в полости черепа дополнительного объема (гематома, опухоль) объем внутричерепного содержимого компенсаторно уменьшается, в первую очередь за счет ликвора, а затем за счет уменьшения кровенаполнения головного мозга. При дальнейшем увеличении в размерах дополнительного патологического внутричерепного объемного образования эти компенсаторные возможности исчерпываются, и внутричерепное давление начинает повышаться.
Клиническими симптомами ВЧГ являются головная боль, рвота, головокружение и нарушение сознания. Охарактеризуем эти симптомы последовательно.
1. Головная боль
Источником болевых ощущений при ВЧГ является давление увеличенного объема внутричерепного содержимого на твердую мозговую оболочку (ТМО), которая имеет большое количество болевых рецепторов. Так как избыточному давлению подвергается вся ТМО, то боль является диффузной. По причине давления на твердую мозговую оболочку изнутри полости черепа головная боль имеет распирающий характер. Следующая характеристика боли – ее постоянный характер. Головная боль при ВЧГ имеет суточную динамику – она достигает максимума в ночные и утренние часы. Так как больной во время сна находится в горизонтальном положении, происходит затруднение оттока венозной крови и ликвора из полости черепа, что приводит к дополнительному увеличению ОВЧС.
2. Рвота
Рвота возникает на высоте головной боли, т.е. в ночные, а чаще в утренние часы, сразу после сна и, следовательно, не связана с приемом пищи. Она не имеет предвестников в виде чувства тошноты и возникает внезапно, не принося облегчения.
3. Головокружение
О головокружении при ВЧГ следует сказать, что оно отличается от вестибулярного головокружения тем, что имеет постоянный и несистемный характер.
4. Нарушение сознания
Речь идет о нарушении сознания, а не о его утрате. ЧМТ всегда сопровождается более или менее длительной утратой сознания в момент травмы. Если при травме не было утраты сознания, то диагноз ЧМТ является сомнительным. Ясное сознание соответствует субъективному ощущению, формирующемуся в результате взаимодействия личности с внутренним и внешним миром, и проявляется прежде всего адекватной реакцией на внешние раздражители. Различают качественные и количественные аспекты сознания. Уровень бодрствования является основной количественной характеристикой сознания. Содержательная часть и ясность сознания представляют собой его качественные характеристики. Во всем мире нарушения сознания оцениваются по шкале комы Глазго, предложенной еще в 60-ых годах прошлого столетия. По этой шкале по баллам оценивают 3 параметра: открывание глаз, словесный ответ и двигательный ответ (рис. 6).

Рис. 6. Школа комы Глазго
Результаты оценки сознания приведены на рисунке 7.

Рис. 7. Результаты оценки сознания по ШКГ
Шкала комы Глазго позволяет провести бальную оценку сознания. Однако является весьма приблизительной и далеко не в полной мере отражает суть происходящего. Неудовлетворенность этой шкалой побудила группу отечественных исследователей во главе с нейрохирургом акад. А.Н. Коноваловым предложить отечественную классификацию нарушений сознания. Также как и в ШКГ в отечественной классификации выделяют ясное сознание, оглушение, сопор и кому. Ясное сознание - это термин, указывающий на то, что индивид адекватно ориентируется в месте, времени, в обстановке, ситуации и в собственной личности. Оглушение делится на две степени тяжести: умеренное (I), глубокое (II). При оглушении I больной сидит, т.к. стоять ему тяжело, но все-таки он в состоянии поддерживать вертикальное положение. Сидит с опущенной головой, гиподинамичен (малоподвижен), не интересуется окружающим. На вопросы отвечает с некоторой задержкой тихим голосом. Пациент доступен для диалога (с ним можно поговорить о его семье, работе и т.д.). Для того чтобы оценить степень нарушения сознания врач должен задать вопросы, позволяющие ему понять ориентируется ли пациент в месте, во времени и собственной личности. Ориентация в месте: «Где вы находитесь?», ориентация во времени: «Какой сейчас год? Какое время года? Какое время суток?», ориентация в собственной личности: «Сколько вам лет?» На все эти вопросы пациент в оглушении I отвечает правильно. При оглушении II пациента доставляют в приемное отделение на каталке, т.к. он не в состоянии поддерживать вертикальное положение. Пострадавший производит впечатление спящего человека. На обращение открывает глаза, фиксирует взор. Пациент не доступен для диалога. На вопросы отвечает односложно с большой задержкой. Часто для того чтобы получить ответ необходимо несколько раз повторить один и тот же вопрос громким голосом, еще лучше «потормошить» больного. По ответам можно судить, что больной дезориентирован в месте, во времени и в собственной личности. Он не правильно называет место, где находится. В приемном покое, или даже в машине скорой помощи вы услышите, что он находится дома, или на работе, или на даче и т.д. Пациент дезориентирован во времени, неправильно называя текущий год, текущий сезон, время суток. Пострадавший также дезориентирован в собственной личности и ошибается в своем паспортном возрасте. Если больного с оглушением II оставить в покое, то он закрывает глаза и засыпает, следовательно, для оглушения II характерны также быстрая истощаемость и сомнолентность (сонливость). Сопор (от лат. sopor — оцепенение, вялость, сон). Больной лежит с закрытыми глазами, производя впечатление спящего. На обращение не реагирует. Словесный контакт отсутствует. В ответ на болевое раздражение открывает глаза, не фиксируя взгляд, на лице появляется гримаса боли, пострадавший может застонать (это максимум, что вы можете от него услышать). Такие реакции не имеют никакого отношения к сознанию. Тем не менее, больной, находящийся в сопоре, все-таки еще находится в сознании. Определить это мы можем на основании его ответа на болевые раздражения, который является целесообразным. Целесообразный (адекватный) ответ на болевое раздражения - это локализация источника раздражения рукой и его устранение (или хотя бы попытка этого действия). Следовательно, при проверке ответа на болевое раздражение мы должны наносить его в разных участках тела. Если больной совершает хотя бы попытку движения рукой в сторону наносимого болевого раздражения, то он находится в сопоре.
Кома (от греч. κῶμα — глубокий сон). Врачи древней Греции назвали это состояние глубоким сном на основании признака непробуждаемости в виде отсутствия открывания глаз в ответ на раздражения. Как следует из выше изложенного, больные в оглушении II, сопоре производят впечатление спящих, но при оглушении II больной открывает глаза («пробуждается») в ответ на обращение, при сопоре – в ответ на болевое раздражение. В случае комы, реакции в виде открывания глаз, мы не увидим ни при каких раздражениях («непробуждаемость»). В ответ же на болевые раздражения возникают лишенные целесообразности, патологические двигательные ответы. В зависимости от их характера, или их отсутствия, а также от состояния витальных функций, кома делится на три степени тяжести: кома I, кома II, кома III.
Кома I . В ответ на болевое раздражение пациент совершает стереотипное медленное, тоническое сгибание верхних конечностей (конечности, если имеется гемипарез) в локтевых суставах. При этом кисти расслаблены и находятся в висячем положении (Рис. 8). Такой ответ также называется декортикационной (de – отсутствие, cortex – кора головного мозга) ригидностью, в состав которой также входит экстензорно-пронаторное положение стоп. Термин «декортикационная ригидность» пришел в медицину из нейрофизиологии. На ранних этапах ее развития функции головного мозга изучали на животных методом перерезок и экстирпаций. При перерезке головного мозга на уровне лучистого венца (под корой) у животных развивалось именно такое перераспределение мышечного тонуса.
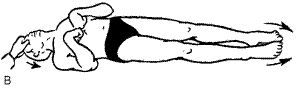
Рис. 8. Кома I. Двигательный патологический ответ на болевое раздражение
Следует сказать, что исследование ответов на болевое раздражения у больных находящихся в коме подразумевает нанесение массивных болевых раздражений (давление на точку выхода I ветви тройничного нерва, давление средним межфаланговым суставом указательного пальца на грудину, давление карандашом на ноготь) (рис. 9).

Рис. 9. Методика исследования двигательного ответа на болевое раздражение у больных, находящихся в коме
При коме первой степени тяжести – витальные (жизненно важные) функции стабильны. У больных определяется адекватное дыхание с частотой дыхательных движений не более 20 и достаточной глубиной дыхательной экскурсии грудной клетки. Артериальное давление (АД) у больных в коме I, как правило, повышено. Повышение артериального давления и появление брадикардии при ВЧГ впервые описал Х. Кушинг. Эта реакция организма на ситуацию внутричерепной гипертензии носит название рефлекса Кушинга. Рефлекс Кушинга имеет компенсаторный характер. При увеличении объема ВЧС артерии коры головного мозга придавливаются к внутренней поверхности костей черепа, что приводит к уменьшению перфузионного давления в них (церебральное перфузионное давление – ЦПД), которое рассчитывается по формуле: ЦПД = системное артериальное давление (САД) – внутричерепное давление (ВЧД). Следовательно, повышение системного артериального давления является компенсаторной реакций, направленной на повышение ЦПД. Из сказанного следует, что проведение гипотензивной терапии при повышении АД у больного с ВЧГ не только бессмысленно, но и вредно. Это правило не распространяется на ситуации, когда верхнее давление превышает 190 мм рт. ст. При таком давлении происходит срыв регуляторных механизмов мозгового кровообращения и помимо суженных сосудов появляются сосуды, находящиеся в состоянии дилатации. В такой ситуации возникает реальная угроза развития церебрального кровоизлияния.
Кома II. В ответ на болевое раздражение у больных возникает экстензорно-пронатороное (экстензия – разгибание, пронация – поворот кнутри) тоническое движение верхними конечностями (рис. 10). Такой ответ называется децеребрационной (de – отсутствие, cerebrum – большой мозг) ригидностью (комментарий см. – кома I). Шея находится в состоянии гиперэкстензии.
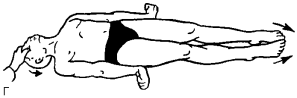
Рис. 10.Кома II. Двигательный ответ на болевое раздражение
В зависимости от состояния витальных функций кома второй степени тяжести делится на кому II А и кому II Б. При коме II А витальные функции стабильны и еще сохраняется рефлекс Кушинга. Для комы II Б характерно нарушение витальных функций. В первую очередь это касается функции дыхания. У больных развиваются патологические типы дыхания. Наиболее часто встречается центральная одышка и реже периодическое дыхание Чейн-Стокса (рис. 11). Центральная одышка характеризуется частым, поверхностным дыханием. Частота дыхательных движений может достигать 60 и более в 1минуту. При такой частоте дыхания грудная клетка не в состоянии совершать достаточный объем дыхательного движения, поэтому дыхание поверхностное.

Рис. 11. Спирография при коме IIБ. 1 – центральная одышка, 2 – дыхание Чейн-Стокса
Так как у больных имеется тризм (патологическое напряжение) жевательной мускулатуры, то выдох совершается через плотно сжатые губы. Поэтому дыхание у этих больных шумное. Следующая характерная черта центральной одышки – равнофазность дыхательных движений. Если в норме выдох длиннее вдоха, то при центральной одышке фаза вдоха равна фазе выдоха. Шумное, частое, равнофазное дыхание послужило поводом для второго названия этого типа дыхания. Центральную одышку еще называют «машинным» или «механическим» дыханием. Второй тип патологического дыхания – дыхание Чейн-Стокса - характеризуется периодами нарастающих по амплитуде дыхательных движений. По достижении максимальной амплитуды следует фаза уменьшения амплитуды дыхания. Между такими периодами имеется фаза апноэ. Эти типы дыхания называются патологическими не только потому, что они отражают патологию дыхательного центра. Они патологические по своей сущности, так как не обеспечивают необходимой оксигенации организма. Эти типы дыхания приводят к развитию гипоксии, в том числе, и головного мозга. При коме IIБ у больного уже выявляется артериальная гипотония, еще не достигающая критических значений (например, у нормотоника может определяться давление 100/60 мм рт. ст.). Но если мы вспомним сказанное о компенсаторном значении повышения системного АД при ВЧГ, то становится понятным, что головной мозг больного испытывает ишемию. Травма, гипоксия и ишемия головного мозга сопровождается травматическим, гипоксическим и ишемическим отеком, что приводит к дальнейшему увеличению объема внутричерепного содержимого и нарастанию ВЧГ. Сказанное делает понятным на данном этапе необходимость реанимационных мероприятий, включающих в себя лечебный наркоз, искусственную вентиляцию легких и поддержание АД на постоянном уровне. Процесс неуклонного роста ОВЧС приводит к ситуации, при которой исчерпываются компенсаторные возможности резервных пространств полости черепа, наступает критическая декомпенсация состояния больного, а ВЧГ переходит в неуправляемую стадию.
На рисунке видно, что за счет резервных пространств полости черепа по мере увеличения внутричерепного содержимого на 1 – 2 участке кривой ВЧГ растет медленно. На 2 – 3 участке рост ВЧГ становится более интенсивным (субкомпенсация). 3 – 4 – резкий скачок внутричерепного давления (декомпенсация, неуправляемая ВЧГ).
Наши терапевтические возможности ограничиваются 1 – 2 – 3 участком кривой. 3 - 4 участок кривой клинически характеризуется развитием комы III, которая является по сути агональным (терминальным) состоянием.
Кома III характеризуется тотальной арефлексией, диффузной мышечной атонией и грубыми нарушениями витальных функций. У больного определяется отсутствие всех рефлексов (сухожильных, защитных, фотореакций зрачков и т.д.), отсутствует двигательная реакция на боль. Дыхательная функция характеризуется брадипноэ не чаще 10 дыхательных движений в минуту. Дыхание нерегулярное по частоте и амплитуде (атактическое дыхание) (рис. 13).
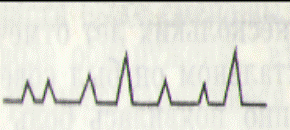
Рис. 13. Кома III. Спирография. Атактический тип дыхания
У больного имеется артериальная гипотония, достигающая критических значений (например, 40/20 мм рт. ст.).
ЭПИЛЕПТИЧЕСКИЙ СИНДРОМ.
Еще одним клиническим синдромом, характеризующим нейрохирургическую патологию головного мозга, является эпилептический синдром. Эпилептические припадки по своему происхождению являются симптомами раздражения или ирритации. В зависимости от того какого типа припадок возникает у пациента, эпилептический синдром может быть отнесен к общемозговому симптомокомплексу (первично генерализованные припадки) или к очаговому (фокальные или вторично генерализованные припадки).
Различают первично генерализованные, фокальные и вторично генерализованные эпилептические припадки. Термин «генерализация» припадка означает утрату сознания во время припадка и его амнезию.
Хотя первично генерализованные припадки не имеют значения для установления топического диагноза, тем не менее, они часто встречаются при ЧМТ и ее последствиях и вполне уместно кратко охарактеризовать их в рамках данной лекции. К первично генерализованным припадкам относятся большой (судорожный) припадок, малый (безсудорожный) припадок, а также абсанс. Термины большой (grand mal) и малый припадок (petit mal), предложенные в 1815 г французским психиатром Жан-Этьеном Домиником Эскиролем (рис.14), прочно утвердились в мировой психиатрической и неврологической литературе.
Большой (судорожный) припадок.
Является наиболее часто встречающимся эпилептическим припадком. Больной теряет сознание и падает. Наблюдаются генерализованные судороги (не путать с понятием генерализованного припадка) тонико-клонического характера в мышцах конечностей, туловища, лица, языка, в дыхательной мускулатуре (рис. 15). Происходит потеря контроля над функцией тазовых органов (непроизвольное мочеиспускание). Появляется пена изо рта, цианоз лица, апноэ. Возможен прикус языка Длительность припадка – несколько минут, после чего судороги прекращаются. По возвращении сознания больной находится в просоночном состоянии (спутанность сознания, заторможенность, дезориентация). Факт припадка амнезируется, о наличии припадков больные узнают со слов окружающих.
Малый (безсудорожный) припадок.
Характеризуется потерей сознания. Вследствие резкого снижения мышечного тонуса больной падает. По факту снижения мышечного тонуса этот припадок имеет еще одно название – атонический. При наличии у больных таких припадков необходимо проводить дифференциальный диагноз с обморочными (синкопальными) состояниями.
Абсанс.
Больной во время повседневной или трудовой деятельности внезапно прекращает ее и «замирает». Он находится без сознания. Ни судорог, ни падения не отмечается. Окружающие видят застывшее выражение лица и бессмысленный взгляд (рис. 16). Длительность припадка – несколько секунд. Затем пациент приходит в сознание и продолжает прерванную деятельность. Если он разговаривал, то продолжает свой разговор именно с того места, где у него случился припадок. Больные знают об этих припадках со слов окружающих, полностью амнезируя их. Картина припадка напоминает остановившийся на несколько секунд кадр кинофильма.
Менингеальный синдром.
Менингеальный синдром – клинический симптомокомплекс раздражения мозговых оболочек, характеризующийся наличием менингеальных симптомов с (или без) изменениями давления и состава спинномозговой жидкости. Для диагностики ЧМТ наиболее актуальными являются два основных менингеальных симптома из группы мышечно-тонических: ригидность затылочных (шейных) мышц и симптом Кернига. Ригидность затылочных мышц определяется следующим образом: в положении больного лежа на спине, врач не может согнуть его голову кпереди, приведя подбородок к грудине из-за напряжения задней группы мышц шеи. Симптом Кернига определяется следующим образом: врач выводит ногу пациента в положение сгибания в тазобедренном и коленном суставах и пытается ее разогнуть. Если в норме это действие не составляет никакого труда, то при положительном симптоме Кернига этого сделать не удается
При ЧМТ менингеальный синдром свидетельствует о наличии субарахноидального кровоизлияния (САК).
Люмбальная пункция
Люмбальная пункция (ЛП) выполняется в положении больного лежа на боку или сидя. Прокол проводится между остистыми отростками третьего и четвертого поясничных позвонков. Игла прокалывает кожу, подкожную клетчатку, апоневроз, межостистую связку, желтую связку, ТМО дурального мешка и проникает в ликворосодержащее пространство. ЛП имеет лечебно-диагностическое значение. С одной стороны мы подтверждаем диагноз САК, а с другой – выводя ликвор, снижаем повышенное внутричерепное давление. Несмотря на безопасность ЛП, она категорически противопоказана даже при подозрении на сдавление головного мозга, так как в этой ситуации сразу после ЛП может произойти дислокация ствола головного мозга. Дело в том, имеются две разноуровневых камеры, содержащих ликвор. Верхняя камера – это полость черепа, нижняя – спинномозговой канал (СМК). При компрессии головного мозга происходит повышение внутричерепного давления, вследствие чего ликвор выдавливается в СМК, где также повышается давление. Повышенное давление в СМК оказывает подпор снизу по отношению к стволу головного мозга. При выведении ликвора из СМК ликворное давление в нем снижается и возникает перепад между высоким давлением в полости черепа и сниженным давлением в СМК, что и является причиной дислокации ствола головного мозга.
Эхо-энцефалоскопия (ЭЭС).
Чтобы избежать этого опасного осложнения, перед ЛП необходимо произвести такой метод обследования, как эхо-энцефалоскопия (ЭЭС) (рис. 77), если в лечебном учреждении отсутствуют другие современные методы нейровизуализации (КТГ, МРТ).
Метод применяется в нейрохирургии с конца 60-ых – начала 70-ых годов прошлого столетия. Основателем метода был Ларс Лекселл (см. рис 30, стр. 27). ЭЭС относится к методам ультразвукового исследования и полное его название двухмерная эхо-энцефалоскопия. Благодаря работам Л. Лекселла были подобраны такие параметры ультразвука (УЗ), что он проникает в полость черепа. Ультразвук, как любой звук, отражается на границе двух сред, отличающихся по своей физической плотности (феномен эха). Датчик имеет двойное значение. Он генерирует ультразвуковое излучение, а также воспринимает отраженный сигнал, который отображается на экране осциллоскопа. Типичной точкой для проведения исследования является точка, расположенная на 4 см над наружным слуховым отверстием и на 2 см кпереди от него. Первые две разноплотностые среды на пути прохождения УЗ – воздушная прослойка под датчиком и кожные покровы головы. Эти две среды резко отличаются по плотности друг от друга и если не устранить воздушную прослойку, то УЗ не проникнет в полость черепа и полностью отразится на этой границе. Чтобы обеспечить проникновение УЗ в полость черепа, на поверхность датчика наносится гелевая смазка. Для ультразвука кожи и кости имеют одинаковую плотность. Следующие среды на пути УЗ, которые имеют существенно различающуюся плотность – ТМО – ликвор субарахноидальных пространств. Отраженный на этой границе сигнал (начальный комплекс - НК) регистрируется датчиком и «запоминается» аппаратом. Кора головного мозга и его белое вещество для УЗ не отличается по плотности, поэтому он проходит через толщу головного мозга, не отражаясь. На пути следования УЗ имеются следующие две среды, обладающих значимо различающейся плотностью. Это вещество головного мозга – ликвор, содержащийся в III желудочке, который в норме располагается строго по средней линии. Датчик воспринимает отраженный на этой границе сигнал (срединный комплекс – М-эхо). Далее УЗ проходит через противоположное полушарие и отражается на границе кора головного мозга – ликвор субарахноидального пространства, где и происходит третье отражения сигнала (конечный комплекс – КК). В результате на экране осциллоскопа появляется суммированная картинка. Исследование проводится последовательно в симметричных точках с двух сторон (рис. 78).
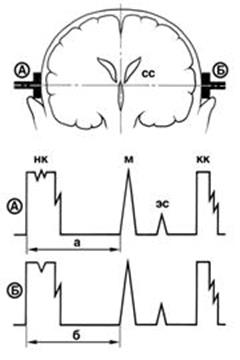
Рис. 78. Эхо-энцефалоскопия. НК – начальный комплекс, М – срединный комплекс, КК – конечный комплекс ЭС – дополнительный не учитываемый сигнал (нижний рог бокового желудочка)
Метод не обладает абсолютной эффективностью, однако, его диагностические возможности весьма велики и приближаются к 76%. Погрешность метода составляет 2 мм. В случае появления дополнительного объема в одном из полушарий головного мозга (при ЧМТ – интракраниальная гематома) III желудочек смещается в противоположную сторону, и при измерении показателей со стороны патологического процесса М-эхо отдаляется от начального комплекса, а при измерении с противоположной стороны приближается к нему (рис. 79). Разница между результатами измерения расстояния от начального комплекса до М-эха с одной и с другой стороны, разделенная на 2 называется смещением М-эха. Для выяснения истинного значения смещения М-эха деление на 2 необходимо, так как мы исследуем отраженный сигнал, и должны иметь в виду, что отраженный эхо-сигнал преодолевает двойное расстояние (туда и обратно). Если значение смещения М-эха равняется 3мм или превышает эту цифру, то необходимо серьезно задуматься о наличие у пациента с ЧМТ интракраниальной гематомы, и проведение ЛП в данном случае противопоказано.
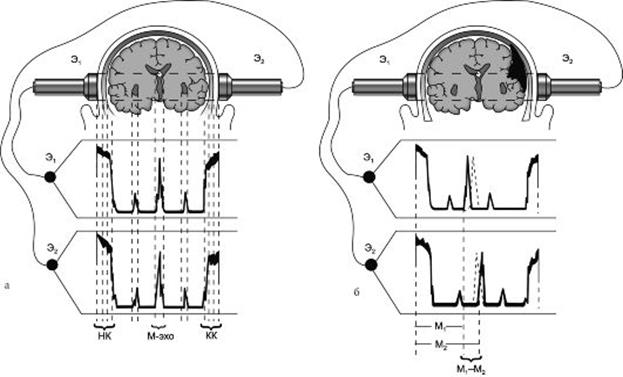
Рис. 79. Эхо-энцефалоскопия в норме (слева) и при патологии (справа)
При исследовании на стороне гематомы можно увидеть расширение и «зазубренность» начального комплекса (сигнал, отраженный от гематомы).
При обследовании пациента с ЧМТ необходимо соблюдать следующий протокол.
1.Тщательный сбор анамнеза. Если больной находится в оглушении II или без сознания, то врач приемного покоя получает анамнестические сведения от службы скорой помощи или сопровождающих родственников.
2. Осмотр пострадавшего, при котором необходимо обращать внимание на все 4 описанных выше синдрома. Клинический осмотр при приеме больного имеет главенствующее значение, так как, именно, он определяет дальнейшую тактику обследования и ведения пострадавшего.
3.Обязательное проведение краниографии в двух проекциях. По показаниям проводится дополнительное рентгеновское обследование (рентгенография костей носа, скуловых костей, рентгенография органов грудной клетки и т.д.).
4.Если определены показания к ЛП, то перед ней пациенту необходимо произвести эхо-энцефалоскопию.
5.ЛП – по показаниям.
6.Все наши диагностические сомнения разрешает КТ. В нейротравматологии предпочтение отдается именно этому методу нейровизуализации. Для этого имеется ряд причин. Метод позволяет оценить как состояние внутричерепного содержимого, так и, в отличие от МРТ, костные изменения. При МРТ необходима длительная экспозиция (до 30 минут), когда больной должен находиться в полностью обездвиженном состоянии. КТ позволяет пошагово прерывать исследование на каждом скане. Мультиспиральная КТ проводится всего за 1 минуту.
Хирургическое лечение ЧМТ.
Показанием к оперативному лечению являются все случаи компрессии головного мозга. В подавляющем большинстве случаев операции проводятся по жизненным показаниям. Если пациент поступает с признаками текущей дислокации ствола головного мозга, то темп подготовки к операции приравнивается к таковому при профузном внутреннем кровотечении. Оперативное вмешательство при дислокации ствола головного мозга приравнивается к реанимационному пособию. Противопоказанием к операции является терминальное состояние больного (кома III). Операция преследует три цели: 1- декомпрессия, 2- тщательный гемостаз, 3- создание условий для профилактики возможной дислокации ствола головного мозга.
1. Декомпрессия подразумевает удаление гематомы или хирургическую обработку вдавленного перелома (рис. 80).
При открытых вдавленных переломах костей черепа иссекаются края инфицированной раны. Скелетируется зона вдавленного перелома и участки кости окружающие его. Рядом с зоной перелома накладывают фрезевое отверстие, через которое кусачками резецируют отломки. Вскрывается ТМО и проводится хирургическая обработка подлежащего очага размозжения. На рисунке показано удаление с помощью аспиратора сгустков крови и орошение зоны операции раствором фурацилина из резиновой груши.
При интракраниальных гематомах проводится резекционная трепанация черепа (РДТЧ) (рис. 81). При гематомах, имеющих объем менее 65 см3 ,оперативное лечение не показано, и такие гематомы подлежат консервативному лечению в условиях КТ-мониторинга состояния внутричерепного содержимого. При консервативном ведении таких больных в случае их стабильного состояния КТ производится с частотой 1 раз в 2 дня. Понятие РДТЧ подразумевает под собой то, что кость по окончании операции не ставится на место, а ТМО после ее вскрытия не ушивается. Кость – абсолютно ригидное образование, ТМО же обладает весьма ограниченными эластическими свойствами. После операции мозг остается прикрытым лоскутом (лоскутами) вскрытой ТМО, надкостницей, височной мышцей и кожей. Это эластичные ткани, способные к растяжению, и в первые семь суток (на вершине травматического отека) мозг выбухает (пролабирует) в трепанационный дефект. Таким образом, при РДТЧ происходит перераспределение коэффициента внутричерепного давления (КВЧД) в сторону трепанационного дефекта, в то время как при герметичном черепе КВЧД направлен вниз, в сторону естественных отверстий черепа. Если мозг пролабирует в трепанационный дефект, то он может ущемляться в нем и травмироваться о его края.
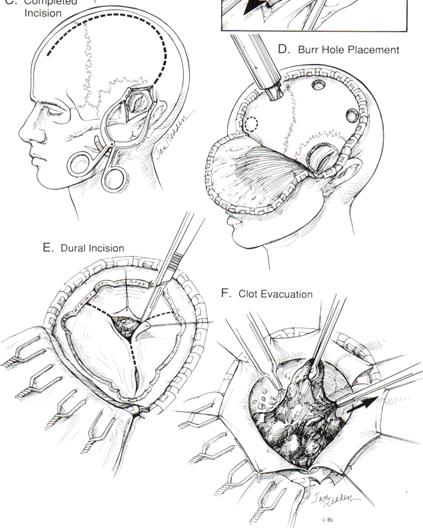
Рис. 81. Этапы трепанации черепа при острой субдуральной гематоме
Для того чтобы устранить эти отягощающие обстоятельства, в нейрохирургии приняты правила формирования трепанационного дефекта, которые следует неукоснительно соблюдать (рис. 82). Трепанационный дефект должен быть широким. Минимальные его размеры 10х12 см. В данном случае нейрохирург должен руководствоваться мудрым афоризмом: «Не жалей череп, но жалей больного». Так как височная кость очень тонкая, то ее край при выбухании мозга в трепанационный дефект может оказывать режущее действия на мозговую ткань, поэтому височная кость резецируется до основания СЧЯ.
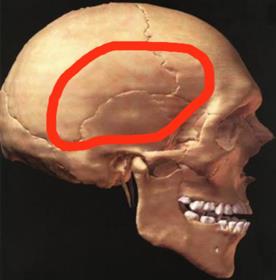
Рис. 82. Требования к формированию трепанационного дефекта при ЧМТ.
Ситуация неправильного оперативного пособия при ЧМТ приведена на рисунке 83.
В данном секционном случае трепанационный дефект расположен в теменной кости и имеет небольшие размеры. Во-первых, хирург не смог полностью удалить субдуральную гематому, вследствие ограниченного интраоперационного визуального контроля. Во-вторых, мозг ущемился в трепанационном дефекте. Зона ущемления – это область центральных извилин. Таким образом, если допустить, что пациент выжил бы, то у него была бы грубейшая неврологическая симптоматика в виде левостороннего гемипареза, чего можно было бы избежать при правильной технике оперативного вмешательства.
Трепанация относится к методам наружной декомпрессии. Существуют также методы внутренней декомпрессии, позволяющие эффективно уменьшать объем внутричерепного содержимого. В первую очередь к ним относится наружное вентрикулярное дренирование по Арендту (наружная вентрикулостомия) (рис. 84).
В передний рог бокового желудочка через фрезевое отверстие вводится дренаж, который выводится на поверхность кожи через подкожный туннель в точке, отстоящей от фрезевого отверстия на 5 – 7 см кзади. По дренажу ликвор оттекает в стерильный резервуар. Общее содержание ликвора в ликвросодержаших пространствах 120 – 150 мл. Ликвор находится в постоянном движении. Он постоянно вырабатывается в хориоидальных сплетениях желудочков (см. стр. 57) головного мозга и всасывается в пахионовых грануляциях (рис. 85).
Пахионовы грануляции это гроздьевидные отростки паутинной оболочки, открывающиеся в субарахноидальные пространства, расположенные по краям сагиттального синуса, и вдающиеся в него, а также в кости черепа. Через них ликвор поступает в венозную кровь. За сутки у больного находящегося в коме ликвор трижды меняет свой состав. Следовательно, при этих условиях в сутки образуется 400 – 450 мл ликвора. Значит, суточный объем декомпрессии составляет 450 см3 . Это большое подспорье при ведении больного. Кроме того наличие вентрикулярного дренажа позволяет проводить контроль внутричерепного давления, коррегируя терапию в зависимости от его колебаний. Следующая мера внутренней декомпрессии – это положение Фовлера (рис. 86), при котором больной полусидит в постели. В этом положении оптимизируется отток ликвора и венозной крови из полости черепа. С той же самой целью при тяжелой ЧМТ больной ведется в лечебном наркозе в режиме полной синхронизации с аппаратом ИВЛ. Больной не должен реагировать на интубационную трубку. Если пациент находится в коме в течение двух дней и выход из комы не предвидится, то ему накладывают трахеостому, через которую осуществляется ИВЛ и проводится бронхоскопическая санация трахеобронхиального дерева.
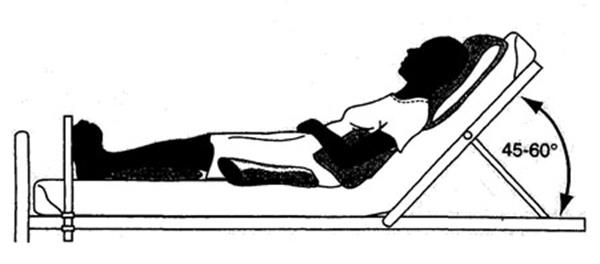
Рис. 86. Положение Фовлера
Стопы больного должны быть с помощью специальной подставки фиксированы в положении тыльного сгибания во избежание образования разгибательных контрактур, которые развиваются у всех больных, длительно находящихся в коме. Постель, в которой находится такой пациент, должна быть оборудована противопролежневым матрасом. Максимальная длительность комы при тяжелой ЧМТ составляет 4 – 5 недель, по прошествии которых больной выходит в сознание или в вегетативное состояние. При вегетативном состоянии стабилизируются витальные функции и восстанавливается цикл сна – бодрствования. В период бодрствования пациент лежит с открытыми глазами. Период сна характеризуется закрытыми глазами. Контакт с окружающим отсутствует. Когнитивные функции сведены к нулю. Больные получают зондовое питание и нуждаются во всестороннем уходе.
Тяжелая травма головного мозга является толчком к развитию травматической болезни головного мозга, в течение которой выделяют 5 периодов:
Острейший – до 2 недель
Острый – до 2 месяцев
Промежуточный – до 6 месяцев
Отдаленный – до 2 лет
Резидуальный (период остаточных явлений) – свыше 2 лет.
Существует шкала исходов тяжелой ЧМТ (рис. 87).

Рис. 87. Шкала исходов ЧМТ Глазго
Хирургическое лечение ЧМТ не ограничивается острым периодом. Так как больным проводится РДТЧ, то неминуемо встает вопрос о проведении краниопластики (закрытие дефекта черепа). При наличии дефекта костей черепа у больных развивается синдром трепанированных. Его клиническая картина определяется метеозависимыми головными болями, болезненностью краев трепанационного дефекта при пальпации и метеотропными колебаниями неврологической симптоматики. Краниопластика проводится по лечебным (синдром трепанированных), косметическим (рис. 88) и профилактическим показаниям. Относительно профилактических показаний необходимо сказать следующее – при наличии трепанационного дефекта даже незначительная травма в зоне трепанационного дефекта может оказаться фатальной.
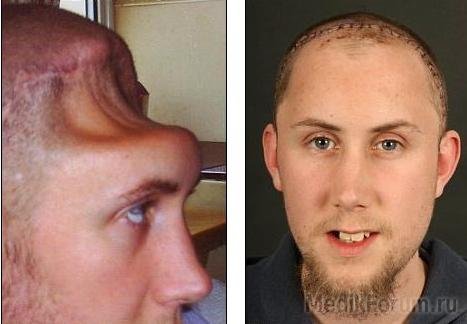
Рис.88. Трепанационный дефект после бифронтальной трепанации черепа. Слева – до, справа – после краниопластики
Различают первичную, первично отсроченную и вторичную краниопластику. Первичная краниопластика проводится, как правило, при хирургической обработке вдавленных депрессионных переломов костей черепа (см. стр. 91, рис. 69). Первично отсроченная краниопластика проводится до 1 месяца после трепанации черепа. Ее проведение возможно у больных, которые быстро и хорошо компенсировались после ЧМТ. Чаще всего это больные, имеющие не больших размеров гематомы и поступающие в стационар в сознании. Наиболее часто проводится вторичная краниопластика через 2 и более месяцев после трепанации черепа (промежуточный период травматической болезни головного мозга).
В зависимости от материалов, применяемых для краниопластики, различают аутокраниопластику и аллокраниопластику. При аутокраниопдастике трепанационный дефект закрывается собственной костью больного. Для этого удаленный костный лоскут подвергается консервации. Консервацию проводят в антисептических растворах (формалин) или в условиях глубокой заморозки (- 70∘). Однако при такой консервации костный лоскут приобретает антигенные свойства и может отторгнуться. Предпочтение отдается консервации костного лоскута в собственных тканях организма. По окончанию трепанации костный лоскут имплантируют под коду живота или бедра. При аллокраниопластике (в случае, когда в силу тех или иных причин костный лоскут не удается сохранить) используются чужеродные материалы. Раньше использовались быстротвердеющие пластмассы – аналоги применяющихся в стоматологии (протокрил, костный цемент). В настоящее время предпочтение отдается пластике титановой сеткой (рис. 89).
Заключение.
В настоящее время послеоперационная летальность при тяжелой ЧМТ достигает 40 – 50%. Однако по некоторым экспертным оценкам она может быть снижена до 18 – 20%. Для этого необходимо соблюдать простейшие правила. Одним из таких правил является обязательная 100%-ная госпитализация всех больных, даже казалось бы с легкой ЧМТ, в стационар. Помимо медицинских мероприятий, направленных на соблюдение этого принципа, большую роль должна играть и просветительная работа среди населения.
СПИСОК ПРИНЯТЫХ СОКРАЩЕНИЙ (в порядке цитирования)
ЧМТ – черепно-мозговая травма
ЗЧМТ – закрытая черепно-мозговая травма
ОЧМТ – открытая черепно-мозговая травма
СГМ – сотрясение головного мозга
УГМ – ушиб головного мозга
СЧЯ – средняя черепная ямка
ПЧЯ – передняя черепная ямка
ВЧГ – внутричерепная гипертензия
ОВЧС – объем внутричерепного содержимого
ТМО – твердая мозговая оболочка
ШКГ – шкала комы Глазго
САД – системное артериальное давление
ЦПД – церебральное перфузионное давление
ВЧД – внутричерепное давление
САК – субарахноидальное кровоизлияние
ОР – очаг размозжения
ДАП – диффузное аксональное поражение головного мозга
ДТП – дорожно-транспортное происшествие
ЭДГ – эпидуральная гематома
КТ – компьютерная томография
СДГ – субдуральная гематома
ВМГ – внутримозговая гематома
СОВЧС – совокупный объем внутричерепного содержимого
ЛП – люмбальная пункция
СМК – спинномозговой канал
ЭЭС – эхо-энцефалоскопия
МРТ – магнитно- резонансная томография
УЗ – ультразвук
НК – начальный комплекс
КК – конечный комплекс
М-эхо – срединный комплекс
РДТЧ – резекционно-декомпрессивная трепанация черепа
КВЧД – коэффициент внутричерепного давления
ИВЛ – искусственная вентиляция легких
Дидактический материал.
Тестовые задания.
СОДЕРЖАНИЕ
1. Предисловие………………………………………………………………5
2. Краткая история…………………………………………………………….6
3. Черепно-мозговая травма………………………………………………33
- Эпидемиология ЧМТ…………………………………………………..33
- Классификация ЧМТ……………………………………………………35
4. Основные клинические синдромы при нейрохирургической
патологии…………………………………………………………………40
- Синдром ВЧГ……………………………………………………………40
- Нарушение сознания……………………………………………………42
- Эпилептический синдром………………………………………………51
- Очаговый неврологический синдром…………………………………54
- Менингеальный синдром………………………………………………61
- Травматическое субарахноидальное кровоизлияние…………………63
- Гипертензионно-дислокационный синдром…………………………66
5. Клиническая характеристика поражений головного мозга
при ЧМТ…………………………………………………………………73
- Сотрясение головного мозга……………………………………………74
- Ушиб головного мозга легкой степени………………………………74
- Ушиб головного мозга средней степени………………………………76
- Ушиб головного мозга тяжелой степени………………………………78
- Сдавление головного мозга……………………………………………80
· Эпидуральная гематома……………………………………………81
· Субдуральная гематома……………………………………………83
· Внутримозговая гематома…………………………………………86
· «Светлый промежуток»……………………………………………89
6. Построение нейрохирургического диагноза……………………………92
- Классификация переломов черепа……………………………………94
- Формулировка диагноза………………………………………………101
- Переломы основания черепа…………………………………………..102
7. Дополнительные методы исследования……………………………….104
- Люмбальная пункция…………………………………………………104
- ЭХО-энцефалоскопия (ЭЭС)…………………………………………105
- Протокол обследования пациента с ЧМТ……………………………108
8. Хирургическое лечение ЧМТ…………………………………………109
- Шкала исходов ЧМТ…………………………………………………116
9. Заключение………………………………………………………………119
10. Список принятых сокращений…………………………………………119
11. Дидактический материал………………………………………………121
12. Список рекомендуемой литературы………………………………….125
ПРЕДИСЛОВИЕ
Вопрос о необходимости преподавания нейрохирургии в медицинских институтах поставил еще в 1937 г. академик Н. Н. Бурденко. Молодые врачи различных специальностей после окончания института должны быть знакомы с основами диагностики и лечения повреждений и заболеваний нервной системы, требующих своевременного распознавания, а иногда и неотложной нейрохирургической помощи. Нейрохирургия, как предмет преподавания в медицинских вузах СССР, был включен в учебную программу с 1972 года. Первое издание учебника «Нейрохирургия», написанного профессором И.М.Иргером, вышло в 1971 году, учебник был переиздан в 1982 году. В течение многих лет он оставался единственным учебным пособием по нейрохирургии для студентов в нашей стране. Многие современные нейрохирурги начали свой путь в нейрохирургию со знакомства с ним. Неплохо зарекомендовал себя учебник «Основы нейрохирургии» венгерского профессора Э. Пастора, переведенный на русский язык в 1985 году. Следующий учебник «Нейрохирургия» для студентов медицинских вузов, написанный С.В. Можаевым, А.А. Скоромцом, Т.А. Скоромцом был издан в 2001 г. В нем были обобщены достижения нейрохирургии и смежных наук за последние два десятилетия ХХ века.
Процесс преподавания нейрохирургии в нашем Университете совершенствуется и существенно изменился за последние 10 лет, возникла необходимость публикации нового учебного пособия по нейрохирургии. В данном пособии освещены основные разделы нейрохирургии, приводятся базовые аспекты предмета, необходимые студенческой аудитории. При его составлении мы следовали мудрому принципу Аристотеля «docendo discimus» (обучая, мы обучаемся сами).
КРАТКАЯ ИСТОРИЯ НЕЙРОХИРУРГИИ
Выделение нейрохирургии в отдельную медицинскую специальность произошло на рубеже XIX и XX веков, но корни ее уходят в глубокую древность. Так, в оставшемся от цивилизации инков Перуанском некрополе примерно 10% черепов имеют следы трепанации, причем характер костных изменений указывает на то, что большинство больных успешно переносили операцию (рис. 1).

Рисунок 1. На рисунке видны черепа из Перуанского некрополя по краям трепанационного отверстия имеются признаки неоостеогенеза, как свидетельство того, что человек, перенесший трепанацию долго жил после нее. На нижнем правом изображении видно, что для проведения трепанации уже использовались специальные инструменты (трепаны)
Около 1/3 трепанаций выполнялось по поводу черепно-мозговых повреждений. Показания к трепанации черепа в остальных 2/3 случаев остаются неясными и возможно имеют культовый характер. Трепанация производилась путем выскабливания кости, а также с помощью долот, кусачек и конических фрез. Инки осуществляли и пластику костных дефектов золотыми или серебряными пластинами.
Во времена Гиппократа — V — IV века до нашей эры трепанация черепа принадлежала к числу обычных операций. Проводилась она исключительно при проникающих травмах, сопровождающихся переломами костей черепа. Операция проводилась с использованием специального трепана. Уже имелись два вида трепанов: корончатый и буравящий. Перу Гиппократа принадлежит труд «О ранах головы», где он излагает современные ему сведения о строении черепа. Там же описаны линейные и оскольчатые переломы костей черепа, дается описание закрытых и открытых переломов. Подробным образом описаны вдавленные оскольчатые переломы и хирургическая тактика их лечения.
В средние века методика трепанации существенных изменений не претерпела (рис.2). Производились трепанации и на Руси.

Рисунок 2. Картина средневекового художника Яна ван Хенессена «Извлечение камней глупости».
Первое чисто нейрохирургическое руководство («Tractatus de Fractura Calvae sive Cranei a Carpo editus») опубликовано в 1518 г. в Болонье Беренгарио да Капри (Berengario da Capri, 1470-1550) - рис. 3. Работа посвящена в первую очередь описанию успешного лечения автором перелома затылочной кости у Лоренцо де Медичи, но в ней даны и обобщающие рекомендации.
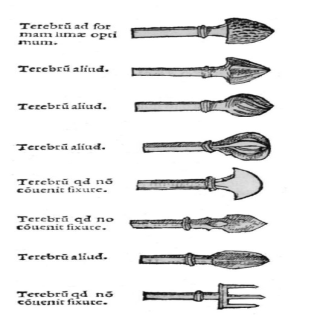
Рисунок 3. Средневековые инструменты для трепанации черепа (из трактата Беренгарио да Капри)
Большой вклад в развитие техники трепанации внес Амбруаз Паре, который подробно описал инструментарий и методику трепанации, удаления остеомиелитически измененной кости, дренирования субдуральных гематом и эмпием, предложил методику репозиции вдавленных переломов черепа. Развитие нейроанатомии в XVII веке связано в первую очередь с именем Т. Виллизия. (Опубликованная им в Лондоне в 1664 г. «Мозговая анатомия» («Cerebri Anatomie», рис. 4) явилась наиболее точным для своего времени руководством. Виллизий также первым предложил термин «неврология», понимая его в чисто анатомическом смысле, т.е. как науку о нервной системе (а не как клиническую дисциплину).
К началу XVIII века в европейских странах произошел переход от кустарного изготовления медицинских инструментов к промышленному. В России также было налажено изготовление медицинских инструментов, и с 1738 г. все штатные врачи, в том числе военные, имели полноценные (для своего времени) хирургические наборы, включая инструменты для трепанации. В 1744 г. Мартын Шеин издал первый русский анатомический атлас. Трепанация черепа в России традиционно применялась в это время при черепно-мозговых травмах (ЧМТ), владеть ее техникой был обязан каждый дипломированный врач. Среди экзаменационных вопросов по хирургии трепанации черепа уделялось далеко не второстепенное значение.
Вторая половина XVIII века характеризуется дальнейшим прогрессом медицинской науки и практики. Концепция патологической анатомии Дж. Морганьи (Giovanni Battista Morgagni,) (рис.5), связывающая каждую нозологию со специфическим патологическим субстратом, изменила философию всей европейской медицины и в том числе обосновала целесообразность удаления опухоли любой локализации.
Первое дошедшее до нас описание нейроонкологического вмешательства, было произведено в 1743 г. Lorenz Heister (1683-1758). Лечебное пособие заключалось в аппликации негашеной извести, опухоль (с мягкими тканями, прилежащей костью и твердой мозговой оболочкой) лизировалась, больной вскоре скончался от инфекции. Вообще, первые нейроонкологические операции в истории медицины были выполнены по поводу гиперостотических (вызывающих локальное утолщение кости) или разрушающих кость опухолей свода черепа (рис. 6). Связано это с относительной простотой прижизненной диагностики таких новообразований.
Этот опыт был обобщен в 1773 г. выдающимся французским хирургом Антуаном Луи (Antoine Louis, 1723-1792, рис. 7) в руководстве «Memoire sur les Tumeurs Fongeuses de la Dure-mere», основанном на 20 случаях, первые из которых датированы серединой XVI века, но в основном операции были произведены либо автором, либо его современниками. Однако, несмотря на отдельные исключения, показатели летальности при нейрохирургических вмешательствах были катастрофическими.
В 1807-1808 гг. в Санкт-Петербурге было издано оригинальное «Руководство к преподаванию хирургии» И.Ф. Буша (рис. 8). В разделе «О повреждениях черепа» автор рекомендовал производить рассечение раны мягких тканей с удалением мелких свободно лежащих костных фрагментов, инородных тел и сгустков крови; крупные костные фрагменты рекомендовалось репонировать, обнаруженным внутричерепным кровоизлияниям «давать выход».
Опубликованное в 1840 г. «Руководство к оперативной хирургии» академика Христиана Саломона (Саломон Х.Х., 1797-1851) явилось квинтэссенцией опыта отечественной хирургии до Пирогова. В отношении повреждений черепа и мозга Саломон придерживался в основном взглядов Буша. Примечательно, что в этом руководстве впервые содержалась рекомендация применять пчелиный воск для гемостаза при кровотечении из кости во время трепанации.
Опыт российской хирургии середины XIX века нашел отражение в «Началах общей военно-полевой хирургии» Н.И. Пирогова, опубликованных в Дрездене в 1865-1866 гг. Николай Иванович Пирогов (1810- 1881, рис. 9) представил комплексный анализ морфологических изменений и патофизиологических и саногенетических механизмов, сопровождающих черепномозговые повреждения. Всего он произвел около 20 трепанаций как в остром, так и в отдаленном периоде черепно-мозговых повреждений. Статистика исходов неясна. Особое значение для развития нейрохирургии сыграл ранний (1851-1854) труд Н.И. Пирогова - известный «ледяной» атлас, заложивший основы топографической анатомии. Опубликованные в 1-й части атласа (1851) рисунки распилов головы поражают точностью и напоминают современные компьютерные томограммы.
Несмотря на созданную к середине XIX века анатомическую и техническую базу, наличие некоторого клинического опыта, развитие нейрохирургии и хирургии вообще тормозилось из-за гнойных осложнений. Действительно, в хирургической практике появилась общая анестезия (в 1844 г. Horace Wells, предложил закись азота; в 1846 г. химик W.T.O. Morton, и хирург J.C. Warren, применили эфир; J.Y. Simpson, в 1847 г. - хлороформ), что позволило удлинить время операции и лучше ориентироваться в ране. Однако вскрытие твердой мозговой оболочки оставалось шагом, влекущим за собой катастрофические последствия в виде инфекционных осложнений. Лондонский хирург Ч. Балланс (Sir Charles Ballance, рис.10), в 1894 г. диагностировавший и успешно удаливший невриному слухового нерва, в своей лекции 1933 года охарактеризовал ситуацию 70-х годов XIX века как «паралич хирургии ... в связи с нагноением, целлюлитом, рожистым воспалением, септицемией, пиемией, острой травматической гангреной и столбняком - болезнями, для которых не существовало средств профилактики и лечения». Показательные операции производились в аудитории на несколько сотен человек. «Хирург оперировал в сюртуке, который ... хранился в операционном театре. Он был перепачкан кровью и гноем от прошлых операций. Инструменты лежали на подносе, покрытом зеленым сукном. Когда требовалась лигатура, служитель театра натягивал ее левой рукой, держа другой конец в зубах, натирал воском и передавал хирургу».
В 1843 г. Оливер Холмс и в 1861 г. Игнац Земмельвейс показали, что «родильная горячка» переносилась грязными руками акушеров, и простое мытье рук до и после каждого исследования значительно уменьшало частоту этой патологии. Тем не менее, разработанная Л. Пастером и Р. Кохом концепция бактериальной природы гнойных осложнений воспринималась хирургами как интересная теория, о практическом применении которой речи не шло до разработки Дж. Листером теории и практики антисептики. Вскоре антисептика стала дополняться элементами асептики; в частности, стали применять автоклавирование части хирургических материалов, мыть руки хирурга и кожу больного щетками, использовать предложенные Холстедом резиновые перчатки и т.д. Внедрение в практику асептики в полном объеме связано с именем Кохера (рис. 11), чья хирургическая клиника в Берне стала ведущим центром разработки и внедрения этой кажущейся сегодня совершенно естественной технологии. На учебу к Кохеру приезжали врачи из многих стран, в том числе и Кушинг - впоследствии выдающийся нейрохирург. Внедрив асептику и ряд общехирургических операций, Кохер, кроме того, усовершенствовал технику трепанации черепа, методы лечения повреждений позвоночника, предложил оригинальную операцию при эпилепсии. Внедрение асептики и антисептики в России произошло очень быстро, и с начала 80-х годов XIX века эта техника уже применялась рутинно не только в большинстве крупных клиник, но и в земских больницах.
Как без анестезии и асептики, развитие нейрохирургии было невозможным и без топической диагностики. До начала второй половины XIX века господствовала концепция функционирования мозга как единого целого. Только после опубликованных в 1861 г. работ П. Брока (Paul Broca,) в 1870 г. и в 1874 г. К. Верникe (Carl Wernicke) утвердилась концепция локализации функций в определенных отделах мозга. Пожалуй, первая в истории медицины операция удаления диагностированной по клиническим проявлениям менингиомы без конвекситального гиперостоза была произведена в 1884 г. итальянским врачом Ф. Дуранте (Francesco Durante). Больная выжила и вновь успешно была через 11 лет оперирована по поводу продолженного роста опухоли. Возможность постановки топического диагноза, точность которого значительно возросла с появлением работ В.М. Бехтерева, поставила не менее актуальную и сегодня задачу выбора оптимального хирургического доступа к выявленному объемному образованию. Однако отсутствие каких-либо нейровизуализационных методик делало ее крайне сложной.
Оригинальное решение задачи проекции очага на поверхность черепа принадлежит Д.Н. Зернову, который в 1889 г. предложил для определения на черепе проекции различных частей мозга прибор, названный энцефалометром. Прибор фиксировался в стандартных точках, практически параллельно орбитомеатальной линии (соединяет верхний край глазницы и наружное слуховое отверстие), и обеспечивал сопоставление всех измерений с атласом (рис. 12).

Рисунок 12. Дмитрий Николаевич Зернов (1834-1917) (а) и его энцефалометр (б) (1889) - прообраз нейронавигации и стереотаксиса
До последних десятилетий XIX века все трепанации в мире были резекционными. В 1873 г. Ю. Космовский показал возможность успешного приживления свободного костного лоскута. Немецкий хирург В. Вагнер (Wilhelm Wagner) в 1889 г. предложил сохранять «ножку» из надкостницы и височной мышцы, обеспечивающую питание костного лоскута, и эта техника на многие годы стала классической. Технически выполнение костно-пластической трепанации черепа до конца XIX века было сложным. Основными инструментами оставались долото и молоток. В 1891 г. профессор Ж. Туасон (Jean Toison) из Лилля (Франция) использовал цепную пилу для соединения фрезевых отверстий для выкраивания костного лоскута. Пила была довольно грубой и широкого применения не получила. Леонардо Джигли (Leonardo Gigli), акушер из Флоренции, предложил в 1894 г. проволочную пилу для симфизотомии при родах. Как и сейчас, пилы Джигли были одноразовыми. Профессор А. Обалинский (Alfred Obalinski) из Краковского университета вскоре применил пилу Джигли для трепанации.
Большой вклад в развитие нейрохирургии внес В. Горслей (Sir Victor A.H. Horsley). Горслей разработал методику стереотаксических вмешательств (рис. 13), различные варианты операций и впервые удалил опухоль спинного мозга.


Рисунок 13. а - Горслей (Sir Victor A.H. Horsley, 1857-1916); б - стереотаксический аппарат Горслея и Кларка (1908)
Приоритет выделения нейрохирургии в отдельную специальность принадлежит России. Впервые необходимость выделения нейрохирургии в самостоятельную специальность обосновал профессор Казанского университета Л.А. Малиновский. В феврале 1893 г. в докладе «К вопросу о хирургическом лечении болезней центральной нервной системы», прочитанном на заседании Общества невропатологов и психиатров при Казанском университете, Малиновский четко сформулировал основные принципы нейрохирургии и поставил вопрос о специальной подготовке хирурга, оперирующего на ЦНС.
Практически это положение было реализовано В.М. Бехтеревым (рис. 14), по инициативе которого в 1897 г. была открыта Нервная клиника Императорской военно-медицинской академии, впервые в мире включавшая в свою структуру операционную и «обособленное помещение для оперируемых» (нейрохирургические палаты). Ученик В.М. Бехтерева Людвиг Мартинович Пуссеп - первый в мире нейрохирург - внес большой вклад в становление нейрохирургии как самостоятельной специальности.
Однако дальнейшее развитие нейрохирургии сдерживалось отсутствием объективных диагностических методов, что вело к большому числу ошибок. Открытие 8 ноября 1895 г. В.К. Рентгеном (рис. 14) Х-лучей принципиально изменило возможности прижизненной диагностики различных заболеваний, включая патологические процессы в полости черепа.
Большой вклад в развитие нейрохирургической техники внес Тьери де Мартель (Thierry de Martel, рис. 16). Основными его изобретениями являются предложенные в 1908 г. применяемый доныне металлический проводник для пилы Джигли и электрический трепан, самоудерживающийся ретрактор, специальный хирургический стол для операций в сидячем положении и соответствующее кресло для хирурга. Также де Мартель впервые применил кинодокументацию операций и одним из первых - интраоперационную фотографию.
Его современник, выдающийся немецкий нейрохирург и невролог О. Фёрстер (Otfrid Foerster, рис. 17), разработал технику интраоперационной электростимуляции моторной коры и электрокортикографии - методов, значительно улучшающих функциональные результаты операций. Также им впервые описаны дерматомы, составлена карта моторной коры головного мозга, предложен гипервентиляционный тест для выявления судорожной активности по электроэнцефалограмме при эпилепсии, разработаны операции при спастичности и болевых синдромах.
Одним из основоположников мировой нейрохирургии признан американский нейрохирург Х. Кушинг (Harvey William Cushing, рис. 19). Его работы по лечению опухолей гипофиза (1912), мостомозжечкового угла (1917) и внутричерепных менингиом (1938) стали классическими для современных нейрохирургов. Предложенные Х. Кушингом вакуумный аспиратор, промывание раны в ходе операции физиологическим раствором, ватные полоски для защиты мозга и многие другие инновации и сегодня используются в ходе нейрохирургических вмешательств.
Многим обязана современная нейрохирургия и другому американскому нейрохирургу - У. Денди (Walter E. Dandy, рис. 20). Он учился у Кушинга, затем стал работать самостоятельно и добился блестящих результатов, в первую очередь в плане радикальности нейроонкологических вмешательств. Он впервые разработал и реализовал концепцию палаты пробуждения, оснащенной соответствующей аппаратурой и постоянным сестринским постом. Не менее важным вкладом Денди в нейрохирургию, явилась разработка таких диагностических методов, как пневмовентрикулография (1918) и пневмоэнцефалография с интравентрикулярным и эндолюмбальным введением воздуха (1919). Эти методы кардинально изменили ситуацию с диагностикой различных поражений мозга. Денди впервые в мире клипировавший церебральную аневризму, является также основателем сосудистой нейрохирургии,
Следующим революционным изобретением в нейрохирургии явилась разработанная в 1927-1934 гг. Э. Монишем (рис. 21) методика церебральной ангиографии, обеспечившая возможность точной диагностики и дифференцированного лечения поражений сосудов мозга. Основываясь на данных церебральной ангиографии, У. Денди в 1936 г. впервые осуществил клипирование внутричерепной артериальной аневризмы. К слову, Э.Мониш предложил и разработал такую методику лечения психических заболеваний, как лоботомия, за что был удостоен Нобелевской премии.
Важным этапом развития нейрохирургии в России стало создание А.Л. Поленовым (рис. 22) в 1917 г. в Петрограде Физико-хирургического института, преобразованного в 1924 г. в Государственный травматологический институт с нейрохирургическим отделением.
Благодаря усилиям ученика Л.М. Пуссепа А.Г. Молоткова (рис. 23), в 1925 г. был основан Институт хирургической невропатологии, после слияния которого с нейрохирургическим отделением Травматологического института в 1938 г. был создан Российский нейрохирургический институт, носящий в настоящее время имя А.Л. Поленова.
Особое значение для отечественной нейрохирургии имело создание Н.Н. Бурденко (рис. 24) в 1924 г. на базе Клиники факультетской хирургии 1-го Московского медицинского института нейрохирургических палат. Верно оценив перспективы новой специальности и подготовив группу специалистов, в 1929 г. Н.Н. Бурденко с В.В. Крамером на базе Государственного рентгеновского института организовали нейрохирургическую клинику, превратившуюся в 1932 г. в Центральный нейрохирургический научно-исследовательский институт (ныне - Научно-исследовательский институт нейрохирургии им. акад.Н.Н. Бурденко РАМН).
Сложившаяся в Советском Союзе система оказания нейрохирургической помощи обеспечила возможность планирования научных исследований, организацию обучения и стандартизацию лечебно-диагностических мероприятий в масштабах всей огромной страны. Для этой цели при Центральном нейрохирургическом институте был создан Нейрохирургический совет, на основе которого возникло Общество нейрохирургов СССР и затем - России. В 1937 г. усилиями Н.Н. Бурденко был создан первый нейрохирургический журнал «Вопросы нейрохирургии», который в настоящее время носит его имя.
Радикально изменило нейрохирургию предложение В. Хауз (W.F. House) использовать для операций на мозге микроскоп и специальный микрохирургический инструментарий (1963). Практически одновременно операционный микроскоп стали использовать W. Lougheed, Th. Kurze, R. Rand, J. Jacobson, M.G. Yasargil и другие нейрохирурги. Существенную роль сыграло предложение Л. Малис (L.I. Malis) использовать для остановки кровотечения биполярную коагуляцию.
Прорыв в сосудистой хирургии связан с изобретением в 1971 г. Ф.А. Сербиненко (рис. 25) отделяемого баллон-катетера. Технология эндовазальных (эндоваскулярных) вмешательств успешно совершенствуется и все шире используется для лечения целого ряда сосудистых заболеваний ЦНС, включая такие опасные, как артериальные аневризмы и артериовенозные мальформации.
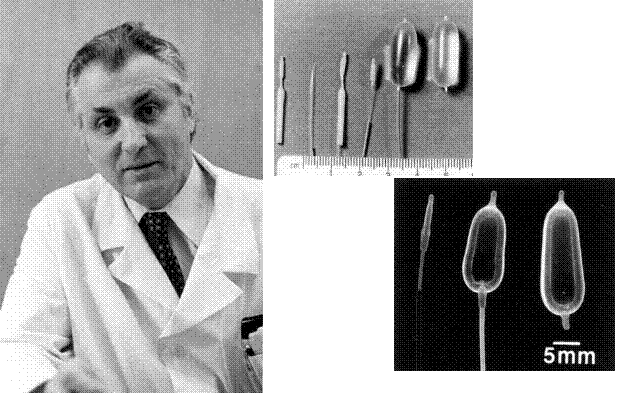
Рис.25. Акад. Ф.А. Сербиненко (1928-2002) – основатель эндоваскулярной нейрохирургии
Важными направлениями современной нейрохирургии являются стереотаксические вмешательства. Стереотаксическая нейрохирургия использует пространственные расчеты, совмещая ориентиры, имеющиеся на аппарате с внутричерепными ориентирами, и позволяет с большой точностью вводить в заданные участки мозга специальные инструменты - биопсийные канюли, электроды для деструкции или стимуляции и пр. Для выполнения таких операций применяются специальные стереотаксические аппараты (рис. 26). В состав аппарата входит фиксируемая на голове больного рама, одним из прототипов которых считается предложенный Д.И. Зерновым энцефалометр. Стереотаксический метод с успехом стал применяться для лечения паркинсонизма, других гиперкинезов и нарушений тонуса мышц, тяжелых болевых синдромов, глубинно расположенных опухолей. Большой вклад в развитие стереотаксической нейрохирургии в Советском Союзе внес профессор Э.И. Кандель.
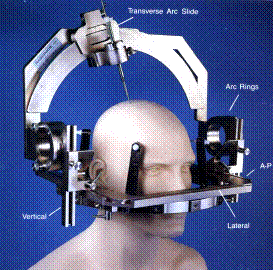

А Б
Рис. 26. Стереотаксическая нейрохирургия. А – стереотаксический аппарат на голове фантома. Б – Э.И. Кандель (1923-1990).
Одновременно с взрослой нейрохирургией с середины прошлого столетия как относительно самостоятельный ее раздел стала развиваться педиатрическая нейрохирургия. В нашей стране пионером педиатрической нейрохирургии был А.А. Арендт (рис. 27), возглавивший первое в СССР детское нейрохирургическое отделение.
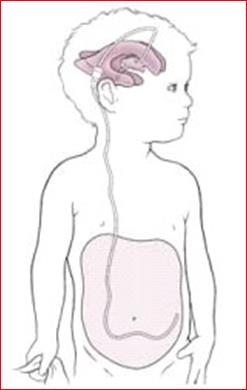
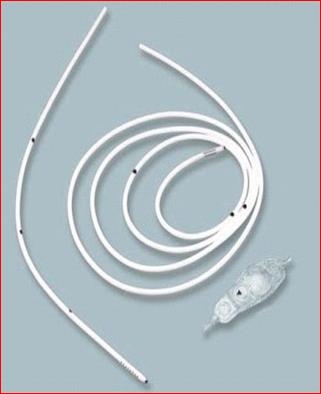
Важным для развития педиатрической нейрохирургии было предложение ряда авторов использовать для лечения гидроцефалии - распространенного в детском возрасте заболевания - клапанных шунтирующих систем, обеспечивающих отведение ликвора за пределы ЦНС (в венозную систему или в брюшную полость) (рис.28).
А Б
Рис. 28. Ликворошунтирующие операции. А – схема вентрикулоперитонеального шунтирования. Б – общий вид шунтирующей системы
Истинный «прорыв» в развитии нейрохирургии связан с появлением нейровизуализационных методик - компьютерной томографии (G. Hounsfield, 1971) (рис. 29), цифровой ангиографии и затем магнитно-резонансной томографии. Возможность визуализации патологического очага позволила применять щадящие, минимально инвазивные доступы, что существенно снизило летальность и повысило качество жизни больных после нейрохирургических вмешательств. Одновременно появилась возможность при проведении стереотаксических вмешательств опираться не на усредненные данные атласов, а воздействовать на индивидуально определенную «мишень».
Во второй половине 20 века бурно развивались стереотаксически ориентированные лучевые методики, позволяющие подвести к очагу патологического процесса высокую дозу лучевой энергии при минимальном воздействии на здоровые ткани. Этот процесс привел к созданию Ларсом Лекселлом (L. Lexell) (рис. 30) в 1951 г гамма-ножа. За его создание автору была присуждена нобелевская премия. Гамма-нож позволяет удалять небольших размеров новообразования головного мозга, не прибегая к хирургическому вмешательству. Развитие и распространение этого метода привело к созданию нового направления в нейрохирургии, которое получило название радиохирургии. В последние годы на основе гамма-ножа создан кибер-нож, отличающийся от первого тем, что в его устройстве нет необходимости жесткой фиксации головы в стереотаксической рамке.
Последние десятилетия отмечены появлением нового направления нейрохирургии. Функциональная нейрохирургия – достаточно молодое и бурно развивающееся высокотехнологичное направление нейрохирургии. В последние годы более часто это направление именуют нейромодуляцией (рис. 31). Современное определение этого направления следующее. Нейромодуляция – это терапевтическое изменение активности центральной, периферической или вегетативной нервной системы посредством электрических или фармакологических воздействий с использованием имплантируемых устройств. Минимальная инвазивность, высокая управляемость и обратимость этих воздействий на нервную систему привели к тому, что в настоящее время нейромодуляция вышла за пределы применения только в неврологии и нейрохирургии и используется в кардиологии, ангиологии, гастроэнтерологии, урологии, проктологии, андрологии и во многих других областях медицины. Наиболее часто направленных изменений функции достигают с помощью слабых импульсных электрических воздействий (электростимуляция) на различные структуры нервной системы посредством имплантируемых электродов, соединенных с программируемыми нейростимуляторами. В зависимости от патологии и цели лечения электроды имплантируются в корковые, подкорковые или стволовые структуры головного мозга, на различные уровни спинного мозга или его корешки, а также рядом с периферическими нервами. Изменяя параметры электростимуляции, можно добиться торможения, активации или других изменений функционирования нервных структур и нейрональных сетей, добиваясь тем самым желаемого клинического эффекта.

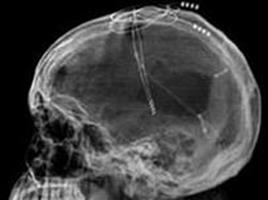
Рис. 31. Один из методов нейромодуляции - глубокая стимуляция головного мозга (электроды вживлены в глубокие структуры головного мозга и посредством проводников, находящихся под кожей соединены с вживленным под кожу нейростимулятором)
Таким образом, как мы видим, история нейрохирургии полна громкими именами. Путь ее развития от познания анатомии головного мозга, разработки хирургических доступов, усовершенствования инструментальной и технической базы до появления возможностей управления функциональным состоянием центральной и периферической нервных систем осуществляется в непрерывно восходящем направлении. Помимо вертикальной составляющей ее развития нейрохирургия развивается и в горизонтальных направлениях. Если в начале своего пути нейрохирургия была единой монолитной наукой, то в настоящее время со всей очевидностью можно говорить о множестве ее ответвлений, принимающих самодовлеющее значение. Речь идет о нейротравматологии, нейроонкологии, сосудистой нейрохирургии, функциональной нейрохирургии, радионейрохирургии и т.д. Безусловно, нейрохирург не может овладеть на высокопрофессиональном уровне знаниями и манипуляционными возможностями каждой из этих специализаций. По этой причине появились нейротравматологи, нейроонкологи, сосудистые нейрохирурги, функциональные нейрохирурги, радионейрохирурги и т.д. – профессионалы в каждом из этих направлений нейрохирургии. Как показывает практика последних десятилетий, дальнейшее развитие нейрохирургии напрямую зависит от научно-технического прогресса.
ЧЕРЕПНО-МОЗГОВАЯ ТРАВМА
Эпидемиология ЧМТ. Черепно-мозговая травма (ЧМТ) – это русскоязычный термин, который не совсем правильно отражает суть явлений. Дело в том, что повреждения черепа, в виде его переломов, встречаются только при ушибах головного мозга и то менее, чем в 50 – 60% случаев, а при сотрясении головного мозга, на долю которого приходится 80% всех ЧМТ, повреждений черепа не бывает. Наверное, правы англоязычные авторы, называя ЧМТ- «head injury» (повреждение головы). Тем не менее, в России исторически сложилась такая ситуация, что этот вид травмы характеризуют, как черепно-мозговую травму.
ЧМТ занимает первое место среди всех травм (40%) и встречается во всех возрастах, но наиболее часто в трудоспособном возрасте (15 – 44 года).
ЧМТ в 2 раза чаще встречается среди мужчин, по сравнению с женщинами, а смертность от ЧМТ среди мужчин в 3 раза выше, чем среди женщин, что свидетельствует о более тяжелом характере травмы у «сильной» части человечества. Ежегодный общий ущерб от ЧМТ в государственном масштабе по данным американских исследователей составляет до 100 миллиардов $. Для того, чтобы наглядно охарактеризовать ущерб, наносимый ЧМТ, достаточно сказать, что на эти средства можно было бы построить 7 гидроэлектростанций. Поэтому ЧМТ является не только серьезной медицинской, но и социальной проблемой.
В популяции около 250 миллионов человек (население США) ЧМТ встречается у 500.000 человек ежегодно (2:1000), а в крупных городах частота ее встречаемости возрастает до 7 случаев на 1000 населения. 50.000 (10%) погибают на догоспитальном этапе и 450.000 поступают в стационары.
То есть мы видим, что речь идет только о засвидетельствованной травме. Если учесть, что до 20% лиц, получивших легкую ЧМТ за медицинской помощью не обращаются, то количество пострадавших увеличится на 100000 человек.
Из поступивших в стационар у 80% (360.000) имеется легкая ЧМТ, у 10% (45.000) - средней тяжести и 10% (45.000) – тяжелая травма. Обшая смертность от ЧМТ составляет 4 – 5 %.
Перманентные последствия в виде инвалидизации имеются у 10% перенесших легкую ЧМТ, у 66% после травмы средней степени тяжести и у 100% с тяжелой ЧМТ. Общий государственный ущерб за счет больных с последствиями ЧМТ составляет в США около 25 миллиардов $.
В мирное время по механизму получения на первом месте находится автодорожная травма (водитель, пассажиры салона во время аварии, сбитые автомобилем пешеходы).
На втором месте стоит бытовая травма. Это случайные падения с ударом головой о твердое покрытие, удары головой о стену и т.д. К бытовой травме относится и травма вследствие криминальных действий (нападения, избиения, драки).
Третье место принадлежит производственной травме и четвертое место отводится спортивной травме.
Классификация ЧМТ. Первая классификация ЧМТ принадлежит Жану-Луи Пти (рис.1) – французскому хирургу и анатому.
Пти предлагал выделять при ЧМТ три основных нозологических формы: сотрясение головного мозга (commotio cerebri) , ушиб головного мозга (contusio cerebri) и сдавление головного мозга (compressio cerebri). Сдавление головного мозга Ж.Л. Пти относил к одной из самостоятельных нозологических форм наравне с сотрясением и ушибом головного мозга.
В основе любой медицинской классификации лежит диагностический принцип - на основании классификации формулируется развернутый диагноз и в соответствии с поставленным диагнозом назначается лечение. Так как медицинские знания совершенствуются и углубляются, то медицинские классификации время от времени подвергаются пересмотру. Не является исключением и классификация черепно-мозговой травмы. Современная классификация ЧМТ выглядит следующим образом (рис. 2)

Рис. 2. Изолированная, сочетанная, комбинированная ЧМТ
Изолированная ЧМТ – это травма, при которой имеются повреждения кожных покровов головы, черепа и головного мозга. Сочетанная ЧМТ – травма, при которой ЧМТ сочетается с травмой конечностей (например: переломы) или сегментов туловища (грудной клетки, брюшной полости). При комбинированной ЧМТ имеет место комбинация различных по своей сути повреждающих факторов (травматический, вследствие воздействия, которого возникает ЧМТ, плюс, например, термический фактор – отморожение, ожоги, или радиационное воздействие). Неврологов и нейрохирургов в большей степени интересует изолированная ЧМТ, классификация которой приведена на рисунке 3.

Рис. 3. Классификация изолированной черепно-мозговой травмы
В данной схеме следует уделить внимание следующим моментам. Во-первых, при ЗЧМТ может быть как сотрясение головного мозга (СГМ), так и ушиб головного мозга (УГМ), но если у пострадавшего имеется ОЧМТ, то речь всегда идет о УГМ. Во-вторых, СГМ является монолитным диагнозом и не подлежит градации, а ушиб головного мозга делится на ушиб легкой, средней и тяжелой степени. В-третьих, компрессия головного мозга встречается только при УГМ. В-четвертых, по современной классификации, в отличие от классификации Ж.-Л. Пти, компрессия головного мозга не является самостоятельной нозологической формой и рассматривается как внутричерепное негнойное осложнение острого периода тяжелой ЧМТ.
ОЧМТ это травма, при которой возникает сообщение полости черепа с внешней средой. Такая ситуация возникает при открытых переломах костей свода черепа (ситуация, при которой имеется рана кожных покровов головы, на дне которой определяется перелом кости черепа), а также при переломах средней (СЧЯ) и передней черепных ямок (ПЧЯ) (рис. 4). При переломах ПЧЯ часто повреждается lamina cribrosa, являющаяся верхней стенкой носовой полости, сообщение полости черепа с внешней средой происходит за счет носовых ходов. В этом случае у пострадавшего имеется такой абсолютный признак перелома ПЧЯ, как истечение ликвора с примесью крови из носа. Этот симптом называется назоликворея. При переломах СЧЯ, когда повреждается пирамида височной кости, вглубь которой вдается наружный слуховой проход, сообщение внешней среды с полостью черепа происходит именно через него. В данном случае при осмотре у пострадавшего выявляется истечение ликвора с примесью крови из наружного слухового прохода. Этот клинический признак перелома СЧЯ является абсолютным и называется отоликвореей.

Рис. 4. Переломы основания черепа
Почему важно выделять ОЧМТ в отдельную нозологическую форму? Если при ОЧМТ, как было сказано выше, имеется сообщение полости черепа с внешней средой, то существует вероятность развития внутричерепной гнойной инфекции – это:
- гнойный менингоэнцефалит
- абсцесс головного мозга
- остеомиелит костей черепа
Поэтому пациент с диагнозом ОЧМТ с первого дня поступления в стационар должен получать антибактериальную терапию, направленную на профилактику этих весьма серьезных гнойных осложнений.
Все другие варианты травмы относятся к закрытой черепно-мозговой травме. Это – ушибленные раны кожи головы, закрытые переломы костей черепа, травмы, при которых кожные и костные повреждения разнесены по поверхности головы, например, кожная рана имеется в лобной области, а перелом локализуется в затылочной кости.
ОСНОВНЫЕ КЛИНИЧЕСКИЕ СИНДРОМЫ ПРИ НЕЙРОХИРУРГИЧЕСКОЙ ПАТОЛОГИИ.
Для того чтобы охарактеризовать тяжесть поражения головного мозга, необходимо представлять, что любое нейрохирургическое заболевание головного мозга (травма, опухоль, сосудистое или воспалительное заболевание) может быть охарактеризовано 4 основными синдромами. Это синдром внутричерепной гипертензии (ВЧГ), синдром очаговой неврологической симптоматики, менингеальный синдром и гипертензионно-дислокационный синдром. Коротко остановимся на этих 4 синдромах.
Синдром внутричерепной гипертензии (ВЧГ).
Синдром ВЧГ относится к общемозговым синдромам. Чтобы представить за счет чего повышается внутричерепное давление при заболеваниях головного мозга, необходимо знать доктрину Монро-Келли, предложенную этими двумя авторами более 200 лет назад. Суть доктрины заключается в следующем. Внутричерепные объемы (рис. 5) заключены в ригидном костном образовании – полости черепа и суммарный объём внутричерепных компонентов (кровь, ликвор и мозговое вещество) остается постоянным.

Рис. 5. Соотношение внутричерепных объемов
Основное место в соотношении внутричерепных объемов принадлежит головному мозгу, на долю которого приходится 76%. 8% объема внутричерепного содержимого (ОВЧС) занимает ликвор. Оставшиеся 16% - это артериальная и венозная кровь, протекающая по сосудам головного мозга и синусам полости черепа. В норме объем полости черепа больше, чем ОВЧС, т.е. в полости черепа имеются так называемые резервные пространства, объем которых увеличивается с возрастом в силу атрофических процессов головного мозга. При появлении в полости черепа дополнительного объема (гематома, опухоль) объем внутричерепного содержимого компенсаторно уменьшается, в первую очередь за счет ликвора, а затем за счет уменьшения кровенаполнения головного мозга. При дальнейшем увеличении в размерах дополнительного патологического внутричерепного объемного образования эти компенсаторные возможности исчерпываются, и внутричерепное давление начинает повышаться.
Клиническими симптомами ВЧГ являются головная боль, рвота, головокружение и нарушение сознания. Охарактеризуем эти симптомы последовательно.
1. Головная боль
Источником болевых ощущений при ВЧГ является давление увеличенного объема внутричерепного содержимого на твердую мозговую оболочку (ТМО), которая имеет большое количество болевых рецепторов. Так как избыточному давлению подвергается вся ТМО, то боль является диффузной. По причине давления на твердую мозговую оболочку изнутри полости черепа головная боль имеет распирающий характер. Следующая характеристика боли – ее постоянный характер. Головная боль при ВЧГ имеет суточную динамику – она достигает максимума в ночные и утренние часы. Так как больной во время сна находится в горизонтальном положении, происходит затруднение оттока венозной крови и ликвора из полости черепа, что приводит к дополнительному увеличению ОВЧС.
2. Рвота
Рвота возникает на высоте головной боли, т.е. в ночные, а чаще в утренние часы, сразу после сна и, следовательно, не связана с приемом пищи. Она не имеет предвестников в виде чувства тошноты и возникает внезапно, не принося облегчения.
3. Головокружение
О головокружении при ВЧГ следует сказать, что оно отличается от вестибулярного головокружения тем, что имеет постоянный и несистемный характер.
4. Нарушение сознания
Речь идет о нарушении сознания, а не о его утрате. ЧМТ всегда сопровождается более или менее длительной утратой сознания в момент травмы. Если при травме не было утраты сознания, то диагноз ЧМТ является сомнительным. Ясное сознание соответствует субъективному ощущению, формирующемуся в результате взаимодействия личности с внутренним и внешним миром, и проявляется прежде всего адекватной реакцией на внешние раздражители. Различают качественные и количественные аспекты сознания. Уровень бодрствования является основной количественной характеристикой сознания. Содержательная часть и ясность сознания представляют собой его качественные характеристики. Во всем мире нарушения сознания оцениваются по шкале комы Глазго, предложенной еще в 60-ых годах прошлого столетия. По этой шкале по баллам оценивают 3 параметра: открывание глаз, словесный ответ и двигательный ответ (рис. 6).

Рис. 6. Школа комы Глазго
Результаты оценки сознания приведены на рисунке 7.

Рис. 7. Результаты оценки сознания по ШКГ
Шкала комы Глазго позволяет провести бальную оценку сознания. Однако является весьма приблизительной и далеко не в полной мере отражает суть происходящего. Неудовлетворенность этой шкалой побудила группу отечественных исследователей во главе с нейрохирургом акад. А.Н. Коноваловым предложить отечественную классификацию нарушений сознания. Также как и в ШКГ в отечественной классификации выделяют ясное сознание, оглушение, сопор и кому. Ясное сознание - это термин, указывающий на то, что индивид адекватно ориентируется в месте, времени, в обстановке, ситуации и в собственной личности. Оглушение делится на две степени тяжести: умеренное (I), глубокое (II). При оглушении I больной сидит, т.к. стоять ему тяжело, но все-таки он в состоянии поддерживать вертикальное положение. Сидит с опущенной головой, гиподинамичен (малоподвижен), не интересуется окружающим. На вопросы отвечает с некоторой задержкой тихим голосом. Пациент доступен для диалога (с ним можно поговорить о его семье, работе и т.д.). Для того чтобы оценить степень нарушения сознания врач должен задать вопросы, позволяющие ему понять ориентируется ли пациент в месте, во времени и собственной личности. Ориентация в месте: «Где вы находитесь?», ориентация во времени: «Какой сейчас год? Какое время года? Какое время суток?», ориентация в собственной личности: «Сколько вам лет?» На все эти вопросы пациент в оглушении I отвечает правильно. При оглушении II пациента доставляют в приемное отделение на каталке, т.к. он не в состоянии поддерживать вертикальное положение. Пострадавший производит впечатление спящего человека. На обращение открывает глаза, фиксирует взор. Пациент не доступен для диалога. На вопросы отвечает односложно с большой задержкой. Часто для того чтобы получить ответ необходимо несколько раз повторить один и тот же вопрос громким голосом, еще лучше «потормошить» больного. По ответам можно судить, что больной дезориентирован в месте, во времени и в собственной личности. Он не правильно называет место, где находится. В приемном покое, или даже в машине скорой помощи вы услышите, что он находится дома, или на работе, или на даче и т.д. Пациент дезориентирован во времени, неправильно называя текущий год, текущий сезон, время суток. Пострадавший также дезориентирован в собственной личности и ошибается в своем паспортном возрасте. Если больного с оглушением II оставить в покое, то он закрывает глаза и засыпает, следовательно, для оглушения II характерны также быстрая истощаемость и сомнолентность (сонливость). Сопор (от лат. sopor — оцепенение, вялость, сон). Больной лежит с закрытыми глазами, производя впечатление спящего. На обращение не реагирует. Словесный контакт отсутствует. В ответ на болевое раздражение открывает глаза, не фиксируя взгляд, на лице появляется гримаса боли, пострадавший может застонать (это максимум, что вы можете от него услышать). Такие реакции не имеют никакого отношения к сознанию. Тем не менее, больной, находящийся в сопоре, все-таки еще находится в сознании. Определить это мы можем на основании его ответа на болевые раздражения, который является целесообразным. Целесообразный (адекватный) ответ на болевое раздражения - это локализация источника раздражения рукой и его устранение (или хотя бы попытка этого действия). Следовательно, при проверке ответа на болевое раздражение мы должны наносить его в разных участках тела. Если больной совершает хотя бы попытку движения рукой в сторону наносимого болевого раздражения, то он находится в сопоре.
Кома (от греч. κῶμα — глубокий сон). Врачи древней Греции назвали это состояние глубоким сном на основании признака непробуждаемости в виде отсутствия открывания глаз в ответ на раздражения. Как следует из выше изложенного, больные в оглушении II, сопоре производят впечатление спящих, но при оглушении II больной открывает глаза («пробуждается») в ответ на обращение, при сопоре – в ответ на болевое раздражение. В случае комы, реакции в виде открывания глаз, мы не увидим ни при каких раздражениях («непробуждаемость»). В ответ же на болевые раздражения возникают лишенные целесообразности, патологические двигательные ответы. В зависимости от их характера, или их отсутствия, а также от состояния витальных функций, кома делится на три степени тяжести: кома I, кома II, кома III.
Кома I . В ответ на болевое раздражение пациент совершает стереотипное медленное, тоническое сгибание верхних конечностей (конечности, если имеется гемипарез) в локтевых суставах. При этом кисти расслаблены и находятся в висячем положении (Рис. 8). Такой ответ также называется декортикационной (de – отсутствие, cortex – кора головного мозга) ригидностью, в состав которой также входит экстензорно-пронаторное положение стоп. Термин «декортикационная ригидность» пришел в медицину из нейрофизиологии. На ранних этапах ее развития функции головного мозга изучали на животных методом перерезок и экстирпаций. При перерезке головного мозга на уровне лучистого венца (под корой) у животных развивалось именно такое перераспределение мышечного тонуса.

Рис. 8. Кома I. Двигательный патологический ответ на болевое раздражение
Следует сказать, что исследование ответов на болевое раздражения у больных находящихся в коме подразумевает нанесение массивных болевых раздражений (давление на точку выхода I ветви тройничного нерва, давление средним межфаланговым суставом указательного пальца на грудину, давление карандашом на ноготь) (рис. 9).

Рис. 9. Методика исследования двигательного ответа на болевое раздражение у больных, находящихся в коме
При коме первой степени тяжести – витальные (жизненно важные) функции стабильны. У больных определяется адекватное дыхание с частотой дыхательных движений не более 20 и достаточной глубиной дыхательной экскурсии грудной клетки. Артериальное давление (АД) у больных в коме I, как правило, повышено. Повышение артериального давления и появление брадикардии при ВЧГ впервые описал Х. Кушинг. Эта реакция организма на ситуацию внутричерепной гипертензии носит название рефлекса Кушинга. Рефлекс Кушинга имеет компенсаторный характер. При увеличении объема ВЧС артерии коры головного мозга придавливаются к внутренней поверхности костей черепа, что приводит к уменьшению перфузионного давления в них (церебральное перфузионное давление – ЦПД), которое рассчитывается по формуле: ЦПД = системное артериальное давление (САД) – внутричерепное давление (ВЧД). Следовательно, повышение системного артериального давления является компенсаторной реакций, направленной на повышение ЦПД. Из сказанного следует, что проведение гипотензивной терапии при повышении АД у больного с ВЧГ не только бессмысленно, но и вредно. Это правило не распространяется на ситуации, когда верхнее давление превышает 190 мм рт. ст. При таком давлении происходит срыв регуляторных механизмов мозгового кровообращения и помимо суженных сосудов появляются сосуды, находящиеся в состоянии дилатации. В такой ситуации возникает реальная угроза развития церебрального кровоизлияния.
Кома II. В ответ на болевое раздражение у больных возникает экстензорно-пронатороное (экстензия – разгибание, пронация – поворот кнутри) тоническое движение верхними конечностями (рис. 10). Такой ответ называется децеребрационной (de – отсутствие, cerebrum – большой мозг) ригидностью (комментарий см. – кома I). Шея находится в состоянии гиперэкстензии.

Рис. 10.Кома II. Двигательный ответ на болевое раздражение
В зависимости от состояния витальных функций кома второй степени тяжести делится на кому II А и кому II Б. При коме II А витальные функции стабильны и еще сохраняется рефлекс Кушинга. Для комы II Б характерно нарушение витальных функций. В первую очередь это касается функции дыхания. У больных развиваются патологические типы дыхания. Наиболее часто встречается центральная одышка и реже периодическое дыхание Чейн-Стокса (рис. 11). Центральная одышка характеризуется частым, поверхностным дыханием. Частота дыхательных движений может достигать 60 и более в 1минуту. При такой частоте дыхания грудная клетка не в состоянии совершать достаточный объем дыхательного движения, поэтому дыхание поверхностное.

Рис. 11. Спирография при коме IIБ. 1 – центральная одышка, 2 – дыхание Чейн-Стокса
Так как у больных имеется тризм (патологическое напряжение) жевательной мускулатуры, то выдох совершается через плотно сжатые губы. Поэтому дыхание у этих больных шумное. Следующая характерная черта центральной одышки – равнофазность дыхательных движений. Если в норме выдох длиннее вдоха, то при центральной одышке фаза вдоха равна фазе выдоха. Шумное, частое, равнофазное дыхание послужило поводом для второго названия этого типа дыхания. Центральную одышку еще называют «машинным» или «механическим» дыханием. Второй тип патологического дыхания – дыхание Чейн-Стокса - характеризуется периодами нарастающих по амплитуде дыхательных движений. По достижении максимальной амплитуды следует фаза уменьшения амплитуды дыхания. Между такими периодами имеется фаза апноэ. Эти типы дыхания называются патологическими не только потому, что они отражают патологию дыхательного центра. Они патологические по своей сущности, так как не обеспечивают необходимой оксигенации организма. Эти типы дыхания приводят к развитию гипоксии, в том числе, и головного мозга. При коме IIБ у больного уже выявляется артериальная гипотония, еще не достигающая критических значений (например, у нормотоника может определяться давление 100/60 мм рт. ст.). Но если мы вспомним сказанное о компенсаторном значении повышения системного АД при ВЧГ, то становится понятным, что головной мозг больного испытывает ишемию. Травма, гипоксия и ишемия головного мозга сопровождается травматическим, гипоксическим и ишемическим отеком, что приводит к дальнейшему увеличению объема внутричерепного содержимого и нарастанию ВЧГ. Сказанное делает понятным на данном этапе необходимость реанимационных мероприятий, включающих в себя лечебный наркоз, искусственную вентиляцию легких и поддержание АД на постоянном уровне. Процесс неуклонного роста ОВЧС приводит к ситуации, при которой исчерпываются компенсаторные возможности резервных пространств полости черепа, наступает критическая декомпенсация состояния больного, а ВЧГ переходит в неуправляемую стадию.
На рисунке видно, что за счет резервных пространств полости черепа по мере увеличения внутричерепного содержимого на 1 – 2 участке кривой ВЧГ растет медленно. На 2 – 3 участке рост ВЧГ становится более интенсивным (субкомпенсация). 3 – 4 – резкий скачок внутричерепного давления (декомпенсация, неуправляемая ВЧГ).
Наши терапевтические возможности ограничиваются 1 – 2 – 3 участком кривой. 3 - 4 участок кривой клинически характеризуется развитием комы III, которая является по сути агональным (терминальным) состоянием.
Кома III характеризуется тотальной арефлексией, диффузной мышечной атонией и грубыми нарушениями витальных функций. У больного определяется отсутствие всех рефлексов (сухожильных, защитных, фотореакций зрачков и т.д.), отсутствует двигательная реакция на боль. Дыхательная функция характеризуется брадипноэ не чаще 10 дыхательных движений в минуту. Дыхание нерегулярное по частоте и амплитуде (атактическое дыхание) (рис. 13).

Рис. 13. Кома III. Спирография. Атактический тип дыхания
У больного имеется артериальная гипотония, достигающая критических значений (например, 40/20 мм рт. ст.).
ЭПИЛЕПТИЧЕСКИЙ СИНДРОМ.
Еще одним клиническим синдромом, характеризующим нейрохирургическую патологию головного мозга, является эпилептический синдром. Эпилептические припадки по своему происхождению являются симптомами раздражения или ирритации. В зависимости от того какого типа припадок возникает у пациента, эпилептический синдром может быть отнесен к общемозговому симптомокомплексу (первично генерализованные припадки) или к очаговому (фокальные или вторично генерализованные припадки).
Различают первично генерализованные, фокальные и вторично генерализованные эпилептические припадки. Термин «генерализация» припадка означает утрату сознания во время припадка и его амнезию.
Хотя первично генерализованные припадки не имеют значения для установления топического диагноза, тем не менее, они часто встречаются при ЧМТ и ее последствиях и вполне уместно кратко охарактеризовать их в рамках данной лекции. К первично генерализованным припадкам относятся большой (судорожный) припадок, малый (безсудорожный) припадок, а также абсанс. Термины большой (grand mal) и малый припадок (petit mal), предложенные в 1815 г французским психиатром Жан-Этьеном Домиником Эскиролем (рис.14), прочно утвердились в мировой психиатрической и неврологической литературе.
Большой (судорожный) припадок.
Является наиболее часто встречающимся эпилептическим припадком. Больной теряет сознание и падает. Наблюдаются генерализованные судороги (не путать с понятием генерализованного припадка) тонико-клонического характера в мышцах конечностей, туловища, лица, языка, в дыхательной мускулатуре (рис. 15). Происходит потеря контроля над функцией тазовых органов (непроизвольное мочеиспускание). Появляется пена изо рта, цианоз лица, апноэ. Возможен прикус языка Длительность припадка – несколько минут, после чего судороги прекращаются. По возвращении сознания больной находится в просоночном состоянии (спутанность сознания, заторможенность, дезориентация). Факт припадка амнезируется, о наличии припадков больные узнают со слов окружающих.
Малый (безсудорожный) припадок.
Характеризуется потерей сознания. Вследствие резкого снижения мышечного тонуса больной падает. По факту снижения мышечного тонуса этот припадок имеет еще одно название – атонический. При наличии у больных таких припадков необходимо проводить дифференциальный диагноз с обморочными (синкопальными) состояниями.
Абсанс.
Больной во время повседневной или трудовой деятельности внезапно прекращает ее и «замирает». Он находится без сознания. Ни судорог, ни падения не отмечается. Окружающие видят застывшее выражение лица и бессмысленный взгляд (рис. 16). Длительность припадка – несколько секунд. Затем пациент приходит в сознание и продолжает прерванную деятельность. Если он разговаривал, то продолжает свой разговор именно с того места, где у него случился припадок. Больные знают об этих припадках со слов окружающих, полностью амнезируя их. Картина припадка напоминает остановившийся на несколько секунд кадр кинофильма.
Дата: 2019-02-25, просмотров: 423.