Венозная гиперемия оказывает повреждающее действие на ткани и органы за счёт ряда патогенных факторов.
• Основные патогенные факторы: гипоксия (циркуляторного типа в начале процесса, а при длительном течении — смешанного типа), отёк ткани (в связи с увеличением гемодинамического давления на стенку венул и вен), кровоизлияния в ткани (в результате перерастяжения и разрывов стенок посткапилляров и венул) и кровотечения (внутренние и наружные).
• Последствия: снижение специфической и неспецифических функций органов и тканей, гипотрофия и гипоплазия структурных элементов тканей и органов, некроз паренхиматозных клеток и развитие соединительной ткани (склероз, цирроз) в органах.
Ишемия
Ишемия — несоответствие между притоком к тканям и органам артериальной крови и потребностью в ней. При этом потребность в кровоснабжении всегда выше реального притока крови по артериям.
Причины
Причины ишемии могут иметь различное происхождение и природу.
• По природе причины ишемии делят на физические, химические и биологические.
† Физические факторы: сдавление артериальных сосудов (например, опухолью, рубцовой тканью, инородным телом, жгутом), сужение или закрытие просвета изнутри (например, тромбом, эмболом, атеросклеротической бляшкой), действие чрезмерно низкой температуры.
† Химические факторы. Многие химические соединения обладают способностью вызывать сокращение ГМК артериальных сосудов и сужение их просвета. Примеры: никотин, ряд ЛС: мезатон, эфедрин, препараты адреналина, АДГ, ангиотензины.
† Биологические факторы: БАВ с сосудосуживающими эффектами (например, катехоламины, ангиотензин II, АДГ, эндотелин), БАВ микробного происхождения: их экзо‑ и эндотоксины, метаболиты с вазоконстрикторным действием.
• По происхождению выделяют ишемии, причина которых имеет эндогенное или экзогенное происхождение (инфекционное и неинфекционное).
Механизмы возникновения ишемии
Механизмы возникновения ишемии представлены на рис. 22–49.
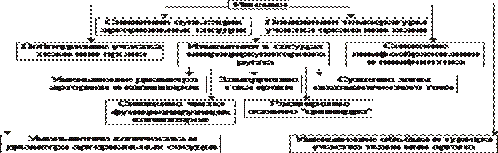
Рис. 22–49. Механизмы возникновения ишемии.
Механизмы, обусловливающие преимущественное снижение притока артериальной крови к тканям и органам: нейрогенный, гуморальный и «механический».
• Нейрогенный механизм (нейротонический и нейропаралитический).
† Нейротонический. Характеризуется преобладанием эффектов симпатической нервной системы на стенки артериол в сравнении с парасимпатической. Это сопровождается повышенным выбросом норадреналина их адренергических терминалей.
Причины: активация симпатических влияний на ткани и органы (например, при различных вариантах стресса, действии на ткани низкой температуры, механической травмы, химических веществ) и повышение адренореактивных свойств стенок артериол (например, при сенсибилизации их к вазоконстрикторным агентам: в условиях повышенного уровня Ca2+ или цАМФ в миоцитах).
† Нейропаралитический. Характеризуется устранением или снижением («параличом») парасимпатических влияний на стенки артериол.
Причины. Торможение или блокада проведения нервных импульсов по парасимпатическим волокнам к артериолам (и в связи с этим — высвобождения ацетилхолина из терминальных нервных волокон в стенках артерий, артериол и прекапилляров). Такая ситуация может наблюдаться при невритах, механических травмах, развитии опухолей, хирургическом удалении ганглиев или пересечении парасимпатических нервов.
• Гуморальный механизм. Заключается в увеличении содержания в тканях веществ с вазоконстрикторным действием (например, ангиотензина II, АДГ, тромбоксана А2, адреналина, ПгF) и чувствительности рецепторов стенок артериол к агентам с сосудосуживающим действием (например, при увеличении в тканях [Ca2+] или [Na+]).
• Этиологический фактор механического характера. Характеризуется наличием механического препятствия движению крови по артериальным сосудам.
• Причины: сдавление (компрессия) артериального сосуда опухолью, рубцом, отёчной тканью, жгутом и уменьшение (вплоть до полного закрытия — обтурации) просвета артериолы (например, тромбом, агрегатом клеток крови, эмболом).
• Эмбол и эмболия.
† Эмбол — образование, циркулирующее в полостях сердца, кровеносных или лимфатических сосудах и в норме в них не встречающееся. По происхождению различают эндогенные и экзогенные эмболы, а по локализации в сосудах — артериальные и венозные.
‡ Экзогенные. Чаще всего — пузырьки воздуха (попадающие в крупные вены при их ранении) и инородные тела (например, осколки пули или ЛС на масляной основе при их введении в холодном состоянии).
‡ Эндогенные.
§ Фрагменты тромбов (тромбоэмболы).
§ Кусочки жировой ткани или кости, образующиеся при размозжении органов или переломах трубчатых костей.
§ Небольшие фрагменты распадающейся опухолевой или разрушенной нормальной ткани.
§ Конгломераты микробных клеток, много‑ и одноклеточные паразиты.
§ Пузырьки газов, в норме растворённых в плазме крови, но образующиеся при быстром переходе от более высокого барометрического давления к более низкому — при разгерметизации самолетов или космических аппаратов, а также при быстром подъёме с больших глубин.
‡ Артериальные эмболы. Закупоривают артериальные сосуды большого круга кровообращения (попадают из лёгочных вен или левых камер сердца), малого круга (заносятся из правых камер сердца или вен большого круга кровообращения).
‡ Венозные. Часто эмболы обнаруживают в мелких венозных сосудах воротной вены.
† Эмболия — циркуляция в кровеносном или лимфатическом русле образования, в норме в нём не встречающегося и закрытие либо сужение им кровеносного или лимфатического сосуда.
Механизмы возникновения ишемии, обусловливающие преимущественно значительное увеличение потребления тканями кислорода и/или субстратов обмена веществ. При этом потребность в кислороде и субстратах метаболизма превышает уровень их реальной доставки к тканям.
• Наиболее частая причина: Значительное повышение функции органа или ткани и возрастание в связи с этим — интенсивности метаболизма в них.
• Примеры.
† Ишемия мышц (включая и миокард) при интенсивной и длительной физической нагрузке.
† Ишемия миокарда при остром значительном повышении уровня АД (например, в условиях гипертензивного криза) и эмоциональном стрессе.
В последнем случае работа сердца значительно возрастает под влиянием избытка катехоламинов, оказывающих положительный хроно- и инотропный эффекты. В этих условиях увеличивается и приток крови к миокарду по коронарным артериям. Однако работа миокарда (и в соответствии с этим потребность в кровоснабжении) возрастает в большей мере. Развивается ишемия миокарда, проявляющаяся приступом стенокардии, а нередко гибелью ишемизированного участка сердца (инфаркт миокарда).
Одновременно, как правило, выявляются и признаки сужения артериальных сосудов сердца в связи с развитием атеросклеротических изменений в них.
Проявления ишемии
Проявления ишемии представлены на рис. 22–50.
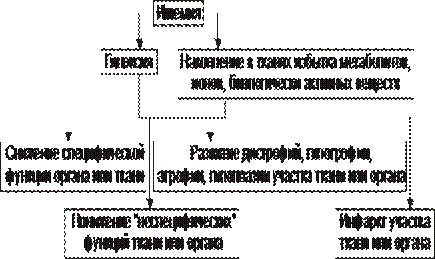
Рис. 22–50. Проявления ишемии.
Последствия ишемии
Основные последствия ишемии, развивающиеся вследствие гипоксии и многочисленных БАВ, представлены на рис. 22–51.

Рис. 22–51. Основные последствия ишемии.
• Характер, выраженность и масштаб последствий ишемии зависит от многих факторов. Наиболее значимыми являются:
† Скорость развития ишемии (чем она выше, тем более значительна степень повреждения тканей).
† Диаметр поражённой артерии или артериолы (чем он больше, тем тяжелее поражение).
† «Чувствительность» ткани или органа к ишемии (она особенно высока у ткани мозга, сердца, почек).
† Значение ишемизированного органа или ткани для организма (ишемия таких органов как мозг, сердце, почки может привести к гибели организма. В отличие от этого, ишемия участка кожи или какой‑либо скелетной мышцы совместима с жизнью).
† Степень развития коллатеральных сосудов и скорость включения или активации коллатерального кровотока в ткани или органе.
• Коллатеральный кровоток — система кровообращения в сосудах вокруг ишемизированного участка ткани и в нём самом.
† Включению (или возрастанию) коллатерального кровообращения способствуют наличие градиента давления крови выше и ниже суженного участка сосуда, накопление в зоне ишемии БАВ с сосудорасширяющим действием (аденозина, ацетилхолина, Пг, кининов и др.), активация местных парасимпатических влияний (способствующих расширению коллатеральных артериол) и высокая степень развития сосудистой сети (коллатералей) в поражённом органе или ткани.
† Группы органов и тканей в зависимости от степени развития артериальных сосудов и анастомозов между ними.
‡ С абсолютно достаточной коллатеральной сетью: скелетная мускулатура, брыжейка кишечника, лёгкие. В указанных образованиях совокупный просвет коллатеральных сосудов равен или превышает диаметр магистральной артерии. В связи с этим прекращение кровотока по ней не вызывает выраженной ишемии тканей в регионе кровоснабжения данной артерии.
‡ С абсолютно недостаточными коллатералями: миокард, почки, головной мозг, селезёнка. В этих органах суммарный просвет коллатеральных артерий значительно меньше диаметра магистральной артериальной ветви. В связи с этим окклюзия её приводит к выраженной ишемии или инфаркту ткани.
‡ С относительно достаточными (недостаточными) коллатералями: стенки кишечника, желудка, мочевого пузыря, кожа, надпочечники. В них совокупный просвет коллатеральных сосудов в более или менее выраженной степени меньше диаметра магистральной артерии. Окклюзия крупного артериального ствола в этих органах сопровождается большей или меньшей степенью их ишемии.
Стаз
Стаз — значительное замедление или прекращение тока крови и/или лимфы в сосудах органа или ткани.
Причины
• Ишемия и венозная гиперемия. Они приводят к стазу вследствие существенного замедления кровотока (при ишемии в связи со снижением притока артериальной крови, при венозной гиперемии в результате замедления или прекращения её оттока) и создания условий для образования и/или активации веществ, обусловливающих склеивание форменных элементов крови, формирования из них агрегатов и тромбов.
• Проагреганты — факторы, вызывающие агрегацию и агглютинацию форменных элементов крови.
Патогенез
Патогенез стаза представлен на рис. 22–52.

Рис. 22–52. Основные звенья патогенеза стаза.
На финальном этапе стаза всегда происходит процесс агрегации и/или агглютинации форменных элементов крови, что приводит к сгущению крови и снижению её текучести. Этот процесс активируют проагреганты, катионы и высокомолекулярные белки.
• Проагреганты (тромбоксан А2, аденозиндифосфат, ПгF, ПгE, катехоламины, АТ к форменным элементам крови) вызывают адгезию, агрегацию, агглютинацию форменных элементов крови с последующим их лизисом и высвобождением из них БАВ (в том числе — проагрегантов, потенцирующих реакции агрегации и агглютинации).
• Катионы. K+, Ca2+, Na+, Mg2+ и высвобождаются из клеток крови, повреждённых стенок сосудов и тканей. Адсорбируясь на цитолемме форменных элементов крови, избыток катионов нейтрализует их отрицательный поверхностный заряд или даже меняет его на обратный. И если неповреждённые клетки (благодаря отрицательному заряду) «отталкиваются» друг от друга, то повреждённые клетки («нейтрализованные») образуют агрегаты. Ещё более активно агрегируют «перезаряженные» клетки крови. Имея положительный поверхностный заряд, они сближаются с «нейтрализованными» клетками и особенно с повреждёнными (имеющими отрицательный заряд), формируя агрегаты, адгезирующие на интиме сосудов.
• Высокомолекулярные белки (например, g‑глобулины, фибриноген) снимают поверхностный заряд неповреждённых клеток (соединяясь с отрицательно заряженной поверхностью клеток с помощью аминогрупп, имеющих положительный заряд) и потенцируют агрегацию форменных элементов крови и адгезию их конгломератов к стенке сосуда (достигается в результате фиксации большого числа белковых мицелл, обладающих адгезивными свойствами, на поверхности форменных элементов крови).
Виды стаза
Все разновидности стаза подразделяют на первичные и вторичные.
• Первичный (истинный) стаз. Формирование стаза первично начинается с активации форменных элементов крови и выделения ими большого количества проагрегантов и/или прокоагулянтов. На следующем этапе форменные элементы агрегируют, агглютинируют и прикрепляются к стенке микрососуда. Это и вызывает замедление или остановку кровотока в сосудах.
• Вторичный стаз (ишемический и застойный).
† Ишемический стаз развивается как исход тяжёлой ишемии в связи со снижением притока артериальной крови, замедлением скорости её тока, турбулентным его характером. Это и приводит к агрегации и адгезии клеток крови.
† Застойный (венознозастойный) вариант стаза является результатом замедления оттока венозной крови, сгущения её, изменения физико‑химических свойств, повреждения форменных элементов крови (в частности, в связи с гипоксией). В последующем клетки крови адгезируют друг с другом и со стенкой микрососудов.
Проявления стаза
При стазе происходят характерные изменения в сосудах микроциркуляторного русла:
• уменьшение внутреннего диаметра микрососудов при ишемическом стазе,
• увеличение просвета сосудов микроциркуляторного русла при застойном варианте стаза,
• большое количество агрегатов форменных элементов крови в просвете сосудов и на их стенках,
• микрокровоизлияния (чаще при застойном стазе).
В то же время проявления ишемии или венозной гиперемии могут перекрывать проявления стаза.
Последствия стаза
При быстром устранении причины стаза ток крови в сосудах микроциркуляторного русла восстанавливается и в тканях не развивается каких‑либо существенных изменений.
Длительный стаз приводит к развитию дистрофических изменений в тканях, нередко — к гибели участка ткани или органа (инфаркт).
Нарушение крово‑ и лимфообращения в сосудах микроциркуляторного русла
Микроциркуляция — упорядоченное движение крови и лимфы по микрососудам, транскапиллярный перенос плазмы и форменных элементов крови, перемещение жидкости во внесосудистом пространстве.
Микроциркуляторное русло. Совокупность артериол, капилляров и венул составляет структурно-функциональную единицу сердечно-сосудистой системы — микроциркуляторное (терминальное) русло. Терминальное русло организовано следующим образом: от терминальной артериолы отходит метартериола, распадающаяся на образующие сеть анастомозирующие истинные капилляры; венозная часть капилляров открывается в посткапиллярные венулы. В месте отделения капилляра от артериол имеется прекапиллярный сфинктер — скопление циркулярно ориентированных ГМК. Сфинктеры контролируют локальный объём крови, проходящий через истинные капилляры; объём же крови, проходящей через терминальное сосудистое русло в целом, определяется тонусом ГМК артериол. В микроциркуляторном русле присутствуют артериоловенулярные анастомозы, связывающие артериолы непосредственно с венулами или мелкие артерии с мелкими венами (юкстакапиллярный кровоток). Стенка сосудов анастомоза содержит много ГМК. Артериовенозные анастомозы в большом количестве присутствуют в некоторых участках кожи, где они играют важную роль в терморегуляции (мочка уха, пальцы). К микроциркуляторному руслу относят также мелкие лимфатические сосуды и межклеточное пространство.
Дата: 2019-02-25, просмотров: 398.