Б1.О.18 ГЕОЛОГИЯ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к выполнению расчетно-графической и контрольной работ
ХИМИЧЕСКИЙ АНАЛИЗ ПРИРОДНЫХ ВОД,
ГРАФИЧЕСКОЕ ИЗОБРАЖЕНИЕ ИХ РЕЗУЛЬТАТОВ
И ОЦЕНКА ПРИГОДНОСТИ ДЛЯ РАЗЛИЧНЫХ ЦЕЛЕЙ
2. 08.03.01 Строительство
(код и наименование направления подготовки, специальности)
Промышленное и гражданское строительство
(наименование профиля подготовки, специализации, направленности программы)
Уровень бакалавриата
(квалификация (степень) выпускника, уровень подготовки)
Очная, заочная
(форма обучения)
УФА 2018
Рекомендовано к изданию методической комиссией факультета природопользования и строительства (протокол № 7 от 28 марта 2018 г.)
Составители: д-р геол.-минерал. наук, профессор Абдрахманов Р.Ф., старший преподаватель Хайдаршина Э.Т.
Рецензент: канд. экон. наук, доцент кафедры землеустройства Кутлияров А.Н.
Ответственный за выпуск: зав. кафедрой природообустройства, строительства и гидравлики, канд. техн. наук, доцент Хасанова Л.М.
г. Уфа, БашГАУ, кафедра природообустройства,
строительства и гидравлики
| ОГЛАВЛЕНИЕ | |
| ВВЕДЕНИЕ | |
| 1 ФОРМЫ ВЫРАЖЕНИЯ РЕЗУЛЬТАТОВ ХИМИЧЕСКОГО АНАЛИЗА | |
| 1.1 Массовая или весовая форма | |
| 1.2 Молярная (эквивалентная) форма | |
| 1.3 Процент – мольная (эквивалентная) форма | |
| 2 ОПРЕДЕЛЕНИЕ СОСТАВА ПРИРОДНЫХ ВОД | |
| 2.1 Жёсткость воды | |
| 2.2 Минерализация воды | |
| 2.3 Содержание растворенных газов, температура, дебит | |
| 3 ХИМИЧЕСКАЯ КЛАССИФИКАЦИЯ ПРИРОДНЫХ ВОД | |
| 3.1 Классификация О.А. Алекина | |
| 3.2 Формула М.Г. Курлова | |
| 3.3 Пересчет из ионной формы в солевую | |
| 4 ГРАФИЧЕСКИЕ МЕТОДЫ ИЗОБРАЖЕНИЯ РЕЗУЛЬТАТОВ АНАЛИЗОВ ВОДЫ | |
| 4.1 Треугольники анионно-катионного состава в сочетании с двумя квадратами | |
| 4.2 Колонки – диаграммы Н.И. Толстихина | |
| 4.3 Гидрохимический профиль А.А. Бродского | |
| 5 ОЦЕНКА КАЧЕСТВА ВОДЫ ДЛЯ РАЗЛИЧНЫХ ЦЕЛЕЙ | |
| 5.1 Оценка качества воды для питья | |
| 5.2 Оценка ирригационных свойств вод | |
| 5.3 Оценка агрессивных свойств вод | |
| 6 ХОД ВЫПОЛНЕНИЯ РАБОТЫ | |
| ЗАКЛЮЧЕНИЕ | |
| БИБЛИОГРАФИЧЕСКИЙ СПИСОК | |
| Приложение А Варианты к заданию |
ВВЕДЕНИЕ
Вода является сильнейшим растворителем горных пород и представляет раствор сложного состава с очень широким диапазоном содержания растворенных веществ как по числу, так и по концентрации. Химический состав воды определяет возможность применения её для различных целей (хозяйственно-питьевого использования, орошения), а также агрессивное свойство по отношению к цементу бетона и пр.[1,2,4,5]. Важнейшими компонентами природных вод являются ионы: Са2+, Mg2+, Na+, K+, NH+4, HCO3-, CO32-, SO42-, NO3-, а также газы: CO2, H2S, O2 и др.Количественное содержание этих ионов в исследуемой воде устанавливается методами аналитической химии [6].
Целью данной практической работы являются – основываясь на знаниях, полученных по курсу «Общая химия» уметь анализировать химический состав природных вод, графически изображать их результаты, оценивать пригодность для различных целей.
ФОРМЫ ВЫРАЖЕНИЯ РЕЗУЛЬТАТОВ ХИМИЧЕСКОГО АНАЛИЗА
Различают весовую, молярную (эквивалентную) и процент молярную (эквивалентную) формы, каждая из которых имеет свои преимущества и недостатки [4,6,7].
Массовая или весовая форма
Массовая или весовая форма представляя собой основную форму выражения результатов химического вещества, характеризуется тем, что содержание ионов в исследуемой воде определяется в весовых единицах – в граммах или миллиграммах на дм3 (г/дм3, мг/дм3).
Существенным недостатком весовой формы следует считать невозможность проверки результатов выполненного анализа, ввиду того, что суммы весового количества анионов и катионов между собой не совпадают.
ОПРЕДЕЛЕНИЕ СОСТАВА ПРИРОДНЫХ ВОД
Жёсткость воды
Жёсткость воды определяется содержанием растворённых солей, кальция и магния. Различают общую, устранимую и постоянную жёсткости воды. Общая жёсткость обусловлена суммарным содержанием ионов Ca2+ и Mg2+, устранимая представляет собой ту часть жёсткости, которая вызывается бикарбонатами Ca2+ и Mg2+ и устраняется кипячением воды, постоянная равно общей жёсткости минус устранимая. Общая жёсткость принято выражать в миллиграмм – моль (эквивалент) на дм3 (ммоль/дм3) и в немецких градусах (оН). Миллиграмм – моль жёсткости соответствует раздельному содержанию в дм3 воды эквивалентных количеств Ca2+ , Mg2+ и CaО, а именно 20,04 мг Ca2+ , 12,16 мг Mg2+ или 28 мг CaО. Немецкий градус жесткости эквиваленте содержанию 10 мг CaО в литре воды. Сопоставляя названные показатели жесткости по величине CaО устанавливаем, что один ммоль жесткости равен 2,8 немецких градусов.
Значение общей жесткости воды в ммоль/дм3 находится суммированием содержания иона Ca2+ и Mg2+ в молярной форме. Умножая полученную величину на 2,8 находим общую жесткость в немецких градусах.
Минерализация воды
Минерализация воды определяется содержанием растворенных минеральных веществ и рассчитывается как арифметическая сумма весовых количеств всех ионов в дм3 воды. При подсчете минерализации суммарное содержание ионов, выраженное в миллиграммах на дм3 переводится в граммы, с округлением до первого знака после запятой.
Пример: сумма ионов составляет 14176 миллиграмм, минерализация воды 14,2 г/ дм3.
Содержание растворенных газов, температура, дебит
Полный химический анализ воды предусматривает определение растворенных газов (СО2, Н2S и др.) содержание которых выражается миллиграммами на дм3 (мг/ дм3). При полевых исследованиях устанавливается температура природных вод (Т) и определяется дебит источников или скважин путем замера вытекающей или откачиваемой из них воды.
Дебит (Д) выражается литрами в секунду (л/с) или кубометрами в сутки (м3/сутки).
Классификация О.А. Алекина
Классификация О.А. Алекина (рисунок 1) сочетает принцип деления подземных вод по преобладающим ионам и по соотношению между ними. По преобладающему аниону О.А. Алекиным /4/ выделяются три класса вод: гидрокарбонатная, сульфатная и хлоридная. По ведущему катиону различают группы кальциевых, магниевых и натриевых вод. Соотношение ионов позволяет установить различные типы вод. При выделении которых содержание ионов выражается в молярной форме (r)
1 тип r 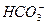 > r Ca2+ + r Mg2+ (гидрокарбонатный натриевый),
> r Ca2+ + r Mg2+ (гидрокарбонатный натриевый),
2 тип r 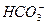 < r Ca2+ + r Mg2+ (сульфатный натриевый),
< r Ca2+ + r Mg2+ (сульфатный натриевый),
3 тип r 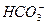 +
+ 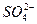 < r Ca2+ + r Mg2+ или r Сl- >r Na+
< r Ca2+ + r Mg2+ или r Сl- >r Na+
4 тип r 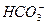 +
+ 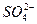 =0
=0
3 тип подразделяется: 3а rCl- < r Na++ r Mg2+ (хлормагниевый),
3б rCl- < r Na++ r Mg2+(хлоркальциевый).
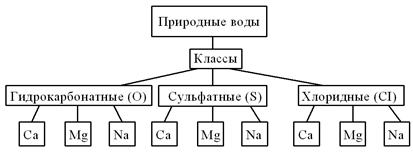
Рисунок 1 Классификация природных вод по О.А. Алекину
Типы гидрокарбонатных: Ca - I,II,III; Mg – I,II,III; Na – I,II,III
Типы сульфатных: Ca - IV,II,III; Mg – IV,II,III; Na – I,II,III
Типы хлоридных: Ca - IV,II,III; Mg – IV,II,III; Na – I,II,III
Эти гидрохимические оценки можно записать и в более сжатой форме. Если классы вод обозначить условными индексами (С-гидрокарбонатные воды, S-сульфатные, Cl-хлоридные), а типы римскими выделить символами ведущих катионов (Ca,Mg, Na), а типы римскими цифрами (I-IV), то химическая характеристика вод указанного состава запишется так: 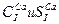 .
.
Эту краткую форму записи следует использовать, указывая класс воды по Алекину в таблице результатов химических анализов природных вод (таблица 5).
Формула М.Г. Курлова
При массовых определениях химического состава природных вод возникает необходимость обобщения, полученных результатов и изображения анализов воды в виде кратких формул, допускающих обзор и интерпретацию аналитического материала. Формула Курлова представляет собой псевдо-дробь, в числителе которой в порядке убывающего содержания записываются анионы, а в знаменателе катионы, выраженные в процентах (дробные величины процентов округляются до целых чисел). Слева от полученной «простой дроби» указывается содержание растворенных газов в мг/ дм3 и величина минерализации воды в г/ дм3, справа от нее температура воды и дебит скважины в м3 /сутки. Образец записи результатов анализа в виде формулы Курлова приводится ниже
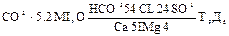 .
.
Наименование водам дается по преобладающим (свыше 20% моль) анионам и катионам в порядке их возрастания (приведенный анализ читается – вода сульфатно-хлоридно-карбонатная, магниево-кальциевая).
С двумя квадратами
Треугольники анионно-катионного состава в сочетании с двумя квадратами – результаты большого числа химических анализов, выраженных в процент – эквивалентной (мольной) форме, можно показать на треугольниках анионного и катионного состава в сочетании с квадратами (рисунок 3). После построения двух равносторонних треугольников, их стороны делятся на 10 частей и через полученные точки проводятся линии параллельные каждой стороне. В вершинах треугольника анионного состава размещаются анионы 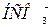 ,
, 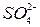 , Cl-, вершины другого треугольника отведены катионами Са, Mg2+, (Na++К+). Точки в вершинах треугольников характеризует 100% содержание ионов, стороны расположенные против вершин соответствуют их нулевому содержанию, линии параллельные – сторонам образуют шкалу, градуированную через 10 процентов (от 10 до 90% ммоль). Пользуясь этой шкалой, проводя линии, соответствующие процентному содержанию анионов и катионов в исследуемой воде, находим точки пересечения прямых.
, Cl-, вершины другого треугольника отведены катионами Са, Mg2+, (Na++К+). Точки в вершинах треугольников характеризует 100% содержание ионов, стороны расположенные против вершин соответствуют их нулевому содержанию, линии параллельные – сторонам образуют шкалу, градуированную через 10 процентов (от 10 до 90% ммоль). Пользуясь этой шкалой, проводя линии, соответствующие процентному содержанию анионов и катионов в исследуемой воде, находим точки пересечения прямых.
Химический состав воды изображается, таким образом, в виде точек на треугольниках анионного и катионного состава. Обе точки получают единое цифровое обозначение, соответствующее порядковому номеру анализа, нанесённого на графах. Проектируя на квадраты результаты анализа, удобно определить типы вод. Для типов I и II квадрат располагается слева от треугольников, а Ша и Шб – справа. При наличии всех четырёх типов вод квадраты и треугольники сочетаются как на рисунок 3.
ЗАКЛЮЧЕНИЕ
Вода является сильнейшим растворителем горных пород и представляет раствор сложного состава с очень широким диапазоном содержания растворенных веществ как по числу, так и по концентрации. Химический состав воды определяет возможность применения её для различных целей (хозяйственно-питьевого использования, орошения), а также агрессивное свойство по отношению к цементу бетона. Количественное содержание этих ионов в исследуемой воде устанавливается методами аналитической химии.
Основываясь на знаниях, полученных по курсу «Общая химия» проделать анализ химического состава природных вод, уметь графически изображать их результаты, оценивать пригодность для различных целей.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
а) Основная литература
1 Абдрахманов, Р. Ф. Пресные подземные и минеральные лечебные воды Башкортостана [Электронный ресурс] / Р. Ф. Абдрахманов ; Российская академия наук, Уфимский научный центр, Ин-т геологии, Академия наук Республики Башкортостан, Отделение наук о земле и природных ресурсов. - Уфа : Гилем, 2014. - 429 с. – Режим доступа: http://biblio.bsau.ru/metodic/28234.pdf
2 Абдрахманов, Р. Ф. Геохимия и формирование подземных вод Южного Урала [Электронный ресурс] / Р. Ф.Абдрахманов, В. Г. Попов ; отв. ред. В. Н. Пучков ; Российская академия наук, Уфимский научный центр, Ин-т геологии, Российская академия естественных наук, Южно-Российский гос. технический ун-т (НПИ). - Уфа: Гилем, 2010. - 420 с. – Режим доступа: http://biblio.bsau.ru/metodic/23668.pdf
3 Ананьев В. П. Специальная инженерная геология [Текст]: учебник / В. П. Ананьев, А. Д. Потапов, Н. А. Филькин. - М. : Высш. шк., 2008.
4 Ананьев, В. П. Инженерная геология и гидрогеология [Текст]: Учебник / В. П. Ананьев, Л. В. Передельский. - М. : Высш. шк., 1980.
5 Ананьев, В. П.Инженерная геология: Учебник / Ананьев В.П., Потапов А.Д., Юлин А.Н. - 7-е изд., стер. - М.: НИЦ ИНФРА-М, 2016. - 575 с. – Режим доступа: http://znanium.com/bookread2.php?book=487346
6 Ананьев, В. П.Специальная инженерная геология[Электронный ресурс]: учебник/ В. П. Ананьев , А. Д. Потапов , Н. А. Филькин - М.: НИЦ ИНФРА-М, 2016. - 263 с – Режим доступа :http://znanium.com/bookread2.php?book=487350
7 Добров, Э. М. Инженерная геология [Текст]: учеб. пособие / Э. М. Добров. - 2-е изд., стер. - М. : Академия, 2008.
8 Добров, Э. М. Инженерная геология [Электронный ресурс] : учеб. пособие для студ. вузов, обучающихся по спец. "Автомобильные дороги и аэродромы" направления подготовки "Транспортное строительство" : допущено УМО по образованию / Э. М. Добров. - М. : Издательский центр "Академия", 2008. - 219 с. – Режим доступа: http://biblio.bsau.ru/metodic/18233.djvu
9 Инженерная геология [Текст]: учебник для студ. вузов, обуч. по строительным спец. : рек. М-вом образования и науки РФ / В. П. Ананьев, А. Д. Потапов. - 6-е изд., стер. - М. : Высш. шк., 2009.
10 Короновский, Н. В. Геология [Текст] : учебник для студ. вузов, обуч. по экологическим спец. : допущено УМО по образованию / Н. В. Короновский , Н. А. Ясаманов - 5-е изд., стер. - М. : Академия, 2008. - 446 с.
11 Лолаев, А. Б. Инженерная геология и грунтоведение [Текст] : учебное пособие для использования в учебном процессе образовательных учреждений, реализующих программы среднего профессионального образования / А. Б. Лолаев, В. В. Бутюгин. - Ростов-на-Дону : Феникс, 2017. - 350 с.
12 Передельский, Л. В. Инженерная геология [Текст]: учеб. пособие / Л. В. Передельский, О. Е. Приходченко. - 2-е изд., доп. и перераб. - Ростов н/Д : Феникс, 2009.
13 Сергеев, Е. М. Инженерная геология[Текст] : учебник для вузов / Е. М. Сергеев. – М: Альянс, 2011
14 Суворов, А. К. Геология с основам гидрологии [Текст]: учеб.пособие / А. К. Суворов. – М. : КолосС, 2007. - 207с.
15 Швецов, Г. И. Инженерная геология, механика грунтов, основания и фундаменты [Текст]: Учеб. / Г. И. Швецов. - 2-е изд., перераб. и доп. - М. : Высш. шк., 1997.
б) Дополнительная литература
1. Бондарик Г.К., Ярг Л.А. Инженерно-геологические изыскания. – М.: КДУ, 2007. - 424с
2. Вознесенский Е.А., Королев В.А., Трофимов В.Т. Грунтоведение. - М.: МГУ, Наука. 2005. - 1024с.
3. Добровольский А.Д., Добролюбов С.А., Михайлов В.Н. Гидрология. - М.: Высшая школа. 2008. - 463с.
4. Толстой, М.П., Малыгин В.А. Геология и гидрогеология. М.: Недра,1988.
5. Пособие к лабораторным занятиям по общей геологии: Учеб. пособие для вузов / В.Н. Павлинов, А.Е. Михайлов, Д.С. Кизевальтер и др. – 4-е изд., перераб. и доп. – М.: Недра, 1983. – 161 с.
6. Кац, Д. М. Основы геологии и гидрогеология [Текст]: учебник / Д. М. Кац. - М. : Колос, 1981.
7. Швецов, Г. И. Инженерная геология, механика грунтов, основания и фундаменты [Текст] : учеб. для студ. вузов / Г. И. Швецов. - 2-е изд., перераб. и доп. - М. : Высш. шк., 1997. - 320 с.
8. Борголов, И. Б. Сельскохозяйственная геология [Текст]: учеб. пособие / И. Б. Борголов. - Иркутск: Изд-во Иркутского ун-та, 2000.
9. Короновский Н.В., Ясаманов Н.А. Геология: учебник для экологических специальностей вузов. - М: Академия. 2006. - 448с.
10. Швецов Г. И. Инженерная геология, механика грунтов, основания и фундаменты [Текст]: Учеб. / Г. И. Швецов. - 2-е изд., перераб. и доп. - М. : Высш. шк., 1997.
11. Ананьев В. П. Инженерная геология и гидрогеология [Текст]: Учебник / В. П. Ананьев, Л. В. Передельский. - М. : Высш. шк., 1980.
12. Милютин А.Г. Геология. - М.:Высшая школа. 2008. - 448с.
13. Болтрамович С.Ф., Жиров А.И., Ласточкин А.Н. Геоморфология. - М.: Академия. 2005. - 528с.
14. Караулов В.Б., Никитина М.И. Геология: основные понятия и термины. Справочное пособие. – Едиториал УРСС, 2007. - 152с.
15. Кашперюк П.И., Потапов А.Д., Глумова Г.М., Юлин А.Н. Инженерная геология и геоэкология. Учебное пособие. – М.: МГСУ, 2007. - 150с.
16. Предельский Л.В., Приходченко О.Е. Инженерная геология. - Р.-Д.: Феникс. 2009. - 460с.
17. Чернышев С.Н., Чумаченко А.Н., Ревелис И.Л. Задачи и упражнения по инженерной геологии. Учебное пособие. – М.: Высшая школа, 2004. - 254с.
18. Шестаков В.М. Гидрогеодинамика. - М.: МГУ. 1995. - 368с.
в) перечень ресурсов информационно-телекоммуникационной сети «Интернет», необходимых для освоения дисциплины (модуля)
1. Электронная библиотека Башкирского ГАУ (http://biblio.bsau.ru) – собственная
2. Электронно-библиотечная система издательства «ЛАНЬ» (http://e.lanbook.com/) – сторонняя
3. Электронная библиотечная система ZNANIUM.COM (http://znanium.com/) – сторонняя
4. Электронно-библиотечная система издательства «ЮРАЙТ» (www.biblio-online.ru) – сторонняя
5. Электронная библиотека технического вуза ООО "Политехрсурс" (www.studentlibrary.ru) – сторонняя
6. Электронная библиотечная система ИД «ТРОИЦКИЙ МОСТ» (www.trmost.ru/lib-main.shtml?pwd) – сторонняя
7. Электронная библиотечная система «BOOK.ru» издательства «КноРус медиа» (https://www.book.ru/) - сторонняя
8. Электронная библиотечная система eLIBRARY.RU (http://elibrary.ru) – сторонняя
9. Электронная библиотека диссертаций (ЭБД) РГБ (www.diss.rsl.ru/) – сторонняя
10. ФГБНУ Центральная научная сельскохозяйственная библиотека Россельхозакадемии (www.cnshb.ru/) – сторонняя
|
| ||
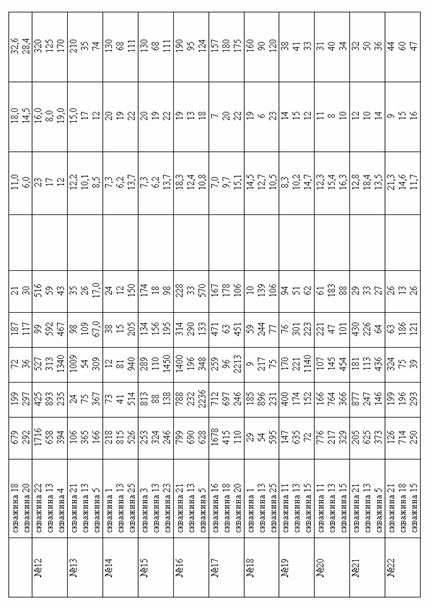
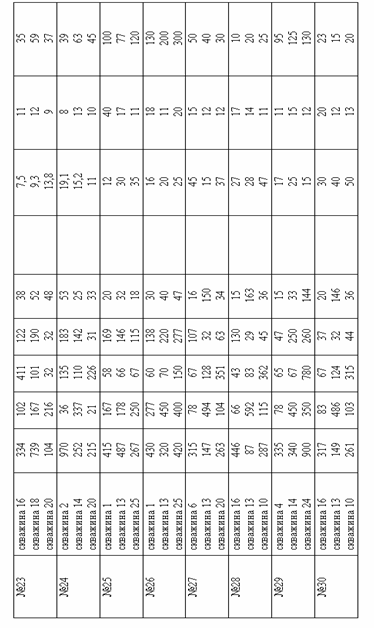
| Продолжение приложения Б |
| |
| Продолжение приложения Б |
|
Б1.О.18 ГЕОЛОГИЯ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к выполнению расчетно-графической и контрольной работ
ХИМИЧЕСКИЙ АНАЛИЗ ПРИРОДНЫХ ВОД,
Дата: 2019-02-25, просмотров: 541.