Иммуноферментный анализ или метод — выявление антигенов с помощью соответствующих им антител, конъюгированных с ферментом-меткой (пероксидазой хрена, бета-галактозидазой или щелочной фосфатазой). После соединения антигена с меченной ферментом иммунной сывороткой в смесь добавляют субстрат/хромоген. Субстрат расщепляется ферментом и изменяется цвет продукта реакции — интенсивность окраски прямо пропорциональна количеству связавшихся молекул антигена и антител. ИФА применяют для диагностики вирусных, бактериальных и паразитарных болезней, в частности для диагностики ВИЧ-инфекций, гепатита В и др., а также определения гормонов, ферментов, лекарственных препаратов и других биологически активных веществ, содержащихся в исследуемом материале в минорных концентрациях (1010-1012 г/л).
Твердофазный ИФА — вариант теста, когда один из компонентов иммунной реакции (антиген или антитело) сорбирован на твердом носителе, напр., в лунках планшеток из полистирола. Компоненты выявляют добавлением меченых антител или антигенов. При положительном результате изменяется цвет хромогена. Каждый раз после добавления очередного компонента из лунок удаляют несвязавшиеся реагенты путем промывания,
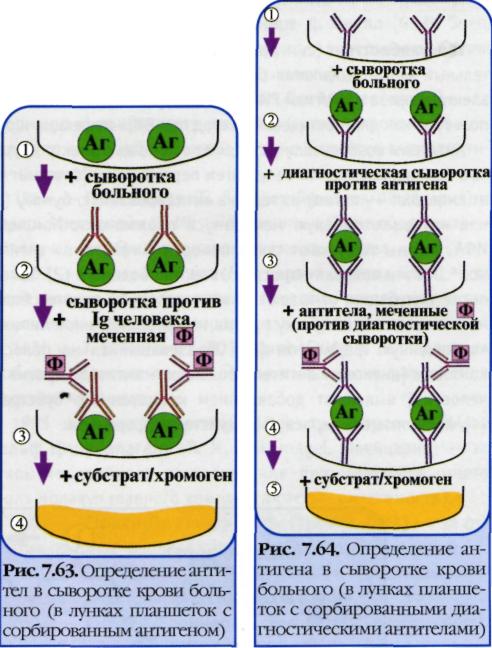
I. При определении антител (левый рисунок) в лунки планшеток с сорбированным антигеном последовательно добавляют сыворотку крови больного, антиглобулиновую сыворотку, меченную ферментом, и субстрат/хромоген для фермента.
II. При определении антигена (правый рисунок) в лунки с сорбированными антителами вносят антиген (напр., сыворотку крови с искомым антигеном), добавляют диагностическую сыворотку против него и вторичные антитела (против диагностической сыворотки), меченные ферментом, а затем субстрат/хромоген для фермента.
Конкурентный ИФА для определения антигенов: искомый антиген и меченный ферментом антиген конкурируют друг с другом за связывание ограниченного количества антител иммунной сыворотки.
Другой тест - Конкурентный ИФА для определения антител: искомые антитела и меченные ферментом антитела конкурируют друг с другом за антигены, сорбированные на твердой фазе.
Иммуноблоттинг — высокочувствительный метод выявления белков, основанный на сочетании электрофореза и ИФА или РИА. Иммуноблоттинг используют как диагностический метод при ВИЧ-инфекции и др.
Антигены возбудителя разделяют с помощью электрофореза в полиакриламидном геле, затем переносят их из геля на активированную бумагу или нитроцеллюлозную мембрану и проявляют с помощью ИФА. Фирмы выпускают такие полоски с «блотами» антигенов. На эти полоски наносят сыворотку больного. Затем, после инкубации, отмывают от несвязавшихся антител больного и наносят сыворотку против иммуноглобулинов человека, меченную ферментом. Образовавшийся на полоске комплекс [антиген + антитело больного + антитело против Ig человека] выявляют добавлением хромогенного субстрата, изменяющего окраску под действием фермента.
57. Вакцины. Определение. Современная классификация вакцин. Требования, предъявляемые к вакцинным препаратам.
Вакцина — медицинский препарат, предназначенный для создания иммунитета к инфекционным болезням.
Классификации вакцин:
1.Живые вакцины - препараты, действующим началом в которых являются ослабленные тем или иным способом, потерявшие свою вирулентность, но сохранившие специфическую антигенность штаммы патогенных бактерий. Примером таких вакцин являются БЦЖ и вакцина против натуральной оспы человека, в качестве которой используется непатогенный для человека вирус оспы коров.
2.Инактивированные (убитые) вакцины – препараты, в качестве действующего начала включающие убитые химическим или физическим способом культуры патогенных вирусов или бактерий, (клеточные, вирионные) или же извлечённые из патогенных микробов комплексы антигенов, содержащие в своём составе проективные антигены (субклеточные, субвирионные вакцины). В препараты иногда добавляют консерванты и адьюванты.
Молекулярные вакцины – в них антиген находится в молекулярной форме или даже в виде фрагментов его молекул, определяющих специфичность т. е. в виде эпитопов, детерминант.
Корпускулярные вакцины – содержащие в своем составе протективный антиген
3.Анатоксины относятся к числу наиболее эффективных препаратов. Принцип получения – токсин соответствующей бактерии в молекулярном виде превращают в нетоксичную, но сохранившую свою антигенную специфичность форму путем воздействия 0.4% формальдегида при 37t в течение 3-4 недель, далее анатоксин концентрируют, очищают, добавляют адьюванты.
4.Синтетические вакцины. Молекулы эпитопов сами по себе не обладают высокой иммуногенностью для повышения их антигенных свойств эти молекулы сшиваются с полимерным крупномолекулярным безвредным веществом, иногда добавляют адьюванты.
5.Ассоциированные вакцины – препараты, включающие несколько разнородных антигенов.
Требования, предъявляемые к современным вакцинам:
Иммуногенность;
Низкая реактогенность (аллергенность);
Не должны обладать тератогенностью, онкогенностью;
Штаммы, из которых приготовлена вакцина, должны быть генетически стабильны;
Длительный срок хранения;
Технологичность производства;
Простота и доступность в применении.
Вакцинопрофилактика. Вакцины из живых бактерий и вирусов. Принципы получения вакцинных штаммов. Способы аттенуации. Примеры вакцин из живых бактерий и вирусов. Преимущества и недостатки аттенуированных вакцин.
Первое поколение вакцин – цельномикробные, цельновирионные
I. Живые:
· Дивергентные – содержат микроорганизмы находящиеся в близком родстве с возбудителями инфекционных заболеваний и обладающие перекрестной иммуногенностью.
1. БЦЖ – против туберкулеза.
2. Ротовирусная.
3. Оспенная (вирус коровьего бешенства).
4. Аттенуированные (ослабленные) вакцины: (Аттенуация (ослабление) возможна путём воздействия на штамм химических (мутагены) и физических (температура) факторов или посредством длительных пассажей через невосприимчивый организм)
Очень опасные и заразные:
· Чумная;
· Туляремийная;
· Сибиреязвенная;
· Бруцеллезная (2 вида);
Против вирусов:
· Паратитная;
· Коревая;
· Краснушная;
· Гриппозная живая, сухая, интраназальная, детская;
· Полимиелитная пероральная типов 1,2 и 3 из штаммов Сэбина (ОПР);
· Герпетическая;
· Аденовирусная;
Вакцины против
· Сыпно-тифозная;
· Вакцина желтой лихорадки;
· Вакцина лихорадки Ку.
Преимущества живых вакцин:
1. По механизму действия они напоминают дикие штаммы и вытесняют последние из организма;
2. Формируют эффективный гуморальный и клеточный иммунитет, так как размножаются и циркулируют в организме;
3. Легко проводить вакцинацию, так как необходимы небольшие дозы и требуется только однократная вакцинация.
Недостатки:
1. Содержат до 99% балласта – реактогенны (много побочных действий);
2. Способны вызывать мутации клеток организма;
3. Содержат вирусы-загрязнители;
4. Трудно дозируются, требуют особых условий хранения;
5. Есть возможность возвращения в вирулентную форму.
!!!Живые вакцины не ставят людям с иммунодефицитами!!!
Между введениями живых вакцин рекомендован интервал не менее 1 месяца, в противном случае возможны тяжелые побочные реакции, иммунный ответ может быть пониженным.
Вакцинопрофилактика. Вакцины из убитых бактерий и вирусов. Принципы приготовления. Примеры убитых вакцин. Ассоциированные вакцины. Преимущества и недостатки убитых вакцин.
II. Убитые (инактивированные). Убитые вакцины изготовляют из микрооргнизмов, убитых физическим (нагревание) или химическим (фенол, формалин, ацетон) методами.
1. Брюшно-тифозная спиртовая вакцина;
2. Лептоспирозная;
3. Холерная;
4. Имовакс Полио;
5. Гриппозная инактивирвоанная жидкая;
6. Вакцина против клещевого энцефалита;
7. ЭнцеВир, Энцепур (клещевой энцефалит);
8. Антирабическая;
9. Паратифная В;
10. Хаврикс (гепатит А);
11. Аваксим (Гепатит А);
12. Геп-А-ин-ВАК (Гепатит А).
Преимущества:
1. Стабильны и безопасны;
2. Легко дозируются.
Недостатки:
1. Реактогенны;
2. Содержат фенол;
3. Требуется вакцинация.
Ассоциированные вакцины.
Это комбинированные вакцины, в результате действия которых иммунтет формируется одновременно к нескольким инфекциям.
АКДС (ассоциированная коклюшно-дифтерийная столбнячная) – из убитых коклюшных бактерий и инактивированных экзотоксинов дифтерии и столбняка.
Тривакцина – из аттенуированных (ослабленных) вирусов кори, краснухи и праротита.
Тетракокк – из анатоксинов дифтерии и столбняка и убитых коклюшных бактерий и инактивированных вирусов полиомиелита.
Молекулярные вакцины: анатоксины. Получение. Использование анатоксинов для профилактики инфекционных заболеваний. Примеры вакцин.
Молекулярные вакцины – в них антиген находится в молекулярной форме или даже в виде фрагментов его молекул, определяющих специфичность т. е. в виде эпитопов, детерминант.
В процессе культивирования природных патогенных микробов можно получить протективный антиген, синтезируемый этими бактериями токсин затем превращается в анатоксин, сохраняющий специфическую антигенность и иммуногенность. Анатоксины являются одним из видов молекулярных вакцин. Анатоксины – препараты, полученные из бактериальных экзотоксинов, полностью лишенные своих токсических свойств, но сохранившие антигенные и иммуногенные свойства. Получение: токсигенные бактерии выращивают на жидких средах, фильтруют с помощью бактериальных фильтров для удаления микробных тел, к фильтрату добавляют 0,4% формалина и выдерживают в термостате при 30-40t на 4 недели до полного исчезновения токсических свойств, проверяют на стерильность, токсигенность и иммуногенность. Эти препараты называются нативными анатоксинам, в настоящее время почти не используются, т. к. содержат большое количество балластных веществ, неблагоприятно влияющих на организм. Анатоксины подвергаю физической и химической очистке, адсорбируют на адъювантах. Такие препараты называются адсорбированными высокоочищенными концентрированными анатоксинами.
Титрование анатоксинов в реакции фолликуляции производят по стандартной фолликулирующей атитоксической сыворотке, в которой известно количество антитоксических единиц. 1 антигенная единица анатоксина обозначается Lf, это то количество анатоксина, которое вступает в реакцию фолликуляции с 1 единицей дифтерийного анатоксина.
Анатоксины применяются для профилактики и реже, для лечения токсинемических инфекций дифтерия, газовая гангрена, ботулизм, столбняк). Так же анатоксины применяются для получения антитоксических сывороток путем гипериммунизации животных.
Примеры препаратов: АКДС, АДС, адсорбированный стафилококковый анатоксин, ботулинистический анатоксин, анатоксины из экзотоксинов возбудителей газовых инфекций.
61. Генно-инженерные вакцины. Получение. Применение. Преимущества и недостатки.
Генно-инженерные вакцины – это препараты, полученные с помощью биотехнологии, которая по сути сводиться к генетической рекомбинации .
Для начала получают ген, который должен быть встроен в геном реципиента. Небольшие гены могут быть получены методом химического синтеза. Для этого расшифровывается число и последовательность аминокислот в белковой молекуле вещества, затем по этим данным узнают очерёдность нуклеотидов в гене, далее следует синтез гена химическим путем.
Крупные структуры, которые довольно сложно синтезировать получаются путем выделения(клонирования), прицельного выщепления этих генетических образований с помощью рестриктаз.
Полученный одним из способов целевой ген с помощью ферментов сшивается с другим геном, который используется в качестве вектора для встраивания гибридного гена в клетку. Вектором могут служить плазмиды, бактериофаги, вирусы человека и животных. Экспрессируемый ген встраивается в бактериальную или животную клетку, которая начинает синтезировать несвойственное ей ранее вещество, кодируемое эксперссируемым геном.
В качестве реципиентов экспрессируемого гена чаще всего используется E. coli, B. subtilis, псевдомонады, дрожжи, вирусы. некоторые штаммы способны переключаться на синтез чужеродного вещества до 50% своих синтетических возможностей – эти штамм называются суперпродуцентами.
Иногда к генно-инженерным вакцинам добавляется адъювант.
Примерами таких вакцин служат вакцина против гепатита В (энджерикс), сифилиса, холеры, бруцеллёза, гриппа, бешенства.
Есть определённые сложности в разработке и применении:
- длительное время к генно-инженерным препаратам относились настороженно.
- на разработку технологии для получения вакцины затрачиваются значительные средства
- при получении препаратов данным способом возникает вопрос об идентичности полученного материала природному веществу.
Третье поколение вакцин – генно-иненерные вакцины
IV. Биосинтетические – искусственно созданные антигены микробов. Для их получения используют дрожжевую клетку, в которую встраивают ген патогенного микроорганизма, отвечающий за синтез данного антигена.
Вакцины от Гепатита В:
· Энджерикс (Бельгия);
· ДНК-рекомбинантная (США);
· Вакцина гепатита В рекомбинантная дрожжевая (Куба);
· Комбиотех ЛТД (Россия).
Преимущества:
4. Меньше побочных эффектов, так как не содержат микроорганизмов;
5. Вызывают узкоспецифический иммуитет;
6. Возможно комплектование по иммуногенным свойствам.
Недостатки:
Менее эффективны по сравнению с традиционными, так как вирусы вариабельны.
V. Векторные (рекомбинантные) вакцины – получают встраиванием генов различных возбудителей в геном ослабленного вируса или бактерии (вектор). Иммунитет формируется к нескольким инфекциям.
| Вирус коровьей оспы | Рекомбинантные вакцины: 3. Моновалентные: · Гриппозная, герпетическая, гепатит В · Малярийный плазмодий; 4. Поивалентные · Против гепатита В, бешенства, клещевого энцефалита, ветряной оспы, гепатита А. |
| Сальмонеллы | Против гепатита В |
VI. Рибосомальные вакцины – получают путем выделения микробных рибосом с матрицей иРНК = иммуномодуляторы.
ИРС-19;
Бронхомунал;
Рибомунил.
Дата: 2019-02-25, просмотров: 507.