МОДЕЛИРОВАНИЕ И РАСЧЕТ РЕАКЦИОННЫХ ПРОЦЕССОВ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ
Методические указания к лабораторному практикуму
Самара
Самарский государственный технический университет
2018
Печатается по решению методического совета нефтетехнологического факультета
УДК 681.3.068(07)
Моделирование и расчет реакционных процессов химической технологии : метод. указ. к лаб. работе / Сост. С.П.Шкаруппа. – Самара: Самар. гос. техн. ун-т, 2018. – 32 с.:ил.
Рассматривается применение метода математического моделирования для описания и исследования химико-технологических процессов, расчета химических ректоров.
Методические материалы предназначены для студентов, обучающихся по следующим направлениям бакалавриата 180302 Химическая технология, Энерго- и ресурсосберегающие процессы в химической технологии, нефтехимии и биотехнологии.
Рецензент канд. техн. наук Н.Г. Кац
© С.П.Шкаруппа, составление, 2017
©Самарский государственный
технический университет, 2017
Материальный баланс.
|
|
|
|
= + +
Тепловой баланс.
|
|
|
|
= + +
Гидросопротивление. (Фиксирует скорость изменения давления в системе).
|
|
|
= +
i = 1…..М - номер потока и их число,
j = 1…..N - суммарное количество компонентов во всех потоках и фазах
Общее число уравнений в системе:
1. Материальный баланс – по количеству компонентов в системе с учетом фазового состава
Уравнений материального баланса = N*M.
2. Тепловой баланс – по количеству независимых потоков.
Уравнений теплового баланса = М
3. Гидродинамика – по количеству независимых потоков.
Уравнений гидродинамики = М
Математические модели химических аппаратов строятся на основе блочного принципа с использованием гидродинамических моделей, учитывающих характер распределения времени пребывания частиц потока реагирующей смеси в данном объёме.
Основу моделирования химических реакторов составляет описание блока кинетической модели.
КИНЕТИКА.
Это отрасль науки, которая занимается изучением скоростей химических реакций. Скорость химической реакции представляет собой первую производную концентрации по времени: r = dC/dt.
Процедура получения кинетического уравнения.
1. Поставить кинетический эксперимент, получить кривые C=f (T,t).
2. Выбрать вид кинетической модели.
3. Определить порядок реакции.
4. Рассчитать константы скорости и вычислить энергию активации.
5. Проверить адекватность кинетического описания. При неадекватности возврат к пунктам 1 или 2.
Уравнения, основанные на классическом законе действующих масс называется классической или формальной кинетикой. Некоторые виды реакций описываются уравнениями специального вида. Вид этих уравнений определяется как теоретически так и на основе экспериментальных данных. Подобная кинетика называется неформальной.
Скорость сложной реакции по любому веществу равна алгебраической сумме скоростей всех стадий по этому веществу. Стадия – это однонаправленный химический процесс, в котором участвуют два или три компонента: исходные для данной стадии и продукт данной стадии.
Н-р: А ® В
А+В ® С
Если в ходе химической реакции концентрация компонента уменьшается, то выражение, описывающее скорость данной реакции берётся со знаком минус. Если же вещество накапливается, то с плюсом. Обобщённое уравнение кинетики многостадийной реакции имеет вид:
rj = Sai *k *PCjn,
Где a - стехиометрический коэффициент,
j – номер компонента.
Правила построения кинетической модели.
1. Задать исходную информацию в виде схемы реакции.
2. В модели будет столько уравнений, сколько веществ в химической системе.
3. В каждом уравнении - столько слагаемых, сколько реакций влияет на концентрацию данного компонента.
4. Каждое слагаемое – это произведение стехиометрических коэффициентов, константы скорости и концентрации вещества в степени своего порядка.
5. Константа скорости умножается на концентрацию компонента, который является исходным для данной стадии.
Тепловой баланс системы.
DТ=DТкин.+DТг/д +DТт/о
Температура принадлежит к числу факторов наиболее сильно влияющих на скорость химической реакции, поскольку протекание большинства химических процессов в значительной степени зависит от явления переноса тепла в системе.
Величина DТкинетич в структуре теплового баланса для всех типов моделей записывается как сумма произведений скорости каждой стадии на соответствующий ей тепловой эффект. Скорость стадии берётся по модулю, а знак сомножителя определяется знаком теплового эффекта.
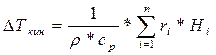 ,
,
где r - плотность реакционной смеси,
ср – теплоемкость реакционной смеси.
Н-р: 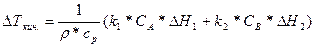
Следующая составляющая в уравнении теплового баланса гидродинамическая DТгидр, характеризует каким образом изменяется температура в потоке в зависимости от скорости перемешивания потока и конструкционных особенностей аппарата, в котором происходит процесс.
1). Модель идеальное смешение.
Гидродинамическая составляющая описывается следующим уравнением:
 ;
; 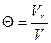 ; где Т0 – температура потока на входе в аппарат, Т – температура на выходе из аппарата
; где Т0 – температура потока на входе в аппарат, Т – температура на выходе из аппарата
2). Модель идеальное вытеснение.
Гидродинамическая составляющая описывается следующим уравнением:
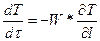 .
.
3). Модель диффузионное однопараметрическое вытеснение.
Гидродинамическая составляющая описывается следующим уравнением:
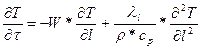 ,где ll – продольная теплопроводность турбулентного потока
,где ll – продольная теплопроводность турбулентного потока
4).Модель диффузионное двухпараметрическое вытеснение.
Гидродинамическая составляющая описывается следующим уравнением:
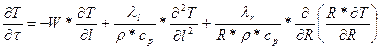
lR – поперечная теплопроводность
5). Ячеечная модель.
Гидродинамическая модель:
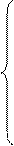
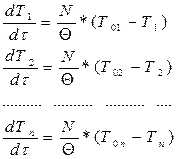
Теплообмен - D Т то.
Учёт стохастической составляющей модели теплообменной аппаратуры позволяет найти распределение температур по длине поверхности теплообмена. Обычно расчёт теплообменной аппаратуры выполняется в следующей последовательности:
1. Составляется тепловой баланс всех потоков приводящих и отводящих тепло Qприх.=Qрасх.
Qпр.=G*Cр*(Тнач - Ткон)
G-количество теплоносителя , Cр- теплоноситель
Тнач,Ткон -начальная и конечная температура теплоносителя.
2). Определяется поверхность теплообмена
F=Qт./k Dtср.t
Анализ процессов, связанных с отводом тепла и теплообменом базируется на исследовании материальных моделей этих процессов, представляющих собой определенные варианты уравнения теплового баланса.
Идеальное смешение.
Модель основана на предположении о полном смешении теплоносителя, поэтому его температура будет постоянной по длине теплообменника.

где К – коэффициент теплопередачи,
F –поверхность теплопередачи,
Т1 –температура потока в аппарате,
Т2 – температура теплоносителя,
Vr – объем аппарата.
Знак «+» - тепло поступает в систему, знак «-» - отвод тепла из системы
Идеальное вытеснение.
В основе модели лежат допущения о постоянстве температуры в поперечном сечении и отсутствии продольного перемешивания.
 ,
,
где dR- диаметр трубы теплообменника.
В зависимости от тепловых режимов все реакторы делятся на:
- изотермические,
- адиабатические ,
- политропные.
В изотермических для поддержания постоянной температуры необходимо подводить или отводить тепло. Его количество соответствует суммарному тепловому эффекту всех реакций протекающих в системе. Так как в таком реакторе температура постоянна, то уравнения теплового баланса нет.
DТ= const. 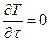
Однако эти реактора сравнительно редко используются в крупномасштабных производствах из-за высокой стоимости оборудования для съёма или подвода тепла.
Реактор называется адиабатическим, если в системе выделяемое в результате химической реакции тепло полностью идёт на изменение температуры при этом теплообмен с окружающей средой полностью отсутствует. В структуре теплового баланса отсутствует третья составляющая DTто=0.
В политропном реакторе изменение температурного режима в системе происходит и за счёт химической реакции и за счёт теплообмена с окружающей средой.
Задания для выполнения лабораторной работы
ВАРИАНТ 1
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
D E (k5) A C (k6)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 6,27E 22 k02 = 2,92E 14 k03 = 2,33E 14
k04 = 8,1E 11 k05 = 1,54E 11 k06 = 2,38E 20
энергии активации (кДж/моль)
Е1 =2,08Е 5 Е2 = 1,35Е 5 Е3 =1,35Е 5
Е4 = 1,15Е 5 Е5 = 1,15Е 5 Е6 = 2,01Е 5
Тепловые эффекты реакции (Дж/кг)
Н1 =700 Н2 = 300 Н3 = 300 Н4 = 200 Н5 = - 100 Н6 = 100
Начальная температура сырья Т= 480 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 3000 Дж/кг*К
Коэффициент теплопередачи К = 410 Вт/м2*К
Плотность сырья r = 700 кг/м3
Поверхность теплопередачи F = 1,2 м2
Объем реактора V = 0,22 м3
Расход сырья С = 0,07 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
__________________________________________________
ВАРИАНТ 2
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А В (k5) В C (k6) С D (k7) A C (k8)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 1,4E 18 k02 = 4,31E 16 k03 = 2,54E 18
k04 = 2,071E 16 k05 = 7,77E 8 k06 = 8,3E 11 k 07 = 2,32E 10 k 08 = 2,713E 17
энергии активации (кДж/моль)
Е1 = 1,3Е 5 Е2 = 1,2Е 5 Е3 =1,34Е 5 Е4 = 1,2Е 5
Е5 = 6,69Е 5 Е6 = 9,36Е 5 Е 7 = 8,09Е 5 Е 8 = 1,34Е 5
Тепловые эффекты реакции (Дж/кг)
Н1 = 1300 Н2 = 200 Н3 = 200 Н4 = 200
Н5 = - 100 Н6 = 100 Н7 = 2 Н8 = 6
Начальная температура сырья Т= 380 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 2600 Дж/кг*К
Коэффициент теплопередачи К = 530 Вт/м2*К
Плотность сырья r = 620 кг/м3
Поверхность теплопередачи F = 1,6 м2
Объем реактора V = 0,38 м3
Расход сырья С = 0,02 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
ВАРИАНТ 3
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А ® С (k5)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 8,63E 13 k02 = 1,71E 7 k03 = 1,19E 8 k04 = 5,5E 10 k05 = 4,48E 5
энергии активации (кДж/моль)
Е1 = 9,85Е 4 Е2 = 5,56Е 4 Е3 = 6,27Е 4
Е4 = 8,2Е 4 Е5 = 4,79Е 4
Тепловые эффекты реакции (Дж/кг)
Н1 = 700 Н2 = 300 Н3 = 300 Н4 = 200 Н5 = 100
Начальная температура сырья Т= 370 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 1900 Дж/кг*К
Коэффициент теплопередачи К = 470 Вт/м2*К
Плотность сырья r = 870 кг/м3
Поверхность теплопередачи F = 2,3 м2
Объем реактора V = 0,17 м3
Расход сырья С = 0,014 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
ВАРИАНТ 4
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А В (k5) В C (k6) С D (k7)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 6,65E 7 k02 = 1,22E 19 k03 = 2,25E 11
k04 = 1,071E 15 k05 = 1,77E 18 k06 = 1,14E 11 k 07 = 1,15E 7
энергии активации (кДж/моль)
Е1 = 5,68Е 4 Е2 = 1,49Е 5 Е3 = 8,99Е 4 Е4 = 1,17Е 5
Е5 = 1,44Е 5 Е6 = 8,36Е 4 Е 7 = 5,68Е 4
Тепловые эффекты реакции (Дж/кг)
Н1 = 700 Н2 = 200 Н3 = 200 Н4 = 200 Н5 = - 100 Н6 = 10 Н7 = 5
Начальная температура сырья Т= 400 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 2900 Дж/кг*К
Коэффициент теплопередачи К = 730 Вт/м2*К
Плотность сырья r = 660 кг/м3
Поверхность теплопередачи F = 2,6 м2
Объем реактора V = 0,27 м3
Расход сырья С = 0,018 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
ВАРИАНТ 5
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
D С (k5) A C (k6)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 4,27E 22 k02 = 2,92E 14 k03 = 2,33E 14
k04 = 8,1E 11 k05 = 2,54E 11 k06 = 2,38E 20
энергии активации (кДж/моль)
Е1 = 2,08Е 5 Е2 = 1,35Е 5 Е3 =1,35Е 5 Е4 = 1,15Е 5
Е5 = 1,15Е 5 Е6 = 2,01Е 5
Тепловые эффекты реакции (Дж/кг)
Н1 =700 Н2 = 300 Н3 = 300 Н4 = 200 Н5 = - 100 Н6 = 100
Начальная температура сырья Т= 470 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 3000 Дж/кг*К
Коэффициент теплопередачи К = 460 Вт/м2*К
Плотность сырья r = 700 кг/м3
Поверхность теплопередачи F = 1,5 м2
Объем реактора V = 0,22 м3
Расход сырья С = 0,07 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
ВАРИАНТ 6
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А В (k5) В C (k6) С D (k7)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 1,5E 17 k02 = 4,41E 15 k03 = 2,44E 17
k04 = 1,071E 16 k05 = 7,7E 8 k06 = 8,3E 11 k 07 = 2,32E 10
энергии активации (кДж/моль)
Е1 = 1,33Е 5 Е2 = 1,24Е 5 Е3 =1,4Е 5 Е4 = 1,29Е 5
Е5 = 6,9Е 5 Е6 = 9,3Е 5 Е 7 = 8,0Е 5
Тепловые эффекты реакции (Дж/кг)
Н1 = 1300 Н2 = 200 Н3 = 200 Н4 = 200 Н5 = - 100 Н6 = 100 Н7 = 2
Начальная температура сырья Т= 390 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 2900 Дж/кг*К
Коэффициент теплопередачи К = 580 Вт/м2*К
Плотность сырья r = 640 кг/м3
Поверхность теплопередачи F = 1,6 м2
Объем реактора V = 0,38 м3
Расход сырья С = 0,02 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
__________________________________________________________________
ВАРИАНТ 7
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А ® Е (k5)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 8,63E 13 k02 = 1,71E 7 k03 = 1,19E 8 k04 = 5,5E 10 k05 = 4,4E 5
энергии активации (кДж/моль)
Е1 = 9,85Е 4 Е2 = 5,56Е 4 Е3 = 6,27Е 4 Е4 = 8,2Е 4 Е5 = 4,7Е 4
Тепловые эффекты реакции (Дж/кг)
Н1 = 700 Н2 = 300 Н3 = 300 Н4 = 200 Н5 = 100
Начальная температура сырья Т= 370 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 1900 Дж/кг*К
Коэффициент теплопередачи К = 470 Вт/м2*К
Плотность сырья r = 870 кг/м3
Поверхность теплопередачи F = 2,3 м2
Объем реактора V = 0,17 м3
Расход сырья С = 0,014 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
___________________________________________________
ВАРИАНТ 8
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А В (k5) В C (k6)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 3,65E 17 k02 = 1,2E 19 k03 = 2,5E 11 k04 = 1,071E 15
k05 = 1,77E 18 k06 = 1,14E 11
энергии активации (кДж/моль)
Е1 = 5,6Е 4 Е2 = 1,4Е 5 Е3 = 8,99Е 4 Е4 = 1,17Е 5
Е5 = 1,44Е 5 Е6 = 8,36Е 4
Тепловые эффекты реакции (Дж/кг)
Н1 = 700 Н2 = 200 Н3 = 200 Н4 = 200 Н5 = - 100 Н6 = 10
Начальная температура сырья Т= 400 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 2900 Дж/кг*К
Коэффициент теплопередачи К = 730 Вт/м2*К
Плотность сырья r = 660 кг/м3
Поверхность теплопередачи F = 2,6 м2
Объем реактора V = 0,27 м3
Расход сырья С = 0,018 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
ВАРИАНТ 9
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
D E (k5)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 6,27E 22 k02 = 2,92E 14 k03 = 2,33E 14
k04 = 8,1E 11 k05 = 1,54E 11
энергии активации (кДж/моль)
Е1 =2,08Е 5 Е2 = 1,35Е 5 Е3 =1,35Е 5 Е4 = 1,15Е 5 Е5 = 1,15Е 5
Тепловые эффекты реакции (Дж/кг)
Н1 =700 Н2 = 300 Н3 = 300 Н4 = 200 Н5 = - 100
Начальная температура сырья Т= 480 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 3000 Дж/кг*К
Коэффициент теплопередачи К = 410 Вт/м2*К
Плотность сырья r = 700 кг/м3
Поверхность теплопередачи F = 1,2 м2
Объем реактора V = 0,22 м3
Расход сырья С = 0,07 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
__________________________________________________
ВАРИАНТ 10
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А В (k5) В C (k6) С D (k7)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 1,4E 18 k02 = 4,31E 16 k03 = 2,54E 18
k04 = 2,071E 16 k05 = 7,77E 8 k06 = 8,3E 11 k 07 = 2,32E 10
энергии активации (кДж/моль)
Е1 = 1,3Е 5 Е2 = 1,2Е 5 Е3 =1,34Е 5 Е4 = 1,2Е 5
Е5 = 6,69Е 5 Е6 = 9,36Е 5 Е 7 = 8,09Е 5
Тепловые эффекты реакции (Дж/кг)
Н1 = 1300 Н2 = 200 Н3 = 200 Н4 = 200 Н5 = - 100 Н6 = 100 Н7 = 2
Начальная температура сырья Т= 380 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 2600 Дж/кг*К
Коэффициент теплопередачи К = 530 Вт/м2*К
Плотность сырья r = 620 кг/м3
Поверхность теплопередачи F = 1,6 м2
Объем реактора V = 0,38 м3
Расход сырья С = 0,02 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
ВАРИАНТ 11
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А ® С (k5)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 8,63E 13 k02 = 1,71E 7 k03 = 1,19E 8 k04 = 5,5E 10 k05 = 4,48E 5
энергии активации (кДж/моль)
Е1 = 9,85Е 4 Е2 = 5,56Е 4 Е3 = 6,27Е 4 Е4 = 8,2Е 4 Е5 = 4,79Е 4
Тепловые эффекты реакции (Дж/кг)
Н1 = 700 Н2 = 300 Н3 = 300 Н4 = 200 Н5 = 100
Начальная температура сырья Т= 370 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 1900 Дж/кг*К
Коэффициент теплопередачи К = 470 Вт/м2*К
Плотность сырья r = 870 кг/м3
Поверхность теплопередачи F = 2,3 м2
Объем реактора V = 0,17 м3
Расход сырья С = 0,014 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
ВАРИАНТ 12
ПОЛУЧИТЬ ЗАВИСИМОСТЬ КОНЦЕНТРАЦИЙ И ТЕМПЕРАТУРЫ ОТ ВРЕМЕНИ ПРЕБЫВАНИЯ В РЕАКТОРЕ ИДЕАЛЬНОГО СМЕШЕНИЯ(ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ) И РЕАКТОРЕ ИДЕАЛЬНОГО ВЫТЕСНЕНИЯ (ИЗОТЕРМИЧЕСКИЙ И АДИАБАТИЧЕСКИЙ), ГДЕ ПРОТЕКАЮТ РЕАКЦИИ
А ® В (k1) В ® С (k2) С ® D (k3) D ® E (k4)
А В (k5) В C (k6)
Исходные данные:
Предэкспоненциальные множители (с-1)
k01 = 6,65E 7 k02 = 1,22E 19 k03 = 2,25E 11
k04 = 1,071E 15 k05 = 1,77E 18 k06 = 1,14E 11
энергии активации (кДж/моль)
Е1 = 5,68Е 4 Е2 = 1,49Е 5 Е3 = 8,99Е 4 Е4 = 1,17Е 5 Е5 = 1,44Е 5 Е6 = 8,36Е 4
Тепловые эффекты реакции (Дж/кг)
Н1 = 700 Н2 = 200 Н3 = 200 Н4 = 200 Н5 = - 100 Н6 = 10
Начальная температура сырья Т= 400 К
Температура хладагента Тх = 300 К
Теплоемкость ср = 2900 Дж/кг*К
Коэффициент теплопередачи К = 730 Вт/м2*К
Плотность сырья r = 660 кг/м3
Поверхность теплопередачи F = 2,6 м2
Объем реактора V = 0,27 м3
Расход сырья С = 0,018 м3/сек
При расчете реактора идеального вытеснения (изотермический и адиабатический) задать шаг интегрирования 0,05 (5 см) и 0,1 (10см), скорость потока 0,5 м/с, 1 м/с, 5 м/с, 10 м/с
Построить графики зависимости конверсии сырья (вещество А) от скорости потока для РИВ адиабатического и изотермического длиной 0,5м и 1 м.
Вывод : сравнительный анализ влияния гидродинамического и теплового режимов на конверсию сырья. Обосновать выбор типа реактора по результатам выполненных расчетов.
Контрольные вопросы
- Признаки классификации химических реакторов.
- Характеристика РИС и РИВ, конструкции.
- Изотермический, адиабатический реакторы, характеристика, конструкции.
- Возможности и преимущества метода математического моделирования.
- Структура и состав математической модели ХТО.
- Особенности создания математического описания химического реактора. Иерархический подход при разработке математической модели химического реактора.
- Начальные и граничные условия математической модели ХТО.
- Исходные данные для расчета химреактора. Способы представления результатов расчета химреактора.
- Основные показатели эффективности работы реакторного блока
- Как используется теория подобия при расчете химреактора.
СОДЕРЖАНИЕ
| 1 | СТРУКТУРА МАТЕМАТИЧЕСКОЙ МОДЕЛИ. СОСТАВ МАТЕМАТИЧЕСКОГО ОПИСАНИЯ. | 4 |
| 2 | МАТЕМАТИЧЕСКОЕ ОПИСАНИЕ СТРУКТУРЫ ПОТОКОВ В АППАРАТЕ (ГИДРОДИНАМИКА). | 6 |
| 3 | ТЕПЛОВОЙ БАЛАНС СИСТЕМЫ. | 9 |
| 4 | СПОСОБЫ РЕШЕНИЯ ДИФФЕРЕНЦИАЛЬНЫХ УРАВНЕНИЙ. | 15 |
| 5 | Задания для выполнения лабораторной работы | 22 |
Учебное издание
Составитель ШКАРУППА Светлана Петровна
МОДЕЛИРОВАНИЕ И РАСЧЕТ РЕАКЦИОННЫХ ПРОЦЕССОВ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ
Дата: 2019-02-25, просмотров: 405.