СИСТЕМ
В зависимости от состава, давления и температуры углеводороды могут находиться в газообразном, жидком или смешанном, а также в твердом состоянии. Сверху нефтяного месторождения находится газовая шапка, в которой растворено некоторое количество легких углеводородов. Часть газа растворено в нефти, а при определенных условиях, весь газ может полностью быть растворенным в нефти. Залежи углеводородов подразделяются на газовые, газоконденсатные, нефтяные и газогидратные. В газогидратных залежах газ соединяется с водой, образуя твердое состояние. Такие залежи приурочены к районам вечной мерзлоты. В газоконденсатных залежах смесь углеводородов находится в газообразном состоянии, т.е. выше критических точек давления и температуры, при которых жидкая и газообразная фазы одинаковы по свойствам. Плотность газоконденсата 0,6 – 0,82 г/см 3. При снижении пластового давления из газоконденсата выпадают углеводороды в виде жидкости, что отрицательно влияет на технологию добычи нефти.
Фазовые превращения. В процессе разработки месторождений в пласте изменяется давление, температура, соотношение объемов нефти и газа, температура, что сопровождается переходом углеводородов из одной фазы в другую. В стволе скважины при передвижении нефти давление быстро меняется, из нефти выделяется большое количество газа и других компонентов (парафина, смол, серы и др.). Для дальнейшей транспортировки нефти к потребителю извлекают максимально возможное количество газовой фазы.







 Углеводородные газы изменяют объем в зависимости от температуры и давления (рис. 4.1а), находясь в жидком, газовом или двухфазовом состоянии.
Углеводородные газы изменяют объем в зависимости от температуры и давления (рис. 4.1а), находясь в жидком, газовом или двухфазовом состоянии.
Зависимость объема углеводородов от давления и температуры имеет критическую точку С- точка росы или конденсации. В точке С кривые области парообразования (левая) и конденсации (правая) сливаются. Каждая из кривых изменения объема углеводородов от давления и температуры имеет три участка. Левая часть соответствует жидкой фазе, правая – газовой, а центральный горизонтальный участок – двухфазовой газожидкостной области. С приближением газовой или жидкой фазы к критической точке свойства фаз становятся одинаковыми, между ними исчезает поверхность раздела. Кривые, проходящие выше критической точки С, характеризуют состояние непрерывного изменения свойств углеводородов без разделения на жидкую и газовую фазы, поверхность раздела между ними исчезает и плотность среды непрерывно плавно изменяется.
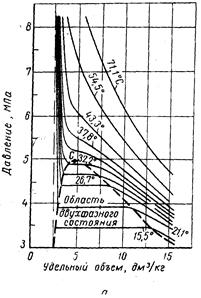
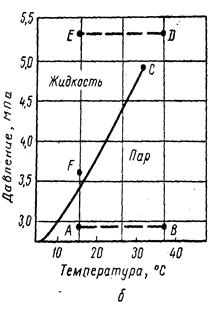
Рис. 4.1. Диаграммы фазового состояния этана
Характерно постоянство давления в двухфазовой области до полного превращения газа в жидкость или жидкости в газ (4.1а). Обе фазы присутствуют в системе при данной температуре, если давление равно упругости насыщенного пара этой жидкости.
Фазовые превращения углеводородов представляются также в координатах «давление – температура». Для однокомпонентной системы кривая точек парообразования и конденсации сливаются, заканчиваясь критической точкой С. Эта точка характеризует наивысшие значения температуры и давления, при которых еще могут существовать две фазы одновременно. Анализируемая зависимость показывает, что одну фазу углеводорода можно перевести в другую, минуя двухфазное состояние, что иллюстрируется графиком (рис. 4.1.б) по линиям АВДЕ F. От точки А газ нагревают до температуры точки В, увеличивают давление до точки Д, затем снижают температуру до точки Е и понижают давление до F. Так по указанной цепочке происходит непрерывное изменение свойств газа, и вещество приобретает свойства жидкости.
Если система многокомпонентная, то она подчинена более сложным зависимостям.
Многокомпонентные углеводородные системы имеют, подобные на однокомпонентную, зависимости фазового состояния в области жидкой и газовой фаз. Имеются отличия в зоне двухкомпонентного состояния. Здесь давление не остается постоянным. В точке кипения оно выше, чем в точке начала конденсации (рис. 4.2а).
Критическая точка температуры смесей газов находится между критическими температурами чистых компонентов, также увеличивается критическая точка давления, она выше, чем для чистых компонентов. Критическое давление смеси повышается с увеличением ее молекулярной массы.
Так как анализ многокомпонентных систем довольно сложен, на практике рассматривается бинарная система с метаном и остальными компонентами совокупно.
 У многокомпонентных систем на диаграммах «давление - температура» кривые точек начала кипения и точек росы не совпадают и образуют фазовую диаграмму (рис. 4.2б).
У многокомпонентных систем на диаграммах «давление - температура» кривые точек начала кипения и точек росы не совпадают и образуют фазовую диаграмму (рис. 4.2б).
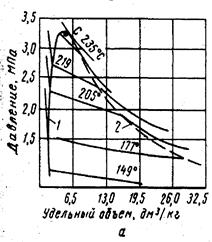
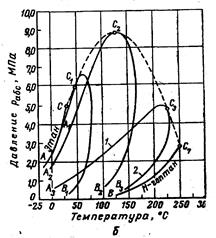
Рис. 4.2. Диаграммы фазового состояния двухкомпонентных систем
а) - зависимость «давление — удельный объем» для смеси н-пентана и н-гептана, б) — диаграмма «давление — температура» для смесей этана с н-гептаном (точки C 1 , С2 и С3 — критические точка смесей; l — линия точек начала парообразования; 2 — линия точек росы.
В области выше критической в многокомпонентной системе с изменением температуры и давления происходят особые фазовые превращения. Все критические точки компонентов смеси соединяются общей огибающей линией.
В связи со сложным составом конденсатных систем и значительным преобладанием в них метана, закономерности фазового состояния изучаются на бинарных смесях. Рассматриваются диаграммы двухкомпонентных систем. С повышением температуры смесь достигает точки кипения, далее в смеси объем газовой фазы увеличивается но, достигнув максимума, начинает уменьшаться до точки начала кипения другого компонента, т.е. две точки парообразования. Так же и при изменении давления при одинаковой температуре имеется две точки росы, между которыми существует двухфазная смесь (рис. 4.2а). Рассмотренные процессы фазовых превращений называют процессами ретроградного испарения и конденсации, а залежи называют газоконденсатными.
Влияние влаги на фазовые превращения углеводородов. Природные газы в пласте контактируют с остаточной водой в коллекторах, а также с подстилающими и краевыми водами, поэтому содержат пары воды. Относительная влажность газа определяется отношением количества паров воды, находящихся в газе при данных условиях, к максимально возможному их количеству при тех же условиях. Абсолютная влажность определяет количество водяных паров, находящихся в единице объема газа, г/м3, г/кг. С повышением температуры влагосодержание газа растет, с повышением давления снижается. Влагосодержание газа уменьшается с ростом концентрации солей в воде, т.к. они понижают парциальное давление паров воды. Увеличение молекулярной массы газа незначительно влияет на влажность газа.
Влажность газа влияет на фазовые превращения углеводородных систем, изменяя точку кипения и точку росы. Давление начала конденсации увеличивается. При снижении давления газовой влагосодержащей смеси при изотермическом состоянии выделяется конденсат и вода.
Фазовое состояние системы «нефть - газ». В зависимости от состава газа и нефти, пластового давления и температуры газ в газовой шапке может быть сухим, жирным или конденсатным. С увеличением глубины залегания число месторождений с газоконденсатной шапкой увеличивается.
С повышением давления при постоянной температуре газовая фаза обогащается компонентами нефти, плотность и молекулярная масса конденсата возрастают. С ростом температуры при постоянном давлении увеличивается содержание конденсата в газовой фазе. При одинаковых условиях в газовой фазе больше растворяется легких нефтей.
Растворимость газа в нефти зависит от его состава и природы, возрастая в последовательности метан, – этан – этилен – пропан. Критические параметры нефтегазовых смесей значительно выше, чем газоконденсатных. На величину критических параметров влияет порода пласта, в связи с адсорбцией асфальто-смолистых компонентов поверхностью твердой породы, что способствует обогащению жидкой фазы легкими фракциями. Остаточная вода способствует увеличению критического давления.
Газогидратные залежи. В определенных термодинамических условиях природный газ в пласте вступает в соединение с пластовой водой, образуя твердые соединения - гидраты газа, в которых молекулы газа заполняют пустоты кристаллической решетки воды с помощью прочных водородных связей. Плотность природных газогидратов составляет 0,9 – 1,14 г/см3. Удельный объем воды в гидратном состоянии возрастает до 1,26 – 1,32 см3/г (льда 1,09 см3/г). Один объем воды, в зависимости от природы газа, связывает от 70 до 300 объемов газа. Гидраты газов характеризуются упругостью газа на порядок ниже упругости пара чистого гидратообразователя. Процесс образования гидратов происходит с выделением тепла. Кристаллогидраты газов характеризуются высокой упругостью, низкой проницаемостью, на 60 – 100 % более высокими скоростями прохождения сейсмических волн
Газогидратные залежи могут формироваться из недонасыщенных газом пластовых вод без наличия литологических покрышек, под ними могут накапливаться залежи свободного газа и нефти. Газогидратные залежи приурочены к районам распространения многолетнемерзлых пород, к охлажденным толщам земной коры на материках и акваториях океана.
Газогидраты обнаружены в отложениях вечной мерзлоты в арктических зонах России, Аляски и Канады и на прибрежных морских площадях многих стран. К настоящему времени, помимо зон вечной мерзлоты, газогидраты по данным геофизических исследований обнаружены в 100 районах, расположенных вдоль восточного и западного побережий Северной и Южной Америки и Евроазиатского континента, в Австралии, Индии, Японии, в Черном, Каспийском и Средиземном морях, озере Байкал и др. В 20 из указанных районов наличие газогидратов уже подтверждено отобранными из скважин образцами. В Соединенных Штатах запасы метана, содержащегося в газогидратах, оцениваются в 8,1 тыс триллионов кубических метров.
Газогидраты не относятся к устойчивым веществам. Они стабильны в условиях определенного, достаточно узкого диапазона температуры и давления. Другая проблема связана с влиянием газогидратов на окружающую среду. По мнению многих исследователей, газогидраты, особенно залегающие под дном океанов и морей, являются основным источником метана в атмосфере. Декомпозиция гидратов на большой площади, вызванная интенсивной эксплуатацией, может спровоцировать неконтролируемое выделение метана в атмосферу. Учитывая, что метан способствует возникновению парникового эффекта почти в 25 раз сильнее углекислого газа, такая возможность серьезно беспокоит экологов.
Изучение характеристик углеводородных залежей. Для выбора режима эксплуатации месторождения необходимо определить параметры залежи: состав газа и содержание в нем конденсата, фазовое состояние системы, изотермы конденсации газа, количество и состав конденсата выделяющегося из 1 м3 газа при различных давлениях и температурах, возможные потери конденсата при эксплуатации месторождения и падении пластового давления в условиях разработки и транспортировки.
Комплект лабораторного оборудования позволяет провести все исследования по определению необходимых характеристик газа. При этом давление и температуру газа принимают соответствующими пластовым. Однако, невозможно соблюсти все условия газогидродинамического подобия процессов фильтрации газоконденсатной смеси в пласте, учесть влияние пористой среды на фазовые превращения, учесть процессы подготовки газа к транспортировке. Сопоставление данных эксплуатации месторождений и лабораторных заключений показало, что отличия могут составить 30 – 40 %.
Фазовые равновесия углеводородных систем. Для прогнозирования фазовых превращений углеводородов при эксплуатации месторождения используют приближенные методы расчета по закону Дальтона-Рауля:
Р У i = Х i Qi ,
где Р - давление смеси, Х i У i - молярные концентрации компонентов в паровой и жидкой фазах, Qi – давление насыщенных паров компонентов смеси в чистом виде, Р Уi - парциальное давление компонента в паровой фазе, Х i Qi - в жидкой фазе того же компонента.
Константой фазового равновесия (коэффициентом распределения i-го компонента в паровую и жидкую фазы Кi) называется отношение молярной доли i-го компонента в паровой фазе Уi к молярной доли его в жидкой фазе Хi
Кi = Уi / Хi
Константу равновесия определяют экспериментальным и расчетным путем. Экспериментально определить константы равновесия достаточно сложно. Расчетный метод состоит в применении уравнений состояния реальных газов, как отношение летучести компонента в паровой фазе к его летучести в жидкой фазе.
S N i =1, L+ V = 1

Каждый компонент имеет два значения давления, при которых константы равновесия равны единице, при давлении насыщенных паров компонентов Q равном общему давлению смеси Р (Q = Р) и в точке схождениядавления (рис. 4.3).
Кажущееся давление схождения всех компонентов нефтей составляет 34,5 – 35 МПа. Давление схождения зависит от температуры смеси. Если температура будет критической, то и давление схождения критическое. При эксплуатации месторождения состав смеси непрерывно меняется, поэтому константы фазового равновесия так же меняются и их рассчитывают по уравнениям. Использование уравнений для определения параметров реальных газов, требует введения поправок. Введено понятие «летучесть», f – исправленное давление,
F » Zр, где Z- коэффициент сжимаемости, р – давление.
Число киломолей жидкой L и газовой V фаз в смеси равна единице при данных давлении и температуре, если состав смеси известен и сумма их концентраций равна единице.
Вопросы для самоконтроля к теме 4.
1. Типы залежей и фазовые состояния в залежах.
2. Фазовое состояние газов с изменением давления и температуры.
3. Особенности фазового перехода компонента углеводорода.
4.Фазовое состояние двухкомпонентных систем.
5.Особенности фазового состояния многокомпонентных систем.
6.Абсолютная и относительная влажность газа и её влияние на фазовые превращения.
7.Фазовое состояние системы «нефть - газ».
8.Газогидратные залежи, их свойства.
9.Фазовые равновесия углеводородных систем. Константы равновесия.
ВЫТЕСНЕНИЕ НЕФТИ И ГАЗА ИЗ
ПОРИСТЫХ СРЕД
Нефть или газ находятся в пустотном пространстве горных пород, которое представляет огромное скопление каналов различного сечения. Поверхность каналов одного кубического метра пород может занимать огромную площадь в несколько сот метров. Между стенками пор горной породы нефтью, газом или водой возникает взаимодействие, величина которого зависит от свойств жидкости и газа и горной породы её содержащей, а так же от площади соприкосновения.
Дата: 2019-02-02, просмотров: 544.