В вязкой нефти присутствуют асфальтены, парафины, смолы, представляющие высокомолекулярные соединения углеводородов. Такие соединения придают нефти коллоидные свойства и влияют на изменение стабильности коэффициента вязкости. Нефть приобретает свойства неньютоновской жидкости в связи с возникновением пространственных структур. При высоких температурах структурно-механические свойства нефти проявляются слабее, а при понижении температур вследствие закачки воды или извлечения нефти на поверхность её температура понижается ниже температуры начала кристаллизации парафина и происходит интенсивное изменение структурно-механических свойств нефти.
На структурно-механические свойства нефти влияют свойства и строение пористой среды. Под влиянием материала скелета пор образование и упрочение пространственных структур происходит тем интенсивнее, чем меньше пористость и проницаемость пород. При движении нефти прочность пространственных структур уменьшается, а в покое – возрастает.
Определение свойств пластовой нефти подразделяются на расчетные и экспериментальные. Применяют комплекс приборов АСМ - 300М для исследования разгазирования нефти, определения зависимости давление - объем, определения вязкости, температуры начала кристаллизации парафина. По определенным данным рассчитывают давление насыщения, коэффициент сжимаемости, газосодержание, плотность, объемный коэффициент и усадку, коэффициент растворимости газа в нефти. Вязкость определяют вискозиметром по времени качения шарика внутри немагнитной трубки заполненной исследуемой жидкостью. Для калибровки вискозиметра используются жидкости с известной вязкостью.
Давление насыщения, коэффициент сжимаемости определяют по зависимости между давлением и объемом нефти. Проба нефти расширяется в полости пресса при снижении давления до начала выделения газа. Давление насыщения определяют по графику зависимости приращения объема от давления в нефти. Началу выделения газа соответствует точка перелома графика. По зависимости между объемом V и давлением выше давления насыщения ∆р, определяют коэффициент сжимаемости:
βн = - D V / (V D р), где ∆V – изменение объема нефти.
Объемный коэффициент, газосодержание и плотность нефти Объемный коэффициент в = Vпл.н / Vдег.н , газосодержание G = Vг / Vпл.н и плотность нефти r пл.н = Мпл.н / Vпл.н определяют по данным однократного разгазирования нефти и определения объема выделившегося газа, дегазированной нефти, массе и плотности нефти.
СВОЙСТВА ПРИРОДНЫХ ГАЗОВ
Химический состав природного газа определяет его физические свойства. Основными параметрами природных газов являются плотность, вязкость, сжимаемость, критическое давление и температура, диффузия, растворимость.
 |
Плотность газа на практике определяется по отношению к массе сухого воздуха (1,293 кг/м3 ), заключенного в том же объеме при нормальных условиях, т.е. определяется относительная плотность газа:
d= ρг / ρв , где ρг - плотность газа, ρв - воздуха.
Относительная плотность метана – 0.554, этана – 1.038, пропана – 1.523, бутана – 2.007
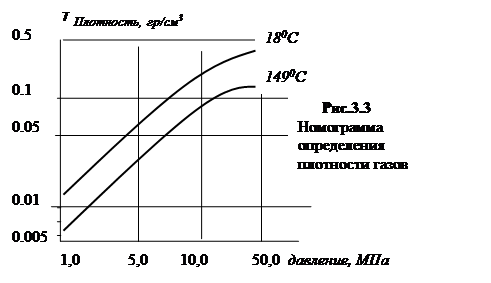
Плотность газов зависит от давления и температуры. Она увеличивается с увеличением давления и понижением температуры (рис.3.3).
Её определяют по изменению скорости истечения из отверстий. Квадраты скоростей истечения газа из отверстий обратно пропорциональны плотностям, прямо пропорциональны квадратам времени истечения одинаковых объемов газов:
V12 / V22 = ρ 2 / ρ 1 = t22 / t12
В газовой смеси определяется средняя кажущаяся молекулярная масса:
M ср = у1 М1+ у2 М2+ + уn М n = S уi Мi,
где М1, М2 М n - относительные молекулярные массы компонентов, у1, у, уn - мольные доли компонентов. Один кило моль любого газа занимает объем 22,4м3. Зная среднюю молекулярную массу газов можно определить их плотность по отношению к воздуху:
d = Мср / Мвозд = М / 28,97.
По известной плотности ρ0 газа при нормальных условиях, можно определить его молекулярную массу:
Мср = 22,4 ρ0
При работе с газом следует учитывать его большую плотность, чем воздуха, а значит, он может накапливаться в помещениях и колодцах и создавать опасность.
Вязкость газа характеризует его состояние и закономерность движения в пластах – это сила внутреннего трения между двумя слоями газа.
Вязкость сухого газа при 00С 13*10-4 Па*с., воздуха – 17*10-6 Па*с. Динамическая вязкость газа связана с его плотностью ρср, средней длиной свободного пути молекул λср, средней скоростью молекул:
µ =( r Vср λср) / 3
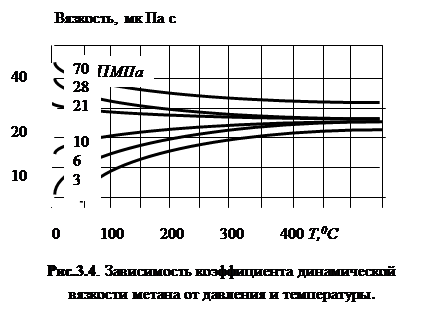
Из приведенной зависимости следует, что при повышении давления плотность газа возрастает и уменьшается средняя длина свободного пробега молекул, но скорость их пробега не изменяется. Поэтому с увеличением давления динамическая вязкость практически остается постоянной. С увеличением температуры средняя скорость молекул возрастает (r и λср постоянны) и поэтому увеличивается вязкость газа (рис. 3.4).
Рассмотренная выше закономерность нарушается, когда давление повышается значительно. При высоких давлениях с увеличением температуры вязкость газа понижается, аналогично изменению вязкости жидкости.
Следует учитывать влияние азота на вязкость газа, при его содержании более 5 %.
Для определения вязкости газов используют методики измерения скорости падения шарика в газе, затухания вращательных колебаний диска и др. В пластовых условиях используют капиллярный метод.
Критическая температура и давление. Для каждого газа существует температура, выше которой он не переходит в жидкое состояние при любых давлениях. Для метана критическая температура равна –82.1 0С, поэтому в недрах земной коры метан не может быть в жидком состоянии. Этан и пропан в земной коре могут находиться в жидком состоянии при давлениях выше критического, ниже которого как бы ни была низка температура, газ не переходит в жидкое состояние.
Диффузия – взаимное проникновение одного вещества в другое при их соприкосновении, что обусловлено движением молекул. Диффузия газов в пластовых условиях происходит через водонасыщенные поры и трещины пород. Явление диффузии газов играет существенную роль при формировании и разрушении залежей газа.
Растворимость газов при небольших давлениях подчиняется закону Генри, согласно которому количество растворенного газа прямо пропорционально давлению и коэффициенту растворимости. Коэффициенты растворимости газов в воде зависят от температуры и минерализации воды. При температурах до 90 0С эта зависимость обратная, при боле высоких температурах – прямая. С ростом минерализации воды растворимость газа падает.
Растворимость углеводородных газов в нефти примерно в 10 раз больше, чем в воде. Чем более жирный газ и более легкая нефть, тем
больше растворимость в ней газов. Растворенный в нефти газ увеличивает объем нефти и уменьшает её плотность, вязкость и поверхностное натяжение. Если объем газа значительно превышает объем нефти, то при давлении более 25 МПа и температуре 95 0С наступает обратная растворимость – жидкие углеводороды растворяются в газе и могут полностью превратиться в газ. При понижении давления из смеси будет выпадать конденсат (жидкие углеводороды).
Миграция нефти через плохо проницаемые породы невозможна, но нефть, растворенная в газе, может мигрировать. Это свойство следует учитывать при прямых и геохимических методах поисков месторождений нефти и газа, а так же при разработке месторождений.
Уравнение состояния газов. Состояние газа характеризуется давлением r, температурой Т, объемом V. Уравнение состояния реальных газов отличается от идеальных, а четкие математические уравнения описывают состояние идеальных газов. Уравнение состояния Ван-дер-Ваальса для реальных газов имеет вид:
(р + а / V2) (V - в) = R Т,
где р – давление, а - сила притяжения молекул, в - объем молекул газа, V –объем газа, Т – температура, R – газовая постоянная.
Однако в промысловом деле имеется смесь газов, что затрудняет применение уравнения. Разработаны другие уравнения для этого случая: Битти – Бриджмена; Бенедикта, Ватта, Рабина. Для практических расчетов пользуются уравнением Клапейрона, учитывающем коэффициент сжимаемости (сверхсжимаемости) реальных газов:
р V = Z m R T ,
где, Z - коэффициент сжимаемости, m – масса.
Реальный газ по свойствам приближается к идеальному при низких давлениях. С повышением давления молекулы газа сближаются, возрастают силы притяжения между ними, и газы сжимаются сильнее, коэффициент сжимаемости уменьшается. С ростом давления свойства газа приближается к свойству жидкости, начинают проявляться взаимоотталкивающие силы между молекулами, и коэффициент сжимаемости вновь возрастает.
Коэффициент сжимаемости газа – это степень изменения его объема при отличии температуры и давления в долях от критических значений. Термодинамические свойства газов, с равными приведенными температурой и давлением, практически одинаковы, т.к. газы находятся в одинаковом приближении к жидкому состоянию. Графики коэффициента сжимаемости газов в приведенных координатах с практической точностью совпадают и используются для вычисления удельных объемов и других параметров любого газа.
Рпр= р /(Σ уi ркр i ), Тпр = Т / (Σ уi Ткр i),
где р,Т - давление и температура газа, уi - мольная концентрация i-го компонента газа. Рпр , Тпр - выражают давление и температуру в долях от критических величин.
Для идеального газа f = р, для реального g = f /р, где g - коэффициент летучести, р – давление. Приближенно f = Z р.
 |
.
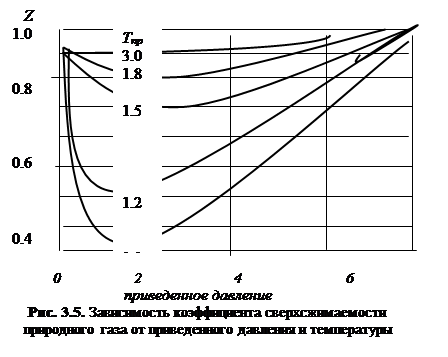
Минимум коэффициента сверхсжимаемости газа обусловлен переходом от силы притяжения между молекулами к силам отталкивания с увеличением давления. При высоких температурах минимум отсутствует, работают силы отталкивания. С увеличением температуры коэффициент сверхсжимаемости газа увеличивается.
С помощью коэффициента сжимаемости определяют объем газа в различных условиях
V = V0 Z (Т / (273 р)) ; V/ V0 = (Z / р) (Т/ 273)
Отклонение законов состояния реальных газов от идеальных учитывают используя функцию давления f - летучесть (фугитивность). Это функция исправленного давления, после учета величины его формулы идеального газа, становится пригодны для определения состояния реального газа (рис. 3.5)
СВОЙСТВА ПЛАСТОВЫХ ВОД
Строение молекулы и структурные особенности воды. Масса воды состоит из 11,11% водорода и 88,89% кислорода. Это простейшее химическое соединение одного атома кислорода и двух атомов водорода. Известно три изотопа водорода – протий, дейтерий, тритий и шесть изотопов кислорода. Поэтому в природных условиях выявлено 18 разновидностей молекул воды. Природная вода в основном состоит из молекул 1Н216О, а остальные разновидности присутствуют в ничтожно малых количествах.
Природная вода обладает многими аномальными физическими свойствами:
1) плавление льда сопровождается сжатием вещества (жидкой воды), которое достигает максимума при температуре 4 0С,
2) Вода имеет аномальные более высокие температуры плавления и кипения,
3) Вода обладает высокой удельной теплоемкостью, теплотой плавления и испарения,
4) Вода имеет аномальную растворяющую способность для солей и высокую диэлектрическую проницаемость,
5) Вязкость воды при повышении давления в интервале температур 0-300С уменьшается, а при более высоких температурах увеличивается.
Аномальные свойства воды зависят от её структуры, которая обусловлена наличием особого типа молекулярной водородной связи. Атом кислорода находится в центре молекулы. Ядра атомов водорода по отношению к ядру атома кислорода составляют между собой угол 105031 в жидкой воде и 1090301 во льду.
Пространственное расположение орбит вращения электронов в молекуле воды создает дипольное распределение электрических зарядов. Молекула воды имеет тетраэдрическое строение с двумя положительными и двумя отрицательными полюсами. Каждая молекула воды взаимодействует с четырьмя другими молекулами, создавая льдоподобную решетку. Такая упорядоченная структура взаимосвязи молекул воды придает ей свойства твердого тела с наличием значительного пространства между молекулами. Молекула воды совершает около 1000 колебаний в секунду.
По одной из моделей структуры воды связь между молекулами воды и других жидкостей с водородными связями осуществляется через водородные мостики, образующих кольцевые структуры. Создаются агрегаты молекул взаимосвязанных между собой. Аномальные свойства воды учитываются при решении вопросов нефтяной геологии. На этой основе могут быть разработаны различные модели использования воды.
В природных условиях встречаются следующие виды воды: конституционная и кристализационная; прочно-связанная; капиллярная; остаточная; свободная (гравитационная). Все указанные виды воды обладают различными свойствами, часто противоположными, и удерживаются в пористой среде различными силами.
Вода в нефтяной залежи занимает пониженные зоны и находится в большинстве случаев под залежъю и вокруг нее и называется подошвенной или краевой. Вода, находящаяся в пропластках называется промежуточной. Верхние и нижние воды залегают выше и ниже нефтяного пласта. В продуктивных пластах залежи вместе с углеводородами также содержится вода, оставшаяся со времени образования залежи, поэтому её называют остаточной.
Водоносные и продуктивные части пластов являются единой связанной гидродинамической системой.
Остаточная вода в залежи находится со времени образования залежи. В пористой среде остаточная вода существует как капиллярно связанная, адсорбционная, пленочная, свободная. С увеличением проницаемости среды количество остаточной воды в породе уменьшается. Содержание остаточной воды в породах может меняться от нескольких процентов до 70% и более от суммарной емкости пор. Наименьшее количество остаточной воды отмечается в пластах со щелочной водой и наибольшее – в присутствии пресной воды. Минерализация остаточной воды зависит от литологии пород коллекторов и находится в пределах 15 – 22%. Остаточная вода имеет плотность 1,2-1,4 г/см3 обладает высокой проводимостью, низкой диэлектрической проницаемостью 2-2,5, температурой замерзания минус 20-193 оС, концентрацией солей 100-300 г/л, повышенным содержанием хлора и повышенной радиоактивностью.
Распределение нефти, остаточной воды и газа в залежи влияет на фазовые проницаемости, а значит и на процессы движения нефти. В пласте остаточная вода может находиться в виде пленки, покрывающей поверхность поровых каналов (гидрофильная поверхность) или в виде отдельных жилок включений в центрах пор (гидрофобная поверхность среды). В последнем случае нефть смачивает поверхность пор. От первоначального распределения жидкостей и газов в пласте зависят характеристики пласта: смачиваемость пород вытесняющими жидкостями, количество остающейся нефти, интенсивность капиллярных процессов.
Определение количества остаточной воды в породе проводят на извлеченном керновом материале. Керн помещают в растворитель (толуол), далее при кипении растворителя отделяется вода. Определяется водо-нефте- газонасыщенность породы.
Быстрый метод определения остаточной воды в керне – центрифугирование. С увеличением скорости оборотов центрифуги жидкость вытесняется с пор все меньшего диаметра. С некоторой скорости вращения увеличение скорости практически не влияет на оставшуюся в порах воду, её и считают остаточной. Изменяя скорость ценрифугирования, и определяя количество выделившейся воды, можно построить зависимость «капиллярное давление – водонасыщенность» и по ней определить среднюю остаточную водонасыщенность пород исследуемого пласта. Применяют также и метод полупроницаемых мембран (перегородок) вытеснения воды из керна азотом, воздухом или нефтью, метод вакуумирования и др.
Переходные зоны нефть-вода (ВНК), нефть-газ (ГНК), вода-газ (ВГК). Водонефтяная зона имеет различную мощность в зависимости от свойств и состава пород и физико-химических свойств воды и нефти. В песчаниках высокой проницаемости мощность переходной зоны исчисляется сантиметрами, в мелкозернистых – метрами (6-8) м.
Для оценки величины переходной зоны используют геофизические методы и экспериментальные. В переходной зоне распределение нефти и воды очень сложное. Для анализа используют зависимость «капиллярное давление - водонасыщенность».
При вытеснении нефти водой во время эксплуатации месторождения на строение водонасыщенного контакта влияет прирост давлений и фазовые проницаемости системы, проницаемость, капиллярный подъем, физико-химические свойства жидкости.
Радиоактивность пластовых вод обусловлена содержанием в них урана, радия и радона. Практически все подземные воды в различной степени радиоактивны. При заводнении залежи поверхностными водами, вокруг залежи образуется оторочка радиоактивных вод, обусловленная как радиоактивностью остаточных подземных вод, так и выщелачиванием из горных пород радиоактивных элементов. Такая радиоактивная оторочка вод является надежным критерием прохождения водо-нефтяного контакта.
Минерализация пластовых вод нефтяных месторождений колеблется от единиц г/м3 до сотен кг/м3. Минеральные вещества представлены солями натрия, кальция, магния и др. Основными солями являются хлориды и карбонаты, сульфаты. Помимо этого в водах может содержаться йод, бром, редкоземельные элементы, органические вещества.
Нефтяные залежи в большинстве случаев находятся в зоне затрудненного водообмена, но иногда присутствуют и пресные воды.
Плотность пластовых вод возрастает с увеличением минерализации и может достигать 1500 кг/м3 при концентрации солей 642,8 кг/м3
Сжимаемость пластовых вод изменяется в пределах (3,7-5,0)10-10м2/Н, а при наличии растворенного газа может значительно увеличиваться
b вг = b в (1+0,05 Vг),
где: b вг - коэффициент сжимаемости воды с растворенным газом, b в – коэффициент сжимаемости чистой воды, Vг количество газа, растворенного в воде, м3/м3.
Термическое расширения воды Е = D V / (V D T ) колеблется от 18 10-5 до 90 10-5 1/град, возрастает с увеличением температуры и уменьшаясь с ростом пластового давления.
Вязкость пластовых вод зависит от температуры и концентра
ции растворенных солей, влияние давления незначительно.

С увеличением температуры вязкость воды уменьшается, а с увеличением минерализации - повышается. На величину вязкости воды влияет не только минерализация, но и состав солей. Наибольшей вязкостью характеризуются хлоркальциевые воды в 1,5 – 2 раза больше, чем чистая вода (рис. 3.6). Газы в воде растворены в небольших количествах и мало влияют на вязкость.
Электропроводность пластовых вод находится в прямой зависимости от их минерализации, так как соли в воде находятся в ионном состоянии, а положительно и отрицательно заряженные ионы являются переносчиками электрических зарядов. Величина удельного сопротивления подземных вод изменяется от 0,02 до 1,00 Ом м. Дистиллированная вода и лед не являются проводниками электрического тока. Так как нефть и газ имеют низкую электропроводность, а минерализованные подземные воды высокую электропроводность, то эти свойства используют для контроля за продвижением водо-углеводородных контактов. Электропроводность воды используют для определения пористости и водо-газо-нефтенасыщенности коллекторов.
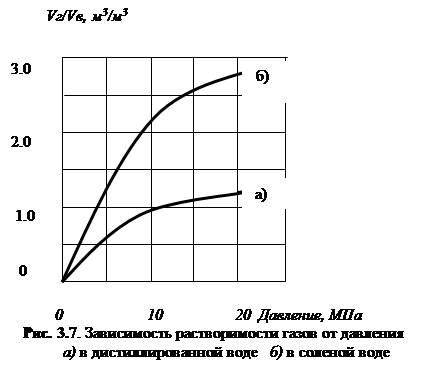
Растворимость газов в воде. Растворимость газов в воде незначительна. Тем не менее, площадь контакта газовой залежи с подстилающей водой очень большая и при высоком давлении вода будет содержать большие объемы газа (рис.3.7). С увеличением температуры растворимость газов сначала уменьшается, а затем возрастает. С увеличением минерализации растворимость газов в воде уменьшается. На растворимость газов в воде так же влияет размер молекул газа. В подземных водах наиболее распространенными газами является кислород, углекислый газ, сероводород, водород, азот и благородные газы, а также метан и тяжелые углеводороды.
 |
Выпадение осадков из пластовых вод может происходить из попутно извлекаемой воды в нефтепромысловом оборудовании и на различных участках пласта. Это отложения карбоната кальция СаСО3, сульфата кальция (Са S О4 2Н2О гипса, Са S О4 ангидрита), сульфата бария Ва S О4 . Помимо этого могут отлагаться другие соли, механические примеси, продукты жизнедеятельности бактерий, частицы нефти, силикаты, парафины. Большинство отложений имеет кристаллическую структуру, сформированную в сложных гидродинамических условиях широкого интервала температур и пересыщений раствора солями, примесями. Пресыщенные растворы образуются при закачке вод, химически несовместимых с пластовыми или в связи с изменением термодинамических условий, химического состава пластовых вод, смешением вод разных горизонтов на забое, а также влиянием других факторов. Для борьбы с отложениями солей используют различные преобразователи солей, растворители. Например, растворы карбоната, бикарбоната натрия и калия, соляную кислоту, гидроокиси натрия и калия, каустическую соду (едкий натрий).
Вопросы для самоконтроля к теме 3
1. Основной состав нефти и газа.
2. Влияние примесных элементов на свойства нефтей и газов.
3. Зависимость плотности и вязкости газов от давления и температуры.
4. Уравнение состояния газов.
5. Коэффициент сжимаемости газа и его зависимость от давления и температуры.
6. Сжимаемость нефти и её зависимость от состава, температуры и давления. Усадка нефти.
7. Давление насыщения нефти газом.
8. Растворимость газов в нефти и ее зависимость от давления. Влияние растворенного газа на параметры нефти.
9. Зависимость плотности нефти от растворенных газов.
10. Вязкость нефти и её зависимость от растворенных газов, давления, температуры.
11. Изменение свойств нефти в пределах залежи.
12. Колориметрические методы определения параметров нефти.
13. Термодинамические свойства газов и нефти.
14. Понятие энтальпии и энтропии.
15. Остаточная вода в залежах и её влияние на фильтрацию нефти.
16. Минерализация, плотность и сжимаемость пластовых вод.
17. Размер переходных зон нефть-вода, вода-газ, нефть-газ.
18. Зависимость вязкости пластовой воды от температуры, давления, минерализации.
19. Зависимость растворимости газов в воде от давления.
Дата: 2019-02-02, просмотров: 1306.