| № п./п. | Компонент | Относит. моляр. масса | РКРi, МПа | ТКРi, К |
| 1 | Метан, СН4 | 16,04 | 4,63 | 190,55 |
| 2 | Этан, С2Н6 | 30,07 | 4,87 | 305,45 |
| 3 | Пропан, С3Н8 | 44,09 | 4,26 | 369,82 |
| 4 | изо-Бутан, i-С4Н10 | 58,12 | 3,65 | 408,13 |
| 5 | н-Бутан, n-С4Н10 | 58,12 | 3,797 | 425,16 |
| 6 | изо-Пентан, i-С5Н12 | 72,15 | 3,381 | 460,4 |
| 7 | н-Пентан, n-С5Н12 | 72,15 | 3,369 | 469,6 |
| 8 | н-Гексан, С6Н14 | 86,17 | 3,031 | 507,4 |
| 9 | н-Гептан, С7Н16 | 100,20 | 2,736 | 640,61 |
| 10 | Азот, N2 | 28,02 | 3,399 | 126,25 |
| 11 | Двуокись углерода, СО2 | 44,01 | 7,387 | 304,15 |
| 12 | Сероводород, Н2S | 34,08 | 9,01 | 373,55 |
Существуют графики для различных диапазонов изменения приведённых параметров, один из которых представлен ниже (рис. 2.1), эмпирические формулы и зависимости для оценки коэффициентов сверхсжимаемости от приведённых давлений и приведённых температур.
При содержании неуглеводородных компонентов в составе нефтяных газов (N2, СО2, Н2S) следует вводить поправки в рассчитанные значения коэффициентов сверхсжимаемости на содержание этих соединений, используя специальные графики (рис. 2.2). Например, в случае содержания в попутном газе азота более 5 % величина коэффициента сверхсжимаемости должна ещё и учитывать его влияние по принципу аддитивности:
z = NN2·zN2 + (1 – NN2)·zув, (2.33)
где NN2 – молярная доля азота в смеси газов;
zN2, zув – коэффициенты сверхсжимаемости азота и углеводородной части смеси газов.
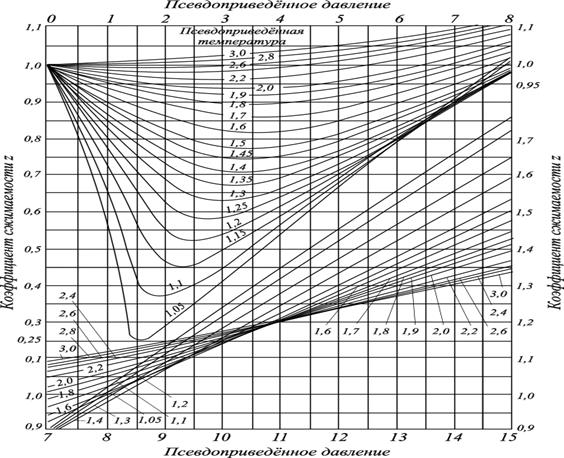
Рис. 2.1. Коэффициенты сверхсжимаемости углеводородных газов,
в зависимости от приведённых параметров

Рис. 2.2. Зависимости коэффициентов сверхсжимаемости азота от давления и температуры
Зная коэффициент сверхсжимаемости (z) и объём, занимаемый газом при нормальных условиях, можно оценить его объём при пластовых условиях по закону Бойля–Мариотта:
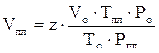 . (2.34)
. (2.34)
Отношение объёма газа при пластовых условиях (Vпл) к объёму газа при нормальных условиях (Vo) называется объёмным коэффициентом (b) газа:
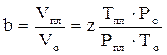 . (2.35)
. (2.35)
Объёмный коэффициент газа используется при пересчёте объёма, занимаемого газом при нормальных условиях на пластовые условия, и наоборот, например, при подсчёте запасов.
Рассмотрим пример. Дан мольный состав (Ni) газа:
Дано: Ni, доли Pкр, МПа Ткр, К Ni·Piкр Ni·Tiкр
СН4 0,8319 4,63 190,55 3,852 158,52
С2H6 0,0846 4,87 305,45 0,412 25,84
C3H8 0,0437 4,26 369,82 0,186 16,16
i-C4H10 0,0076 3,797 408,13 0,029 3,10
n-C4H10 0,0168 3,650 425,16 0,061 7,14
i-C5H12 0,0057 3,381 460,04 0,019 2,62
n-C5H12 0,0032 3,369 479,6 0,011 1,53
C6H12 0,0063 3,031 507,4 0,019 3,19
Определить, какой объём будет занимать 1000 м3 газа на поверхности в пластовых условий: Р = 10 МПа, Т = 50 °С?
Решение. Используя данные таблицы, мы находим коэффициенты сжимаемости (z) и объёмный коэффициент газа (b) для пластовых условий.
Рассчитаем приведённые температуру (2.31) и давление (2.32) для нашего состава и пластовых условий:
Tпр = (50 + 273,15) /S (Ni ∙Tiкр) = 323,15/(0,8319·190,55 + 0,0846·305,45 + 0,0437·369,82 + 0,0076·408,13 + 0,0168·425,16 + 0,0057·460,04 + 0,0032·479,6 + 0,0063·507,4) = 323,15/(158,52 + 25,84 + 16,16 + 3,10 + 7,14 + 2,62 + 1,53 + 3,19) = 323,15/218,1 = 1,48.
Рпр = 10/S(Ni·Piкр) = 100/(0,8319·4,63 + 0,0846·4,87 + 0,0437·4,26 + 0,0076·3,797+ 0,0168·3,65 + 0,0057·3,381 + 0,0032·3,369 + 0,0063·3,031) = 10/(3,852 + 0,412 + 0,186 + 0,029 + 0,061 + 0,019 + 0,011 + 0,019) = 10/4,589 = 2,179.
По графикам (рис. 2.1) находим значение z как функцию:
z = f(Тпр = 1,48) и f(Pприв = 2,179) и определяем величину z.
Для нашего случая величина z = 0,81.
Объём газа в пластовых условиях определяем, используя закон Бойля–Мариотта:
Vпл = z·Vo·(273,15 + t°)·Po/(273,15·Pпл);
Vпл = 0,81·1000·323,15·0,1/(273,15·10) = 9,58.
Объёмный коэффициент газа оценивается отношением объёмов газа в пластовых условиях к объёму газа при н.у.:
b = Vпл./Vo = z ·273,15 + t°)·Po /(273,15·Pпл);
b = 9,58/1000 = 0,81·323,15·0,1/(273,15·10) = 0,00958.
Вязкость газов
Вязкость газа характеризует его состояние исходя из некоторых положений кинетической теории газов.
При низких давлениях и температурах динамическая вязкость газа оценивается из теории соударения частиц и зависит от средней длины пробега молекул ( 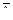 ), от средней скорости движения молекул (
), от средней скорости движения молекул (  ) и от их плотности газа:
) и от их плотности газа:
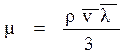 , (2.36)
, (2.36)
где r – плотность газа;
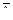 – средняя длина пробега молекул газа;
– средняя длина пробега молекул газа;
 – средняя скорость молекул газа.
– средняя скорость молекул газа.
Из анализа (2.36) следует, что с возрастанием температуры средняя длина свободного пробега молекул и средняя скорость движения молекул увеличиваются, а следовательно, и вязкость газа возрастает, несмотря на уменьшение величины плотности (рис. 2.3).
Давление, МПа

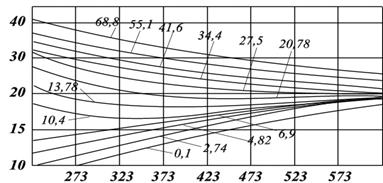
Температура, К
Рис. 2.3. Зависимости коэффициентов динамической вязкости нефтяного газа плотности 0,6 от температуры при различных давлениях
Отмеченный характер изменения вязкости газов объясняется спецификой проявления внутреннего трения. Вязкость газа характеризует способность газа оказывать сопротивление перемещению одной части газа относительно другой. Количество движения из слоя в слой передаётся вследствие перелёта молекул газа в движущиеся относительно друг друга слои. При этом возникают силы, тормозящие движения одного слоя и увеличивающие скорость движения другого. С повышением температуры увеличивается скорость и количество движения, передаваемое в единицу времени и, как следствие, возрастает величина вязкости газа.
Повышение давления от 0,1 до 1,2 МПа (рис. 2.4) не влияет на величину вязкости газа, поскольку уменьшение средней длины пробега молекулы и средней скорости движения молекулы компенсируется увеличением величины плотности. Эти закономерности при давлениях выше 1,2 МПа изменяются.
Вязкость углеводородного газа при нормальных условиях невелика и не превышает значения 0,01 сантипуаза (сПз) ≈ 10 мкПа·с:
1 пуаз = 0,1 н·с/м2 = 0,1 Па·с; 1 сПз = 1 мПа·с = 1·103 мкПа·с.
Неуглеводородные компоненты: азот, углекислый газ, сероводород, гелий, в том числе и воздух являются более вязкими составляющими природного газа. Величины вязкости для них изменяются в диапазоне от 0,01 до 0,025 сПз.
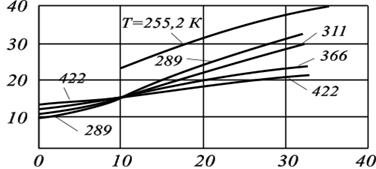
Давление, МПа
Рис. 2.4. Зависимости вязкости газа от давления при различных
температурах
Особое влияние на величину вязкости газа оказывает азот. При содержании в углеводородном газе более 5 % азота следует учитывать его влияние на вязкость газа и оценивать средневзвешенную вязкость смеси по принципу аддитивности:
μсм = Na·μa + (1– Na)·μуг, (2.37)
где μсм – динамическая вязкость смеси газов;
μа и μуг – динамические вязкости азота и углеводородов;
Na – молярная доля азота в составе газа.
Дата: 2018-12-28, просмотров: 464.