Лабораторная работа №5. « Карбоновые кислоты, гидрокси-, оксо- кислоты»
Карбоновые кислоты -органические соединения, содержащие одну или несколько карбоксильных групп —COOH. В живых организмах обнаружены карбоновые кислоты алифатического (жирные кислоты), ароматического (бензойная, салициловая) и гетероциклического (никотиновая) рядов. По числу карбоксильных групп различают монокарбоновые (жирные кислоты), дикарбоновые (малоновая, фумаровая, щавелевая, янтарная), трикарбоновые (изолимонная, лимонная) и поликарбоновые кислоты. Карбоновые кислоты могут быть насыщенными (предельными) и ненасыщенными (непредельными). Карбоновые кислоты играют важную роль в обмене веществ, являясь продуктами превращения углеводов, белков, жиров и других соединений. При физиологических значениях pH в клетках карбоновые кислоты находятся в основном в виде солей. В большом количестве в организмах встречаются эфиры карбоновых кислот (липиды, ацетилхолин и др.). Важное место в обмене веществ занимают активированные производные карбоновых кислот, например, тиоэфиры карбоновых кислот с коферментом А (ацетилКоА, ацил-КоА). К другим производным карбоновых кислот относятся гидроксикислоты, имеющие одну или несколько гидроксильных групп (—OH), кетокислоты, содержащие кетогруппу (>C=O) (альфа-кетоглутаровая, пировиноградная, щавелевоуксусная), аминокислоты, амиды карбоновых кислот (никотинамид, аспарагин, глутамин).
Цель занятия: сформировать знания биологической роли и реакционной способности карбоновых кислот и их функциональных производных. Сформировать знания реакционной способности гидрокси- и оксокислот с учетом взаимного влияния функциональных групп, умения прогнозировать химические свойства гетерофункциональных соединений.
Контрольные вопросы
1.Сравните кислотные свойства этановой и этандиовой кислот. Напишите уравнения реакций образования солей с Са(ОН)2.
2.Напишите уравнения реакций декарбоксилирования малоновой и 2-аминопентандиовой кислот.
3.Напишите уравнения реакций получения функциональных производных карбоновых кислот: изопропилового эфира пропановой кислоты, амида бутановой кислоты; ацетил-КоА и малонил-КоА.
4.Напишите схему реакции гидролиза этилацетата в кислой среде.
5.Напишите схему реакции гидролиза метилпропионата в щелочной среде.
6.Напишите схемы реакций окисления молочной и яблочной кислот in vivo, назовите продукты.
7.Напишите таутомерные формы пировиноградной кислоты (ПВК). Приведите уравнение реакции ПВК (в енольной форме) с АТФ с образованием фосфоенолпирувата (ФЕП).
8.Приведите схему реакции восстановления ПВК in vivo .
ОПЫТ 1. Качественная реакция 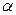 -гидроксикислот с хлоридом железа ( III ) (качественная реакция на молочную кислоту).
-гидроксикислот с хлоридом железа ( III ) (качественная реакция на молочную кислоту).
В две пробирки налейте по 0,5мл раствора хлорида железа (III) и добавьте такое же количество раствора фенола; появляется характерное окрашивание. В одну пробирку прибавьте 0,5мл молочной кислоты, в другую для сравнения – уксусной. Отметьте изменение окраски растворов, результаты наблюдений запишите в таблицу .
Таблица 1.
| Опыт | Цвет раствора | Уравнение реакции |
| фенол + FeCl3 | ||
| молочная кислота+комплекс железа с фенолом | ||
| уксусная кислота+комплекс железа с фенолом |
Выводы
1. Запишите в таблицу 1 уравнения протекающих реакций и наблюдения, сделанные в опыте.
2.Сделайте вывод о силе кислот. Расположите фенол, молочную, уксусную кислоты в ряд по увеличению кислотных свойств.
ОПЫТ 2. Открытие щавелевой кислоты в виде кальциевой соли.
В пробирку налейте 1 мл раствора оксалата натрия, затем добавьте в раствор 0,5мл раствора хлорида кальция. Что при этом наблюдаете? С кристаллами оксалата кальция можно встретиться при клиническом исследовании мочи, они имеют форму почтовых конвертов и хорошо видны под микроскопом.
Выводы
1.Запишите уравнения образования оксалата кальция и цвет выпавшего осадка.
Выводы.
1. Запишите цвет образовавшегося раствора. Чем он обусловлен? Почему эта реакция называется биуретовой?
2. Все ли белки дают биуретовую реакцию?
Выводы
1. Какой процесс произошел после добавления концентрированной азотной кислоты?
2. Данная реакция позволяет установить наличие в белке ароматических аминокислот. Назовите эти аминокислоты?
3. Напишите схему реакции тирозинового остатка белка с азотной кислотой.
Выводы.
1. Какого цвета раствор образуется при растворении осадка гидроксида меди (II)?
2. Какой структурный фрагмент глюкозы обусловливает участие в растворении осадка?
3. Напишите схему реакции образования комплексной соли иона Cu2+ с диольным фрагментом глюкозы:
4. Как называется реактив, используемый в опыте (соли меди в щелочной среде без нагревания)?
Выводы.
1. Какой структурный фрагмент глюкозы обусловливает участие в данной реакции?
2. Напишите схему реакции, назовите продукты реакции и укажите цвет образовавшегося осадка.
3. Укажите состав реактива Фелинга и условия протекания реакции на наличие альдегидной группы.
4. Какие свойства (восстановительные/ окислительные) проявляет глюкоза в данной реакции?
5. Какая таутомерная форма глюкозы обладает данными свойствами?
Выводы
1.Объясните, почему фруктозу нельзя отличить от глюкозы реакцией с реактивом Фелинга.
Выводы
1. Запишите схему реакции, используя циклическую форму фруктозы.
Лабораторная работа №8. «Ди- и полисахариды»
Многие дисахариды – сахара, молекулы которых построены из двух остатков моносахаридов, связанных гликозидной связью являются важнейшими пищевыми веществами для человека (сахароза, лактоза, мальтоза, изомальтоза, трегалоза и др.), а также входят в состав лечебных средств (лактоза, мальтоза, сахароза). Полисахариды (гликаны) - высокомолекулярные углеводы - сахара, молекулы которых построены из большого количества моносахаридных остатков, связанных гликозидными связями и образующих неразветвленные (линейные) или разветвлённые цепи с молекулярной массой от нескольких тысяч до нескольких миллионов. В состав простейших полисахаридов входят остатки только одного типа моносахарида (гомополисахариды), более сложные полисахариды (гетерополисахариды) состоят из остатков двух или более типов моносахаридных остатков и могут быть построены из регулярно повторяющихся дисахаридных блоков. Гликоген у человека и животных, крахмал, инулин у растений — запасающиеся углеводные вещества - энергетический резерв живых организмов. Целлюлоза и гемицеллюлозы клеточной стенки растений, хитин беспозвоночных и грибов —структурные полисахариды. Гетерополисахариды (гликозаминогликаны – гиалуроновая кислота, хондроитинсульфаты, дерматансульфаты, кератансульфаты и др.) – важнейшие структурные полисахариды всех типов соединительной ткани человека и животных. Гепарансульфаты входят в состав базальных мембран и поверхностных антигенов всех клеток человека и животных, гепарин – противосвертывающее вещество (антикоагулянт) крови. Липополисахариды бактерий и разнообразные гликопротеины поверхности животных клеток обеспечивают специфичность межклеточного взаимодействия и иммунологических реакций.
Практически все известные природные полисахариды и их многочисленные синтетические производные применяются в медицине или прямо как лечебные средства (гепарин, гиалуроновая кислота, ходроитинсульфаты, частично деполимеризованные декстраны и др.), или как вспомогательные вещества (крахмал, циклодекстрины, агар, пектины, хитин, хитозан, целлюлоза и ее эфиры и др.). Инулин применяется в клинической диагностике функционального состояния почек.
Цель занятия: сформировать знания принципов химического строения и основных химических свойств дисахаридов, гомо- и гетерополисахаридов во взаимосвязи с их биологическими функциями.
Контрольные вопросы
1. Напишите уравнения реакций гидролиза сахарозы, мальтозы, лактозы.
2. Приведите структурные формулы компонентов таутомерного равновесия в растворе мальтозы.
3. Приведите структурную формулу дисахаридного фрагмента амилозы, укажите тип гликозидной связи.
4. Приведите фрагмент структуры амилопектина (глиеогена). Укажите виды связей между моносахаридными звеньями.
5. Приведите структурную формулу дисахаридного фрагмента целлюлозы и укажите тип гликозидной связи.
6. Приведите структурные формулы дисахаридных фрагментов гиалуроновой кислоты и хондроитин-4-сульфата. Укажите все типы гликозидных связей. Опишите структурное сходство и различие этих гетерополисахаридов.
7. Опишите применение полисахаридов в лечебных целях на примерах декстранов, целлюлозы и гепарина.
Выводы
1.Зарисуйте структурную формулу сахарозы
2.Объясните, почему сахароза не обладает восстановительными свойствами.
Выводы.
1. Какой дисахарид является компонентом сыворотки молока. К каким дисахаридам он относится?
2. Какова причина наличия восстановительных свойств у данного дисахарида?
3. Какой из моносахаридных остатков в молекуле этого дисахарида способен к цикло-оксо-таутомерии?
4. Напишите уравнение реакции взаимодействия окисления данного дисахарида с образованием лактобионовой кислоты.
Выводы.
1. Укажите причину появления окраски раствора крахмала при добавлении йода.
2. Какая фракция крахмала обеспечивает появление этого окрашивания.
3. Зарисуйте схематически расположение молекул I2 в структуре этой фракции
4. Что является причиной исчезновения окрашивания при нагревании?
Список литературы.
Основная:
1. Н. А. Тюкавкина. Биоорганическая химия. М., Дрофа, 2014.
2. В. А. Попков. Общая и биоорганическая химия. М., Академия, 2011.
Дополнительная:
1. Под ред. Н. А. Тюкавкиной. Органическая химия. Книга 1. Основной курс. М., Дрофа, 2008.
2. Под ред. Н. А. Тюкавкиной. Органическая химия. Книга 2. Специальный курс. М., Дрофа, 2008.
3. И. И. Грандберг. Органическая химия. М., Дрофа, 2009.
4. И. И. Грандберг, Н. Л. Нам. Органическая химия. М., Юрайт, 2012.
5. Д. Хельвинкель. Систематическая номенклатура органических соединений. Пер. с англ. М., БИНОМ, 2012.
6. О. А. Реутов, А. Л. Курц, К. П. Бутин. Органическая химия. В 4-х частях. М., БИНОМ, 2007.
7. В.И.Слесарев. Химия. Основы химии живого. С-Пб., Химиздат.2000
8. Практикум по общей и биоорганической химии. Под ред. Проф. В.А.Попкова. М., ACADEMA, 2005.
Лабораторная работа №5. « Карбоновые кислоты, гидрокси-, оксо- кислоты»
Карбоновые кислоты -органические соединения, содержащие одну или несколько карбоксильных групп —COOH. В живых организмах обнаружены карбоновые кислоты алифатического (жирные кислоты), ароматического (бензойная, салициловая) и гетероциклического (никотиновая) рядов. По числу карбоксильных групп различают монокарбоновые (жирные кислоты), дикарбоновые (малоновая, фумаровая, щавелевая, янтарная), трикарбоновые (изолимонная, лимонная) и поликарбоновые кислоты. Карбоновые кислоты могут быть насыщенными (предельными) и ненасыщенными (непредельными). Карбоновые кислоты играют важную роль в обмене веществ, являясь продуктами превращения углеводов, белков, жиров и других соединений. При физиологических значениях pH в клетках карбоновые кислоты находятся в основном в виде солей. В большом количестве в организмах встречаются эфиры карбоновых кислот (липиды, ацетилхолин и др.). Важное место в обмене веществ занимают активированные производные карбоновых кислот, например, тиоэфиры карбоновых кислот с коферментом А (ацетилКоА, ацил-КоА). К другим производным карбоновых кислот относятся гидроксикислоты, имеющие одну или несколько гидроксильных групп (—OH), кетокислоты, содержащие кетогруппу (>C=O) (альфа-кетоглутаровая, пировиноградная, щавелевоуксусная), аминокислоты, амиды карбоновых кислот (никотинамид, аспарагин, глутамин).
Цель занятия: сформировать знания биологической роли и реакционной способности карбоновых кислот и их функциональных производных. Сформировать знания реакционной способности гидрокси- и оксокислот с учетом взаимного влияния функциональных групп, умения прогнозировать химические свойства гетерофункциональных соединений.
Контрольные вопросы
1.Сравните кислотные свойства этановой и этандиовой кислот. Напишите уравнения реакций образования солей с Са(ОН)2.
2.Напишите уравнения реакций декарбоксилирования малоновой и 2-аминопентандиовой кислот.
3.Напишите уравнения реакций получения функциональных производных карбоновых кислот: изопропилового эфира пропановой кислоты, амида бутановой кислоты; ацетил-КоА и малонил-КоА.
4.Напишите схему реакции гидролиза этилацетата в кислой среде.
5.Напишите схему реакции гидролиза метилпропионата в щелочной среде.
6.Напишите схемы реакций окисления молочной и яблочной кислот in vivo, назовите продукты.
7.Напишите таутомерные формы пировиноградной кислоты (ПВК). Приведите уравнение реакции ПВК (в енольной форме) с АТФ с образованием фосфоенолпирувата (ФЕП).
8.Приведите схему реакции восстановления ПВК in vivo .
ОПЫТ 1. Качественная реакция 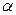 -гидроксикислот с хлоридом железа ( III ) (качественная реакция на молочную кислоту).
-гидроксикислот с хлоридом железа ( III ) (качественная реакция на молочную кислоту).
В две пробирки налейте по 0,5мл раствора хлорида железа (III) и добавьте такое же количество раствора фенола; появляется характерное окрашивание. В одну пробирку прибавьте 0,5мл молочной кислоты, в другую для сравнения – уксусной. Отметьте изменение окраски растворов, результаты наблюдений запишите в таблицу .
Таблица 1.
| Опыт | Цвет раствора | Уравнение реакции |
| фенол + FeCl3 | ||
| молочная кислота+комплекс железа с фенолом | ||
| уксусная кислота+комплекс железа с фенолом |
Выводы
1. Запишите в таблицу 1 уравнения протекающих реакций и наблюдения, сделанные в опыте.
2.Сделайте вывод о силе кислот. Расположите фенол, молочную, уксусную кислоты в ряд по увеличению кислотных свойств.
ОПЫТ 2. Открытие щавелевой кислоты в виде кальциевой соли.
В пробирку налейте 1 мл раствора оксалата натрия, затем добавьте в раствор 0,5мл раствора хлорида кальция. Что при этом наблюдаете? С кристаллами оксалата кальция можно встретиться при клиническом исследовании мочи, они имеют форму почтовых конвертов и хорошо видны под микроскопом.
Выводы
1.Запишите уравнения образования оксалата кальция и цвет выпавшего осадка.
Дата: 2018-12-28, просмотров: 510.