Наглядные пособия:
Рисунки: 1. Реакции последовательного восстановления убихинона вдыхательной цепи; 2. Антиоксиданты водной фазы; 3. Механизм антиоксидантного действия витамина Е; 4. Окислительно-восстановителные превращения α-токоферола и сопряженных с ним коантиоксидантов; 5. Витамин С, 6. Витамин А; 7. Повреждающее действие свободных радикалов на компоненты клетки; 8. Образование супероксида в ЦПЭ,
V Наименование лабораторной работы:
VI Перечень вопросов для проверки исходного уровня знаний:
ЛАБОРАТОНАЯ РАБОТА №1
Количественное определение малонового диальдегида в ткани печени.
ОБОРУДОВАНИЕ: баня, ФЭК.
ПРИНЦИП МЕТОДА.
Основан на определении малонового диальдегида (МДА) как показателя перекисного окисления липидов при инкубации гомогенатов тканей в присутствии кислорода. В присутствии прооксидантов МДА определяется по специфической цветной реакции в кислой среде с 2-тиобарбитуровой кислотой (ТБК).
ХОД РАБОТЫ.
В трех центрифужных пробирках приготовить инкубационную смесь реактивов по следующей схеме:
| Реактивы | 1 пробирка “опытная” | 2 пробирка “контроль” | 3 пробирка “опытная” с добавлением про- оксидантов |
| Трис-буфер 0,15 М | 3,4 мл | 3,4 мл | 1,4 мл |
| Сульфат железа FeSO4 | - | - | 1 мл |
| Аскорбиновая кислота | - | - | 1 мл |
| ТХУ 10 раствор с ЭДТА | - | 1 мл | - |
| Гомогенат печени | 1,0 мл | 1,0 мл | 1,0 мл |
Все пробирки поместить в термостат при 37оС на 15 минут. После инкубации остановить реакцию в 1 и 3 пробирках, добавляя в них по 1 мл ТХУ с ЭДТА, перемешать. Все пробирки центрифугировать в течение 20 минут при 3000 об/мин. Надосадочную жидкость осторожно слить в чистые пробирки. Затем в другие чистые пробирки отобрать по 4 мл надосадочной жидкости, добавить по 2 мл свежеприготовленного раствора ТБК (тиобарбитуровая кислота) и поместить пробирки в кипящую баню на 15 минут. Пробирки охладить в холодной воде и определить оптическую плотность на ФЭКе с зеленым светофильтром (длина волны 540 нм) в кювете 10 мм.
РЕЗУЛЬТАТЫ:
Активность ПОЛ выражается количеством микромолей МДА, накопленного за период инкубации в 1 мл гомогената
.
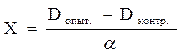 , где
, где
Х - количество МДА, накопленного за период инкубации в 1 мл гомогената,
- молярный коэффициент экстинкции для малонового диальдегида при реакции с ТБК, численно равный 0.156.
Dоп и D конт - оптические плотности "опытной" и "контрольной" пробирок соответственно.
Рассчитать активность ПОЛ в 1 и 3 пробирках и сделать вывод об активности ПОЛ и влиянии ионов Fe2+ и аскорбата на перекисное окисление липидов.
РАСЧЕТ И ВЫВОДЫ:
ЛАБОРАТОНАЯ РАБОТА №2
Количественное определение каталазы в крови.
ПРИНЦИП МЕТОДА.
В основе количественного определения активности каталазы лежит определение количества перекиси водорода, разложенной ферментом за определенный промежуток времени. О количестве расщепленной перекиси водорода судят по разности количества перманганата калия. израсходованного на титрование перекиси водорода до и после действия каталазы.
Активность каталазы выражают с помощью каталазного числа. Каталазным числом называют количество мг перекиси водорода, которое разлагается под действием 1 мкл крови.
ХОД РАБОТЫ.
Работу проводят по следующей схеме:
| Р е а к т и в ы | Стаканчик № 1 (опыт) | Стаканчик № 2 (контроль) |
| Кровь | 1 мл | 1 мл |
| Вода дистиллированная | 7 мл | 7 мл |
| Перекись водорода 1% | 2 мл | - |
| Серная кислота 10% | - | 5 мл |
| Стаканчики оставляют на 30 мин при комн. t, изредка встряхивая Через 30 мин | ||
| Перекись водорода 1% | - | 2 мл |
| Серная кислота 10 % | 5 мл | - |
Действие каталазы в кислой среде прекращается, т. к. этот фермент действует при рН=7,4. Поскольку в контрольную пробу серную кислоту приливали до добавления перекиси водорода, то в контроле все добавленное количество перекиси водорода остается нерасщепленным.
Содержимое каждого стаканчика необходимо титровать раствором перманганата калия до розового окрашивания, не исчезающего в течение 30 сек.
Рассчитать каталазное число (КЧ) по формуле:
КЧ = (А - В) х 1,7,
где:
А - кол-во 0,1 N раствора КМnО4, пошедшее на титрование контрольной пробы в мл.
В - кол-во 0,1N раствора КМnО4, пошедшее на титрование опытной пробы в мл.
1,7 - это коэффициент, показывающий, сколько мг Н2О2 содержится в 1мл 0,1н. раствора Н2О2.
В норме каталазное число колеблется от 10 до 15 единиц у взрослых и 7,5 - 9,9 единиц у детей.
РАСЧЕТ И ВЫВОДЫ:
Самостоятельная работа: составление тестов и кроссворда по теме ПОЛ.
Тестовый контроль:
Тема: ПОЛ.
Дата: 2018-12-28, просмотров: 333.