Образование АФК, известных как прооксиданты, наблюдается во многих метаболических процессах и является обязательным атрибутом нормальной аэробной жизни. Функционирование и развитие клеток, а так же организма в целом, в кислородсодержащем окружении не могло бы быть возможным без существования защитных систем, основу которых составляют ферментативные и неферментативные антиоксиданты. Постоянное образование прооксидантов в живых организмах уравновешено их дезактивацией антиоксидантами, поэтому для поддержания гомеостаза необходима непрерывная регенерация антиоксидантной способности. Отсутствие или сбои этой непрерывности сопровождаются накоплением окислительных повреждений и приводят к возникновению окислительного стресса.
Классификация АОС системы:
А.Специфическая АОС:
· Специализированные ферментные системы:
ü Супероксиддисмутаза (СОД);
ü Каталаза (КАТ);
ü Глутатионпероксидаза и глутатион трансфераза (ГПО и ГТ)
(локализуются преимущественно внуриклеточноо0
· Специализированные неферментные системы:
ü Жирорастворимые антиоксиданты (АО): витамины Е,А,К; стероидные гормоны; влавоноиды; полифенолы (витамин Р, убихинон).
ü Аскорбатная АО-система;
ü Тиолдисульфидна система на основе глутатиона;
ü Ароматические соединения.
Б. Неспецифическая АОС
Основными функциями специфической АОС являются:
1. ограничение интенсивности реакции свободнорадикального и перекисного окисления, т.е. разрушение, образующихся АФК и продуктов их дальнейших превращений;
2. защита чувствительных к окислительным повреждениям биомолекул мембран, внутри - и внеклеточных структур от действия свободных радикалов и перекисных соединений;
3. восстановление окислительных молекулярных повреждений. В целом основная задача системы антиоксидантной защиты состоит в предотвращении и ограничении развития патологических состояний, вызываемых окислительными повреждениями структур организма.
Неспецифическая АОС
Функция: предотвратить условия в процессе аутоокисленисубстратов (микросомальное окисление).
Ферментативное звено АОС
К ферментам, защищающим клетки от действия активных форм кислорода, относят супероксиддисмутазу, каталазу и глутатионпероксидазу; Наиболее активны эти ферменты в печени, надпочечниках и почках, где содержание митохондрий, цитохрома Р450 и пероксисом особенно велико.
СОД - это ключевой водорастворимый фермент. Превращает супероксидные анионы в пероксид водорода: 2 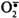 + 2H+ → H2O2 + O2 интка, железа и имидазол гистидина. Локализуется в цитоплазме. Обладает высокой термоустойчивостью, устойчив к действию протеаз, обладает широким оптимумом рН каталитической активности.
+ 2H+ → H2O2 + O2 интка, железа и имидазол гистидина. Локализуется в цитоплазме. Обладает высокой термоустойчивостью, устойчив к действию протеаз, обладает широким оптимумом рН каталитической активности.
Изоферменты СОД находятся и в цитозоле и в митохондриях и являются как бы первой линией защиты, потому что супероксидный анион образуется обычно первым из активных форм кислорода при утечке электронов из дыхательной цепи.
СОД - индуцируемый фермент, т.е. синтез его увеличивается, если в клетках активируется перекисное окисление. Пероксид водорода, который может инициировать образование самой активной формы ОН•, разрушается ферментом каталазой: 2Н2О2 → 2 Н2О + О2.
Каталаза (КАТ) находится в основном в пероксисомах, где образуется наибольшее количество пероксида водорода, а также в лейкоцитах, где она защищает клетки от последствий "респираторного взрыва".
КАТ обеспечивает расщепление перекисси водорода до двух молекул воды и кислорода. Из-за большго молекулярного веса практичеки не проникает через мембрану клетки.
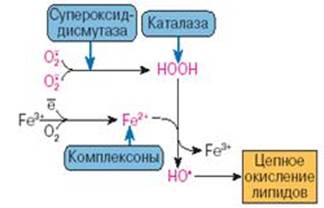
| Рис.2. Антиоксиданты водной фазы |
Глутатионпероксидаза (ГПО) - важнейший фермент, обеспечивающий инактивацию АФК, так как он разрушает и пероксид водорода и гидропероксиды липидов. Он катализирует восстановление пероксидов с помощью трипептида глутатиона (γ-глутамилцистеинилглицин). Сульфгидрильная группа глутатиона (GSH) служит донором электронов и, окисляясь, образует дисульфидную форму глутатиона, в которой 2 молекулы глутатиона связаны через дисульфидную группу.
Н2О2 + 2 GSH → 2 Н2О + G-S-S-G.
Окисленный глутатион восстанавливается глутатионредуктазой:
GS-SG + NADPH + Н + → 2 GSH + NADP+.
Глутатионпероксидаза, которая восстанавливает гидропероксиды липидов в составе мембран, в качестве кофермента использует селен (необходимый микроэлемент пищи). При его недостатке активность антиоксидантной защиты снижается.
ГПО является главной ферментативной системой плазмы крови: внеклеточных жидкостей и гидроперекисей липидов (ГПО 4), которая будучи липофильным соединением эффективно взаимодействует с гидроперекисями фосфотидилхолина, холестерина и эфиров холестерина в липопротеинах низкой плотности (ЛПНП), восстанавливая их, следовательно, защищая от окислительной модификации. Кроме того ГПО 4 совместно с токоферолом практически полностью подавляет ПОЛ в биологических мембранах благодаря тому, что витамин Е эффективно восстанавливает пероксирадикалы, а фермент разлагает гидроперекиси, препятствуя тем самым их вовлечению в окислительный цикл.
Глутатионтрансфераза (ГТ)
ГТ, в отличие от селенсодержащей ГПО, для которой лучшими субстратами являются гидрофильные гидроперекиси с малым размером молекул, эффективно восстанавливает гидрофобные гидроперекиси с большим объемом молекулы: гидроперекиси полиненасыщенных жирных кислот (линолевой и арахидоновой), фосфолипидов.
Вместе с тем во всех водных и липидных фазах организма могут протекать радикальные окислительные процессы, в защите от которых важную роль играют антиоксиданты-ингибиторы органических радикалов, среди которых важное место занимают соединения фенольного типа.
В настоящее время выделено несколько тысяч фенольных соединений, среди которых выраженным антиоксидантным эффектом обладают витамины Е и К, убихиноны, триптофан и фенилаланин, а так же большинство растительных (флавоноиды) и животных пигментов.
Неферментативнгое звено АОС
Витамин Е (α-токоферол) - наиболее распространённый антиоксидант в природе - является липофильной молекулой, способной инактивировать свободные радикалы непосредственно в гидрофобном слое мембран и таким образом предотвращать развитие цепи перекисного окисления. Различают 8 типов токоферолов, но α-токоферол наиболее активен.
Витамин Е отдаёт атом водорода свободному радикалу пероксида липида (ROO•), восстанавливая его до гидропероксида (ROOH) и таким образом останавливает развитие ПО. Свободный радикал витамина Е, образовавшийся в результате реакции, стабилен и не способен участвовать в развитии цепи. Наоборот, радикал витамина Е непосредственно взаимодействует с радикалами липидных перекисей, восстанавливая их, а сам превращается в стабильную окисленную форму -- токоферолхинон.
В антирадикальной защите липопротеинов плазмы крови и клеточных мембран α-токоферолу принадлежит ведущая роль – одна его молекула защищает ≈10000 молекул ненасыщенных жирных кислот, при этом считается, что α-токоферол способен обезвредить не менее 60% образующихся пероксильных радикалов. Окисление α-токоферола со свободными радикалами компенсируется биорегенерацией молекул этого антиоксиданта в реакциях восстановления коантиоксидантами (АН), редокс-потенциал которых ниже, чем у радикала α-токоферола (α-Тф-О.). В результате такой реакции не только происходит восстановление витамина Е, но и предотвращается возможность инициации α-токофероксильным радикалом окисления липидов:
α-Тф-О. + RH→ α-Тф-ОH + R. (1)
α-Тф-О. + АH→ α-Тф-ОH + А. (2)
В физиологических условиях вторая реакция обычно превалирует над первой, так как константа скорости реакции α-Тф-О. с НЖК не превышает 103М-1с-1, в то время как для реакции (1) константа скорости может достигать значений 104-107М-1с-1.К наиболее изученным коантиоксидантам относятся убихинол, аскорбиновая кислота (АК), билирубин.
Витамин Е (а-токоферол) ингибирует свободнорадикальное окисление путём отдачи электрона, что приводит к инактивации радикала липида, а витамин Е превращается в стабильный, полностью окисленный токоферолхинон.
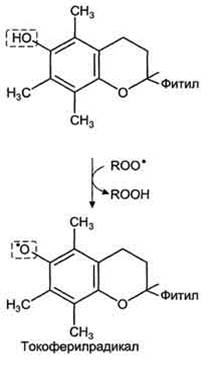
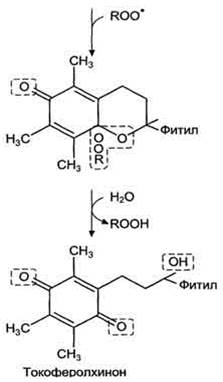
Рис. 3. Механизм антиоксидантного действия витамина Е.
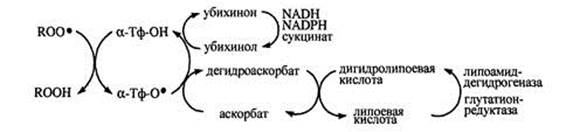
Рис.4. Окислительно-восстановителные превращения α-токоферола и сопряженных с ним коантиоксидантов.
Витамин С (Рис.5.) (аскорбиновая кислота) также является антиоксидантом и участвует с помощью двух различных механизмов в ингибировании ПОЛ. Во-первых, витамин С восстанавливает окисленную форму витамина Е и таким образом поддерживает необходимую концентрацию этого антиоксиданта непосредственно в мембранах клеток. Во-вторых, витамин С, будучи водорастворимым витамином и сильным восстановителем, взаимодействует с водорастворимыми активными формами кислорода - 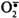 , Н2О2, ОН• и инактивирует их.
, Н2О2, ОН• и инактивирует их.
β-Каротин, предшественник витамина А (рис.6.), также обладает антиоксидантаьш действием и ингибирует ПОЛ. Показано, что растительная диета, обогащённая витаминами Е, С, кароти-ноидами, существенно уменьшает риск развития атеросклероза и заболеваний ССС, подавляет развитие катаракты - помутнения хрусталика глаза, обладает антиканцерогенным действием. Имеется много доказательств в пользу того, что положительное действие этих компонентов пищи связано с ингибированием ПОЛ и других молекул и, следовательно, с поддержанием нормальной структуры компонентов клеток.
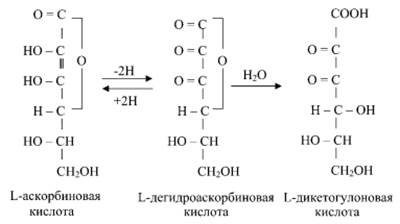 Рис.5. Витамин С.
Рис.5. Витамин С.
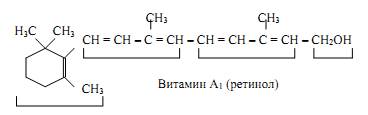 Рис. 6. Витамин А
Рис. 6. Витамин А
АК превосходит другие антиоксиданты плазмы в защите липидов от перекисного окисления, так как только это соединение достаточно реакционноспособно, чтобы эффективно ингибировать инициацию ПОЛ в водной фазе.
Важными внеклеточными антиокислителями являются альбумины – простые гидрофильные белки плазмы крови, которые являются основными носителями SН групп. SН содержащим соединениям принадлежит ведущая роль в защите клеток от ОН-радикала, образующегося в реакции Фентона или в результате разложения молекул воды под действием ионизирующих излучений.
Необходимо отметить наличие антирадикальных свойств у белков, хелатирующих ионы железа и других металлов с переменой валентностью. В первую очередь это трансферрин, лактоферрин и церулоплазмин. Основная роль трансферрина и близкого ему по структуре лактоферрина, содержащегося в молоке и выделяющегося фагоцитами при их активации, состоит в акцептировании «свободного» железа, что препятствует образованию радикалов НО, в реакциях Фентона, катализируемых ионами Fe. Значимую роль в этом процессе играет церулоплазмин, Cu-содержащий белок, обеспечивающий окисление Fe 2+ до Fe3+ и делающий тем самым железо доступным для связывания трансферрина.
Наиважнейшим антиоксидантом внеклеточной жидкости является мочевая кислота (МК). Ввиду высокого ее содержания в плазме крови человека некоторые исследователи считают, что на нее приходится 35-65% защиты липопротеинов от окисления, 10-15% ингибирования НО. и 12% ингибирования синглетного кислорода. Кроме того МК может выступать синергистом с радикалами α-токоферола и аскорбиновой кислотой, что усиливает их антиоксидантное действие.
В последние годы широко обсуждается роль активных форм кислорода (АФК) и инициируемых ими свободнорадикальных процессов при различных патологических процессах. В нормальных условиях активность этих процессов находится на невысоком уровне, но при стрессовых ситуациях происходит усиленное образование АФК, под действием которых происходит избыточная и неконтролируемая активация процессов перекисного окисления липидов (ПОЛ), что в конечном итоге может привести к патологическому состоянию, которое сопровождается дисбалансом ферментативных и неферментативных компонентов системы антиоксидантной защиты. Характерным проявлением окислительного стресса является интенсификация процессов перекисного окисления липидов, индикатором которой служит увеличение содержания хотя бы одного из его продуктов. Данные о содержании продуктов ПОЛ в биологических объектах могут нести в себе информацию о глубине и степени патологического процесса. В качестве количественных маркеров наиболее часто используются такие интермедиаты ПОЛ, как диеновые конъюгаты (ДК), а также один из его конечных продуктов – малоновый диальдегид (МДА).
II Цель деятельности студентов на занятии
Студент должен знать:
1. АФК. Каким действием они обладают;
2. Источники образования АФК;
3. ПОЛ в норме;
4. ПОЛ при патологии;
5. Стадии ПОЛ;
6. АОС, классификация, функции;
7. Ферментативное звено АОС;
8. Описать действие СОД, характеристики;
9. КАТ. Механизм действия;
10. ГПО и ГП. Механизм действия;
11. Неферментативное звено АОС;
12. Роль ионов меди, цинка, железа и других металлов в АОС;
13. «Окислительный стресс»;
Студент должен уметь:
1. Уметь писать реакцию, катализируемую СОД;
2. Уметь писать реакцию, катализируемую КАТ;
3. Уметь писать реакцию, катализируемую ГПО;
4. Написать стадии ПОЛ;
5. Роль витамина Е в стрессовой ситуации.
III Содержание обучения:
Основные вопросы:
1. АФК. Механизм действия;
2. Источники АФК в организме;
3. ПОЛ в норме;
4. Особенности ПОЛ в условиях патологии;
5. Стадии ПОЛ;
6. АОС, классификация, функции;
7. Ферментативное звено АОС;
8. Характеристики СОД. Механизм действия;
9. КАТ. Механизм действия;
10. ГПО и ГП. Механизм действия;
11. Неферментативное звено АОС;
12. Роль витамина Е в стрессовой ситуации.
13. Роль витамина А,К в защите клеток от действия АФК;
14. Роль ионов меди, цинка, железа и других металлов в АОС;
15. «Окислительный стресс».
Дата: 2018-12-28, просмотров: 444.