Строение сплавов, фазы и компоненты.
Что называют металлическими сплавами?
Металлическими сплавами называют сплавы металлов с металлами и неметаллами, у которых сохраняются металлические свойства (прочность, металлический цвет, пластичность, теплопроводность).
Что называют компонентами сплавов?
Элементы или химические соединения, образующие сплав, называются компонентами. Компонентами металлических сплавов могут быть не только металлы, но и неметаллы. В зависимости от числа компонентов сплавы могут быть: двойные (Fe – C); тройные (Cu – Zn – Al); четверные; сложные.
В зависимости от физико-химического взаимодействия компонентов в сплавах образуются фазы, число и тип которых характеризуют состояние сплава.
Что называют фазой? Структурой?
Фазой называют однородную часть сплава, отделенную от других частей сплава поверхностью раздела, и характеризующуюся определенным составом, свойствами, типом кристаллической решетки.
Что называют структурой?
Под структурой понимают форму, размеры и характер взаимного расположения фаз в сплаве. Фазовый состав и структура, определяющие свойства сплава, зависят от состава и технологии его обработки.
5.1.5. Охарактеризуйте строение сплавов.
В жидком состоянии образующие сплав элементы обычно неограниченно растворяются друг в друге, образуя жидкие растворы. В твердом состоянии элементы могут образовывать три вида взаимодействия:
1) механические смеси, представляющие собой смесь двух или нескольких фаз;
2) твердые растворы, когда один компонент растворяется в другом, который называется растворителем;
3) химические соединения, когда компоненты вступают в химические взаимодействия.
5.1.6.Охарактеризуйте механические смеси.
Механические смеси образуются в случае, если элементы, входящие в состав сплава, при затвердевании из
жидкого состояния не растворяются друг в друге и не взаимодействуют друг с другом, например, Pb – Sb. Каждый элемент сохраняет свою кристаллическую решетку. При металлографическом анализе на шлифе видны кристаллиты разных компонентов, образующих механическую смесь.
Охарактеризуйте твердые растворы.
Твердыми растворами называют фазы, в которых один из компонентов сплава сохраняет свою кристаллическую решетку, а атомы другого компонента располагаются в решетке первого компонента (растворителя), изменяя ее размеры. Таким образом, твердый раствор, состоящий из двух компонентов, имеет один тип решетки и представляет собой одну фазу.
Различают твердые растворы замещения и твердые растворы внедрения.
При образовании твердого раствора замещения (рис.1,б) атомы растворенного компонента замещают часть атомов растворителя в его кристаллической решетке. Все металлы в той или иной степени взаимно растворяются друг в друге в твердом состоянии, образуя твердые растворы ограниченной растворимости. Например, в алюминии может растворяться до 5,5 % Cu. Если же оба компонента имеют однотипные кристаллические решетки, а атомные диаметры различаются не более чем на 8-15%, то возможно образование твердых растворов неограниченной растворимости. Неограниченно растворяются в твердом состоянии металлы с ГЦК решеткой, имеющие небольшую разницу в атомных размерах, как Au и Ag, Ni и Сu.
При образовании твердого раствора внедрения (рис.1,в) атомы растворенного компонента располагаются в междоузлиях (пустотах) кристаллической решетки растворителя. Твердые растворы внедрения образуются только в тех условиях, когда диаметр атома растворенного элемента невелик (С, В, N, Н, О). Концентрация второго компонента в твердом растворе обычно невысока и всегда ниже, чем в твердых растворах замещения.
Диаграммы состояния и принцип их построения.
Рис. 1. Диаграмма состояния, кривые охлаждения и схемы структур сплав системы Pb - Sb при полном охлаждении до комнатной температуры.
Система сплавов Pb-Sb включает в себя составы со 100 % РЬ и 0 % Sb, т. е. чистый свинец, и со 100 % Sb и 0 % РЬ, т. е. чистую сурьму. Кривые охлаждения для этих чистых металлов имеют по одному горизонтальному участку, характеризующему температуру кристаллизации: соответственно для свинца 327 °С и для сурьмы 631 °С. На диаграмме состояния эти температуры находятся на осях ординат, где содержатся соответственно чистый свинец и чистая сурьма. Структура чистых металлов представляет собой однородные зерна.Сплав, содержащий 13 % Sb и 87 % РЬ, также имеет один горизонтальный участок, т. е. одну критическую точку (245 °С) температуру затвердевания этого сплава. Этот сплав характеризуется тем, что в нем происходит одновременная кристаллизация жидкой фазы кристаллов РЬ и Sb (в общем случае компонентов и В) с образованием механической смеси. Такая механическая смесь двух (или более) видов кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой. Сам сплав 13 % Sb и 87 % РЬ является эвтектическим, а его микроструктуру представляет собой попеременно чередующиеся выделения сур мы в свинцовой основе (рис.1). Принято эвтектическую реакцию записывать так: Ж —> Pb + Sb, или в общем виде Ж —> А + В.
Кристаллизация любого сплава, имеющего 0 % < Sb < 13%, начинается с выделения кристаллов РЬ. Эти сплавы затвердевай в интервале температур, и на кривых охлаждения имеются критические точки, соответствующие началу и концу затвердевания (например, сплав с 5 % Sb, рис. 1). Все они называются доэвтектическими сплавами, претерпевают эвтектическое превращение при охлаждении ниже температуры 245 °С и имеют после окончательного охлаждения структуру РЬ + Э(РЬ + Sb), рис. 1. В этой структуре имеется две структурные составляющие: кристаллы РЬ и эвтектика Э(РЬ + Sb), которые получаются на ба; двух фаз: кристаллов РЬ и кристаллов Sb.
Кристаллизация любого сплава с концентрацией 100 % > Sb > 13 % начинается с выделения кристаллов Sb. Эти сплавы также затвердевают в интервале температур - начала и конца затвердевания (например, сплав с 40% Sb, рис.1). При охлаждении ниже температуры 245 °С в них протекает эвтектическое превращение. Эти сплавы называются заэвтектическими и имеют после охлаждения окончательную структуру Sb + Э(РЬ + Sb), рис. 1. Структура заэвтектических сплавов также является двухфазной (кристаллы Sb и РЬ) и состоит из двух структурных составляющих: кристаллов Sb и эвтектики Э (Pb + Sb).
На диаграмме можно выделить три характерные зоны: область, где существует только жидкая фаза, - выше системы линий, ограниченной точками: температура 327 °С - эвтектическая точка 245 °С - температура 631 °С; область, где существует только твердая фаза (кристаллы РЬ и Sb), - ниже эвтектической линии (вся горизонтальная линия на уровне температуры 245 °С с концами в месте ее пересечений с ординатами со 100 % РЬ и 100 % Sb); область, где одновременно сосуществует жидкая и твердая фаза (область с жидко-твердой фазой) - между линиями, ограничивающими соответственно жидкое и твердое состояние сплавов.
Линия, ограничивающая на диаграмме область жидкой фазы сплавов, называется линией ликвидус. Линия, ограничивающая область полностью затвердевшего сплава от остальной области на диаграмме состояний, называется линией солидус.
5.3.2. Охарактеризуйте диаграмму состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (диаграмма II рода)
Исходные данные: оба компонента неограниченно растворимы в твердом и жидком состоянии и не образуют химических соединений.
Компоненты: химические элементы А, В (К = 2).
Фазы: жидкость Ж, кристаллы α- твердого раствора (Ф = 2).
Примером сплавов с такими диаграммами состояния являются сплавы системы Cu - Ni .
Если два компонента (А и В) неограниченно растворяются в жидком и твердом состоянии, то они не могут при затвердевании образовывать собственных кристаллов во всех сплавах на базе этих компонентов. Соответственно при кристаллизации в этих сплавах будут выделяться кристаллы α-твердого раствора, а, следовательно, максимальное число фаз в этих сплавах равняется двум (жидкость и α-твердый раствор). В этом случае в соответствии с правилом фаз кристаллизация всех сплавов будет протекать только в интервале температур (кристаллизация при постоянной температуре у сплавов возможна только при наличии трех фаз) и, соответственно, на диаграмме состояния отсутствует горизонтальная линия, а присутствуют только наклонные кривые (рис..2)
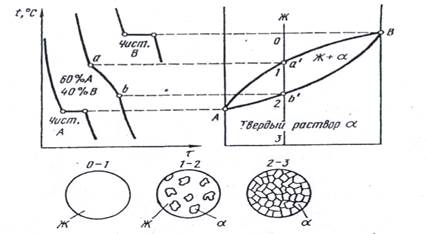
Рис. 2. Диаграмма состояния, кривые охлаждения и схемы типовых структур сплавов с неограниченной растворимостью в твердом состоянии.
На диаграмме (рис. 2) присутствуют три области: обл. выше линии Аа'В - жидкость; область между линиями Аа АЬ'В - жидкость и твердый раствор. Ниже линии АЬ'В - область твердого раствора. Линия Аа'В является линией ликвидус, а линия А ь 'В - линией солидус.
Кристаллизация любого сплава начинается выпадением жидкого расплава отдельных кристаллов твердого раствора,
например, в точке а', рис. 2) и заканчивается полным затвердением твердого раствора (например, в точке Ь', рис.2). Но так в интервале кристаллизации (например, между точками а' рис.2) сплавы находятся в двухфазном состоянии (Ж + а)
при понижении температуры должно изменяться соотношение количества жидкой и твердой фазы в двухфазной области - количество жидкости уменьшается, а количество α-твердого раствора растет. Кроме того, при понижении температуры будут меняться также составы жидкой и твердой фаз.
Рис. 5. Диаграмма состояния с устойчивым химическим соединением.
Примером диаграмм этого типа является диаграмма состояния сплавов системы Mg—Ca.
Химическое; соединение (например, АnВm ) характеризуется определенным соотношением компонентов (например, п % компонента А и т % компонента В). На оси концентрации компонентов (ось абсцисс) химическое соединение обозначает точку, из которой выходит вертикальная линия, фактически разбивающая диаграмму на две простые диаграммы, в которых химическое соединение выступает уже в качестве самостоятельного компонента и, соответственно, образует эвтектики с компонентом А по реакции Ж → А + АnВm (I простая диаграмма) и с компонентом В по реакции Ж → В + АnВm (II простая диаграмма).
Кристаллизация сплавов в пределах I и II простых диаграмм проходит аналогично кристаллизации сплавов, образующих эвтектику из чистых компонентов (диаграмма I рода). Поэтому после окончательного остывания у эвтектического сплава на I простой диаграмме структура будет состоять только из эвтектики Э(А + АnВm), у эвтектического сплава на II простой диаграмме - из эвтектики Э (В + АnВm); у доэвтектических сплавов соответственно на I простой диаграмме и на II простой диаграмме структура будет иметь вид: A + Э(А + АnВm) и АnВm + Э(В + АnВm); у заэвтектических сплавов на I простой диаграмме - АnВm + Э(А + АnВm ) и у заэвтектических сплавов на II простой диаграмме - В + Э(В + АnВm ).
Строение сплавов, фазы и компоненты.
Дата: 2018-11-18, просмотров: 1203.