Строение атома является сложным. Это подтверждают открытия таких явлений, как электрон, рентгеновские лучи и радиоактивность. В результате теоретических исследований и многочисленных опытов была построена теория строения атома. Особенно важный вклад в создание теории строения атома внёс английский физик Эрнест Резерфорд (1871 – 1937), который проводил опыты по изучению прохождения альфа-частиц через тонкие металлические пластины золота и платины.
Резерфорд в 1906 году предложил провести зондирование атомов тяжёлых элементов альфа-частиц с энергией 4,05 МэВ, которые испускались ядром урана или радия. Таким образом предлагалось изучить рассеяние (изменение направления движения) альфа-частиц в веществе.
Масса альфа-частицы примерно в 8000 раз больше массы электрона. Положительный заряд равен по модулю удвоенному заряду электрона 2е. Скорость альфа-частицы составляет 1/15 скорости света или 2 * 107 м/с. Альфа-частица – это полностью ионизированный атом гелия.
Упрощенная схема опытов Резерфорда изображена на рис. 1.1. Альфа-частицы испускались радиоактивным источником 1, помещённым внутри свинцового цилиндра 2 с узким каналом 3. Узкий пучок альфа-частиц из канала падал на фольгу 4 из исследуемого материала, перпендикулярно к поверхности фольги. Из свинцового цилиндра альфа-частицы проходили только через канал, а остальные поглощались свинцом. Прошедшие сквозь фольгу и рассеянные ею альфа-частицы попадали на полупрозрачный экран 5, который был покрыт люминесцирующим веществом (сульфатом цинка). Это вещество было способно светиться при ударе об него альфа-частицы. Столкновение каждой частицы с экраном сопровождалось вспышкой света. Эта вспышка называется сцинтилляция (от латинского scintillation – сверкание, кратковременная вспышка света). За экраном находился микроскоп 6. Чтобы не происходило дополнительного рассеяния альфа-частиц в воздухе, весь прибор размещался в сосуде с достаточным вакуумом.
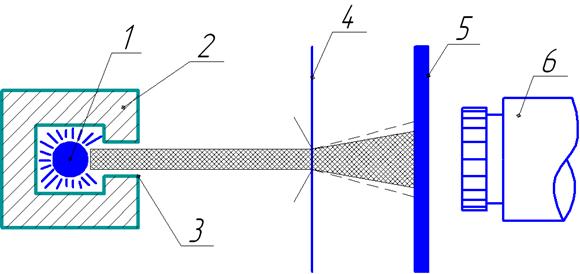
Рис. 1.1. Упрощённая схема опытов Резерфорда.
В отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа-частиц. Но когда на пути движения альфа-частиц помещали тонкую золотую фольгу толщиной примерно 0,1 мк (микрон), то наблюдаемая на экране картинка сильно менялась: отдельные вспышки появлялись не только за пределами прежнего кружка, но их можно было даже наблюдать с противоположной стороны золотой фольги.
Подсчитывая число сцинтилляций в единицу времени в разных местах экрана, можно установить распределение в пространстве рассеянных альфа-частиц. Число альфа-частиц быстро убывает с увеличением угла рассеяния.
Наблюдаемая на экране картина позволила заключить, что большинство альфа-частиц проходит сквозь золотую фольгу без заметного изменения направления их движения. Однако некоторые частицы отклонялись на большие углы от первоначального направления альфа-частиц (порядка 135о…150о) и даже отбрасывались назад. Исследования показали, что при прохождении альфа-частиц сквозь фольгу примерно на каждые 10000 падающих частиц только одна отклоняется на угол более 10о от первоначального направления движения. Лишь в виде редкого исключения одна из огромного числа альфа-частиц отклоняется от своего первоначального направления.
Тот факт, что многие альфа-частицы проходили сквозь фольгу, не отклоняясь от своего направления движения, говорит о том, что атом не является сплошным образованием. Так как масса альфа-частицы почти в 8000 раз превосходит массу электрона, то электроны, входящие в состав атомов фольги, не могут заметно изменить траекторию альфа-частиц. Рассеяние альфа-частиц может вызывать положительно заряженная частица атома – атомное ядро.
Атомное ядро – это тело малых размеров, в котором сконцентрированы почти вся масса и почти весь положительный заряд атома.
Чем ближе альфа-частица подходила к ядру, тем больше была сила электрического взаимодействия и тем на больший угол частица отклонялась. На малых расстояниях от ядра положительно-заряженная альфа-частица испытывает значительную силу отталкивания F от ядра, которую определяют по закону Кулона:
| F = | 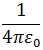
| • | 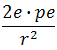
|
где r – расстояние от ядра до альфа-частицы; ε0 – электрическая постоянная в единицах измерения СИ; p – число протонов в ядре; е = 1,6*10-19 Кл – абсолютное значение элементарного электрического заряда (заряда электрона); 2e – заряд альфа-частицы
На рисунке 1.2 показаны траектории альфа-частиц, пролетающих на различных расстояниях от ядра.
Резерфорд смог ввести формулу, связывающую количество рассеянных на определённый угол альфа-частиц с энергией альфа-частиц и протонов р в ядре атома. Опытная проверка формулы подтвердила её справедливость и показала, что количество протонов в ядре равно числу внутриатомных электронов Z и определяется атомным номером химического элемента (то есть порядковым номером элемента в периодической системе Д.И.Менделеева):
p = Z
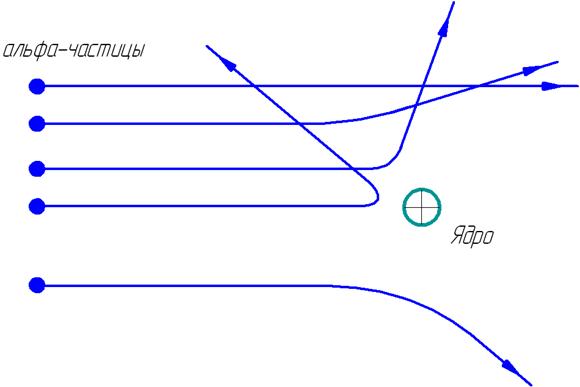
Рис. 1.2. Траектории альфа-частиц.
Подсчитывая количество альфа-частиц, рассеянных на различные углы, Резерфорд смог оценить линейные размеры ядра. Чтобы положительное ядро могло отбросить альфа-частицу назад, потенциальная энергия электростатического (кулоновского) отталкивания у границ ядра атома должна равняться кинетической энергии альфа-частицы:
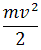
| = | 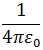
| • | 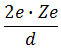
|
Оказалось, что ядро имеет диаметр:
dя = 10-13…10-12 см = 10-15…10-14 м
Линейный диаметр самого атома:
da = 10-8 см = 10-10 м
Планетарная модель атома
После анализа многочисленных опытов, Резерфордом в 1911 году была предложена планетарная модель атома (ядерная модель атома).
Согласно этой модели в центре атома находится положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Вокруг ядра вращаются по орбитам отрицательно заряженные электроны. Электроны движутся вокруг ядра на относительно больших расстояниях, подобно тому, как планеты вращаются вокруг солнца. Из совокупности этих электронов образуется электронная оболочка или электронное облако.
Атом в целом нейтрален, следовательно, абсолютное значение суммарного отрицательного заряда электронов равно положительному заряду ядра: число Z*e протонов в ядре равно числу электронов в электронном облаке и совпадает с порядковым номером (атомным номером) Z атома данного химического элемента в периодической системе Д.И.Менделеева.
Например, атом водорода имеет порядковый номер Z = 1, следовательно, атом водорода состоит из положительного ядра с зарядом, равным абсолютному значению заряда электрона. Вокруг ядра вращается один электрон. Ядро атома водорода названо протоном. Атом лития имеет порядковый номер Z = 3, следовательно, вокруг ядра атома лития вращаются 3 электрона.
Дата: 2018-09-13, просмотров: 1226.