Введение
В последнее время большое значение приобретают нозокомиальные грибковые инфекции, что связано с увеличением их возникновения и сложностью диагностики и лечения. Целью этой курсовой работы является проанализировать последние литературные данные и исследования и выявить динамику внутрибольничных инфекций, вызванных грибами рода рода Candida. Определить основные причины и факторы этих заболеваний, и выявить группы риска людей, подверженных к возникновению у них нозокомиальных грибковых инфекций.Так же целью является описать эпидемиологию и рассмотреть наиболее часто встречающиеся клинические проявления нозокомиальных кандидозов. Актуальность работы в том, что в ней систематизируются все имеющиеся знания, рассматриваются основные принципы клинической диагностики нозокомиального кандидоза, наиболее рациональные методы лечения и проведения профилактики, что очень важно для уменьшения случаев инфицирования нозокомиальными штаммами Candida и в целом для снижения количества внутрибольничных грибковых заболеваний.
Глава 1. Понятие, причины и динамика внутрибольничных инфекций, вызванных грибами рода Candida
Понятие о внутрибольничной инфекции
По определению ВОЗ, нозокомиальная инфекция - это любое клинически распознаваемое инфекционное заболевание, которое развивается у пациента в результате его обращения в больницу за лечебной помощью или пребывания в ней, а также любое инфекционное заболевание сотрудника больницы, развившееся вследствие его работы в данном учреждении, вне зависимости от времени появления симптомов (после или во время нахождения в больнице).
Согласно другим, наиболее часто используемым критериям, к нозокомиальным можно отнести инфекции в случаях, когда пациент повторно поступает в стационар с установленной инфекцией, явившейся следствием предыдущей госпитализации, или, если инфекция, не находившаяся в стадии инкубации на момент поступления, развилась не ранее чем через 48 ч после госпитализации.
В зависимости от различных факторов, число госпитализированых пациентов, у которых развиваются нозокомиальные инфекции, колеблется от 3 до 5%.
Примерно 90% всех нозокомиальных инфекций имеет бактериальное происхождение, а вирусные, грибковые возбудители и простейшие встречаются значительно реже. [2,12] Но в последние годы отмечается все более возрастающая роль грибов, и особенно Candida spp., как возбудителей нозокомиальной инфекции. [10]
Глава 2. Эпидемиология нозокомиального кандидоза
Группы риска
К группам риска по инфицированию нозокомиальным кандидозом относятся:
- Пациенты с лейкемией и другими онкологическими заболеваниями, проходящие химиотерапию;
- Пациенты, подвергшиеся пересадке костного мозга или печени;
- Пациенты, перенесшие абдоминальные операции или операции на сердечно-сосудистой системе;
- Пациенты с ожогами;
- Недоношенные дети и новорожденные с низкой массой тела при рождении;
- Наркоманы;
- Пациенты с центральными катетерами, включая катетеры для гемодиализа;
- Пациенты, находящиеся на перитонеальном диализе;
- Иммунодефицитные пациенты, включая пациентов с ВИЧ;
- Пациенты, получающие лечение кортикостероидами;
- Пациенты, получающие антибиотики широкого спектра;
- Пациенты с постоянными мочевыми катетерами.[13]
Факторы риска
Основные факторы, способствующие увеличению частоты грибковых инфекций в ОИТ, включают:
- Расширение объема оперативных вмешательств, в том числе трансплантации органов.
- длительная противоопухолевая терапия, использование иммуносупрессоров. [10]
- Применение антибиотиков широкого спектра действия. Одним из важных факторов подавления нормальной микрофлоры считается нерациональная антимикробная терапия. Было показано, что ряд антибиотиков непосредственно стимулируют деление клеток С. albicans. Например, тетрациклины вызывают десквамацию кишечного эпителия, облегчая тем самым проникновение грибов в ткани.
- Постановка центрального венозного катетера.
- Химиотерапия.
- Лечение кортикостероидами.
- Катетеризация мочевого пузыря (постоянные катетеры).
- Присутствие искусственных органов/тканей (например, искусственный клапан сердца).
- Тотальное парентеральное питание (получение пиши не через пищеварительный тракт, а путем внутримышечных или внутривенных инъекций, особенно применение жировых эмульсий).
- Нейтропения. [13,9]
Учитывая трудности ранней диагностики генерализованной кандидозной инфекции, неспецифический характер ее клинических проявлений, решающее значение приобретает определение факторов риска развития этого крайне неблагоприятного осложнения. Выделение групп больных с высоким риском возникновения системного кандидоза позволяет не только обеспечить более высокий и целенаправленный уровень клинико-лабораторного мониторинга, но и своевременно начать "упреждающую" фунгицидную терапию (профилактику). Кроме того, выделение факторов риска системного кандидоза позволяет рационально относиться к применению фунгицидных средств и устранить порочную практику их назначения каждому больному, получающему антибиотики.
Определению факторов риска системного кандидоза посвящены многочисленные и достаточно репрезентативные исследования с использованием достоверных методов статистического анализа. Остальные факторы риска представлены в приложении 2.
Особое значение для возникновения патологической колонизации Candida spp. и развития системного кандидоза у больных имеют 4 группы факторов:
1) тяжесть основного заболевания;
2) применение антибиотиков широкого спектра действия;
3) факторы, связанные с многокомпонентным инвазивным мониторингом и методами интенсивного лечения;
4) факторы, обусловленные характером хирургического заболевания и оперативного вмешательства.
Однако следует учитывать, что так называемые агрессивные методы мониторинга и лечения сами по себе не являются независимыми факторами риска развития системного кандидоза, а используются у весьма тяжелой категории больных, у которых причинами развития кандидоза являются другие более значимые этиопатогенетические факторы (кишечная недостаточность с повреждением барьерной функции энтероцитов, интестинальная патологическая колонизация грибами и т.д.).
Для хирургической практики особое значение в качестве причины риска абдоминального кандидоза и кандидемии имеет ряд следующих факторов:
- перфорации ЖКТ (особенно толстой кишки);
- несостоятельность анастомозов пищеварительного тракта;
- послеоперационный перитонит;
- хирургические вмешательства по поводу острого панкреатита;
- различные формы деструктивного панкреатита и инфицированного панкреонекроза;
- состояние после спленэктомии.
Необходимо подчеркнуть важное место Candida spp. в развитии инфекционных осложнений панкреонекроза. Высеваемость грибов в этих случаях достигает 21%, причем основным путем является транслокация из толстой кишки. При панкреонекрозе интраабдоминальный кандидоз становится фактором необратимости патологического процесса. [10,15]
Диагностика кандидоза
Своевременный диагноз системного кандидоза представляет значительные трудности, поскольку клиническая симптоматика неспецифична. Поэтому решающая роль в диагностике кандидоза принадлежит лабораторным методам исследования – микроскопическим, культуральным, газохроматофическим и молекулярным.
Клинико-лабораторные проявления инвазивного кандидоза следующие:
- гипертермия, сохраняющаяся, несмотря на применение антибактериальной терапии;
- гистологические признаки грибковой инфекции (микроскопия биосубстрата: соскоб слизистой оболочки, кожи, раневое отделяемое, мокрота, биоптат; определение активновегетирующих клеток и псевдомицелия);
- выделение грибов кандида из крови и других стерильных анатомических зон;
- многофокусная колонизация Candida (в различных анатомических зонах) у больных, имеющих факторы риска;
- выявление при томографическом или ультразвуковом обследовании образований, подозрительных в отношении грибкового поражения (легкие, печень, селезенка);
- выявление грибкового эндофтальмита (экссудативное изменение сетчатки глаза желто-белого цвета);
- положительные серологические реакции (например, антигеновый тест Ramco).
Следует еще раз подчеркнуть, что диагностика грибковой инфекции, особенно у хирургических больных в ОИТ, представляет сложную задачу и базируется на сочетании неспецифических клинических признаков и данных микробиологического, гистологического, рентгенологического и серологического обследований. [5]
Микробиологическая диагностика
Поверхностный и кожно-слизистый кандидоз выявляют при микроскопии соскобов кожи и слизистой оболочки и выделением культуры возбудителя. Диагностику диссеминированных форм часто затрудняет недоступность поражённых органов для биопсии. В случаях, позволяющих получить образцы ткани, обнаруживают дрожжеподобные клетки и гифы.
Кандиды хорошо растут как на простых (среды Сабуро и др.), так и на кровяных или сывороточных средах. Оптимальная температура составляет 30-37 °С, оптимальный рН — 6,0-6,8, Колонии С. albicans на агаре Сабуро беловато-кремовые, блестящие, напоминают капли майонеза, Отличительными признаками С. albicans считают следующие.
• Способность ферментировать глюкозу и мальтозу с образованием кислоты и газа.
• При росте в жидких белковых средах при 37 °С через 2-4 ч бластоспоры подавляющего большинства штаммов С. albicans образуют особые выросты — ростовые трубки. Штаммы, не образующие их, — авирулентны.
• При культивировании при температуре 22-25 °С либо по мере истощения глюкозы в среде (4-7-е сутки) или на «голодных» средах С. albicans образует хламидиоспоры [14].
Гемокультура, а также выделение Candida из любой другой анатомической зоны, включая асцетическую жидкость, перитонеальный экссудат или ликвор, следует рассматривать как показание к проведению целеноправленной противогрибковой терапии. Необходимо иметь в виду, что в настоящее время серологические и биологические методы идентификации Candida находятся в процессе разработки, а их клиническая значимость пока точно не установлена.
Серологические методы включают определение антител к Candida spp. с помощью различных методов: агглютинации, иммуноэлектрофореза и иммуноделюции. К сожалению, интерпретация получаемых данных часто затруднительна, поскольку антитела обнаруживаются и у здоровых людей, и в случаях обычной колонизации. Более того, эти методы дают отрицательный результат при грибковой инфекции у больных с иммунодефицитными состояниями и в начальной стадии системного кандидоза. Большей информативностью обладают серологические методы определения антигенов Candida, однако они также обладают лишь умеренной чувствительностью в случаях системного кандидоза.
Перспективным методом диагностики является хроматографическое определение метаболитов грибов – D-арабинитола в различных биологических жидкостях и тканях инфицированных больных. Большинство патогенных Candida spp. (кроме C.crusei и C.glabrata) продуцируют значительное количество D-изомера арабинитола, и в сыворотке больных при инвазивном кандидозе определяется его повышенное содержание, а также повышение отношения D-арабинитол/креатинин. Разумеется, использование этого метода требует дорогостоящей хроматографической аппаратуры. Кроме того, инвазивный кандидоз во многих случаях протекает без кандидемии, что не может не отражаться на содержании D-арабинитола в крови и снижает диагностическую ценность метода. Весьма информативным является метод молекулярной лабораторной диагностики – полимеразная цепная реакция (ПЦР), позволяющая определить специфические ДНК Candida albicans. Чувствительность ПЦР достигает 100%, а специфичность – 98%.
В соответствии с требованиями протоколов оценки эффективности фунгицидных средств критериями диагноза кандидозной инфекции у хирургических больных являются следующие.
· Колонизация Candida – выделение Candida spp. из любого биологического материала (кроме гемокультуры) при отсутствии любых симптомов или признаков инфекционного процесса.
· Кандидемия – одна и более положительная гемокультура с выделением Candida spp.
· Кандидозная уроинфекция – выделение более 105 колоний Candida spp. в 1 мл мочи или данные микроскопического исследования биоптата тканей мочевыводящих органов.
· Интраабдоминальный кандидоз включает интраабдоминальные абсцессы или перитонит, вызванный Candida spp.
· Интраабдоминальный кандидозный абсцесс диагностируют в случае выделения из гнойно-воспалительного очага Candida spp.
· Кандидозный перитонит подтверждается выделением грибов Candida из перитонеального экссудата при лапаротомии или из дренажей брюшной полости.
· В случаях смешанного бактериального и кандидозного перитонита Candida spp. рассматривается как патоген только при одновременном выделении его из крови или при повторном выделении их при отсутствии улучшения состояния больного, несмотря на адекватное хирургическое или антибактериальное лечение.[1]
Лечение кандидоза
Инвазивные кандидозы чрезвычайно трудны для лечения. Имеющиеся сейчас данные поддерживают предположение, что задержка начала терапии при кандидемии связана со значительно более высокой смертностью, что делает важным раннее лечение. Несколько недавних исследований обнаружили, что смертность от кандидемии значительно увеличивается, если активная противогрибковая терапия была начата позже, чем через 24 часа после получения положительной культуры крови. Действительно, получение культуры в течение 12 часов является необходимой для улучшения исхода заболевания.
Из-за трудностей в подтверждении диагноза лабораторными методами, эмпирическое применение терапии часто основывается на клиническом диагнозе диссеминированного кандидоза. Руководства по эмпирической терапии диссеминированного кандидоза широко доступны. В целом, благодаря их подходящему профилю токсичности, высокой биодоступности при приеме перорально, низкой цене и импрессивной эффективности в рандомизированных клинических тестах, у гемодинамически стабильных пациентов терапия флуконазолом является предпочтительной. Недавно на международном симпозиуме были доложены результаты клинического исследования о том, что флуконазол может быть менее эффективным в лечении инвазионного кандидоза по сравнению с анидулофунгином. Однако, данные этих исследований пока не доступны в публикации, прошедшей экспертную оценку. Более того, каспофунгин и микафунгин подобно анидулофунгину проявили себя не хуже дезоксихолата амфотерицина В и липосомального амфотерицина В соответственно.
Так как флуконазол не может адекватно лечить значительную часть Candida glabrata, широкий спектр препаратов, таких как полиены, эхинокандины, или, возможно, вориконазол, предпочтительны, когда требуется срочно начать лечение против всех возможных видов, как это бывает у нестабильных пациентов. Естественно следует избегать применения вориконазола, когда инфекцию у таких пациентов вызывают азол-резистентные штаммы, такие как Candida glabrata или Candida krusei, или если пациент принимал флуконазол в течение последних 30 дней.
Если требуется препарат широкого спектра действия, то дезоксихолат амфотерицина В, липидный комплекс амфотерицина В, липосомальный амфотерицин В, вориконазол, каспофунгин, микафунгин или анидулафунгин - все они приемлемы в качестве препаратов первой линии.
На основании данных четырёх больших, рандомизированных, сравнительных исследований выявлено, что для лечения инвазивного кандидоза подходят все три эхинокандина (каспофунгин, микафунгин, анидулофунгин). Три этих эхинокандина по структуре, фармокинетически и фармакодинамически сходны, все три имеют схожую активность на экспериментальных моделях, и все имеют схожие данные рандомизированных клинических исследований.
Профилактика кандидоза
Показания к профилактике генерализованного кандидоза
Существуют показания для профилактического назначения противогрибковых препаратов у хирургических больных и больных другого профиля в критических состояниях:
-перфорация кишечника;
-несостоятельность анастомозов пищеварительного трактата;
-вторичный распространенный перитонит;
-хирургические вмешательства на поджелудочной железе;
-панкреонекроз;
-состояние после спленэктомии;
-длительная (более 7 сут) ИВЛ;
-длительное парентеральное питание;
-полиорганная недостаточность (дисфункция более 2 систем/органов);
-иммунодепрессивные состояния (в частности, длительная кортикостероидная терапия).
рофилактика нозокомиального кандидоза включает в себя профилактическое назначение противогрибковых препаратов пациентам из групп риска. В настоящее время арсенал антимикотических средств, используемых для профилактики вполне достаточный, что позволяет свести до минимума вероятные побочные эффекты этих препаратов. Следует отметить, что полиеновые препараты для перорального применения – нистатин и леворин – не всасываются, поэтому могут применяться только для лечения и профилактики местных поверхностных микозов, в частности орофарингеального.. Наиболее широко в хирургии и интенсивной терапии используют 2 препарата – амфотерицин В и флуконазол.
Амфотерицин В – полиеновое антимикотическое средство – более 30 лет используется в клинической практике. Обладает широким спектром действия в отношении различных штаммов Candida spp. за исключением Candida lusitaniae . Амфотерицин входит в состав комбинированного режима интестинальной селективной деконтаминации, достаточно широко используемой в хирургии и интенсивной терапии для предотвращения патологической колонизации и транслокации грибов.
Амфотерицин В обладает высокой токсичностью, наиболее значимым его побочным действием является повреждение канальцевого аппарата почек. Отчасти нефротоксичность амфотерицина В может быть снижена с помощью предварительной инфузии 500 мл изотонического раствора хлорида натрия или пентоксифиллина.
Липосомальные формы амфотерицина B обладают меньшей нефротоксичностью, однако очень дороги. В связи с этим клинический опыт применения липосомального амфотерицина В весьма ограничен, что пока не позволяет доказательно оценить эффективность этих препаратов в хирургии и интенсивной терапии.
Флуконазол широко используют для профилактики кандидозной инфекции. Флуконазол высокоактивен в отношении Candida albicans, однако не действует на Candida crusei, многие штаммы C.glabrata. Флуконазол можно применять как парентерально, так и перорально. Этот препарат не обладает нефротоксичностью, частота развития других побочных эффектов (включая гипокалиемию, головную боль, диарею, кожные высыпания) при использовании дифлюкана, значительно реже, чем при лечении амфотерицином.
В литературе отсутствуют стандартные рекомендации дозирования флуконазола для профилактики и лечения инвазивного кандидоза. Рекомендуемая профилактическая доза флуконазола составляет 50–400 мг/сут в зависимости от степени риска генерализованной грибковой инфекции. В большинстве стран Европы при кандидемии флуконазол применяют в дозе 400 мг/сут в течение 10–14 дней. В Японии такую дозу назначают лишь в случаях нестабильности гемодинамики, обычная доза составляет 100–200 мг/сут. В США максимально допустимая доза не превышает 400 мг/сут.
К другим видам профилактики относятся:
- Рациональное применение антибиотиков.
- Строгое соблюдение правил асептики при постановке внутривенных катетеров.
- Использование парентерального питания только в случае необходимости. Растворы для парентерального питания должны готовиться в аптеке, по возможности, в помещении с ламинарным потоком воздуха. Открытые флаконы с липидными растворами должны заменяться не реже, чем каждые 12 часов. [13]
Заключение
В курсовой работе были проанализированы последние литературные данные и исследования и систематизированы знания по возникновению, лечению и профилактике нозокомиальных инфекций, вызванных грибами рода Candida. Исходя из литературных данных, выявляется увеличение частоты нозокомиальных заболеваний, вызванных родом Candida, что связанно с увеличением количества больных в стационарах, более длительным их там нахождением и увеличением объема оперативных вмешательств. Были выделены группы риска людей, среди них, основные это: пациенты принимающие иммуносупрессоры, пациенты с катетерами и пациенты, находящиеся на параэнтеральном питании. Диагностика нозокомиальных грибковых заболеваний включает лабораторные микробиологические и серологические исследования, на основании результатов которых назначается лечениями препаратами такими как флуконазол, амфотерицин В и другие. Профилактика включает в себя назначение профилактических препаратов и соблюдение правил асептики.
Список литературы
1. Внутрибольничные грибковые инфекции: эпидемиология, диагностика и лечение/Joshua Perlroth, Bryan Choif , Brad Spellberg// Medical Mycology. - June 2007. - № 45. – с .321-346.
2. Гайдуль, К.В Внутрибольничные инфекции. Некоторые аспекты эпидемиологии, диагностики, лечения и профилактики: краткое информационное пособие для практикующих врачей / К.В. Гайдуль, А.А. Муконин. – Научно-информационный центр ОО «АБОЛмед», 2005.
3. Дрожжевые грибы: идентификация и резистентность к противогрибковым препаратам в онкогематологическом стационаре/Багирова Н.С., Дмитриева Н.В.//Инфекции и антимикробная терапия.- 2001.- Том 3; №6.- с. 178–182.
4. Инфекции, вызванные грибами, у пациентов отделений реанимации и интенсивной терапии//КазНМУ Кафедра анестезиологии и реаниматологии. http://www.kazanesthesia.kz/mikoz.php
5. Кандида альбиканс РНИФ (IgA, IgG, IgM)/ Регистрационное удостоверение ФС №2006/1519 от 03.10.2006 г.- Перевод на русский язык ЗАО «АНАЛИТИКА», Москва, 2007.
6. Кандидозная инфекция в отделении интенсивной терапии/ Багдатьев В.Е, Бурова С.А, Смирнов А.В// Успехи медицинской микологии. – Том 2, глава 2. – с. 209-210.
7. Кандидурия и кандидоз мочевыводящих путей: врачебная тактика/Климко Н.Н.//Рациональная антимикробная терапия для практического врача.- 2002.- Том 4;№3.
8. Микотические инфекции: клиника, диагностика, лечение/Клясова Г.А.//Инфекции и антимикробная терапия.- 2000.- Том 2; №6.- c.184–189.
9. Мониторинг грибковых инфекций в ОРИТ/ Н.В. Белобородова, Т.Ю. Вострикова// Клиническая микробиологическая антимикробная химиотерапия. – 2009. – Том 11; №1. – с. 22-30.
10. Нозокомиальная грибковая инфекция в хирургии и интенсивной терапии: состояние проблемы/Б.Р.Гельфанд, В.А.Гологорский, Е.Б.Гельфанд, Г.В.Лысенко//Consilium medicum.- 2001.- том 3;№11.
11. Нозокомиальная кандидурия: алгоритм диагностики и лечения/Белобородов В.Б., Синякова Л.А.// Consilium medicum.-2003.- Том 5; №7.
12. Нозокомиальные инфекции: эпидемиология, патогенез, профилактика, контроль / Козлов Р.С.// Клиническая микробиология и антимикробная химиотерапия. – 2000. - №1, том 2. - с.16-30.
13. Основы инфекционного контроля: практическое руководство/ Патрисия Экерман [и др.]; 2-ое издание. - Руководство подготовлено при поддержке Бюро Европы и Евразии, Агентства США по международному развитию (АМР США).
14. Позднеев О.К. Медицинская микробиология: учебник для вузов/ О.К. Поздеев. - под ред. Акад. РАМН В.И. Покровского. – М.: Геотар-Мед, 2001. – 778с.
15. Современные возможности диагностики грибковых инфекций у пациентов отделений интенсивной терапии и реанимиации/ Илюкевич Г.В., Доценко Ю.Н.//БелМАПО, РНПЦ МР и ЭЧ.
16. Современные проблемы диагностики и лечения грибковых инфекций мочевыводящих путей/ Мазо Е.Б., Попов С.В., Шмельков И.Ю.// РМЖ. Независимое издание для практикующих врачей.- № 2046. http://www.rmj.ru/articles_4365.htm.
17. Флуконазол в лечении грибковых инфекций у онкологических больных/Сельчук В.Ю., Петухова И.Н., Багирова Н.С., Кулага Е.В., Дмитриева Н.В.//РМЖ. Независимое издание для практикующих врачей.- №616. http://www.rmj.ru/articles_1033.htm.
18. Candida species и кандидемии. Состояние пробемы (Обзор)/Н.П. Елинов// Научно-исследовательский институт медицинской микробиологии им. П.Н. Кашкина Санкт-Пертербугрской медицинской академии последипломного образования, Россия. http://www.rusmedserv.com/mycology/html/kandidoz5.htm.
Приложения
сandida гриб внутрибольничный инфекция
Приложение 1. Частота выделения Candida ssp. У госпитализированных больных
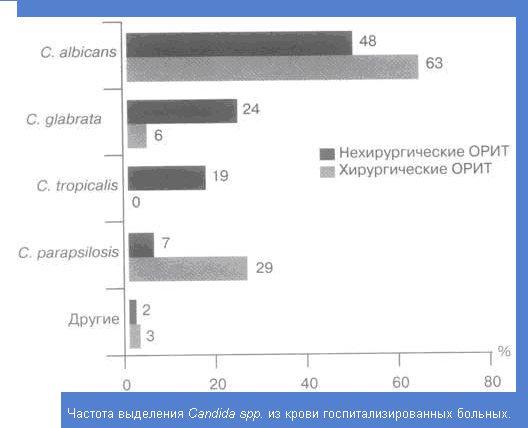
Приложение 2. Факторы риска кандемии и диссиминированного кандидоза

Приложение 3. Области инфекции, вызванные грибами рода Candida
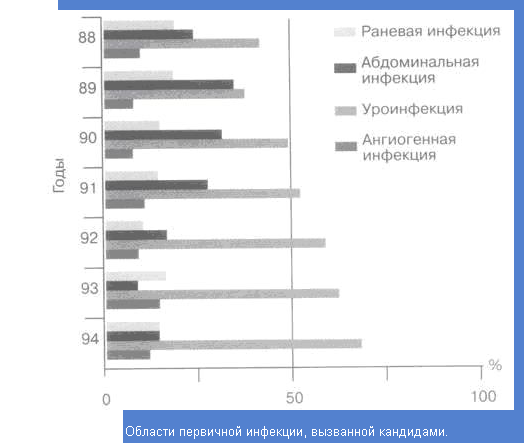
Введение
В последнее время большое значение приобретают нозокомиальные грибковые инфекции, что связано с увеличением их возникновения и сложностью диагностики и лечения. Целью этой курсовой работы является проанализировать последние литературные данные и исследования и выявить динамику внутрибольничных инфекций, вызванных грибами рода рода Candida. Определить основные причины и факторы этих заболеваний, и выявить группы риска людей, подверженных к возникновению у них нозокомиальных грибковых инфекций.Так же целью является описать эпидемиологию и рассмотреть наиболее часто встречающиеся клинические проявления нозокомиальных кандидозов. Актуальность работы в том, что в ней систематизируются все имеющиеся знания, рассматриваются основные принципы клинической диагностики нозокомиального кандидоза, наиболее рациональные методы лечения и проведения профилактики, что очень важно для уменьшения случаев инфицирования нозокомиальными штаммами Candida и в целом для снижения количества внутрибольничных грибковых заболеваний.
Глава 1. Понятие, причины и динамика внутрибольничных инфекций, вызванных грибами рода Candida
Дата: 2019-12-10, просмотров: 386.