По основному закону теплопередачи:
F = 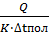 , где F – площадь поверхности теплопередачи
, где F – площадь поверхности теплопередачи
K = 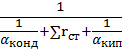 , где K – коэффициент теплопередачи
, где K – коэффициент теплопередачи
1) Определим коэффициент теплопередачи конденсирующегося пара 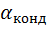 .
.
При конденсации греющего пара на пучке вертикальных труб, выражение для коэффициента теплопередачи имеет следующий вид:
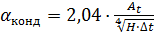
At (при tконд = 113,5 ̊С) = 7150 (1, табл. 4.6)
Примем температуру наружной стенки трубы tст 1 меньшей, чем tконд и равной tст 1 = 110,6 ̊С
∆t = tконд - tст 1 = 113,5 – 110,6 = 2,9 K
 =7904
=7904 
2) Определим суммарное сопротивление стенки:
∑rст = 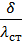 + rзагр,1 + rзагр,2 , где
+ rзагр,1 + rзагр,2 , где
δ – толщина стенки трубы (0,002 м по приложению 1)
λ – коэффициент теплопроводности трубы
rзагр,1 и rзагр,2 – термические сопротивления загрязнений
rзагр, 1 =  = 1,724·10-4
= 1,724·10-4 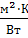
rзагр, 2 = 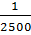 = 4·10-4
= 4·10-4 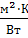
Коэффициент теплопроводности для стали:
λст = 46,5 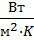
∑rст =  + 1,724·10-4 + 4·10-4 = 6,15·10-4
+ 1,724·10-4 + 4·10-4 = 6,15·10-4 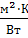
tст,2 = tст, 1 – q1·∑rст,
q1 = 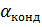 ·(tконд – tст, 1)
·(tконд – tст, 1)
q1 = 7904·(113,5 – 110,6) = 22922 Вт
tст,2 = 110,6 – 22922·6,15·10-4 = 95,5 ̊С
3) Определим коэффициент теплоотдачи кипящего раствора
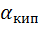 = b3·
= b3· 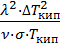
b = 0,075·[1 + 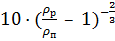 ]
]
Находим плотность пара и плотность раствора при температуре кипения:
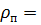 0,335
0,335 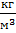 (1, табл. LVI)
(1, табл. LVI)
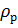 = 1306
= 1306 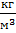 (приложение 2)
(приложение 2)
b = 0,075·[1 + 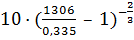 ] = 0,078
] = 0,078
Найдем кинематическую вязкость:
ν = 
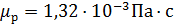 (приложение 2)
(приложение 2)
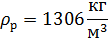
ν =  = 1·10-6
= 1·10-6 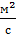
Поверхностное натяжение раствора при температуре кипения:
σ ≈ 80·10-3 
Коэффициент теплопроводности при температуре кипения раствора:
λ = 0,648 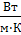 (приложение 2)
(приложение 2)
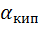 = 0,0783·
= 0,0783· 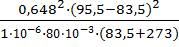 = 1006
= 1006 
K = 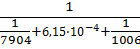 = 576,2
= 576,2 
F =  = 29,4 м2
= 29,4 м2
Выбор аппарата
Найденную площадь поверхности теплообмена увеличим на 10-20 % для обеспечения запаса производительности:
F = 1,2·29,4 = 35,3 м2
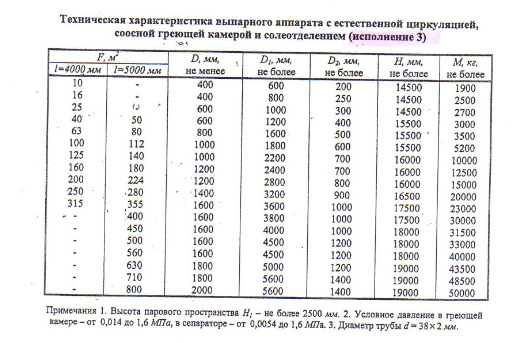
По приложению 1 выберем аппарат с F = 40 м2
Техническая характеристика выпарного аппарата (исполнение 3)
| F, м2 | D, мм не менее | D1, мм не более | D2, мм не более | H, мм не более | М, кг не более |
| l=4000 мм | |||||
| 40 | 600 | 1200 | 400 | 15500 | 3000 |
Расчет расхода оборотной воды в теплообменном аппарате
Температуру воды на выходе tк из конденсатора примем на 4 ̊ ниже температуры конденсации паров t0 :
t0 = 69,1 - ∆´´´ = 69,1-1 = 68,1 ̊ C
tк = 68,1 - 4 = 64,1 ̊ C
Начальную температуру оборотной воды примем tн = 12 ̊ C
Энтальпия паров при температуре t0 :
Iп = 2622,9·103 Вт
Расход оборотной воды:
Gв = W· 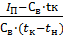
Gв = 0,1944· 
Gв = 2,0965 
Приложение 1. Техническая характеристика выпарного аппарата
Приложение 2
Формулы для расчета теплофизических параметров растворов
Плотность растворов
Плотность растворов ρ(t) в диапазоне температур 0 ÷ 100 ̊С может быть вычислена по формуле:
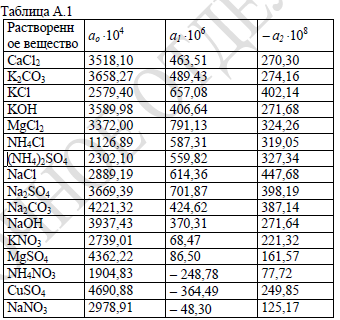
lg(ρр) = lg(ρ0) + (a0 + a1·t + a2·t2)·x
где ρ –плотность раствора, кг/м3;
x–массовая концентрация растворенного вещества, кг растворенного вещества/ кг раствора;
t – температура, ̊С;
а0, а 1, а 2 – коэффициенты, приведенные в таблице А1;
ρ0 – плотность воды, которая может быть рассчитана по формуле:
ρ0 = 1000 - 0,063·t - 0,00355·t2
Таблица А.1
Растворенное вещество
Вязкость растворов
Вязкость μ(t) растворов в диапазоне температур 0 ÷ 100 ̊С может быть вычислена по формуле:
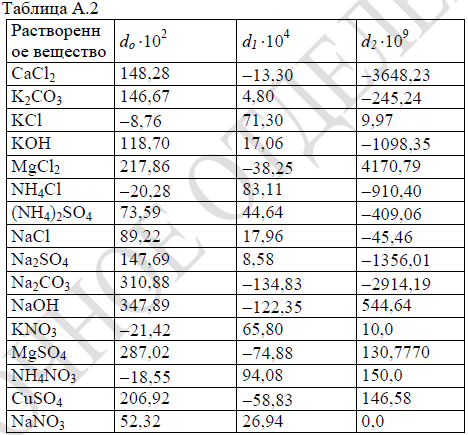
lg(μр) = lg(μ0) + (d0 + d1·t + d2·t2)·x
где μ – динамический коэффициент вязкости раствора, Па∙с;
x–массовая концентрация растворенного вещества, кг растворенного вещества/кг раствора;
t – температура, ̊С;
d0, d1, d2 – коэффициенты, приведенные в таблице А.2;
μ0 – вязкость воды, которая может быть рассчитана по формуле:
μ0(t) = 0,59849·(43,252+t)-1,5423
Теплопроводность растворов
Теплопроводность λ(t) растворов в диапазоне температур 0 ÷ 100 ̊С может быть вычислена по формуле:
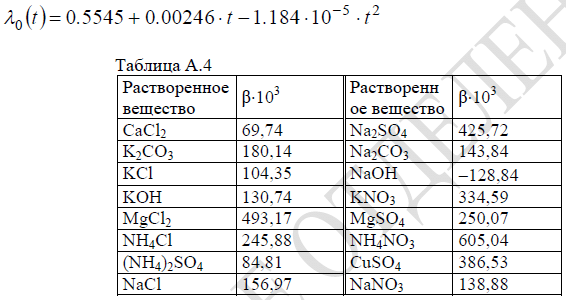
λ(t) = λ0(t)·(1-β·x)
где λ – теплопроводность, Вт/м/К;
x – массовая концентрация растворенного вещества, кг растворенного вещества/кг раствора;
t – температура, ̊С;
β– коэффициент, приведенный в таблице А.4;
λ0 – теплопроводность воды, которая может быть рассчитана по формуле:
Литература.
1. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи к курсу процессов и аппаратов химической технологии. Перепечатка с изд. 1987 г. – М.: ООО «РусМедиаКонсалт», 2004. - 576 с.
2. Н. Б. Варгафтик. Справочник по теплофизическим свойствам газов и жидкостей. Издание второе, дополненное и переработанное 1972 г. – 721 с.
3. Справочник химика том 3. Химическое равновесие и кинетика свойства растворов. Электродные процессы. Издание 2, дополненное и переработанное 1965 г. – 1005 с.
Дата: 2019-07-31, просмотров: 429.